季节性及常年性AC

过敏性结膜炎(含花粉症)
一目了然的要点
Section titled “一目了然的要点”1. 什么是过敏性结膜炎
Section titled “1. 什么是过敏性结膜炎”过敏性结膜疾病(allergic conjunctival disease:ACD)定义为「以Ⅰ型变态反应为主的结膜炎症性疾病,伴有由抗原引起的自觉症状和他觉所见」1)。仅具有过敏体质并不足以诊断,必须有瘙痒感、异物感、眼分泌物、流泪等自觉症状和结膜炎性改变才能确诊为ACD。
日本眼科过敏学会《过敏性结膜疾病诊疗指南第3版》(以下简称本指南)根据结膜增生性变化(眼睑结膜乳头增生·巨大乳头·角膜缘结膜肿胀或堤防状隆起)的有无、是否合并特应性皮炎、以及是否有异物引起的机械刺激来分类疾病类型1)。
- 过敏性结膜炎(AC):结膜无增殖性变化的病型。症状呈季节性发作者称为季节性过敏性结膜炎(SAC),常年发作者称为常年性过敏性结膜炎(PAC)。其中花粉引起的SAC也称为「花粉性结膜炎」,以杉树花粉及当地主要花粉为代表抗原1)。
- 特应性角结膜炎(AKC):合并面部特应性皮炎的慢性ACD。常伴有结膜纤维化及角膜新生血管、混浊1)。Hogan等人于1952年首次报告了5例伴有双眼角结膜炎的特应性湿疹病例2)。
- 春季角结膜炎(VKC):结膜出现增殖性变化的重症型。可伴有角膜上皮病变、持续性角膜上皮缺损、盾形溃疡、角膜斑块等多种角膜病变1)。
- 巨大乳头性结膜炎(GPC):由隐形眼镜、义眼、手术缝线等机械刺激引起,在上眼睑结膜出现增殖性变化的病型。本指南将其定义为隐形眼镜相关乳头性结膜炎中乳头直径达1mm以上的最重症型1)。
日本的流行病学
Section titled “日本的流行病学”以眼科为主导的全国性调查包括:1993~1995年日本眼科医师会过敏眼病调查、1993年厚生省现场调查、2017年日本眼科过敏研究会患病率调查1, 4)。2017年的患病率调查显示,患病率、病型分布及年龄分布如下所述。
| 指标 | 调查结果 |
|---|---|
| ACD总体患病率 | 48.7%(从1993年的15-20%显著增加) |
| 柳杉/扁柏引起的 SAC | 37.4% |
| 常年性过敏性结膜炎(PAC) | 14.0% |
| 柳杉/扁柏以外的 SAC | 8.0% |
| 特应性角结膜炎(AKC) | 5.3% |
| 春季角结膜炎(VKC) | 1.2% |
| 巨乳头性结膜炎(GPC) | 0.6% |
| ACD总体年龄分布 | 40多岁为高峰,10多岁为小高峰 |
| SAC地域分布不均 | 首都圈及中部地区偏高 |
来源:日本眼科过敏学会诊疗指南制定委员会《过敏性结膜疾病诊疗指南第3版》1)以及冈本等人《2017年度日本眼科过敏学会过敏性结膜疾病实况调查》4)。
PAC在10多岁和40多岁有两个峰值,SAC从儿童期起患病率随年龄增长而上升。SAC合并过敏性鼻炎的比例高达6570%1)。AKC据估计在2540%的特应性皮炎患者中并发5)。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”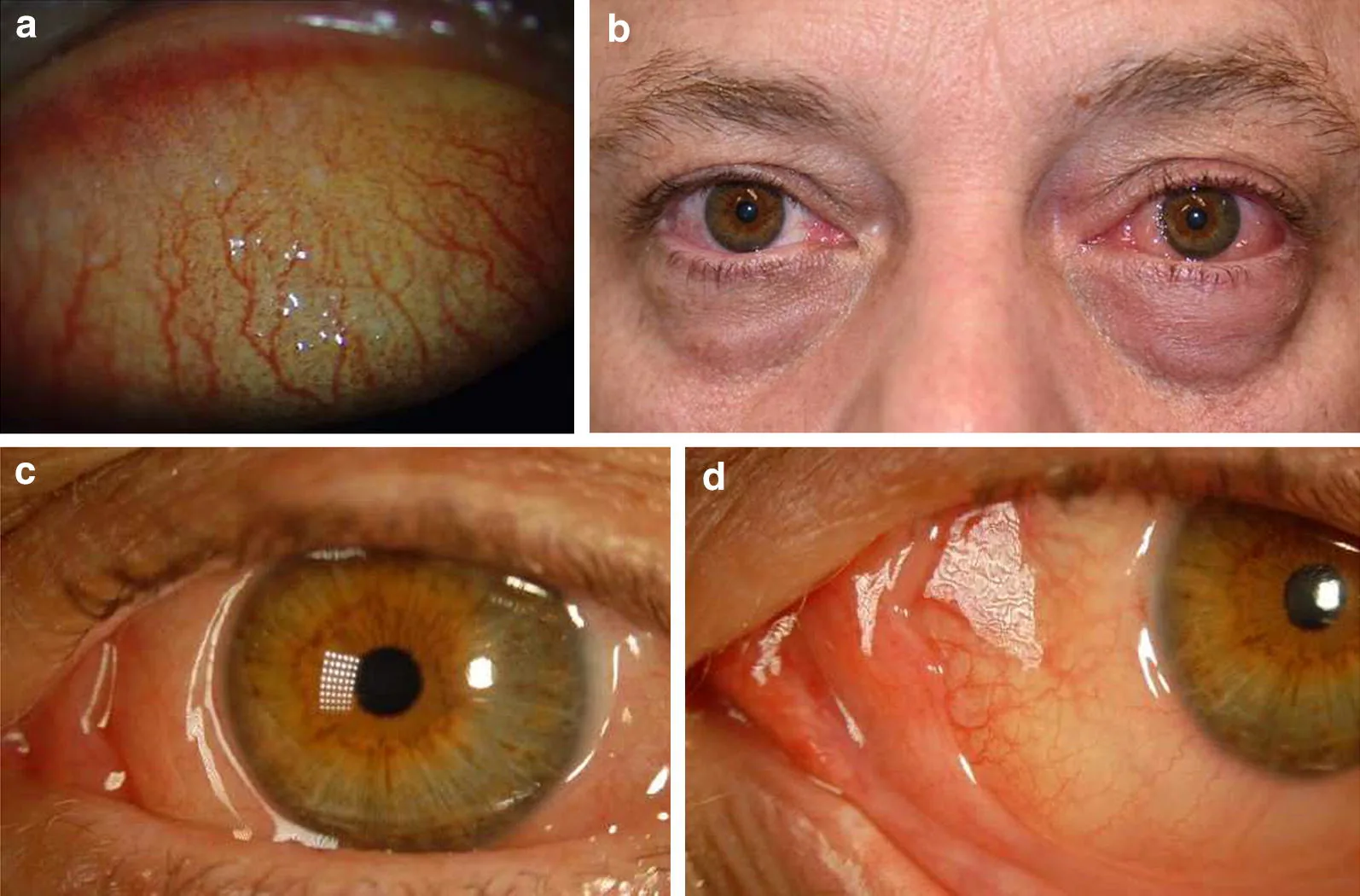
ACD的代表性自觉症状为瘙痒感、异物感和眼部分泌物,其中眼瘙痒是特异性最高的症状1)。
- 眼瘙痒:ACD最特征性的症状。肥大细胞释放的组胺刺激感觉神经末梢引起。儿童和老年人可能不主诉瘙痒,而表达为异物感或不适感1)。
- 异物感:主诉为「沙砾感」。多由大量结膜乳头在眨眼时与角膜接触引起1)。
- 眼部分泌物:以浆液性、黏液性为主,特征为白色或半透明的丝状黏稠分泌物。与以中性粒细胞为主的细菌性分泌物性状不同1)。VKC有时可见黄色黏性分泌物。
- 流泪·充血:发生频率高但特异性低。
- 眼痛·畏光·视力下降:见于伴有角膜病变的情况,与严重程度相关1)。
- GPC特有的主诉:始于使用隐形眼镜时的轻度异物感,随后常依次自觉镜片易移位、易变脏、眼部分泌物增多、视物模糊。
临床所见与评估标准
Section titled “临床所见与评估标准”本指南针对眼睑结膜、球结膜、角膜缘、角膜各部位制定了严重程度评估标准1)。以下列举代表性项目。
| 部位 | 项目 | 严重程度参考 |
|---|---|---|
| 眼睑结膜 | 充血 | 轻度:数条、中度:多条、重度:血管无法辨认 |
| 眼睑结膜 | 乳头 | 轻度0.1〜0.2mm、中度0.3〜0.5mm、重度0.6mm以上 |
| 眼睑结膜 | 巨大乳头 | 直径1mm以上。未达上眼睑结膜的1/2为中度、1/2以上为重度 |
| 眼球结膜 | 水肿 | 局灶=轻度,弥漫=中度,囊泡=重度 |
| 角膜缘 | Trantas斑 | 1 |
| 角膜 | 上皮病变 | 点状表层角膜炎→落屑样点状表层角膜炎→盾形溃疡 |
来源:基于本指南表2-2制作1)。
各类型的特征性表现
Section titled “各类型的特征性表现”春季角结膜炎 眼睑型
春季角结膜炎 轮部型
特应性角结膜炎
巨大乳头性结膜炎
3. 原因与风险因素
Section titled “3. 原因与风险因素”不同病型的原因抗原分布差异很大。本指南将包含螨虫、屋尘、桤木、柳杉、扁柏、黄花茅、鸭茅、艾蒿、豚草、念珠菌、链格孢、猫上皮、狗上皮等的「PAC套餐」列为血清抗原特异性IgE抗体检测的保险适用项目1)。
| 病型 | 主要原因抗原 | 季节性 |
|---|---|---|
| 季节性过敏性结膜炎(SAC) | 杉・桧(春)、鸭茅・梯牧草等禾本科(初夏)、豚草・艾蒿等菊科(秋) | 有 |
| 常年性过敏性结膜炎(PAC) | 螨虫・屋尘、霉菌、宠物皮屑 | 无 |
| 特应性角结膜炎(AKC) | 多致敏(螨虫・屋尘・花粉・食物等)、特应性素质 | 慢性 |
| 春季角结膜炎(VKC) | 屋尘・螨虫多见,但对花粉・动物皮屑等多抗原也有反应 | 有加重 |
| 巨乳头性结膜炎(GPC) | 隐形眼镜材料・镜片沉积物、义眼、暴露缝线 | 无 |
风险因素与背景
Section titled “风险因素与背景”- 特应性体质・家族史:支气管哮喘、过敏性鼻炎、特应性皮炎的家族史会增加风险。AKC 与丝聚蛋白基因异常等皮肤屏障功能障碍相关5)。
- 城市生活・环境因素:空气污染、吸烟、干燥环境可能成为 ACD 的加重因素6)。
- 杜匹鲁单抗:用于重症特应性皮炎治疗的 IL-4 受体 α 链抗体杜匹鲁单抗,据报道结膜炎并发风险比为 2.64,在 AKC 治疗过程中也需注意1)。
- 揉眼习惯:因瘙痒导致的慢性揉眼是圆锥角膜和特应性白内障的风险因素5, 12)。尤其是 AKC 中,慢性机械刺激促进角膜结构脆弱化,与青年发病的圆锥角膜有关联5)。
日本眼科过敏学会的指南建议:佩戴护目镜或普通眼镜,可能的话停止佩戴隐形眼镜改用框架眼镜,使用不含防腐剂的人工泪液洗眼(不可用自来水,会损伤角膜),外出时穿着光滑材质的外套并在玄关脱下,回家后洗脸、漱口。此外,在花粉飞散预测日的大约2周前开始使用抗过敏眼药水的「初期疗法」也有效。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”诊断标准(本指南)
Section titled “诊断标准(本指南)”诊断基于临床症状、I型过敏体质、眼部局部I型过敏反应这3个要素,分3个阶段进行1)。
- 临床诊断(仅A):存在ACD特有的临床症状。
- 临床确诊诊断(A+B):除临床症状外,泪液中总IgE抗体阳性、血清抗原特异性IgE抗体阳性,或与推定抗原一致的皮肤反应阳性。
- 确诊诊断(A+B+C或A+C):在上述基础上,结膜刮取物中嗜酸性粒细胞阳性。
A:有临床症状/B:有I型过敏体质/C:结膜存在I型过敏反应。
本指南将自觉症状和他觉所见分别按「特异性:高/中/低」进行整理,重度眼瘙痒、巨大乳头、轮部增殖、盾形溃疡被认为是特异性最高的所见1)。
- 结膜刮片嗜酸性粒细胞检查:点眼麻醉后将上眼睑翻转,用玻璃棒轻轻按摩睑结膜,然后用刮匙采集黏液涂布于载玻片。进行Hansel染色或Giemsa染色,在光学显微镜下即使确认到1个嗜酸性粒细胞也判定为阳性1, 3)。
- 泪液总IgE抗体检测(Allerwatch®):由和光制药/Minaris Medical的快速诊断试剂盒,采用免疫层析法以泪液为样本进行检测。对ACD的敏感度为73.6%,特异度为100%1)。各病型的阳性率为SAC 61.9%、PAC 65.4%、AKC 80.5%、VKC 94.7%、GPC 75.0%,总体为72.2%3)。
- 滴眼激发试验:将已知抗原液滴眼以确认结膜炎症状诱发的方法,但在日本无保险适用且未标准化1)。
全身过敏因素检查
Section titled “全身过敏因素检查”- 血清抗原特异性IgE抗体检测:选择以螨虫、屋尘、杉树、柏树、鸭茅、豚草、艾蒿、狗/猫上皮等PAC套餐项目为主的检测项目。保险适用范围最多为13个项目1, 3)。作为筛查用途,可使用能够同时检测多项的View Allergy 39(Thermo Fisher Diagnostics)和Mast Immunosystems V(Minaris Medical),同样在保险适用范围之内3)。
- 皮肤反应测试(点刺试验·划痕试验):风团直径达到3mm以上,或达到阳性对照风团的一半以上时判定为阳性。同时使用阳性对照(确认无假阴性)和阴性对照(确认无机械性荨麻疹)。组胺H₁受体拮抗剂和三环类抗抑郁药可能导致假阴性,因此需要注意检测前的停药期3)。对于有严重支气管哮喘、过敏反应史或重大心血管疾病的病例,需谨慎评估。
本指南图2-40的临床诊断流程图将眼痒或充血为主诉的病例首先根据有无结膜增殖性变化进行分类,无增殖性变化时根据有无季节性判断为SAC/PAC,有增殖性变化时若佩戴隐形眼镜则判断为GPC,未佩戴隐形眼镜则根据有无特应性皮炎来区分AKC/VKC1)。
本指南列举了以下疾病作为鉴别对象1)。
- 病毒性结膜炎:腺病毒(流行性角结膜炎、咽结膜热)、单纯疱疹病毒、水痘-带状疱疹病毒、肠道病毒、SARS-CoV-2等。急性发病、单眼发病、耳前淋巴结肿大为参考依据,腺病毒可通过快速诊断试剂盒检测抗原。
- 细菌性结膜炎:金黄色葡萄球菌、肺炎链球菌、流感嗜血杆菌等为致病菌。通过黏液脓性黄至黄绿色眼部分泌物及结膜刮片中的多核白细胞进行鉴别。
- 衣原体性结膜炎:成人表现为单眼急性滤泡性结膜炎,下眼睑结膜穹窿部巨大滤泡为其特征。
- 结膜滤泡症:见于儿童下眼睑结膜穹窿部的粟粒大滤泡,无自觉症状,无明显病理意义。
- 干眼症:伴有BUT缩短,常与过敏性结膜炎合并存在1)。
若眼痒感强烈、双眼发病、以浆液性或黏液性白色分泌物为主,且存在过敏体质(合并过敏性鼻炎或皮炎、家族史),应考虑过敏性结膜炎。另一方面,若急性发病、从单眼开始、伴有黏液脓性或黄色分泌物、耳前淋巴结肿大、发热或咽痛,则应考虑感染性结膜炎,并进行腺病毒快速检测或结膜刮片检查。两者的诊断标准详见日本眼科过敏学会指南第3版。
5. 标准治疗方法
Section titled “5. 标准治疗方法”本指南指出,所有类型的一线治疗均为抗过敏滴眼液,根据严重程度可加用类固醇滴眼液和免疫抑制滴眼液1)。对于难治性重症病例,口服类固醇、类固醇睑结膜下注射、结膜乳头切除术等外科治疗也是可选方案。
抗过敏滴眼液
Section titled “抗过敏滴眼液”抗过敏滴眼液根据其作用机制大致分为两类1, 13)。
- 介质释放抑制剂:抑制肥大细胞脱颗粒,阻止组胺、白三烯、血栓素A₂等介质的释放,从而减轻Ⅰ型过敏性即发反应。通过抑制炎症细胞在结膜的局部浸润,对迟发相也有作用。
- 组胺H₁受体拮抗剂:竞争性抑制肥大细胞释放的组胺与H₁受体结合,从而减轻充血和眼痒。据报道,其对瘙痒的速效作用优于介质释放抑制剂。
下表总结了代表性药物。
| 分类 | 通用名 | 代表性商品名 | 浓度和用法 |
|---|---|---|---|
| 介质释放抑制剂 | 吡嘧司特钾 | 阿乐吉萨滴眼液 | 0.1% 每日2次 |
| 介质释放抑制剂 | 曲尼司特 | 利扎本滴眼液 | 0.5% 每日4次 |
| 介质释放抑制剂 | 异丁司特 | 凯塔斯滴眼液 | 0.01% 每日4次 |
| 介质释放抑制剂 | 阿西他扎司特水合物 | 泽贝林滴眼液 | 0.1% 每日4次 |
| H₁受体拮抗剂 | 酮替芬富马酸盐 | 扎迪腾滴眼液 | 0.05% 每日4次 |
| H₁受体拮抗剂 | 左卡巴斯汀盐酸盐 | 立复汀滴眼液 | 0.025% 每日4次 |
| H₁受体拮抗剂 | 奥洛他定盐酸盐 | 帕坦洛滴眼液 | 0.1% 每日4次 |
| H₁受体拮抗剂 | 依匹斯汀盐酸盐 | 阿雷吉昂滴眼液/阿雷吉昂LX滴眼液 | 0.05% 每日4次/0.1% 每日2次 |
来源:本指南表2-61)。
酮替芬、奥洛他定和依匹斯汀除具有组胺H₁受体拮抗作用外,体外研究也证实具有抑制介质释放的作用。阿雷吉昂LX不含防腐剂,因此易于为隐形眼镜佩戴者处方。
初始治疗(季节性过敏性结膜炎)
Section titled “初始治疗(季节性过敏性结膜炎)”本指南推荐在花粉飞散预测日约2周前,或症状刚出现时就开始使用抗过敏滴眼液的初始治疗1)。这可以减轻花粉飞散高峰期的症状,部分报告显示约30%的患者其花粉症症状本身得到了抑制。对于常年性过敏性结膜炎,为全年维持肥大细胞膜稳定,介质释放抑制剂也有效。
按病型的治疗方针
Section titled “按病型的治疗方针”1) 季节性和常年性过敏性结膜炎(SAC / PAC)
Section titled “1) 季节性和常年性过敏性结膜炎(SAC / PAC)”- 首选:抗过敏滴眼液(介质释放抑制剂或H₁拮抗药)1)。
- 症状严重或伴有鼻炎症状时:口服抗过敏药,必要时联合使用NSAID滴眼液1)。
- 抗过敏滴眼液无法控制时:类固醇滴眼液短期联合使用。本指南CQ1对SAC/PAC使用类固醇滴眼液弱推荐1)。原则是不作为首选,在定期测量眼压的基础上短期使用。
- 对于佩戴隐形眼镜者或合并干眼症者,选择不含防腐剂的制剂。
2) 特应性角结膜炎(AKC)
Section titled “2) 特应性角结膜炎(AKC)”- 首选抗过敏滴眼液。效果不佳时,联合使用类固醇滴眼液或免疫抑制滴眼液1)。
- 本指南CQ3对AKC使用类固醇滴眼液强推荐1)。
- CQ7对AKC使用他克莫司滴眼液强推荐(但在日本仅春季卡他性结膜炎适用医保)1, 8)。环孢素滴眼液对AKC有条件推荐1)。
- 需要并行治疗特应性眼睑炎,必须与皮肤科、过敏科协作5)。
- 处方口服类固醇时,需与内科、皮肤科专家协作1)。
- 在接受包括度普利尤单抗在内的生物制剂和口服环孢素全身治疗的病例中,需注意度普利尤单抗相关结膜炎的并发风险比为2.641)。
3) 春季角结膜炎(VKC)
Section titled “3) 春季角结膜炎(VKC)”按照本指南的治疗流程图(图2-42)逐步加强治疗1, 7)。
- 首先以抗过敏滴眼液为基础进行处方。
- 中度以上病例加用免疫抑制滴眼液。他克莫司滴眼液在 CQ7 中被强烈推荐(基于证据的疗效已确立),环孢素滴眼液在 CQ4 中被有条件推荐1, 8, 9)。
- 两种药物仍无改善的重症病例,进一步加用类固醇滴眼液(CQ2:强烈推荐)1)。
- 对于增殖性病变,环孢素+类固醇联合(CQ6),以及重症病例的他克莫司+类固醇联合(CQ9)均为有条件推荐1)。
- 滴眼液无法控制的最重症病例,可考虑口服类固醇、类固醇睑结膜下注射、结膜乳头切除、角膜斑块刮除术1)。睑结膜下注射使用曲安奈德或倍他米松磷酸钠混悬液,但需注意眼压升高,避免反复使用及用于10岁以下儿童1)。
- 症状改善后,将类固醇滴眼液转换为低效价制剂后逐渐减量停药,以抗过敏滴眼液和免疫抑制滴眼液两种药物进行控制。
主动疗法:当缓解期延长时,免疫抑制滴眼液从每日2次→每日1次→每周2次逐步减量,最终维持少量维持剂量。为防止复发,根据症状调整用药量1)。
4) 巨大乳头性结膜炎(GPC)
Section titled “4) 巨大乳头性结膜炎(GPC)”- 去除病因最为重要。若由隐形眼镜引起,原则上应停止佩戴。重新佩戴时,应更换为日抛型软性隐形眼镜、更改镜片材质或形状、指导揉搓清洗及更换护理用品1)。
- 首选抗过敏滴眼液(主要为介质释放抑制剂),重症病例短期联合使用类固醇滴眼液(例如:0.1%氟甲龙 每日4次)。滴眼期间需测量眼压。
- 若由义眼引起,考虑更换义眼或更改种类1)。
免疫抑制滴眼液(VKC 医保适用)
Section titled “免疫抑制滴眼液(VKC 医保适用)”环孢素滴眼液
他克莫司滴眼液
两种药物均可引起滴眼时的刺激感或灼热感,使用期间需注意疱疹性角膜炎等感染并发症。儿童和成人均可用于VKC1)。
其他注意事项
Section titled “其他注意事项”AKC并发症的外科治疗
Section titled “AKC并发症的外科治疗”AKC病程中出现的并发症,有时需要分别进行外科治疗5)。
- 羊膜移植:用于持续性角膜上皮缺损。
- 角膜移植:用于角膜混浊、重度溃疡、角膜变薄,但AKC患者排斥反应率高,术后仍需严格的炎症管理。
- 白内障手术:用于表现为前囊下及后囊下混浊的特应性白内障。
- 眼睑手术:矫正倒睫、眼睑外翻、眼睑内翻。
6. 病理生理学·详细发病机制
Section titled “6. 病理生理学·详细发病机制”Ⅰ型过敏反应的即时相与迟发相
Section titled “Ⅰ型过敏反应的即时相与迟发相”过敏性结膜炎的基本发病机制为Ⅰ型(速发型)过敏反应。
即时相(接触过敏原后约15分钟内):过敏原到达结膜后,与致敏的结膜肥大细胞表面的IgE抗体发生交联,导致肥大细胞脱颗粒,组胺、类胰蛋白酶、白三烯、前列腺素等化学递质同时释放10, 11)。释放的组胺通过H₁受体引起毛细血管扩张、血管通透性增加、感觉神经刺激和黏液分泌增加,表现为眼痒、结膜充血、结膜水肿和流泪。
迟发相(数小时后):细胞因子(IL-4、IL-5、IL-13等)和黏附分子(ICAM-1、VCAM-1等)的表达导致嗜酸性粒细胞、中性粒细胞、淋巴细胞和嗜碱性粒细胞浸润到结膜局部10, 11)。嗜酸性粒细胞释放的主要碱性蛋白(MBP)和嗜酸性粒细胞阳离子蛋白(ECP)等组织损伤性蛋白会损伤角结膜上皮,引起点状表层角膜炎、迁延性角膜上皮缺损、盾形溃疡等角膜病变14)。
Th2细胞与春季角结膜炎及特应性角结膜炎的特殊病理
Section titled “Th2细胞与春季角结膜炎及特应性角结膜炎的特殊病理”轻度SAC/PAC以Ⅰ型即时相为主,而春季角结膜炎和特应性角结膜炎中Th2细胞(2型辅助T细胞)在病理形成中发挥核心作用1, 13)。在动物模型中,Ⅰ型过敏反应单独无法诱导强烈的结膜嗜酸性粒细胞浸润,只有涉及Th2细胞时才能诱导高度嗜酸性粒细胞浸润。春季角结膜炎巨乳头的病理组织学可见嗜酸性粒细胞浸润、成纤维细胞增生、细胞外基质沉积,以及大量T细胞浸润。据报道,泪液中嗜酸性粒细胞数量与角膜病变严重程度指标相关13)。
在特应性角结膜炎的结膜组织中,除Ⅰ型超敏反应外,以T细胞、巨噬细胞、树突状细胞浸润为特征的Ⅳ型(迟发型)超敏反应也参与其中。杯细胞增生、上皮内嗜酸性粒细胞和肥大细胞浸润、固有层单核细胞浸润是组织学特征,角膜知觉减退和结膜杯细胞密度减少也有报道5, 14)。
花粉的萌出机制
Section titled “花粉的萌出机制”杉树花粉颗粒较大,无法直接穿过结膜上皮。但当花粉吸收泪液水分后破裂(萌出)时,抗原蛋白(如Cry j 1、Cry j 2等)溶出并通过结膜上皮,到达深层肥大细胞从而启动过敏反应。人工泪液通过稀释泪液和冲走花粉起到预防作用,正是基于这一机制。
巨乳头性结膜炎的机制
Section titled “巨乳头性结膜炎的机制”GPC 的发病机制中Ⅰ型过敏的参与并不总是明确,接触镜及其沉淀物、暴露的缝线等引起的反复机械刺激以及对镜片材质和沉淀蛋白的免疫反应被认为是主要原因1)。结膜组织可见嗜酸粒细胞、肥大细胞、嗜碱粒细胞浸润,但血清抗原特异性IgE抗体阳性率和嗜酸粒细胞阳性率低于其他病型1)。
AKC并发症的机制
Section titled “AKC并发症的机制”AKC特征性眼部并发症的发病机制归纳如下5, 12)。
- 圆锥角膜:与长期揉眼引起的角膜反复机械损伤以及慢性炎症导致的角膜结构脆弱化有关。
- 特应性白内障:以囊膜下前部和后部混浊为特征,独立于类固醇使用而发生晶状体混浊。
- 单纯疱疹角膜炎:AKC患者发生双眼疱疹性角膜炎的风险较高,免疫抑制治疗期间需特别注意。
- 视网膜脱离:在特应性皮炎患者中发生率较高,被认为与揉眼行为有关。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”奥马珠单抗(抗IgE单克隆抗体)是一种用于支气管哮喘和慢性荨麻疹的生物制剂,海外病例报告和小规模观察性研究报告了其对难治性春季角结膜炎和重症特应性角结膜炎的疗效。在日本,该药尚未获批用于眼部疾病,目前被视为试验性治疗选择11)。
JAK抑制剂(如乌帕替尼等):通过选择性抑制JAK-STAT通路来阻断IL-4/IL-13信号,正在探索其在避免度普利尤单抗相关结膜炎的同时改善皮肤和眼部症状的可能性。
新型作用机制滴眼液
Section titled “新型作用机制滴眼液”同时抑制补体C5和白三烯B4的滴眼液(rVA576)已进入I期临床试验,多种同时靶向多个靶点的新型分子正在开发中。
一级预防与生活习惯
Section titled “一级预防与生活习惯”益生菌:有报告指出,产前和产后补充益生菌可能使特应性疾病发病率降低高达30%,但尚未建立结论性证据。也有观点认为,抗生素的使用可能通过改变肠道菌群增加特应性疾病的风险。
母乳喂养:有研究表明,尤其在出生后3个月之前的母乳喂养可能是特应性疾病的保护因素。关于维生素和矿物质补充剂,尚未获得有益的证据。
8. 参考文献
Section titled “8. 参考文献”- 日本眼科アレルギー学会診療ガイドライン作成委員会. アレルギー性結膜疾患診療ガイドライン(第3版). 日眼会誌. 2021;125(8):741-785. https://www.nichigan.or.jp/member/journal/guideline/detail.html?dispmid=909&itemid=429
- Hogan MJ. Atopic keratoconjunctivitis. Trans Am Ophthalmol Soc. 1952;50:265-281.
- 庄司純, ほか. アレルギー性結膜疾患診断における自覚症状、他覚所見および涙液総IgE検査キットの有用性の検討. 日眼会誌. 2012;116(6):485-493. CiNii: https://cir.nii.ac.jp/crid/1520290883483009152
- 岡本茂樹, ほか. 2017年度日本眼科アレルギー学会アレルギー性結膜疾患実態調査. 日眼会誌. 2022;126(7):625-635. https://journal.nichigan.or.jp/Disp?mag=0&number=7&start=625&style=abst&vol=126&year=2022
- Chen JJ, Applebaum DS, Sun GS, Pflugfelder SC. Atopic keratoconjunctivitis: A review. J Am Acad Dermatol. 2014;70(3):569-575.
- Leonardi A, Castegnaro A, Valerio AL, Lazzarini D. Epidemiology of allergic conjunctivitis: clinical appearance and treatment patterns in a population-based study. Curr Opin Allergy Clin Immunol. 2015;15(5):482-488.
- 福島敦樹. 春季カタルのパターン治療のためのプロトコール. あたらしい眼科. 2013;30(4):491-496.
- Ohashi Y, Ebihara N, Fujishima H, et al. A randomized, placebo-controlled clinical trial of tacrolimus ophthalmic suspension 0.1% in severe allergic conjunctivitis. J Ocul Pharmacol Ther. 2010;26(2):165-174.
- Takamura E, Uchio E, Ebihara N, et al. A prospective, observational, all-prescribed-patients study of cyclosporine 0.1% ophthalmic solution in the treatment of vernal keratoconjunctivitis. Nippon Ganka Gakkai Zasshi. 2011;115(6):508-515.
- Sánchez-García S, Habernau Mena A, Quirce S. Biomarkers in inflammatory allergic conjunctivitis: a systematic review for biomarkers. Clin Transl Allergy. 2019;9:27.
- Leonardi A, Bogacka E, Fauquert JL, et al. Ocular allergy: recognizing and diagnosing hypersensitivity disorders of the ocular surface. Allergy. 2012;67(11):1327-1337.
- 内尾英一. 免疫抑制点眼薬の使用法. 日眼会誌. 2015;119(3):136-141.
- Kumar S. Vernal keratoconjunctivitis: a major review. Acta Ophthalmol. 2009;87(2):133-147.
- Wakamatsu TH, Satake Y, Igarashi A, et al. IgE and eosinophil cationic protein (ECP) as markers of severity in the diagnosis of atopic keratoconjunctivitis. Br J Ophthalmol. 2012;96(8):1127-1131.
