卡他性

结膜炎
一目了然的关键点
Section titled “一目了然的关键点”1. 什么是结膜炎
Section titled “1. 什么是结膜炎”结膜炎(conjunctivitis)是结膜炎症的总称。其特征是结膜血管扩张引起的充血和水肿,通常伴有眼部分泌物。患病率因病因、年龄和季节而异。
结膜炎大致分为感染性和非感染性。
- 感染性:病毒、细菌、衣原体是代表性的病原体。成人感染性结膜炎约80%为病毒性,细菌性次之。在儿童中,细菌性和病毒性几乎以相同比例发生。
- 非感染性:过敏性结膜炎最为常见,15~40%的人口患病。也有继发于药物毒性或全身性疾病(如结节病)的病例。
在感染性结膜炎中,流行性角结膜炎(EKC)、咽结膜热(PCF)、急性出血性结膜炎(AHC)的发病情况受厚生劳动省传染病监测体系的监控。
近年来,结膜炎作为COVID-19的眼部症状受到关注。住院患者中结膜炎的总发生率约为5.9%,重症病例中上升至12.7%4)。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”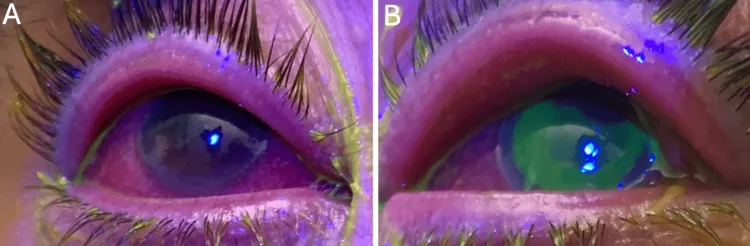
结膜炎常见的自觉症状如下。
- 异物感:由角膜上皮损伤或结膜乳头的机械性刺激引起。感染性和非感染性均可出现。
- 充血:由结膜血管扩张引起。是最常见的体征。
- 眼分泌物(眼屎):性状因病因不同而异(详见后文)。
- 流泪:由反射性泪液分泌增多引起。也与上皮损伤引起的疼痛有关。
- 瘙痒感:是过敏性结膜炎(ACD)最具特征性的症状。由肥大细胞释放的组胺刺激三叉神经C纤维引起。
眼分泌物的性状是推断病因的重要线索。
| 病因 | 眼分泌物性状 |
|---|---|
| 淋球菌 | 大量、黄色、纯脓性 |
| 肺炎链球菌、流感嗜血杆菌 | 多量、黄白色、浆液脓性 |
| 葡萄球菌 | 多量、灰白色 |
| 腺病毒 | 多量、浆液纤维素性 |
| 过敏 | 中量、纤维素性 |
结膜炎的临床表现因病因和病因而异,表现多样。
滤泡性
结膜滤泡:以B细胞为主的淋巴滤泡。好发于下眼睑穹窿部。
浆液性眼分泌物:病毒性感染的特征。
耳前淋巴结肿大:见于腺病毒和衣原体感染。
化脓性
大量脓性眼分泌物:从睑裂溢出的黄色奶油状分泌物。
眼睑肿胀和结膜水肿:反映重度炎症。
角膜穿孔风险:淋菌性结膜炎特有。
其他重要所见:
- 结膜乳头:由多种慢性炎症引起。直径1mm以上称为巨大乳头,常见于春季角结膜炎和接触镜相关巨乳头性结膜炎。在裂隙灯显微镜下,乳头中央有血管分布,而滤泡的血管位于周围,以此鉴别。
- 结膜出血:肠道病毒结膜炎的特征性出血斑。ACD中几乎不见。
- 结膜水肿(chemosis):由血浆成分漏出引起。多见于ACD,但急性感染也可发生。
- 伪膜:严重炎症导致纤维蛋白和中性粒细胞凝固成膜状物。多见于腺病毒结膜炎(尤其是婴幼儿)。婴幼儿上皮结构未成熟,感染的上皮整体脱落,剥离时出血少。成人剥离时则会出血。
- 结膜瘢痕化:炎症后遗症,不可逆。重症病例可导致睑球粘连。
- 多发性角膜上皮下浸润(MSI):EKC发病5~10天后出现在角膜表层的点状浸润。EKC的特征性表现。
- 结膜充血与睫状充血的鉴别:结膜充血在穹窿部最明显,越靠近角膜缘越弱,表层呈鲜红色。睫状充血在角膜缘最明显,深层呈紫红色。
COVID-19相关结膜炎可见滤泡反应、结膜水肿和浆液性分泌物3)。也有伪膜性炎症和结膜下出血的报道3)。
眼分泌物的性状有助于推断病因。大量黄色奶油状脓性分泌物提示淋球菌,黄白色浆液脓性分泌物提示肺炎球菌或流感嗜血杆菌,浆液纤维素性分泌物提示腺病毒。但确诊需要微生物学检查。
3. 原因与风险因素
Section titled “3. 原因与风险因素”细菌性结膜炎的病原菌
Section titled “细菌性结膜炎的病原菌”细菌性结膜炎的病原菌因发病年龄层而异。
| 年龄层 | 主要病原菌 |
|---|---|
| 新生儿 | 淋球菌・衣原体・单纯疱疹病毒 |
| 婴幼儿 | 流感嗜血杆菌・肺炎链球菌・莫拉菌 |
| 成人 | 葡萄球菌属 |
| 老年人 | 葡萄球菌、肺炎球菌、棒状杆菌属 |
近年来,耐甲氧西林金黄色葡萄球菌(MRSA)、耐青霉素肺炎球菌(PRSP)、耐药物流感嗜血杆菌(BLNAR)等耐药菌呈增加趋势,有些病例的结膜炎变得难治。
淋球菌是唯一能感染健康角膜上皮的细菌,炎症波及角膜时可能导致穿孔。在成人中作为性传播感染发病。据报道,日本氟喹诺酮耐药淋球菌的比例超过80%2)。
病毒性结膜炎的病因
Section titled “病毒性结膜炎的病因”引起结膜炎的代表性病毒有以下三类。
- 腺病毒:占引起结膜炎的病毒的65~90%。有流行性角结膜炎(EKC)和咽结膜热(PCF)两种临床类型。EKC的主要病原体为新型D种54型、56型、64型等。PCF的病原体为腺病毒3型、4型、7型等。
- 肠道病毒:急性出血性结膜炎(AHC)的病因。有肠道病毒70型(EV70)和柯萨奇病毒A24变异株(CA24v)。潜伏期短,为半天至1天。约1周内痊愈,不留后遗症。
- 疱疹病毒:单纯疱疹病毒(HSV)占急性结膜炎总数的1.3~4.8%。通常为单眼性。眼睑周围的水疱和有无角膜炎对鉴别诊断很重要。
衣原体结膜炎
Section titled “衣原体结膜炎”沙眼衣原体感染引起的结膜炎可分为沙眼和包涵体性结膜炎。目前在日本常见的是包涵体性结膜炎,是与性传播感染相关的结膜感染之一。对于抗菌药物无效且迁延不愈的滤泡性结膜炎(滤泡可变得巨大),应怀疑衣原体感染。衣原体具有仅在细胞内增殖的特性,因此治疗需要较长时间。
过敏性结膜炎
Section titled “过敏性结膜炎”这是对一过性过敏原(如花粉)或持续性过敏原(如尘螨)产生的I型过敏反应。目前或既往特应性疾病(湿疹、哮喘、荨麻疹、鼻炎)病史是危险因素。春季至夏季更为常见。
新生儿结膜炎
Section titled “新生儿结膜炎”新生儿结膜炎以产道感染(垂直感染)为主。不同病原微生物至发病的潜伏期各有特征。淋球菌在出生后13天、衣原体在310天、莫拉菌在7~10天以后发病。淋球菌性结膜炎有较高的角膜穿孔风险。
在日本,采用氟喹诺酮类滴眼液进行新生儿眼部预防,但已有氟喹诺酮耐药淋球菌导致突破性感染的报道2)。
全身性疾病伴发的结膜炎
Section titled “全身性疾病伴发的结膜炎”结膜充血可作为全身感染症的部分症状出现。见于麻疹、风疹、川崎病、登革热等疾病,这些情况无需滴眼治疗。川崎病中,双侧非化脓性结膜炎(角膜缘回避模式)是诊断标准之一7)。
COVID-19的眼部症状中结膜炎最为常见6)。SARS-CoV-2的ACE-2受体在角膜和结膜中表达,眼表面可能成为感染靶标3)。也有报道结膜炎作为COVID-19的唯一症状出现3)。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”结膜炎的诊断基于临床表现和微生物学检查。
微生物学检查
Section titled “微生物学检查”检测病原微生物的微生物学检查是诊断的关键8)。
- 涂片镜检:对眼部分泌物或结膜刮取物的涂片进行显微镜检查。
- Giemsa染色:多用途筛查染色。使用简易快速染色液Diff-Quick®可在15秒内获得与传统方法几乎等效的染色结果8)。所有微生物均染成蓝色。
- Gram染色:鉴别细菌的阳性与阴性。使用简易试剂盒Faber G®可在3分钟内完成染色8)。
- 细菌性结膜炎以中性粒细胞为主,病毒性则以淋巴细胞(单核细胞)为主的浸润。
- 分离培养检查:可鉴定病原菌并进行药物敏感性试验。采样时使用运输培养基拭子,并迅速送检培养。建议冷藏保存。但细菌性结膜炎中病原菌检出率仅约半数。推荐培养的病例包括新生儿、复发例、治疗抵抗例及疑似淋菌感染例。
快速诊断试剂盒
Section titled “快速诊断试剂盒”- 腺病毒抗原检测试剂盒:采用免疫层析法(Adenocheck®、Cypria® Adeno Eye)进行快速诊断。灵敏度约为80%,需注意假阴性。也可使用以泪液为标本的低侵入性试剂盒。
- Allerwatch®泪液IgE:采用免疫层析法测定泪液总IgE值。特异性几乎为100%。灵敏度因严重程度而异,过敏性结膜炎约为60%,春季卡他性结膜炎约为90%。
- 嗜酸粒细胞染色(Eosinostain®等):结膜分泌物中检出嗜酸粒细胞即可诊断为ACD。
衣原体及疱疹病毒的检查
Section titled “衣原体及疱疹病毒的检查”衣原体可通过结膜刮片的荧光抗体法或PCR进行诊断。若其他科室已确诊衣原体感染,则无需在眼科再次检查。单纯疱疹病毒采用荧光抗体法或PCR有效,但因泪液中存在无症状排出,即使阳性也可能不代表病原性。
感染性结膜炎的鉴别可参考以下临床所见。
| 病因 | 结膜所见 | 潜伏期 | 耳前淋巴结 |
|---|---|---|---|
| 腺病毒(EKC) | 急性滤泡性(重症) | 约7天 | 有 |
| 腺病毒(PCF) | 急性滤泡性(轻症) | 约7天 | 有 |
| 肠道病毒(AHC) | 急性出血性 | 半天到1天 | 有 |
| 细菌性 | 卡他性 | 不定 | 无 |
| 衣原体 | 亚急性滤泡性 | 不定 | 有 |
5. 标准治疗方法
Section titled “5. 标准治疗方法”结膜炎的治疗根据病因选择。基于正确诊断确定治疗方法是基本原则。
细菌性结膜炎的治疗
Section titled “细菌性结膜炎的治疗”初期治疗采用经验性治疗,根据培养结果调整用药。
- 成人:针对葡萄球菌,选择氟喹诺酮类(左氧氟沙星、加替沙星、莫西沙星等)或头孢类抗菌滴眼液。每日滴眼3~4次。
- 儿童:考虑流感嗜血杆菌、肺炎链球菌、莫拉菌,选择头孢类、大环内酯类。氟喹诺酮类中,托氟沙星(Ozeks®・Tosflo®)在儿童中有医保适应证。
- 新生儿:β-内酰胺类头孢甲肟(Bestron®滴眼用0.5%)为首选。每日滴眼5次。
抗菌滴眼液的效果通常在数日内显现,约1周治愈。若病程迁延,需考虑耐药菌、衣原体感染、过敏性结膜炎、泪小管炎的可能。
特殊类型的细菌性结膜炎
Section titled “特殊类型的细菌性结膜炎”- 淋菌性结膜炎:常对氟喹诺酮类耐药。首选头孢类,但对多重耐药淋菌需联合使用头孢曲松(Rocephin®)静脉滴注2)。
- MRSA:使用氧氟沙星滴眼液(Ofsalon®)、万古霉素眼膏,或阿贝卡星®自配滴眼液(1安瓿溶于20mL生理盐水)。
- 莫拉菌性结膜炎:通常大多数抗菌药物有效。氟喹诺酮类滴眼液每日3次。眼睑炎、外眦炎时使用眼膏每日2次。
衣原体结膜炎的治疗
Section titled “衣原体结膜炎的治疗”- 新生儿:氧氟沙星(Tarivid®)眼膏0.3%每日5次,疗程约8周。重症或伴有全身症状时,联合使用阿奇霉素(Zithromac®小儿细粒10%)10mg/kg每日1次,共3日。
- 成人:除长期局部治疗外,加用口服阿奇霉素或多西环素。
病毒性结膜炎的治疗
Section titled “病毒性结膜炎的治疗”- 腺病毒:目前尚无有效的抗病毒药物。使用抗菌眼药水预防继发感染和非甾体抗炎眼药水。对于MSI,类固醇眼药水有效。感染预防措施(洗手、器械消毒、诊室清洁)最为重要。
- 疱疹性结膜炎:使用阿昔洛韦(Zovirax®)眼膏每日5次。对于带状疱疹,需全身使用抗疱疹病毒药物,因此仅有结膜炎时通常无需局部治疗。
- 咽结膜热:参照EKC对症治疗。禁止游泳1个月。
- 急性出血性结膜炎:无特异性治疗方法,仅使用抗菌眼药水预防继发感染。约1周内可痊愈,不留后遗症。
过敏性结膜炎的治疗
Section titled “过敏性结膜炎的治疗”轻症~中等症
抗组胺眼药水:奥洛他定(Patanol®)、依匹斯汀(Alesion®)、左卡巴斯汀(Livostin®)等。
肥大细胞稳定剂:色甘酸钠(Intal®)等。花粉季开始前预防用药有效。
重症
假膜性结膜炎的治疗
Section titled “假膜性结膜炎的治疗”治疗原发病是基本原则。结膜炎症使用类固醇眼药水(地塞米松每日4~6次或氟米龙每日3次)。假膜在引起角膜上皮损伤时,用镊子小心去除。注意尽量减少对结膜的侵袭和出血。木样结膜炎若涉及氨甲环酸,停药后可改善5)。
目前不存在对腺病毒有效的抗病毒药物。有时会使用抗菌眼药水预防继发感染,但不推荐常规使用。多数在1~2周内自然痊愈。出现MSI(多发性角膜上皮下浸润)时,类固醇眼药水有效。
6. 病理生理学及详细发病机制
Section titled “6. 病理生理学及详细发病机制”结膜是覆盖眼睑内面和前部巩膜的薄而富含血管的黏膜,由非角化复层扁平上皮构成。结膜杯细胞分泌的黏蛋白(MUC-5AC)有助于泪膜稳定。黏膜固有层中散在分布着副泪腺(Krause腺、Wolfring腺),分泌泪液。
感染性结膜炎的机制
Section titled “感染性结膜炎的机制”- 细菌性:由结膜常驻菌群的异常增殖或外部直接感染引起。细菌从结膜上皮层有时浸润至固有层。淋球菌通过菌毛和外膜蛋白粘附于黏膜上皮细胞,并能侵入健康角膜上皮。细胞壁外膜的脂寡糖(LOS)作为内毒素发挥作用。
- 病毒性(腺病毒):传染性强,潜伏期估计为5~12天,感染期10~14天。以淋巴细胞为主的炎症为主体,特征为滤泡反应。在EKC中,作为免疫反应,角膜上皮下出现MSI。
- 衣原体:原体侵入宿主细胞内变为网状体并进行增殖。再次变化为原体后释放到细胞外。治疗药物仅对网状体有效,因此消灭原体需要长期治疗。
过敏性结膜炎的机制
Section titled “过敏性结膜炎的机制”以I型过敏反应为基础。过敏原交联表面IgE受体后,结膜的肥大细胞被激活,释放组胺、白三烯、前列腺素和细胞因子。这些物质增强血管通透性,引起水肿及嗜酸粒细胞、中性粒细胞的浸润。
假膜性及木样结膜炎的机制
Section titled “假膜性及木样结膜炎的机制”伪膜是由纤维蛋白、中性粒细胞和渗出物组成的膜样物,在强烈炎症作用下形成于结膜表面。木质性结膜炎是由于PLG基因隐性突变导致的I型纤溶酶原缺乏症5)。纤溶酶原是纤溶系统主要酶——纤溶酶的前体,其缺乏会导致黏膜表面纤维蛋白清除障碍,形成木质样(woody)的厚伪膜5)。
COVID-19相关结膜炎的机制
Section titled “COVID-19相关结膜炎的机制”SARS-CoV-2利用ACE-2受体侵入宿主细胞。ACE-2受体在角膜和结膜中也有表达3),眼表面可能成为感染靶点。也有研究指出病毒可能通过鼻泪管排入气道3)。重症COVID-19中结膜炎的高发生率可能反映了全身性细胞因子风暴波及眼表面4)。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”Reproxalap(RASP抑制剂)
Section titled “Reproxalap(RASP抑制剂)”针对季节性过敏性结膜炎患者的3期INVIGORATE研究(交叉、四重盲法)报告显示,0.25% reproxalap滴眼液相比赋形剂显著改善了瘙痒评分(平均差 -0.50,p < 0.001)和结膜充血评分(平均差 -0.14,p < 0.001)1)。Reproxalap是一种通过化学方式捕获反应性醛类物质(RASP)的新型作用机制药物,可间接调节NF-κB和炎症小体等炎症级联反应的上游环节1)。由于现有抗组胺药的FDA不良事件报告中45%为「治疗失败」,该药有望成为一种新的治疗选择1)。
氟喹诺酮耐药淋球菌的应对
Section titled “氟喹诺酮耐药淋球菌的应对”日本已报告由氟喹诺酮耐药 Neisseria gonorrhoeae(左氧氟沙星MIC 12 μg/mL)引起的新生儿淋菌性结膜炎2)。尽管使用了左氧氟沙星滴眼液进行预防性给药,仍发生感染,经头孢噻肟静脉注射和阿奇霉素口服后治愈2)。全基因组分析确认了gyrA和parC基因的错义突变2)。部分欧洲国家即使停止常规新生儿眼部预防用药,也未见淋菌性结膜炎增加的报告2),提示应加强母体筛查并重新构建预防策略。
COVID-19与结膜炎的关联
Section titled “COVID-19与结膜炎的关联”一项纳入11项研究、2308例患者的荟萃分析显示,重症COVID-19患者的结膜炎发生率显著升高(OR 2.4、95%CI 1.4–4.0、p = 0.002)4)。这一关联在亚洲人(OR 2.5)和欧洲地中海地区(OR 2.3)中均得到确认4)。关于结膜炎是否可作为COVID-19严重程度的标志物,尚需进一步的前瞻性研究。
木样结膜炎的治疗进展
Section titled “木样结膜炎的治疗进展”关于合并先天性脑积水的患者迟发性木样结膜炎,有报道称采用他克莫司0.01%滴眼液、20%自体血清、新鲜冰冻血浆(FFP)滴眼联合外科切除,可使症状暂时消失5)。在部分国家和地区,纤溶酶原滴眼液及静脉注射已可供使用,被认为是未来有前景的治疗选择5)。
8. 参考文献
Section titled “8. 参考文献”- Starr CE, Nichols KK, Lang JR, Brady TC. The Phase 3 INVIGORATE Trial of Reproxalap in Patients with Seasonal Allergic Conjunctivitis. Clin Ophthalmol. 2023;17:3867-3875.
- Mizushima H, Komori M, Yoshida CA, Miyairi I. Neonatal Gonococcal Conjunctivitis Caused by Fluoroquinolone-Resistant Neisseria gonorrhoeae. Emerg Infect Dis. 2025;31(10):2043-2045.
- Ozturker ZK. Conjunctivitis as sole symptom of COVID-19: A case report and review of literature. Eur J Ophthalmol. 2020.
- Loffredo L, Fallarino A, Paraninfi A, et al. Different rates of conjunctivitis in COVID-19 eastern and western hospitalized patients: a meta-analysis. Intern Emerg Med. 2022;17:925-928.
- Ghassemi H, Atighehchian M, Asadi Amoli F. Delayed-onset ligneous conjunctivitis as a rare association with congenital hydrocephalous: a case report and review of the literature. Digit J Ophthalmol. 2022;28.
- Zou H, Zhang K, Chen X, Sha S. Vogt-Koyanagi-Harada disease after SARS-CoV-2 infection: Case report and literature review. Immun Inflamm Dis. 2024;12:e1250.
- Wang W, Wang H, Wang H, Cheng J. Kawasaki disease with shock as the primary manifestation: How to distinguish from toxic shock syndrome? Medicine. 2024;103(31):e39199.
- 感染性角膜炎診療ガイドライン(第3版). 日本眼科学会.
