前部睑缘炎

睑缘炎
1. 什么是睑缘炎
Section titled “1. 什么是睑缘炎”睑缘炎是以眼睑边缘为中心的炎症性疾病。也称为睑缘炎(marginal blepharitis)。它是眼科最常见的疾病之一,发生于所有年龄和种族。通常不直接威胁视力,但重症化可能导致角膜上皮障碍和角膜新生血管。
根据解剖部位大致分为前部睑缘炎和后部睑缘炎。前部睑缘炎是从睫毛根部到皮肤侧的炎症,根据病因分为葡萄球菌性(溃疡性)睑缘炎和脂溢性(鳞屑性)睑缘炎。两者并存的混合型也不少见。后部睑缘炎以睑板腺的炎症为主,通常作为**睑板腺功能障碍(meibomian gland dysfunction, MGD)**处理3)4)。
MGD在日本眼科学会的《睑板腺功能障碍诊疗指南2023》中被定义为“因各种原因导致睑板腺功能弥漫性异常的状态,伴有慢性眼部不适”4)。MGD主要分为分泌减少型和分泌增加型两大类,其中分泌减少型占大多数4)。
此外,与毛囊蠕形螨(Demodex folliculorum)和皮脂蠕形螨(Demodex brevis)寄生相关的蠕形螨性睑缘炎作为一种病型备受关注1)。约30%的慢性睑缘炎患者存在蠕形螨寄生,在难治性病例中,驱虫治疗可能有效。
日本流行病学(MGD诊疗指南2023)
Section titled “日本流行病学(MGD诊疗指南2023)”日本一项针对6至96岁居民的人群研究显示,MGD的患病率随年龄增长而明显上升4)。
- 19岁及以下:0%
- 20岁年龄段:11.8%
- 30岁年龄段:5.6%
- 40岁年龄段:21.6%
- 50岁年龄段:32.8%
- 60岁年龄段:41.9%
- 70岁年龄段:48.4%
- 80岁:63.9%
关于性别差异,有多项报告指出男性及绝经后女性更为多见4)。危险因素除年龄增长外,还包括亚洲人、居住在农村、终端显示设备作业、吸烟、佩戴软性隐形眼镜、长期使用青光眼滴眼液等4)。美国调查显示,37%~47%的眼科门诊患者存在眼睑炎体征,葡萄球菌性眼睑炎多见于相对年轻者(平均42岁)和女性。也有报告指出,蠕形螨相关眼睑炎在60岁以上人群超过80%,70岁以上接近100%1)。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”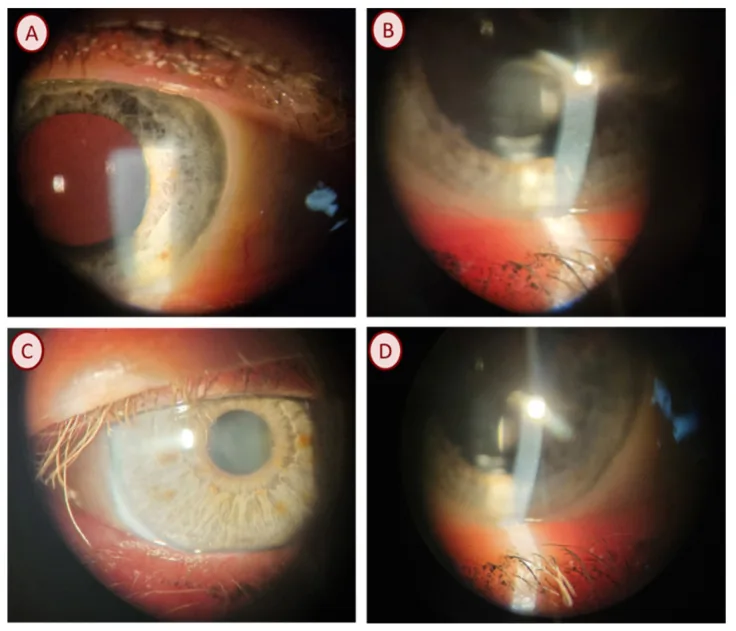
慢性睑缘炎的主要症状为眼睑灼热感、异物感和瘙痒感。有时可伴有充血、溢泪、眼分泌物、视物模糊和畏光。症状易在清晨加重,特征为缓解与加重反复交替。葡萄球菌性睑缘炎常自觉急剧的灼热感和睑缘发红。而脂溢性睑缘炎则以相对温和的慢性灼热感和异物感发病。
MGD的特征性表现为眼部不适感、压迫感、干燥感、疲劳感以及被描述为”黏糊糊的感觉”的异常感4)。仅凭自觉症状进行鉴别诊断较为困难,需要结合裂隙灯显微镜所见进行综合判断4)。
蠕形螨睑缘炎的特征为夜间至清晨的瘙痒感强烈,据报告80%的患者日常生活受到干扰,47%出现夜间驾驶困难,34%主诉隐形眼镜佩戴或化妆受限1)。
使用裂隙灯显微镜、特别是配合弥散器进行观察是基本方法。各病型的所见整理如下。
后部睑缘炎(MGD)
开口部所见:可见睑板腺开口闭塞(plugging, pouting, ridge)、排列紊乱、黏膜皮肤交界处前后移位、睑缘不规则、睑缘毛细血管扩张4)。睑板压迫时可挤出黄色液态或固态内容物。
伴随所见:脂溢性者可在下睑缘形成睑板腺泡沫。重症病例伴有睑板肥厚及睑结膜乳头增生。泪液脂质层减少可引起蒸发过强型干眼,易合并弥漫性表层角膜炎3)4)。
蠕形螨睑缘炎
病理体征:睫毛根部的**圆柱状头皮屑(cylindrical dandruff)**是具有重要病理意义的体征,与 collarettes 一样可作为诊断线索1)2)。伴有结膜充血、睑缘发红、肿胀、毛细血管扩张以及睫毛过度脱落。
特殊类型:Demodex brevis 潜伏在睑板腺内,睫毛拔取检查可能无法检出。有报告称,在清洁睑缘后挤压排出睑板脂并直接在显微镜下观察可检出5)。儿童病例中也有伴有角膜溃疡和新生血管的重症角膜炎的报告,因此在治疗抵抗性角膜炎中,鉴别蠕形螨感染至关重要2)。
岛崎分类(睑板脂挤出评估)
Section titled “岛崎分类(睑板脂挤出评估)”在日本临床实践中,广泛采用岛崎分类,即通过中等力度压迫睑板中央来评估睑板脂性状的方法。
- 0级:轻压即可顺利排出透明睑板脂(正常)
- 1级:轻压可排出混浊的睑板脂
- 2级:中等度以上压迫可排出混浊的睑板脂
- 3级:强力压迫也无法排出睑板脂
2级及以上视为异常,用于MGD诊断标准中「睑板脂分泌低下」的判断4)。
3. 病因与风险因素
Section titled “3. 病因与风险因素”眼睑炎的病因是多因素性的,不同类型的主要病因各不相同。
葡萄球菌性眼睑炎与眼表葡萄球菌增殖相关。46〜51% 的患者金黄色葡萄球菌培养呈阳性,显著高于健康对照者的 8%。细菌外毒素可引起邻近角结膜上皮的点状上皮病变。Moraxella 菌是眦部眼睑炎的重要原因。
脂溢性眼睑炎与脂溢性皮炎合并发生频率很高,有报告称 95% 的患者伴有脂溢性皮炎。酒渣鼻性皮炎在所有类型眼睑炎患者中占 20〜42%,被认为是眼睑炎的重要病因之一。
MGD的发生机制在日本MGD诊疗指南2023中总结如下4)。分泌减少型MGD的主要病理改变是睑板腺导管上皮过度角化和腺泡萎缩,腺泡萎缩不仅继发于阻塞,也可能是由衰老等引起的腺细胞原发性损伤。
MGD的危险因素(指南 BQ-5, BQ-6)4):
- 年龄:多项研究强烈支持
- 性别:男性和绝经后女性更常见
- 眼部因素:亚洲人、视频终端工作、软性隐形眼镜佩戴、长期使用青光眼滴眼液、眼部手术史
- 生活因素:吸烟、居住在农村地区
- 全身疾病:糖尿病、脂质代谢异常、高血压、甲状腺功能亢进症
- 伴眼表炎症的疾病:酒渣鼻、干燥综合征、Stevens-Johnson综合征、移植物抗宿主病(GVHD)
- 激素因素:绝经、雄激素减少
蠕形螨(Demodex folliculorum 和 Demodex brevis)寄生于皮脂腺、毛囊和睑板腺,其排泄物和分泌物会引发毛囊阻塞和炎症1)。IL-1β 和 IL-17 等炎性细胞因子以及 MMP-9 被激活。蠕形螨还作为金黄色葡萄球菌、Acinetobacter baumannii、Streptococcus pneumoniae 等细菌的载体,据报道可能促进眼表重复感染1)。
与干眼的关联也很重要。50% 的葡萄球菌性眼睑炎患者伴有干眼症。在 MGD 中,泪液脂质层不足导致蒸发过强,干眼合并率达 25~40%3)。MGD 和干眼具有相互加重的关系。
4. 诊断和检查方法
Section titled “4. 诊断和检查方法”问诊和基本检查
Section titled “问诊和基本检查”诊断首先基于病史采集和裂隙灯显微镜检查。确认发病是急性还是慢性、双侧还是单侧、有痛性还是无痛性。询问全身性疾病(Sjögren综合征、酒渣鼻、糖尿病、特应性皮炎、甲状腺疾病、鼻窦炎)、过敏史、化妆品和眼药水使用史、隐形眼镜佩戴史以及吸烟史。
视诊和触诊评估眼睑发红、肿胀(弥漫性或局限性)、压痛以及湿疹的有无。对于单侧、有痛性、局限性肿胀,需鉴别麦粒肿和急性霰粒肿;对于双侧、弥漫性、有痛性肿胀,需鉴别眼睑脓肿和眼眶蜂窝织炎。
裂隙灯显微镜所见
Section titled “裂隙灯显微镜所见”使用裂隙灯显微镜,特别是配合弥散镜,观察以下内容4):
- 睑缘:睫毛套袖状鳞屑、鳞屑、毛细血管扩张、新生血管、瘢痕、黏膜皮肤移行部位置
- 睫毛:脱落、乱生、束状排列(脂溢性睫毛)、圆柱状头皮屑
- 睑板腺开口:阻塞(plugging、pouting、ridge)、排列紊乱
- 睑板脂挤压:用手指或专用镊子压迫睑板中央,用岛崎分类评估
- 眼表面:结膜充血、角结膜上皮损伤(荧光素染色)
日本MGD诊断标准(MGD工作组2010/指南2023)
Section titled “日本MGD诊断标准(MGD工作组2010/指南2023)”分泌减少型MGD的诊断基于以下3项均为阳性4)。
| 诊断项目 | 阳性判定 |
|---|---|
| 自觉症状 | 有眼不适感、异物感、压迫感等症状 |
| 开口部周围所见 | 血管扩张、黏膜皮肤移行部移位、眼睑缘不规则中的任意1项以上 |
| 开口部闭塞所见 | 栓子等闭塞所见 且 岛崎分类 grade 2 以上 |
2010年MGD工作组提出的这一诊断标准被广泛使用,但国际上尚无统一的诊断标准4)。
辅助检查(MGD诊疗指南2023 CQ)
Section titled “辅助检查(MGD诊疗指南2023 CQ)”- 睑板腺红外成像:可非侵入性观察睑板腺形态。可量化缺失面积、腺体缩短和扩张,推荐用于MGD诊断4)
- 泪膜破裂时间(TBUT):MGD常缩短,但非特异性检查4)
- 裂隙灯下观察睑板脂:建议实施4)
- 荧光素染色:评估角结膜上皮损伤最具通用性4)
- 泪液渗透压测定:有助于诊断并发干眼,据报道316 mOsm/L以上时敏感性59%、特异性94%
蠕形螨的检测
Section titled “蠕形螨的检测”拔取睫毛的显微镜检查是基本方法。Lee 等人通过拔取上下眼睑各 4 根睫毛,在光学显微镜下鉴定 D. folliculorum 的成虫和幼虫2)。然而,D. brevis 隐藏于睑板腺内,因此睫毛拔取可能检测不到。Zhang 和 Liang 在眼睑缘抗菌处理后挤压睑板分泌物(meibum)进行显微镜观察,检测到 15 只 D. brevis,并报告了有睑板分泌物内仅存在 D. brevis 而不伴外表所见表现的睑缘炎病例5)。
其他检查与鉴别诊断
Section titled “其他检查与鉴别诊断”对于重度复发性前部眼睑炎或治疗抵抗病例,应进行眼睑缘细菌培养(葡萄球菌、莫拉菌属)。对于显著的左右不对称、单侧难治性霰粒肿样病变,中老年需考虑眼睑活检以排除皮脂腺癌。皮脂腺癌已知可伪装为难治性眼睑炎或霰粒肿样病变。
鉴别诊断包括霰粒肿、眼睑脓肿、眼眶蜂窝织炎、疱疹性眼睑炎(VZV、HSV)、过敏性眼睑炎、眼睑皮炎(接触性、药物性、特应性)、湿疹性眼睑炎以及皮脂腺癌。
5. 标准治疗方法
Section titled “5. 标准治疗方法”睑缘炎是一种慢性疾病,治疗的基础是控制症状和炎症体征。目前没有强有力的证据表明可以完全治愈,需要长期管理。治疗方案以日本MGD诊疗指南20234)为主要依据。
一线选择:眼睑护理(热敷、眼睑清洁、睑板脂按压)
Section titled “一线选择:眼睑护理(热敷、眼睑清洁、睑板脂按压)”热敷在MGD诊疗指南2023中被描述为「强烈推荐实施」4)。通过将眼睑温度升高至睑板脂的熔点,溶解睑板脂并促进分泌,同时还可改善眼睑血流。指导患者使用市售的热敷眼罩,在家中每天2次、每次5分钟以上进行。热毛巾虽然简便但温度调节困难,湿润状态下会因汽化热而冷却,因此为次选方案。
**眼睑清洁(lid hygiene)**在同一指南中被描述为「弱推荐实施」4)。使用水浸湿的棉球或市售的清洁剂(如婴儿洗发水稀释液),用棉签正确清洁睫毛根部。预期可改善自觉症状、睑板腺开口部所见、睑板脂分级、TBUT、角结膜上皮损伤。需注意不同种类的清洁剂可能会引起不良事件4)。
睑板脂压出对阻塞性MGD有效,弱推荐使用4)。门诊使用有田式睑板腺压出镊(Inami公司)等专用器具,间隔约10天至1个月实施。栓子较大时,在点眼麻醉后用镊子或注射针去除。
抗菌·抗炎治疗
局部抗菌药:对于葡萄球菌性睑缘炎,睡前在睑缘涂抹杆菌肽或红霉素眼膏,使用2〜8周。阿奇霉素水合物滴眼液可改善MGD的主观症状、开口部所见和睑板脂分级,指南弱推荐使用4)。
口服抗菌药:四环素类和大环内酯类药物用于抗炎和脂质调节作用。采用四环素从1,000 mg/日逐渐减至250 mg/日、盐酸米诺环素从200 mg/日逐渐减至100 mg/日、多西环素100 mg口服每日2次,3〜4个月内逐渐减量、联合使用克拉霉素等大环内酯类。这些药物被认为通过抑制细菌产生的酶活性和抑制生物膜形成而发挥效果。
局部类固醇:炎症严重时短期联合使用0.1%氟米龙。MGD指南建议与眼睑清洁和热敷联用以改善自觉症状、TBUT、眼睑缘所见和睑板腺分泌物质量,弱推荐4)。在日本,仅在合并眼睑炎时适用医保4)。
人工泪液·辅助滴眼液:辅助用于合并蒸发过强型或泪液分泌减少型干眼的病例。每日使用4次以上时选择无防腐剂制剂。单独MGD使用地夸磷索钠滴眼液不在医保范围内,指南弱推荐不对单独MGD使用4)。
蠕形螨睑缘炎的治疗
茶树油(TTO):主要成分萜品烯-4-醇(T4O)通过抑制乙酰胆碱酯酶发挥杀螨作用1)。使用浓度为5–50%。有报告称每周1次50%TTO眼睑清洁和每日0.4%PHMB清洁持续6周后所有病例均改善2)。
口服及外用抗寄生虫药:伊维菌素(作用于寄生虫GABA受体诱导麻痹)与甲硝唑(通过硝基自由基损伤DNA)联合使用被认为最有效1)。口服和外用均可考虑。
机械清洁:联合睑缘清洁与热敷,坚持每日眼睑护理。
辅助治疗:合并干眼症时添加人工泪液。
以下比较针对蠕形螨的药物作用机制。
| 治疗法 | 作用机制 | 备注 |
|---|---|---|
| TTO | AChE抑制1) | 广泛可得 |
| 伊维菌素 | GABA 受体抑制1) | 与甲硝唑联用增强疗效1) |
| 甲硝唑 | DNA 损伤1) | 口服/外用 |
特殊类型的治疗
Section titled “特殊类型的治疗”- 眦部眼睑炎:使用对葡萄球菌敏感性高的抗菌滴眼液或眼膏。
- 疱疹性眼睑炎(HSV):阿昔洛韦软膏(舒维疗软膏)从每日5次开始,随改善情况减少次数。联合使用抗菌滴眼液每日3次以预防混合感染。原则上不联合使用类固醇。
- 疱疹性眼睑炎(VZV·眼部带状疱疹):从发病早期开始全身给予阿昔洛韦或盐酸伐昔洛韦可促进病变早期改善。
其他辅助治疗
Section titled “其他辅助治疗”MGD指南弱推荐不使用环孢素A滴眼液,因其效果有限4)。IPL(强脉冲光)治疗在证据上被强烈推荐,但在日本尚未作为医疗器械获批且无医保覆盖,因此现阶段仅为弱推荐4)。
基本方法包括热敷、眼睑按摩和眼睑清洁三个步骤3)4)。首先,用干净的毛巾或热敷眼罩敷在眼睑上,每天2次,每次5分钟以上。然后,轻轻垂直按摩上下眼睑,促进睑板腺分泌。最后,用水浸湿的棉球或专用清洁剂仔细擦拭睫毛根部。急性期缓解后,每日坚持护理也很重要。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”葡萄球菌性睑缘炎的发病涉及细菌毒素对眼表面的直接刺激以及针对金黄色葡萄球菌的细胞免疫增强。细菌外毒素可引起邻近角结膜上皮的点状上皮损伤。细菌脂肪酶作用于睑板腺脂质产生游离脂肪酸,引发炎症并导致进一步的腺管阻塞,形成恶性循环。
MGD的本质是睑板腺终末导管的阻塞3)。日本MGD诊疗指南明确指出:「分泌减少型睑板腺功能障碍的主要病理状态是导管上皮过度角化和腺泡萎缩」4)。腺泡萎缩不仅可继发于睑板腺阻塞,也可能由年龄等因素导致的腺细胞原发性损伤引起4)。导管上皮过度角化和睑脂黏稠度升高导致阻塞进行性加重,进而引起腺体脱落、萎缩和分泌减少。
泪膜脂质层由外侧的非极性层和内侧的极性层构成,有助于防止蒸发和维持光学表面的平滑3)。睑板腺脂质供应减少会导致蒸发过强型干眼和泪液渗透压升高,进而诱发眼表炎症和上皮损伤3)。脂质层组成的变化(神经酰胺和胆固醇增加)已被证明会导致睑板腺脂质膜的破坏和不稳定3)。
在蠕形螨寄生中,螨虫的排泄物和分泌物会引起毛囊的物理性阻塞,并激活宿主的过敏反应1)。炎症性细胞因子如IL-1β、IL-17以及MMP-9被诱导产生。此外,有报道指出D. folliculorum可作为金黄色葡萄球菌、Acinetobacter baumannii、Streptococcus pneumoniae等细菌的载体,可能促进眼表的重复感染1)。D. brevis被报道潜伏在睑板腺内并呈现类似MGD的表现,部分病例仅凭外部表现难以诊断5)。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”针对蠕形螨相关睑缘炎的新疗法开发近年来正在积极推进中。
Lotilaner滴眼液0.25%(XDEMVY) 是一种异噁唑啉化合物,通过抑制Demodex的GABA受体和谷氨酸激活氯离子通道来诱导痉挛性麻痹1)。在III期临床试验(Saturn-2试验,412例)中,每日两次滴眼,持续6周,睫毛袖套状物消失率达到56%,螨虫清除率为51.8%,红斑消失率为31.1%1)。90.7%的参与者报告了良好的耐受性,副作用轻微,包括灼热感和轻度视力下降1)。该药已获得美国FDA批准,欧洲预计将于2027年左右获批,日本尚未确定批准时间1)。
IPL(强脉冲光)疗法 通过照射宽带光,利用光热分解作用使蠕形螨失活并杀灭1)。体外实验证实螨虫温度升至约49°C时即可被杀死。据报道,经过4次IPL治疗后,OSDI、泪膜脂质层、TBUT、睑板腺分泌均有显著改善,螨虫数量减少1)。有报告指出,与单独使用TTO相比,IPL在1个月后的改善更快且更显著。在日本MGD诊疗指南中,IPL在循证医学上被强烈推荐,但由于在日本尚未获批为医疗器械且不纳入医保,因此仅为弱推荐4)。
BlephEx 是一种使用旋转式微海绵机械去除眼睑缘碎屑、蠕形螨和袖套状鳞屑的方法1)。还预期具有破坏细菌生物膜的效果。据报道,与TTO联合使用时,OSDI参数和螨虫数量均有显著改善,但其长期有效性仍需进一步研究验证1)。
天然精油的探索也在进行中,据报道,鼠尾草油可在7分钟内杀死螨虫,薄荷油可在11分钟内杀死螨虫1)。蓖麻油、佛手柑油和黑种草籽油的协同效应也在研究中。
Czepińska-Myszura等人指出,「在新型治疗方法中,只有Lotilaner滴眼液在大规模临床试验中被证实具有高效性,而IPL和眼睑清洁疗法仅在有限的患者群体中得到验证」1)。
Lee等人分析了9例蠕形螨睑缘炎,报告所有病例均为 D. folliculorum,并且儿童病例(5岁、13岁和14岁)也出现了伴有角膜溃疡和新生血管的严重角膜炎2)。儿童的蠕形螨感染容易被忽视,在复发性角膜炎中,蠕形螨的鉴别诊断非常重要2)。此外,Zhang和Liang报告了一例46岁男性患者,其无外表所见,仅在睑板腺分泌物中发现15只 Demodex brevis,表明在难治性病例中,睑缘清洁后的睑板腺分泌物直接观察有助于诊断5)。
截至2025年,洛替拉纳滴眼液0.25%(XDEMVY)已获得美国FDA批准,但在日本和欧洲尚未获批1)。欧洲预计将在2027年左右获批。日本的批准时间尚未确定,目前以TTO和抗寄生虫药物治疗为主。
8. 参考文献
Section titled “8. 参考文献”- Czepińska-Myszura A, Kozioł MM, Rymgayłło-Jankowska B. Pharmacotherapy of Demodex-Associated Blepharitis: Current Trends and Future Perspectives. Pharmacy. 2025;13(5):148.
- Lee YI, Seo M, Cho KJ. Demodex Blepharitis: An Analysis of Nine Patients. Korean J Parasitol. 2022;60(6):429-432.
- Sabeti S, Kheirkhah A, Yin J, Dana R. Management of Meibomian Gland Dysfunction: a Review. Surv Ophthalmol. 2020;65(2):205-217.
- マイボーム腺機能不全診療ガイドライン作成委員会. マイボーム腺機能不全診療ガイドライン. 日眼会誌. 2023;127(2):109-228.
- Zhang N, Liang L. Demodex in Meibum. Ophthalmology. 2024.
