诊断标准

Stevens-Johnson综合征
一目了然的要点
Section titled “一目了然的要点”1. 什么是Stevens-Johnson综合征?
Section titled “1. 什么是Stevens-Johnson综合征?”Stevens-Johnson综合征(SJS)是一种急性皮肤黏膜疾病,表现为突发高热、结膜炎、皮疹,随后全身皮肤和黏膜出现糜烂和水疱。中毒性表皮坏死松解症(TEN)是包括SJS重症型在内的疾病类型。多数病例在发病前有用药史,也是一种严重的药物不良反应。该病以1922年美国儿科医生Albert Mason Stevens和Frank Chambliss Johnson报告的两例伴有发热、结膜炎、皮肤和口腔黏膜糜烂的儿童病例命名。此后,1956年Alan Lyell报告了中毒性表皮坏死松解症(TEN),两者被归类为同一谱系的重症药疹。
| 分类 | 皮肤病变面积 |
|---|---|
| SJS | 体表面积小于10% |
| SJS/TEN重叠 | 体表面积的10%~30% |
| TEN | 体表面积超过30% |
SJS和TEN的眼部表现相似,仅凭眼部表现难以区分两者。因此,在眼科中,常将SJS和TEN统称为广义的SJS。发病机制和眼部后遗症也作为几乎相同的疾病谱来处理。
该病发病率极低,每年每百万人中仅有数例,但可发生于包括儿童在内的所有年龄段,无性别差异。美国报告的年发病率为每百万人12.35例8)。死亡率很高:SJS为4.8%,TEN为14.8%3),有报告称TEN的死亡率最高可达30%1)。
SJS/TEN眼部并发症的发生率约为70%,成人中为53%~88%8)。同时出现假膜和角结膜上皮缺损的严重眼部并发症约占所有SJS/TEN病例的40%10)。由于死亡率高,急性期以全身管理为主,但最常见的后遗症是眼部损害,包括因严重角膜混浊导致的视力障碍和干眼症,可持续终生11)。进展为角膜上皮干细胞衰竭的病例,从角膜缘向心性供应的角膜上皮细胞不足,伴有结膜来源血管的组织侵入角膜表面。这种不可逆的变化是视力障碍的核心,因此发病后数天内急性期治疗的质量是决定预后的最重要因素13)。
SJS/TEN常在儿科、皮肤科或急诊科被首先识别,但在眼部症状先于皮肤病变的病例中,患者可能首先就诊于眼科。在伴有全身发热和皮疹的发病形式中,常需与急性双眼结膜炎鉴别。因此,即使是普通眼科医生,也需要通过多学科协作促进早期诊断和综合治疗。初诊时应评估全身症状和皮肤黏膜表现,若出现双眼结膜炎伴发热,应积极与皮肤科和急诊科协作。疑似病例应尽早住院治疗,眼科在急性期积极干预直接有助于改善视力预后。
SJS和TEN属于同一疾病谱,根据皮肤受累面积分类。体表面积小于10%为SJS,10%~30%为SJS/TEN重叠,超过30%为TEN。眼部表现相似,难以区分,因此眼科统称为广义的SJS。死亡率为SJS 4.8%,TEN 14.8%3)。严重眼部并发症的发生率约占所有SJS/TEN病例的40%10)。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”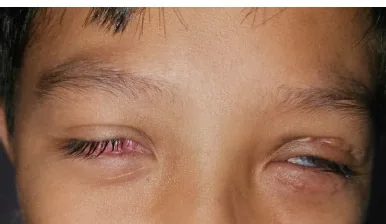
- 双眼充血、异物感、眼痛:眼部症状出现的同时或数日内,出现以躯干为主的皮疹。
- 视力下降:由急性期的角结膜上皮缺损和慢性期的角膜混浊引起。
- 干燥感、畏光:慢性期干眼症导致持续存在。
- 倦怠感、咽痛:许多病例在发病前出现类似感冒的前驱症状。
临床所见(医生检查确认的所见)
Section titled “临床所见(医生检查确认的所见)”急性期(发病时)
- 双眼结膜充血:与黏膜疹和皮疹几乎同时出现的重度充血。
- 假膜形成:急性期的特征性所见,呈翼状附着于结膜表面。
- 角结膜上皮缺损:可能范围广泛。持续性上皮缺损可并发角膜感染、角膜融解或穿孔。
- 眼睑红肿:重症时眼睑无法睁开。也可出现睫毛脱落。
- 角膜假膜:住院数日后可能出现4)。
- 急性期眼部所见直接与严重程度分级相关:Sotozono 等人的急性期眼部严重程度分级根据假膜、上皮缺损、角膜上皮缺损的有无分为0~3级11)。
如果在皮疹出现前就诊眼科,可能被误诊为病毒性结膜炎。必须确认有无发热和全身皮疹。
慢性期(瘢痕期)
- 重度干眼症:几乎所有病例都因泪腺导管阻塞而合并泪液分泌不足。也常合并睑板腺功能障碍。
- 倒睫:持续多年,使眼表状况恶化。通常需要每月拔除3-4次,与毛周期同步。
- 睑球粘连:穹窿消失,睑结膜与球结膜粘连。
- 结膜侵入角膜:角膜上皮干细胞消失后,结膜组织覆盖角膜表面,导致视力障碍。
- 上皮角化:重症病例中,角结膜表面像皮肤一样角化。
- Vogt栅栏消失:这是角膜缘角膜上皮干细胞消失的临床体征。
眼部并发症的严重程度不一定与皮肤病变范围相关。有报告称,未使用眼药水的眼睛比对侧眼损伤更严重,表明SJS/TEN本质上是一种全身性免疫疾病1)。
预测眼部并发症的发生,急性期是否有假膜形成、角膜上皮缺损和结膜充血是重要因素。日本一项多中心研究报告称,急性期出现假膜形成或角膜上皮缺损的病例,慢性期严重眼后遗症的发生率很高11)。因此,在急性期应每天或每隔几天详细记录眼部表现,并随时间推移追踪分级。
3. 病因与风险因素
Section titled “3. 病因与风险因素”SJS/TEN通常由药物给药诱发。在儿童中,支原体感染常为前驱因素。发病前常出现乏力、咽痛等感冒样症状,认为某种病毒感染是诱因,但详细机制不明。从开始用药到发病的潜伏期通常较短,多为4天至1个月,最常在开始使用可疑药物后2-3周内发病。但也有长期用药后发病的病例,因此仅凭用药时间不能否定因果关系。
| 病因分类 | 代表性药物/因素 |
|---|---|
| 抗菌药 | 磺胺类药物(如复方新诺明)最常见 |
| 抗癫痫药物 | 卡马西平、苯妥英、拉莫三嗪 |
| 镇痛解热药 | 非甾体抗炎药(NSAIDs) |
| 降尿酸药物 | 别嘌醇 |
| 抗肿瘤药物 | 免疫检查点抑制剂(ICIs) |
| 感染 | 支原体感染(尤其儿童)、单纯疱疹病毒 |
特别是抗癫痫药物引起的病例报道较多。有报道称卡马西平和苯妥英联合使用35天后发病的病例3),以及换用拉莫三嗪后发生TEN的病例7)。NSAIDs的发病机制被认为与抑制前列腺素产生有关。
近年来,免疫检查点抑制剂(ICIs)引起的SJS/TEN也有报道。替雷利珠单抗的上市后调查中,在3795例不良事件中发现了3例TEN5)。ICI诱导的SJS/TEN中位发病时间为32天,一项对305例患者的随访报告显示69例死亡4)。
滴眼液也可能诱发SJS/TEN。有报道称,使用磺胺类碳酸酐酶抑制剂布林佐胺滴眼液后,发生了全身性SJS/TEN重叠(体表面积99%)的病例1)。通过结膜和鼻黏膜的全身吸收,可能在遗传易感个体中引发全身免疫反应。
COVID-19疫苗接种后也有SJS/TEN的报道2)。疫苗诱导的SJS/TEN倾向于在1-8天内发病,比药物诱导的(2-3周)更短2)。
HLA基因型与SJS/TEN易感性密切相关。建议在别嘌醇给药前检测HLA-B58:01,在卡马西平给药前检测HLA-B15:02 8)。此外,据报道,在伴有严重眼部并发症的日本SJS/TEN患者中,HLA-A*02:06显示出强相关性 12)。这些HLA多态性的分析在确定致病药物和用药前筛查中起着重要作用。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”眼部并发症分级
0级:无眼部病变。推荐预防性使用人工泪液 11)。
1级:仅有结膜充血,无角膜病变。推荐抗生素滴眼液每日3次,类固醇滴眼液每日6次 8)。
2级:角膜病变,无假膜。在上述治疗基础上,推荐羊膜移植(Prokera或amniotic membrane transplant; AMT)8)。
3级:角膜病变伴假膜。推荐包括AMT在内的积极治疗8)。
SCORTEN全身严重程度评估:SCORTEN(中毒性表皮坏死评分)是广泛用于SJS/TEN预后预测的评分系统,评估7个项目:年龄≥40岁、合并恶性肿瘤、心率≥120次/分、表皮剥脱面积≥10%、血清尿素氮升高、血糖升高、血清碳酸氢根降低。评分越高,死亡率越高,是客观判断是否需要重症监护和全身管理的指标。眼科医生通过与皮肤科、急诊科协作并共享SCORTEN,有助于制定治疗策略。
辅助检查与鉴别
Section titled “辅助检查与鉴别”- 裂隙灯显微镜检查:评估假膜、结膜充血、角结膜上皮缺损、睑球粘连。
- 荧光素染色:显示角结膜上皮缺损的范围。
- 结膜囊培养:慢性期感染加重时,检查是否携带MRSA或MRSE。
- 印迹细胞学:确认结膜上皮向角膜侵入以及杯细胞的存在。
- 眼前节OCT及活体共聚焦显微镜:有助于评估POV和角膜上皮,以及诊断角膜缘干细胞缺乏症8)。
- HLA基因型检测:用于确定致病药物和用药前筛查8)12)。
- 病毒性结膜炎:急性期仅表现为眼部症状时可能误诊。注意全身发热和皮疹。
- 眼瘢痕性类天疱疮:慢性期表现为瘢痕性角结膜病,类似。为自身免疫性疾病,病程缓慢;印迹细胞学和免疫组织化学有助于鉴别。
- 葡萄球菌性烫伤样皮肤综合征(SSSS):需根据TEN诊断标准排除。SSSS主要发生于儿童,表皮剥脱发生在颗粒层水平(浅层),与TEN(真皮坏死)在组织病理学上不同。
- 化学伤或热烧伤后角膜缘干细胞缺乏症:通过病史鉴别8)。
- 急性出血性结膜炎:作为病毒性双眼结膜炎,与急性期SJS相似,但可通过不伴有全身发热和皮疹进行鉴别。
- 眼睑炎/睑板腺炎:作为慢性期睑缘变化的鉴别对象,但根据有无瘢痕形成进行区分。
5. 标准治疗方法
Section titled “5. 标准治疗方法”急性期治疗
全身治疗:发病早期即进行类固醇冲击疗法(甲泼尼龙500~1000 mg/日×3天×1~2个疗程)10)。重症病例可加用IVIG疗法(0.4~1.0 g/kg/日×3~5天)或血浆置换疗法。在全身状况允许的情况下,早期大剂量给药对于抑制眼表炎症进展至关重要。可加用环孢素(3~5 mg/kg/日)、依那西普、英夫利西单抗等TNF-α抑制剂,尤其在类固醇抵抗或迁延病例中报道有效。全身管理需要在烧伤病房或重症监护室进行体温管理、液体管理、营养管理和感染预防,由多学科团队进行综合治疗。
眼部局部治疗:频繁滴用倍他米松滴眼液或眼膏,每日6~10次,以防止睑球粘连形成。同时使用抗生素滴眼液预防感染。能否保存角膜上皮干细胞是决定慢性期视力预后的最大因素11)13)。
早期羊膜移植(AMT):推荐用于2级及以上病例8)。有报道称,10例极重症病例中有9例达到了BCVA 20/208)。由于35%的病例会发生感染性角膜炎,需要额外的抗生素预防8)。发病后24~48小时内的眼科评估和早期AMT干预可改善视力预后13)。羊膜移植可通过缝合完全覆盖球结膜、穹窿部和睑结膜,或使用无需缝合的环形装置如Prokera。Prokera可在治疗室放置,避免了急性期的侵入性手术,因此在临床中的应用正在扩大。羊膜具有抗炎、抗血管生成和抗瘢痕形成的特性,通过持续释放生长因子和抗炎细胞因子促进眼表创面愈合。
慢性期治疗
干眼管理:频繁滴用不含防腐剂的人工泪液、透明质酸滴眼液、瑞巴派特滴眼液(促进黏蛋白分泌和抗炎作用)、地夸磷索滴眼液(促进水分和黏蛋白分泌),并联合使用泪点栓。SJS慢性期的干眼不仅仅是泪液量减少,而是伴有睑板腺功能障碍导致的脂质层异常、杯状细胞减少导致的黏蛋白缺乏、结膜上皮角化的复合型重症干眼。因此,单用一种药物难以管理,需要补充泪膜各成分的多药联合策略。防腐剂会加重角结膜上皮损伤,因此所有滴眼液应尽可能选择不含防腐剂的制剂。
倒睫管理:每月按毛周期定期拔除3~4次。对于细而脱色的睫毛,使用钛镊或缝合镊有效。复发性病例可加做睫毛毛根切除的眼整形手术或睫毛电解术(毛根破坏手术)。SJS后的倒睫与普通老年性内翻不同,是由于睑缘后部轻度内翻(marginal entropion)波及毛根部瘢痕组织,导致睫毛生长方向改变所致。因此,不仅需要单纯拔除,还需要对原发病即睑缘瘢痕化进行积极治疗。长期倒睫若不处理,可导致假性翼状胬肉、角膜散光和角膜混浊,因此早期干预是理想的。
炎症管理:使用低浓度类固醇滴眼液抑制慢性炎症,减缓瘢痕性变化进展。注意MRSA/MRSE的携带,根据培养结果选择适当的抗菌药物。伴有严重眼后遗症的SJS/TEN患者结膜囊内MRSA/MRSE携带率高,这可能导致眼表面炎症复发和感染性角膜炎,因此需定期进行结膜囊培养,必要时考虑使用万古霉素或利奈唑胺等对MRSA有效的抗菌药物。慢性期使用类固醇滴眼液时需注意眼压升高和继发性青光眼,定期测量眼压。
巩膜镜与视力康复:角膜缘支撑型硬性接触镜和巩膜镜对重症干眼和不规则眼表面的视功能改善有效。
用于视力改善的巩膜镜:对于角膜表面不规则的重症干眼患者,巩膜镜或BostonSight PROSE(眼表生态系统假体置换)等角膜缘支撑型大直径接触镜是有用的。通过在镜片与角膜之间保持缓冲液,可以光学矫正角膜的微小不规则,并维持持续的湿润环境,抑制上皮损伤的进展。许多双眼SJS患者不仅获得屈光矫正,还能减轻疼痛、畏光和异物感。
对于结膜组织侵入角膜导致的严重视力障碍,进行角膜缘干细胞移植(LSCT)或培养黏膜上皮移植。角膜缘干细胞移植根据手术方式不同有三种类型,自体角膜缘干细胞移植的系统评价报告:结膜角膜缘自体移植(CLAu)的解剖/功能成功率为81%/74.4%,单纯角膜缘上皮移植(SLET)为78%/68.6%,培养角膜缘上皮移植(CLET)为61.4%/53%9)。CLAu和SLET的效果显著优于CLET(p=0.0048)9)。
培养黏膜上皮移植包括使用自体口腔黏膜上皮片的方法,在日本,自体口腔黏膜上皮移植被认定为先进医疗13)。对于双眼SJS等无法获得自体角膜缘组织的病例,采集患者自身少量口腔黏膜,在培养基中展开为上皮片,然后以羊膜或纤维蛋白胶为载体移植到角膜表面。制备培养上皮片时,使用添加视黄醇和EGF的培养基以排除异种来源物质。有时也联合使用丝裂霉素C抑制成纤维细胞活性。移植后,继续联合使用类固醇滴眼液和免疫抑制剂,以防止眼表面炎症复发。
穿透性角膜移植术(PKP)可用于角膜瘢痕病例,但在角膜缘干细胞缺失的状态下,容易发生上皮化不全,单独PKP的预后有限8)。因此,对于重度LSCD,常选择两步手术:首先通过角膜缘干细胞移植或培养黏膜上皮移植稳定眼表面,然后针对角膜混浊分期进行板层角膜移植或穿透性角膜移植13)。
波士顿人工角膜(Boston keratoprosthesis; KPro)用于其他治疗难以恢复视力的重症病例8)。特别是在双眼SJS且无自体移植片来源的病例中,使用钛制光学部和组织部的II型(mucous membrane-covered)已被报道为克服慢性结膜化和眼睑粘连的手段。然而,青光眼、视网膜脱离、感染、装置暴露等长期并发症并不少见,需要终身严格管理。在布林佐胺诱发的SJS/TEN病例中,对睑球粘连和角膜瘢痕施行PKP,视力改善至0.051)。
由于白内障手术等眼科手术可能诱发眼表炎症复发,即使是轻症病例,术后也需要口服类固醇进行充分抗炎。术前应通过结膜囊培养确认MRSA或MRSE等携带情况,必要时预防性使用抗菌滴眼液。白内障手术建议缩小切口,用粘弹剂保护眼表,并尽可能缩短手术时间。
急性期眼表的充分抗炎最为重要。除了全身性类固醇脉冲疗法(甲泼尼龙500-1000 mg/日×3天)10)外,还需要频繁使用局部倍他米松滴眼液。如果能在急性期保存角膜上皮干细胞,角膜透明度很可能得以维持。对于2级及以上病例,早期加用羊膜移植即使在重症病例中也可望获得良好的视力预后8)。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”SJS/TEN的病理生理学解释为:在遗传易感性背景下,对药物代谢物产生过度的细胞免疫反应,随后引起广泛的上皮细胞凋亡以及继发性炎症和组织损伤。虽然表皮和粘膜上皮细胞是全身共同的靶点,但在眼表,由于角膜缘干细胞的位置、血流和泪液成分的组合,炎症更容易长期持续,并直接导致组织再生能力的丧失。
SJS/TEN被归类为IV型(迟发型)超敏反应。药物代谢物在MHC I类分子上呈递,CD8+细胞毒性T淋巴细胞(CTL)发挥核心作用5)。活化的CD8+ T细胞分泌TNF-α和IFN-γ,诱导角质形成细胞产生一氧化氮(NO)。NO通过Fas/Fas配体途径促进角质形成细胞死亡5)。广泛的角质形成细胞凋亡导致表皮全层坏死和剥脱,组织病理学上表现为表皮基底层的完全坏死。皮肤活检确认Nikolsky征阳性和表皮基底层坏死有助于与SSSS等疾病鉴别。
颗粒溶素(granulysin)已被确定为SJS/TEN中角质形成细胞死亡的主要介质5)。NK细胞也通过CD94/NKG2C受体与角质形成细胞上的HLA-E分子结合介导角质形成细胞死亡5)。TNF-α上调表皮中细胞死亡相关分子的表达,最终导致广泛的表皮剥脱5)。
此外,有观点认为皮肤和黏膜上皮下血管壁的免疫复合物沉积引起的血管炎也参与其中,微循环障碍被认为是糜烂形成和伤口愈合延迟的一个因素。NSAIDs的共同机制——前列腺素产生的抑制也被推测与SJS/TEN的发病有关13)。
在眼部,上皮剥脱和半桥粒的丧失可能在免疫细胞浸润之前发生8)。早期角质形成细胞中尽管没有免疫细胞,但出现基底部空泡化,提示免疫浸润前的细胞因子调节异常8)。这表明眼表炎症可能先于或与全身药物反应同时发生,这为急性期频繁局部使用类固醇作为疾病干预而非单纯对症治疗提供了依据。
在后期,CD8+细胞毒性T淋巴细胞浸润并靶向角质形成细胞8)。在慢性期,中性粒细胞持续存在于结膜组织中,可能驱动免疫调节异常并导致角膜缘干细胞损伤8)。持续的慢性炎症导致结膜纤维化和瘢痕化,进而引起杯状细胞减少、副泪腺阻塞和睑板腺功能障碍,不可逆地破坏泪膜。为了打破这一慢性循环,即使对于轻微炎症,也需要长期使用低浓度类固醇滴眼液进行抑制。
角膜上皮干细胞的解剖与丧失机制
Section titled “角膜上皮干细胞的解剖与丧失机制”角膜上皮干细胞存在于角膜缘上皮的基底细胞中,占所有基底细胞的比例不到1%。这些干细胞在向角膜中心方向向心性移动的同时增殖和分化,维持整个角膜上皮的更新。角膜缘上皮的解剖特征是具有称为Vogt栅栏(POV)的放射状皱襞结构,其中含有丰富的血管、神经以及构成干细胞微环境的特殊微环境。POV在正常情况下在上方和下方易于观察,但在10岁以下或70岁以上的健康眼中可能无法清晰观察到,因此诊断时不应仅凭POV消失,而应结合结膜上皮侵入和上皮染色差异等发现进行评估。
当急性期出现广泛的角结膜上皮缺损导致角膜缘干细胞消失时,结膜来源的上皮会覆盖角膜表面,导致混浊和新生血管形成。这个过程称为角膜缘干细胞缺乏症(LSCD)8)。SJS是慢性LSCD的主要原因之一,在一项单中心738只眼的研究中,10.4%的病例由SJS引起8)。近年来,通过结合印迹细胞学鉴定杯状细胞、活体共聚焦显微镜直接观察POV基底细胞、以及前段OCT分层评估上皮厚度等方法,正在尝试客观诊断LSCD的严重程度和分布8)。
HLA多态性与药物反应
Section titled “HLA多态性与药物反应”HLA-A02:06与日本人伴有严重眼部并发症的SJS/TEN密切相关12)。已针对不同药物鉴定出易感HLA类型,如HLA-B58:01(别嘌醇)、HLA-B15:02(卡马西平)和HLA-B57:01(阿巴卡韦),给药前筛查正逐渐能够预防发病8)。这些HLA多态性作为关键分子,调节T细胞受体(TCR)与药物/药物代谢物之间的相互作用。已提出半抗原假说和p-i(药理相互作用)假说,认为药物分子本身或其反应性代谢物直接结合HLA分子的肽结合沟,改变自身肽的呈递,从而诱导异常的自身反应性T细胞应答。阐明这些分子机制将为未来的预防策略和安全药物选择奠定基础。
ICI诱导SJS/TEN的机制
Section titled “ICI诱导SJS/TEN的机制”在PD-1抑制剂诱导的SJS/TEN中,正常皮肤中通常检测不到的PD-L1表达在淋巴细胞和角质形成细胞中显著上调5)。这导致活化的CD8+ T细胞介导的角质形成细胞死亡5)。
在急性期,当角膜上皮干细胞(位于角膜缘上皮的基底细胞)消失时,角膜上皮的再生变得不可能。角膜表面被带有血管和结缔组织的结膜组织覆盖,变得不透明且凹凸不平。在慢性期,中性粒细胞的持续存在驱动免疫调节异常并维持干细胞损伤8)。泪腺导管的阻塞也导致泪液分泌不足,干眼和角膜混浊持续终生。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”免疫检查点抑制剂诱发的SJS/TEN
Section titled “免疫检查点抑制剂诱发的SJS/TEN”随着ICI使用的扩大,SJS/TEN的报告正在增加。在一项对13例替雷利珠单抗诱发的SJS/TEN(中国)的研究中,9名为男性,平均年龄为73.15±7.13岁5)。治疗方案多样,包括单独使用类固醇、类固醇+IVIG、类固醇+IVIG+环孢素等,12名患者得到改善5)。
对于一例初始使用类固醇和IVIG治疗无效的替雷利珠单抗诱发的SJS/TEN病例,联合使用TNF-α抑制剂(重组人TNF受体II-抗体融合蛋白)和血液净化后得到改善5)。TNF-α抑制剂在SJS/TEN治疗中的应用作为一种新的治疗策略正受到关注。
培养角膜上皮片与再生医学
Section titled “培养角膜上皮片与再生医学”针对角膜缘干细胞缺乏症的再生医学近年来取得了显著进步。通过在培养基中添加视黄醇和EGF,可以在不使用饲养细胞或血清的情况下制备角膜上皮片,并且不含异种物质的移植材料正在临床应用中13)。自体口腔黏膜上皮移植也可用于双眼LSCD的自体细胞来源,适用于SJS等重症眼表疾病13)。SLET作为LSCT中操作简便且成本较低的手术方式正在普及,现有研究的综述显示其效果优于CLET9)。此外,一种将口腔黏膜上皮细胞片附着在羊膜基质上的产品已作为再生医疗产品上市,针对双眼LSCD的临床应用正在推进。iPS细胞来源的角膜上皮细胞片的临床研究也在日本进行,作为无法获得自体细胞来源的双眼疾病患者的下一代治疗手段备受期待。
滴眼液引起的全身性SJS/TEN
Section titled “滴眼液引起的全身性SJS/TEN”据报道,磺胺类滴眼液也可能引起全身性SJS/TEN。一例患者在开始使用布林佐胺滴眼液6天后出现了覆盖体表面积99%的全身性反应1)。研究表明,通过结膜和鼻黏膜的吸收途径可能在遗传易感个体中诱发全身性免疫反应1)。这一发现表明,即使眼科使用的滴眼液也可能成为全身性重症药疹的诱因,对有药物过敏史的患者处方时需要谨慎判断。
SJS/TEN相关的全身并发症
Section titled “SJS/TEN相关的全身并发症”已有SJS/TEN合并暴发性1型糖尿病的病例报道3)。推测全身性免疫反应破坏了胰岛β细胞,这表明在SJS/TEN管理中进行血糖监测的重要性3)。此外,SJS/TEN的全身并发症还包括急性间质性肺炎、急性肾损伤、肝功能障碍和凝血异常等,因此在全身管理中必须持续监测多器官功能。
长期随访体系的建立
Section titled “长期随访体系的建立”遗留严重眼后遗症的SJS/TEN患者需要终身接受多种治疗的组合,包括角膜移植、角膜缘干细胞移植、人工角膜和巩膜镜。此外,还需要持续治疗干眼症、倒睫和慢性结膜炎,定期进行视野和眼压评估,以及处理继发性青光眼和白内障。因此,单一机构或科室难以应对,需要以角膜专家为中心的长期随访体系,并与皮肤科、风湿免疫科、口腔颌面外科和康复科进行多学科协作。为维持患者生活质量,低视力护理和就业支持也很重要,建议早期引入视觉康复。关于医疗费用补助制度,SJS/TEN相关的严重眼后遗症可能部分纳入指定难治性疾病“重症多形渗出性红斑(急性期)”及后遗症角膜疾病的框架,因此建议与医疗社会工作者合作提供信息。
8. 参考文献
Section titled “8. 参考文献”- Lu H, Xu W, Wu Y, Zhang M, Ma S. Ocular administration of brinzolamide leading to Stevens-Johnson syndrome/toxic epidermal necrolysis overlap: A case report and review. Medicine. 2025;104(49):e46362.
- Padniewski JJ, Jacobson-Dunlop E, Albadri S, Hylwa S. Stevens-Johnson syndrome precipitated by Moderna Inc. COVID-19 vaccine: a case-based review of literature comparing vaccine and drug-induced Stevens-Johnson syndrome/toxic epidermal necrolysis. Int J Dermatol. 2022.
- Zhang X, Huang D, Lou D, Si X, Mao J. Stevens-Johnson Syndrome/Toxic epidermal necrolysis complicated with fulminant type 1 diabetes mellitus: a case report and literature review. BMC Endocr Disord. 2024;24:172.
- Zhou Y, Xue H, Lu C, et al. Treatment of Tislelizumab-Induced Toxic Epidermal Necrolysis and Agranulocytosis: A Case Report and Literature Review. Curr Drug Saf. 2025;20(3):361-365.
- Yu H, Li Y, Qu X, Zhu J, Liu Z, Mu Z. Stevens-Johnson syndrome/toxic epidermal necrolysis induced by tislelizumab: a case report and literature review. Front Immunol. 2025;16:1689877.
- Zhang M, Wu R, Jia M, Sun S, Zhang L, Tang T. Sintilimab-induced erythema multiforme drug eruption in the treatment of sigmoid colon cancer: A case report and literature review. Medicine. 2023;102(41):e35659.
- Zhang L, Yang P, Zhu Y, Liu K, Sun Z. Toxic epidermal necrolysis following lamotrigine replacement therapy in a woman planning pregnancy: a case report and literature review. BMC Womens Health. 2025;25:371.
- Hu JCW, Trief D. A narrative review of limbal stem cell deficiency & severe ocular surface disease. Ann Eye Sci. 2023;8:13.
- Shanbhag SS, Nikpoor N, Donthineni PR, Singh V, Chodosh J, Basu S. Autologous limbal stem cell transplantation: a systematic review of clinical outcomes with different surgical techniques. Br J Ophthalmol. 2020;104(2):247-253.
- 重症多形滲出性紅斑に関する調査研究班. Stevens-Johnson症候群および中毒性表皮壊死症(TEN)診断基準2005. 厚生労働科学研究費補助金 難治性疾患克服研究事業.
- Sotozono C, Ueta M, Nakatani E, et al. Predictive Factors Associated with Acute Ocular Involvement in Stevens-Johnson Syndrome and Toxic Epidermal Necrolysis. Am J Ophthalmol. 2015;160(2):228-237.
- Ueta M, Sotozono C, Inatomi T, et al. HLA class I and II gene polymorphisms in Stevens-Johnson syndrome with ocular complications in Japanese. Mol Vis. 2008;14:550-555.
- Kinoshita S, Koizumi N, Ueta M, Sotozono C. New surgical approaches to the management of Stevens-Johnson syndrome and toxic epidermal necrolysis. Cornea. 2015;34 Suppl 11:S97-S103.
