RRMS
复发缓解型MS:最常见的亚型。复发持续超过24小时,发作间期有完全或部分缓解。

多发性硬化症(Multiple Sclerosis; MS)是一种中枢神经系统(CNS)白质出现炎性脱髓鞘病变,导致多种神经症状反复发作和缓解的疾病。其特征是胶质增生导致的瘢痕硬化性病变,通常仅累及中枢神经,周围神经系统不受影响。
美国估计患病率为1~1.5/1000人1)。全球有210万人患病,在北半球和南半球的高纬度地区分布较多。平均发病年龄为15~45岁,诊断时平均年龄为30岁。好发年龄为15~50岁,女性多见(20岁后期为高峰),男女比例为1:2.9。
MS有四种主要亚型。RRMS(复发缓解型)常在25-29岁发病,SPMS常在40-49岁发病1)。
RRMS
复发缓解型MS:最常见的亚型。复发持续超过24小时,发作间期有完全或部分缓解。
SPMS
继发进展型MS:从RRMS转变而来。即使在缓解期,残疾也进行性累积。
PPMS
原发进展型MS:从发病起残疾就进行性累积。无复发,缓慢进展。
CIS
临床孤立综合征:可能发展为MS的首次临床发作。可早期开始治疗。
75%的患者首发症状为单一主诉,45%表现为运动/感觉症状,20%表现为视觉症状。
眼部症状
全身神经症状
恶化呈急性至亚急性发作,持续数天至数月。85%的患者症状改善或消失,但10–15%留有后遗症。
常表现为单眼疼痛性视力下降。92%出现眼眶痛,特征为眼球运动时加重。此外,体温升高(如洗澡、运动)导致症状暂时恶化的Uhthoff现象也可出现。
MS的确切原因尚不清楚,但认为自身免疫机制参与发病。
遗传因素有关,但同卵双胞胎的一致率仅为25-30%。虽然已鉴定出HLA多态性和100多个风险基因位点,但认为不仅遗传易感性,环境因素也在发病中起重要作用。
采用2017年McDonald标准(2024年修订版)。基本是证明中枢神经系统脱髓鞘病变的时间和空间多发性(DIT/DIS)。2024年修订中,视神经被添加为第五个地形区域。在日本,也有2015年厚生劳动省的多发性硬化诊断标准。
空间多发性(DIS)的五个地形区域如下。
时间多发性(DIT)的证明:两次或以上发作,或MRI上强化与非强化病灶同时存在、新发T2病灶、CSF寡克隆带可作为替代 1)。
PPMS的诊断需要至少1年的残疾进展,并且满足以下至少两项:脑T2病灶、脊髓T2病灶(两个或以上)、CSF寡克隆带 1)。
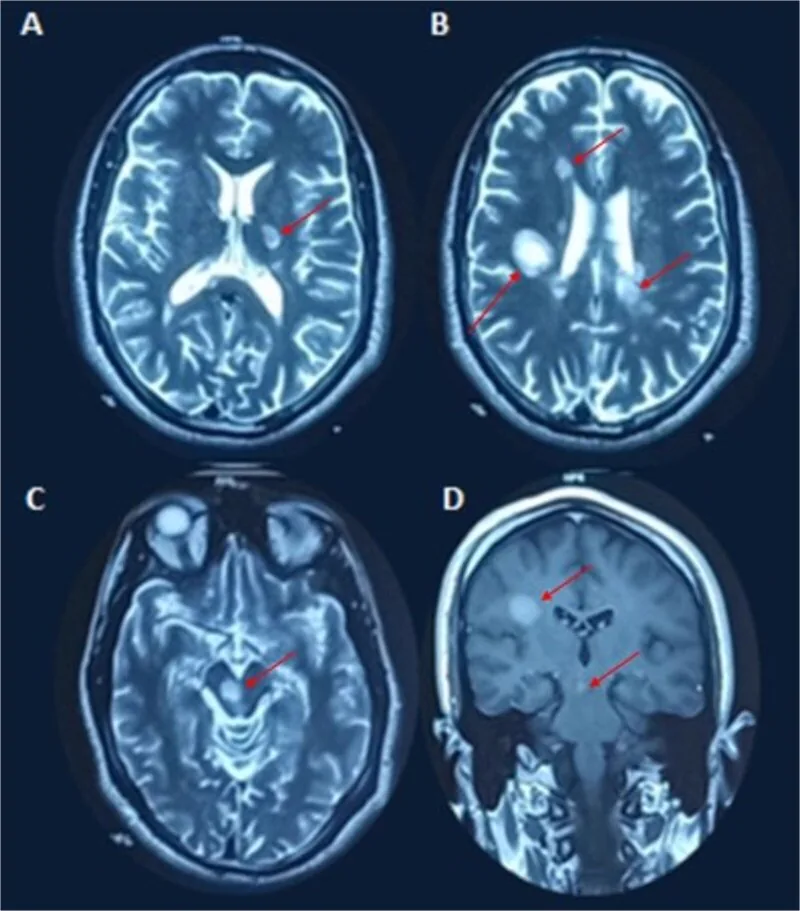
脱髓鞘斑块表现为T2高信号病灶或钆增强病灶。
当MRI不确定或用于预测疾病进展时,VEP有用1)。它可以在MRI可视化之前检测早期、无症状的脱髓鞘。65%的病例出现潜伏期延长和振幅降低。
与以下疾病的鉴别很重要,非典型病例应进行附加检查。
| 疾病类别 | 主要鉴别诊断 |
|---|---|
| 脱髓鞘疾病 | NMO(德维克病)、ADEM、MOGAD |
| 感染性 | 结节病、结核、梅毒、莱姆病 |
| 自身免疫性 | 系统性红斑狼疮、干燥综合征、白塞病 |
| 视神经疾病 | 非动脉炎性前部缺血性视神经病变、Leber遗传性视神经病变、中毒性/代谢性视神经病变 |
非典型病例的附加检查:抗AQP4抗体(排除视神经脊髓炎)、抗MOG抗体(排除MOG抗体相关疾病)、血清神经丝轻链检测、梅毒血清学检查(VDRL/RPR/FTA-ABS)、抗核抗体(系统性红斑狼疮)、血管紧张素转换酶/溶菌酶(结节病)。
日本的标准治疗是甲泼尼龙1000毫克/日静脉滴注,连续3天的类固醇冲击疗法。3天滴注后不进行口服泼尼松龙(后续治疗)。口服类固醇治疗被认为会增加复发率,不应进行。
即使不治疗,约80%的病例在发病后3周内视力开始改善,但冲击疗法可缩短恢复期。超过90%的视神经炎病例有望恢复视力。
如果类固醇冲击疗法无效,则进行血液净化疗法(血浆置换)。在国外,使用甲泼尼龙500-1000毫克/日,持续3-5天。视神经炎治疗试验(ONTT)显示,高剂量甲泼尼龙静脉注射可改善视功能、对比敏感度和色觉的恢复时间,但未显示最终视力预后的改善。
视力下降和视野缺损改善后,应与神经内科医生合作考虑DMT以预防复发。
主要DMT及其有效性如下所示。
| 药物 | 作用机制 | 给药方式 | 相对风险降低 |
|---|---|---|---|
| 干扰素β | 调节T/B细胞活性和细胞因子分泌 | 自行注射 | 残疾进展RR 0.71 |
| 醋酸格拉替雷 | 调节调节性T细胞 | 自行注射 | 复发RR 0.82 |
| 那他珠单抗 | 抑制炎症细胞进入中枢神经系统 | 静脉输注 | 复发RR 0.56 |
| 芬戈莫德 | S1P受体调节剂 | 口服 | 新T2病灶RR 0.65 |
| 特立氟胺 | 嘧啶合成抑制剂 | 口服 | 残疾进展RR 0.76 |
| 富马酸二甲酯 | 减轻氧化应激和炎症 | 口服 | 复发RR 0.64 |
| 阿仑单抗 | 抗CD52单克隆抗体 | 静脉输注 | 残疾进展RR 0.44 |
抗CD20单克隆抗体(ocrelizumab、rituximab、ofatumumab)已成为复发型MS的标准治疗3)。
即使没有脑部病变的视神经炎,15年后仍有25%发生MS;有脑部病变者,78%会转化为MS。
即使脑MRI无病变,15年后仍有25%发生MS;有脑病变者,78%转化为MS。发生视神经炎的患者应与神经内科协作,考虑使用DMT预防复发。
MS被认为是一种自身免疫性疾病。T淋巴细胞将髓鞘视为异物,激活巨噬细胞、细胞因子和抗体,破坏髓鞘和轴突。髓鞘缺失导致电脉冲传导障碍,神经信号传递受损。
活动性斑块
泡沫状巨噬细胞:吞噬髓鞘的巨噬细胞聚集。
血管周围浸润(perivascular cuffing):淋巴细胞围绕血管的特征性表现。
水肿性局灶性脱髓鞘病变:见于急性加重期。
慢性斑块
髓鞘脱失:可用Luxol fast blue染色确认。轴突保留但再髓鞘化不完全。
NAWM病变:外观正常的白质中弥漫性胶质增生、小胶质细胞激活和血脑屏障破坏。与局灶性白质病变相比,与临床残疾的相关性更高。
少突胶质细胞负责中枢神经系统的再髓鞘化1)。这依赖于成体少突胶质细胞前体细胞(OPC),但现有的成熟少突胶质细胞不能参与再髓鞘化1)。
再髓鞘化失败的主要原因如下1)。
此外,还观察到皮质和皮质下灰质损伤,当脑膜中形成B细胞滤泡样淋巴结构时,已知会导致更严重的临床病程1)。
通过抑制CD40L,阻断T细胞与抗原呈递细胞(包括B细胞)共刺激的新方法。
Vermersch等人(N Engl J Med 2024)的2期试验显示,frexalimab在MRI结局(8-12周的新钆增强病灶)方面显示出优于安慰剂的明确疗效,并且血清NfL(神经组织损伤的生物标志物)的降低也得到了证实3)。对于进展型MS,还预期具有使小胶质细胞和巨噬细胞失活的效果,理论上可通过阻断斑块边缘小胶质细胞的CD40L信号实现神经保护3)。
目前面临的挑战是确立其相对于现有高效DMT(抗CD20药物)的临床优势3)。
铁依赖性细胞死亡——铁死亡已被证明参与MS的神经元死亡。
Tang等人(2025)解读了Woo等人(Cell, 2024)的研究,报道了以下级联反应:谷氨酸兴奋毒性→钙超载→内质网应激→STING1从STIM1解离→非典型通路激活→自噬→GPX4(脂质过氧化中和酶)的自噬降解→铁死亡4)。在人类多发性硬化症标本和小鼠模型中均证实了神经元中STING1表达升高。STING1抑制剂(C176、H151)在动物模型中减少了自噬依赖性GPX4降解,并显示出神经保护作用4)。
在研究阶段,通过CD40L抑制剂frexalimab使小胶质细胞和巨噬细胞失活从而实现神经保护3),以及通过抑制STING1来抑制铁死亡(铁依赖性细胞死亡)4)被认为是有前景的。两者目前均处于临床试验或研究阶段,并非标准治疗。