视神经炎

视神经脊髓炎谱系疾病(NMOSD)
一目了然的要点
Section titled “一目了然的要点”1. 什么是视神经脊髓炎谱系疾病(NMOSD)?
Section titled “1. 什么是视神经脊髓炎谱系疾病(NMOSD)?”视神经脊髓炎谱系疾病(NMOSD)是一种中枢神经系统的炎症性、抗体介导的自身免疫性疾病。以前称为Devic病,长期以来被视为多发性硬化(MS)的一种亚型。然而,2004年发现针对水通道蛋白4(AQP4)的自身抗体(AQP4-IgG)后,它被确立为一种独立的疾病实体。
历史背景:1870年,Sir Thomas Clifford Allbutt首次描述了脊髓炎与视神经受累之间的关联。后续研究认识到它是一种不同于MS的疾病,现在以NMOSD这一综合概念来理解。
流行病学如下:
- 发病率:AQP4阳性NMOSD的估计年发病率为每百万人0.4-7.3例1)
- 性别比例:男女比例约为1:9,女性显著占优。
- 发病年龄:主要好发于中年(40
60岁),高峰在3545岁。 - 种族:在非洲裔和亚洲裔人群中更常见1)
- 与妊娠的关系:约20%~47%的女性在妊娠期间或分娩/流产后1年内首次发病。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”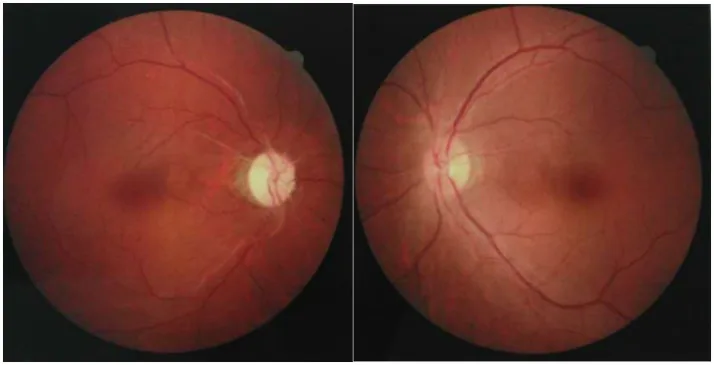
NMOSD的症状因受累部位而异。
- 急剧视力下降:主要症状之一。特征是对类固醇治疗抵抗。
- 眼痛:伴视神经炎,约半数病例出现。
- 色觉异常:典型表现为红色饱和度下降。
- 视野缺损:不仅限于中心暗点,还可出现水平偏盲、双颞侧偏盲或同向偏盲,因为病变可累及视交叉和视束。
- 感觉障碍和截瘫:脊髓炎导致的运动和感觉障碍。
- 膀胱直肠功能障碍:脊髓炎相关的自主神经功能障碍
- 顽固性呃逆、恶心呕吐:最后区病变的特征性症状
- 眼球运动障碍:由脑干病变引起
- 嗜睡症(发作性睡病样):由间脑/下丘脑病变引起
发病初期可能出现流感样症状(发热、肌痛、头痛)。
脊髓炎
LETM(长节段横贯性脊髓炎):连续病变累及3个或以上椎体节段。约85%的AQP4+ NMOSD患者在急性脊髓炎时出现。
完全性脊髓综合征:累及运动、感觉和自主神经三条通路。
严重功能障碍:超过30%的患者在发作最低点依赖轮椅。37-44%的AQP4+ NMOSD患者最终需要助行器。
最后区综合征
顽固性呃逆:持续数天至数周,对常规止吐药无反应。
恶心和呕吐:由于最后区缺乏血脑屏障,AQP4-IgG容易直接到达该部位。
NMOSD的核心诊断发现:无法解释的顽固性呃逆应积极怀疑NMOSD。
NMOSD的视神经炎更严重、双侧性、复发率高,视力预后差。在AQP4+ NMOSD中,60-69%的患者至少一只眼永久性视力障碍低于20/200。此外,它容易累及视交叉,导致双颞侧偏盲等多种视野缺损,这也是与MS的区别。
3. 病因和风险因素
Section titled “3. 病因和风险因素”NMOSD的确切病因尚未完全阐明。自身免疫耐受丧失被认为是根本原因。
主要风险因素如下:
- 女性:男女比例约为1:9,女性占绝对优势
- 种族:亚洲人和非洲人发病风险较高
- 合并自身免疫性疾病:系统性红斑狼疮(SLE)、干燥综合征、重症肌无力等
- NMOSD患者中10-30%合并干燥综合征。儿童病例也有报道5)
- 与重症肌无力的合并发生率为2~3%1)
- 恶性肿瘤(副肿瘤性NMOSD):估计3~5%的NMOSD为副肿瘤性2)3)
- 已有乳腺癌、肺癌、卵巢畸胎瘤等的报道3)
- 有假说认为肿瘤内AQP4表达会诱发自身免疫反应2)
- 畸胎瘤相关NMOSD多见于年轻女性(平均年龄32.7岁)2)
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”诊断标准(2015年国际共识)
Section titled “诊断标准(2015年国际共识)”AQP4-IgG阳性NMOSD的诊断标准需满足以下三项:
- 至少1个核心临床特征
- AQP4-IgG阳性(使用最佳检测方法)
- 排除其他诊断
AQP4-IgG阴性或未检测的NMOSD诊断标准需满足以下四项:
- 至少2个核心临床特征(其中1个必须是视神经炎、LETM或最后区综合征)
- 空间多发性
- 满足额外的MRI要求
- 排除其他诊断
**主要临床特征(6项)**如下:
- 视神经炎
- 急性脊髓炎
- 最后区综合征(顽固性呃逆、恶心呕吐)
- 急性脑干综合征
- 症状性发作性睡病/急性间脑综合征
- 症状性大脑综合征
下表显示了主要抗体检测方法的比较。
| 检测方法 | 灵敏度 | 特异度 | 备注 |
|---|---|---|---|
| CBA(细胞基检测法) | 69.7~100% | 85.8~100% | 推荐方法 |
| ELISA法 | 略逊于CBA | 略逊于CBA | 日本医保覆盖 |
- AQP4-IgG:对NMOSD具有疾病特异性。建议在急性发作时和免疫抑制治疗开始前检测1)
- CBA(细胞基检测法):目前推荐的检测方法。ELISA的假阳性率据称是CBA的5倍1)
- MOG-IgG:约30%的AQP4-IgG阴性NMOSD患者呈阳性1)
- 脑脊液寡克隆带(OCB):NMOSD中阳性率低(10~20%),MS中为88%。阴性提示NMOSD1)
- 脑脊液白细胞计数:>50/μL、中性粒细胞或嗜酸性粒细胞的存在是区分NMOSD与MS的线索
- 临界闪烁频率(CFF):用于评估视神经炎活动性,NMOSD中降低
影像诊断(MRI)
Section titled “影像诊断(MRI)”- 脊髓MRI:LETM最具特征性。中央灰质为主。伴有脊髓肿胀、T1低信号、Gd增强。约85%的AQP4+ NMOSD在急性脊髓炎时表现为LETM 1)
- 视神经MRI:必须使用脂肪抑制序列。双侧、长节段炎症(≥50%)为特征。后部及视交叉受累是AQP4+ NMOSD的典型表现 1)
- 脑MRI:可见最后区病变、第四脑室周围脑干病变、下丘脑/第三脑室周围病变、广泛白质病变等
- NMOSD的特点:与MS不同,无症状的新发T2病变罕见(3–13%)。通常不需要监测MRI 1)
- 多发性硬化(MS)
- MOG抗体相关疾病(MOGAD)
- 急性播散性脑脊髓炎(ADEM)
- 系统性红斑狼疮
- 神经白塞病
- 在老年患者中,需与缺血性视神经病变、颈椎病性脊髓病、脊髓梗死、原发性中枢神经系统淋巴瘤鉴别
可以。即使AQP4-IgG阴性或未检测,若满足两个以上核心临床特征、附加MRI要求,并排除其他疾病,仍可诊断NMOSD。此外,约30%的AQP4-IgG阴性病例MOG-IgG阳性,建议检测两种抗体。AQP4-IgG阴性病例中后期血清转换者不足1%。
5. 标准治疗
Section titled “5. 标准治疗”一线治疗:类固醇冲击疗法
- 甲泼尼龙1000mg/日静脉滴注,连续3天
- 如视力无改善,间隔3-4天后考虑再次进行1个疗程
- NMOSD的视神经炎对类固醇耐药性高,若反应不充分,应尽早考虑下一步治疗
二线治疗:血浆置换疗法
在类固醇冲击无效时实施。以下方法可供选择。
- 单纯血浆置换(PE):效果最强,但对身体损伤也最大
- 双重膜滤过血浆置换(DFPP)
- 免疫吸附疗法(IA):可选择性地清除抗体
效果顺序为单纯血浆置换 > 双重膜滤过 > 免疫吸附。1个疗程进行5-6次,治疗后需住院直至体内IgG水平恢复。需要注意的是,对于“视神经炎”,可能不在医保覆盖范围内,需向患者说明。
预防复发(维持治疗)
Section titled “预防复发(维持治疗)”在AQP4+ NMOSD中,首次发作后应尽早开始维持治疗1)。血浆置换后,通常转为泼尼松龙5-10mg/日联合硫唑嘌呤50-100mg/日。
证据水平高的生物制剂如下。
补体抑制剂
- 依库珠单抗:900mg静脉注射,每周1次×4次,然后1200mg每2周维持给药1)
- 拉武利珠单抗:基于体重的负荷剂量(2,400–3,000 mg)→ 从第15天起每8周3,000–3,600 mg1)
B细胞清除疗法
- 利妥昔单抗:375 mg/m² 静脉注射,每周一次×4次,或1,000 mg×2次(间隔2周)→ 每6个月1,000 mg×2次1)
- 伊奈利珠单抗:300 mg 静脉注射,间隔15天两次→ 每6个月一次1)
IL-6受体抑制剂
- 萨特利珠单抗:120 mg 皮下注射,每4周一次1)
血浆置换疗法是下一个选择。可选择单纯血浆置换、双重膜滤过血浆置换或免疫吸附。单纯血浆置换被认为效果最好,但对身体负担也较大。一个疗程进行5–6次,治疗后需要住院管理。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”NMOSD本质上是一种星形细胞病。发病机制如下。
抗体产生与血脑屏障(BBB)穿越
在外周,B细胞分化为分泌AQP4-IgG的浆母细胞。IL-6促进这种分化并增强血脑屏障的通透性。最后区缺乏血脑屏障,可能成为AQP4-IgG进入中枢神经系统的途径。
星形胶质细胞损伤的级联反应
AQP4-IgG与星形胶质细胞足突上高表达的AQP4水通道结合,通过以下途径导致星形胶质细胞损伤:
- 补体经典途径激活:AQP4-IgG的Fc部分激活补体,形成膜攻击复合物(MAC),直接损伤星形胶质细胞。
- 抗体依赖性细胞介导的细胞毒性(ADCC):NK细胞和中性粒细胞通过Fcγ受体损伤星形胶质细胞。
- C5a过敏毒素释放:招募粒细胞(中性粒细胞、嗜酸性粒细胞),导致继发性轴突损伤和脱髓鞘1)。
与多发性硬化的病理差异
多发性硬化以CD8+ T细胞为核心,主要表现为白质脱髓鞘;而视神经脊髓炎谱系疾病中CD4+ T细胞参与更多,形成累及灰质和白质的坏死性病变。
分布原因
AQP4通道在视神经、最后区和脊髓中分布丰富,因此这些区域被选择性靶向。
生物标志物
- 血清GFAP:反映星形胶质细胞损伤,发作时升高。
- 血清神经丝轻链(NfL):反映轴突损伤,与发作严重程度相关1)。
涉及的细胞因子包括IL-6、IL-10、IL-17a、G-CSF、TNF-α和BAFF/APRIL。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”副肿瘤性NMOSD的机制阐明与肿瘤筛查
Section titled “副肿瘤性NMOSD的机制阐明与肿瘤筛查”估计3-5%的NMOSD为副肿瘤性。与卵巢畸胎瘤相关的病例已被特别详细地研究。
Ikeguchi等人(2021)对6例卵巢畸胎瘤相关AQP4+ NMOSD进行了综述2)。所有患者均为女性,平均发病年龄32.7岁(15-50岁)。6例中83%(5/6)出现恶心和呕吐,83%脑脊液寡克隆区带阳性,83%有背侧脑干病变。病理分析显示,肿瘤内GFAP阳性神经组织中有AQP4免疫反应性和淋巴细胞浸润,提示肿瘤内AQP4抗原呈递触发自身免疫反应。肿瘤切除后,60%(3/5)的病例AQP4-IgG转为阴性。
Ding等人(2021)对43例副肿瘤性NMOSD进行了综述3)。88.4%为女性,乳腺癌和肺癌是最常见的肿瘤类型。尤其强调50岁及以上NMOSD患者进行肿瘤筛查的重要性。
即使年轻患者也建议进行包括畸胎瘤在内的肿瘤筛查。
难治性病例的免疫吸附疗法
Section titled “难治性病例的免疫吸附疗法”对于对类固醇、血浆置换和利妥昔单抗等治疗无效的难治性NMOSD,已有报道称Protein-A免疫吸附疗法(IA)有效。
Fan等人(2024)对一名35岁合并干燥综合征且对类固醇冲击和IVIG无反应的难治性NMOSD女性患者进行了三次Protein-A免疫吸附治疗4)。一周内,视力障碍、截瘫和本体感觉障碍显著改善,并确认AQP4-IgG、IgA、IgG和IgM迅速下降。随访4年未观察到复发或进展。
合并自身免疫性疾病病例的特征
Section titled “合并自身免疫性疾病病例的特征”NMOSD合并各种自身免疫性疾病的实际情况正逐渐明朗。
Zhu等人(2025)报告了一名11岁发病的14岁女性NMOSD病例5)。该患者AQP4-IgG阳性,病程中确诊为原发性干燥综合征。通过甲泼尼龙、IVIG以及从霉酚酸酯(MMF)转换为他克莫司维持缓解。虽然成人NMOSD病例中有20-30%报告合并自身免疫性疾病,但该病例表明儿童病例中也可能存在这种合并症5)。
8. 参考文献
Section titled “8. 参考文献”- Cacciaguerra L, Flanagan EP. Updates in NMOSD and MOGAD Diagnosis and Treatment. Neurol Clin. 2024;42(1):77-114.
- Ikeguchi R, Shimizu Y, Shimomura A, et al. Paraneoplastic AQP4-IgG-Seropositive Neuromyelitis Optica Spectrum Disorder Associated With Teratoma: A Case Report and Literature Review. Neurol Neuroimmunol Neuroinflamm. 2021;8(5):e1045.
- Ding M, Lang Y, Cui L. AQP4-IgG positive paraneoplastic NMOSD: A case report and review. Brain Behav. 2021;11(9):e2282.
- Fan W, Chen X, Xiao P, et al. Protein-A immunoadsorption combined with immunosuppressive treatment in refractory primary Sjögren’s syndrome coexisting with NMOSD: a case report and literature review. Front Immunol. 2024;15:1429405.
- Zhu G-q, Hu R-x, Peng Y, et al. A Chinese girl with neuromyelitis optica spectrum disorder coexisting with primary Sjogren’s syndrome: a case report and literature review. Front Immunol. 2025;16:1559825.
