典型ON
一线治疗:类固醇脉冲疗法(甲泼尼龙1000mg/日静脉滴注×3天)。超说明书用药。
脉冲后:开始口服泼尼松龙0.5mg/kg/日,然后每3-4天减量5-10mg。
首次无效时:间隔4-5天后进行第二次脉冲。
效果:缩短恢复期,但发病1年后的最终视力无显著差异。
积极适应症:双眼发病、高度视功能障碍、唯一功能眼、复发、MRI脱髓鞘斑、患者强烈希望早期改善。

视神经炎是由于某种原因导致视神经发炎而引起视功能下降的疾病。在排除感染性和非感染性(中毒性、遗传性、压迫性)视神经病变后,大多数为特发性,认为由自身免疫机制引起。
好发年龄为15~45岁,女性多见,表现为单眼急性视神经病变。视功能障碍在数天至2周内进展,随后在5周内显示恢复趋势。
| 病型 | 特征 |
|---|---|
| 特发性(自身免疫机制) | 最常见。通常为单相病程 |
| 抗AQP4抗体阳性(NMOSD相关) | 约占特发性病例的10%。激素抵抗,男女比例1:9 |
| 抗MOG抗体阳性(MOGAD) | 双侧、视盘水肿、长节段病变。激素敏感但易复发 |
| MS相关 | 高达75%的MS患者一生中至少经历一次ON |
| CRION | 激素依赖、复发性。2003年Kidd等人提出5) |
| 感染性 | 梅毒、病毒等。使用激素前必须排除 |
初诊时检测抗AQP4抗体,阴性则按特发性处理。
日本年发病率为成人每10万人1.6例。好发年龄15-45岁,女性约占70%。全球患病率估计为每10万人1-5例。
与多发性硬化(MS)的关系非常密切,特发性视神经炎发病后15年内转化为MS的累积概率为50%。如果初次发病时脑MRI无脱髓鞘病变,转化率仅为25%,但若存在1个或以上病变,则可达78%。
儿童的好发年龄为9~10岁,年龄越小越容易出现双眼性和严重的视力障碍,尤其5岁以下更为显著。儿童转化为MS的比例,安达等报告约为30%,沟田等报告为16%。
MOGAD的年发病率估计为每百万人1.6~4.8例。1)
特发性视神经炎约50%在15年内转化为MS。但初次发病时脑MRI无脱髓鞘病变者转化率仅为25%。发病后应通过脑MRI进行风险评估,并与神经内科协作进行随访观察。
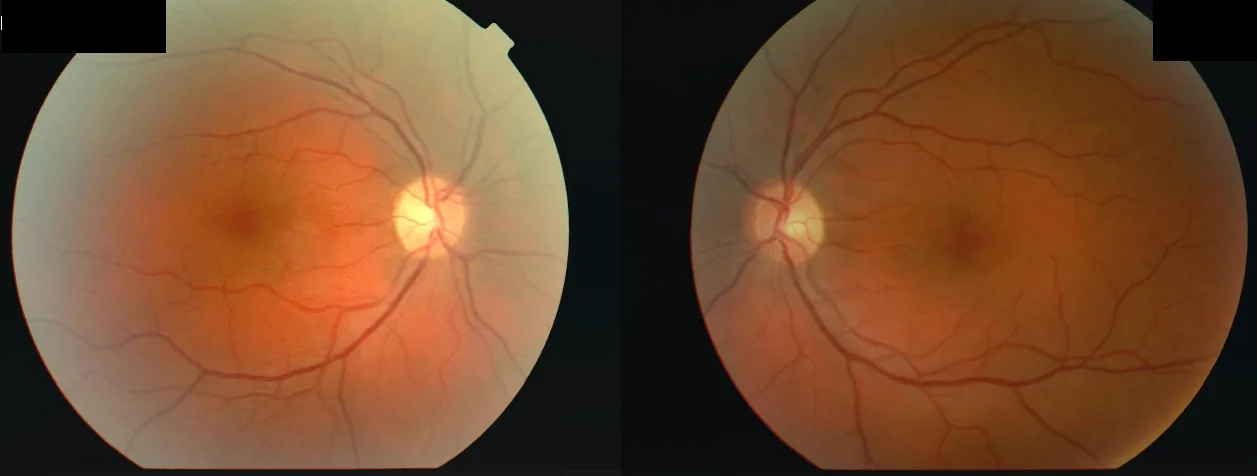
呈急性发病模式,以下症状具有特征性:
出现以下征象时怀疑非典型视神经炎,进行详细病因检查。
| 特征 | MOG-ON | AQP4-ON | MS-ON | CRION |
|---|---|---|---|---|
| 性别比(男:女) | 1:1 | 1:7~9 | 1:3 | 1:1.7~2.3 |
| 双眼受累 | 31%~84% | 13%~82% | 极为罕见 | 有 |
| 视乳头水肿 | 45%~92% | 7%~52% | 11%~14% | 轻度 |
| 眼痛 | 73%~92% | 28%~50% | 10%~46% | 有 |
| 最低视力 | 中度至重度 | 中度至重度 | 轻度至中度 | 多样 |
| 恢复 | 良好 | 可能不良 | 良好 | 激素依赖 |
来源: Jeyakumar N, et al. Eye. 20241)
儿童视神经炎较成人更常表现为伴有视盘充血、肿胀的典型视乳头炎,而非球后视神经炎。炎症不仅限于视盘,而是累及整个视神经。双眼受累占50%~75%,前部视神经炎型占50%~75%。
Uhthoff征是指体温升高时出现一过性视力障碍的现象。患者在洗澡或运动后自觉视力下降或视物模糊。症状在数分钟内出现,1小时内消失。该征象多见于多发性硬化相关的视神经炎,但其他视神经病变也有报道,并非多发性硬化特有。
抗AQP4抗体阳性视神经炎是一种难治性亚型,约占特发性视神经炎的10%。与普通视神经炎相比,发病时视力更差,对激素治疗反应不佳,复发更频繁,且易转为双眼受累。诊断必须检测血清抗AQP4抗体。
在怀疑自身免疫机制的特发性病例中,小胶质细胞等炎症相关细胞浸润视神经并引起炎症。反复炎症会导致神经纤维累积性损伤,进而发展为视神经萎缩。
有假说认为病毒感染可触发自身免疫反应,部分患者脑脊液中可检测到麻疹、水痘、流感等病毒抗体。在儿童中,已知与伴有发热、头痛的急性播散性脑脊髓炎(ADEM)相关。
据报道,疫苗接种和感染可触发MOGAD发病,推测机制包括旁观者激活等导致免疫耐受破坏。1)
有COVID-19感染后或疫苗接种后发生视神经炎的报道。从疫苗接种到视神经炎发病的中位时间为18天,55例中14例MOG-IgG阳性。11)
视神经炎是临床诊断。根据急性单眼视力下降、眼球运动痛、RAPD阳性、视野缺损的组合进行诊断。
典型ON和非典型ON的MRI表现区别如下。
| 特征 | 典型ON(MS相关) | 非典型ON |
|---|---|---|
| 强化模式 | 短节段强化 | 长节段强化(≥1/2) |
| 病变部位 | 前部(球后视神经) | 向后延伸(视交叉和视束) |
| 视神经鞘 | 无强化 | 视神经鞘和眼眶脂肪强化 |
NMOSD-ON、MOG-ON和MS-ON的影像学特征比较:
| 特征 | NMOSD-ON | MOG-ON | MS-ON |
|---|---|---|---|
| 受累模式 | 双侧 | 双侧 | 单眼 |
| 好发部位 | 颅内和视交叉 | 球后(前部) | 球后和管内 |
| 病变长度 | 长范围 | 长范围 | 短节段 |
| 视神经鞘增强 | 罕见 | 50%阳性 | 无报道 |
来源: Jeyakumar 20241); Cacciaguerra & Flanagan4)
测量视乳头周围视网膜神经纤维层(pRNFL)厚度。急性期可见pRNFL增厚(MOG-ON中位数164μm vs MS-ON 103μm)。慢性期出现pRNFL变薄,复发次数与pRNFL减少相关。pRNFL低于50μm阈值时,视野平均偏差显著恶化。1)
可见P100潜伏期延长。该发现反映脱髓鞘。
若病程不典型,则检测以下项目。
评估视神经炎是否为MS的首发症状。通过证明中枢神经系统炎症性脱髓鞘病变的时间和空间多发性,并排除其他疾病来诊断。如果脑室周围、皮质/近皮质、幕下和脊髓四个区域中至少两个区域存在T2高信号病变,则可证明空间多发性。
| 分类 | 主要鉴别疾病 | 鉴别要点 |
|---|---|---|
| 脱髓鞘性 | MS相关视神经炎、NMO | 抗体检测、MRI |
| 免疫介导性 | CRION、结节病、SLE | 类固醇依赖性、全身表现 |
| 感染性 | 梅毒、疱疹、结核 | 使用类固醇前必须排除 |
| 遗传性 | Leber遗传性视神经病变 | 年轻男性、双眼、无痛→基因检测 |
| 药物性 | 乙胺丁醇、利奈唑胺 | MRI无强化 |
| 血管性 | 非动脉炎性前部缺血性视神经病变 | 老年人、通常无痛、视盘部分苍白水肿 |
| 儿童 | 急性播散性脑脊髓炎 | 伴有发热、头痛、意识障碍 |
有报告称,诊断为球后视神经炎的病例实际上是眼眶淋巴瘤引起的压迫性视神经病变。如果存在非典型特征,不应轻易使用类固醇,而应进行详细检查。9)
通常,成人进行的FA(荧光眼底造影)、CFF和动态视野检查不适用于儿童;诊断依据眼底所见和头部MRI。
在典型ON中,仅在视神经的短节段出现造影增强。相反,非典型ON表现为视神经的长节段造影增强(超过长度的一半)、向后延伸(至视交叉和视束)以及视神经鞘的造影增强。这些MRI表现直接关系到病因的鉴别诊断。
特发性视神经炎的视力预后良好。超过90%的视神经炎病例通过观察或全身类固醇给药后视力改善。根据ONTT的长期结果,发病1年后的视力达到0.5以上者占93%,达到1.0以上者占70%以上。
对于矫正视力相对较好的特发性视神经炎,可口服甲钴胺1500μg/日(超说明书用药)进行观察。
典型ON
一线治疗:类固醇脉冲疗法(甲泼尼龙1000mg/日静脉滴注×3天)。超说明书用药。
脉冲后:开始口服泼尼松龙0.5mg/kg/日,然后每3-4天减量5-10mg。
首次无效时:间隔4-5天后进行第二次脉冲。
效果:缩短恢复期,但发病1年后的最终视力无显著差异。
积极适应症:双眼发病、高度视功能障碍、唯一功能眼、复发、MRI脱髓鞘斑、患者强烈希望早期改善。
抗AQP4抗体阳性ON
急性期:类固醇脉冲疗法(首选)。
无效时:间隔3-4天再次脉冲→仍无效→考虑血浆置换。
血浆置换:单纯血浆置换 > 双重膜滤过血浆置换 > 免疫吸附疗法(按疗效排序)。1疗程5-6次。
维持疗法:泼尼松龙5-10mg/日 + 硫唑嘌呤50-100mg/日。
注意:与特发性ON不同,口服类固醇预防复发很重要。
抗MOG抗体阳性ON(MOGAD)
急性期:类固醇脉冲疗法高度有效。完全恢复50%,部分恢复44%。13)
复发倾向:类固醇依赖性很强,口服泼尼松龙减量期间(特别是低于10mg/日或停药后2个月内)70%复发。14)
维持疗法:IVIg(≥1g/kg/4周可显著减少复发)。15) 利妥昔单抗可能不如AQP4-ON有效。
治疗开始时机:通常在第二次发作后开始(因为>50%为单相性)。
CRION(慢性复发性炎症性视神经病)
急性期:甲泼尼龙静脉注射1mg/kg×3-5天。
中间期:口服泼尼松1mg/kg,逐渐减至最小有效剂量。
长期维持:硫唑嘌呤、甲氨蝶呤、环磷酰胺、霉酚酸酯是候选药物。IVIG也是选择之一。
注意:停药会导致复发,因此需要长期持续治疗。
标准剂量(1mg/kg/天)的口服泼尼松龙单药治疗在ONTT中与安慰剂或静脉类固醇相比复发率更高,因此不推荐。
甲泼尼龙30mg/kg/天×3天。视力预后通常良好。
积极进行类固醇治疗。如果对类固醇冲击反应不佳,可选择大剂量免疫球蛋白静脉滴注或血浆置换疗法。
合并MS的病例在视力改善后考虑预防复发的治疗。与神经内科协作,考虑疾病修饰药物(干扰素β、醋酸格拉替雷、芬戈莫德、那他珠单抗等)。
根据ONTT的结果,类固醇脉冲疗法可缩短恢复时间,但对发病一年后的最终视力无显著影响。特发性视神经炎中,93%未经治疗的患者视力恢复至0.5以上。但抗AQP4抗体阳性病例对类固醇耐药,需要包括早期血浆置换在内的积极治疗。
由于CRION是一种停药后复发的疾病,即使在症状缓解后,通常也需要长期免疫抑制治疗。在确定类固醇的最小有效剂量后,联合使用非类固醇免疫抑制剂,并个体化设计治疗方案。
在怀疑自身免疫机制的特发性病例中,小胶质细胞等炎症相关细胞浸润视神经并引起炎症。
反复经历视神经炎症会导致神经纤维累积性损伤,进而发展为视神经萎缩。
抗AQP4抗体与补体结合,攻击视神经内的胶质细胞——星形胶质细胞,从而发病。视神经和视交叉的星形胶质细胞高表达AQP4,容易成为攻击目标。
MOG-IgG(主要是IgG1亚类)靶向CNS髓鞘表面的MOG。补体途径的激活和抗体依赖性细胞吞噬参与脱髓鞘。然而,与AQP4-IgG相比,补体激活较弱。在MOGAD中,CD4阳性T细胞和巨噬细胞为主,而在MS中,CD8阳性T细胞占优势。1)4)
尽管MOG不在视网膜中表达,但MOG-ON会导致视网膜神经节细胞损伤。谷氨酸毒性和视神经乳头血脑屏障的脆弱性被认为是其机制。1)
IL-6增加血脑屏障通透性并促进浆母细胞分化的机制也受到关注。
CRION最初被提出作为涵盖类固醇反应性和复发性视神经炎的综合症。5) 随后对CRION队列的抗体检测发现,高达22%为AQP4-IgG阳性,高达25%为MOG-IgG阳性。6)7)8) 因此,CRION被认为是一种包含MOG抗体相关视神经炎和AQP4抗体相关视神经炎等异质性病因的综合症诊断。
病毒感染触发自身免疫反应的假说已被提出。有报道在一些ON患者的脑脊液中检测到水痘-带状疱疹病毒和单纯疱疹病毒的DNA。在MOGAD中,疫苗接种或感染导致的免疫耐受破坏(旁观者激活、分子模拟)被认为是可能的机制。1)
针对AQP4阳性NMOSD,已出现具有1级证据的生物制剂。4)
这两种药物对AQP4阳性NMOSD均有确凿证据,但对MOGAD的适应症尚未确立。
萨特利珠单抗(NCT05271409)和罗扎诺利昔单抗(NCT05063162)的III期随机对照试验正在进行中。托珠单抗(IL-6受体抗体)的超说明书使用已被报道可预防复发长达29个月。1)
已有COVID-19感染后出现脱髓鞘性视神经炎的病例报道。Jossy等人(2022)报告了感染恢复期发生视神经炎的病例,所有患者经类固醇冲击治疗后视力恢复。10)
COVID-19疫苗接种后发生视神经炎的报道逐渐增多,从接种到发病的中位时间为18天。55例中14例MOG-IgG阳性,无AQP4-IgG阳性病例。11)也有SARS-CoV-2感染后出现MOG抗体相关视神经炎的病例报道。12)
随着MOG-IgG和AQP4-IgG抗体检测的普及,部分既往诊断为CRION的病例正被重新分类为MOGAD或NMOSD。未来,基于抗体谱的疾病概念重新定义有望推进。