典型ON
第一線治療:類固醇脈衝療法(甲基培尼皮質醇1000mg/日靜脈滴注×3天)。仿單外使用。
脈衝後:開始口服培尼皮質醇0.5mg/kg/日,然後每3-4天減量5-10mg。
首次無效時:間隔4-5天後進行第二次脈衝。
效果:縮短恢復期,但發病1年後的最終視力無顯著差異。
積極適應症:雙眼發病、高度視功能障礙、唯一功能眼、復發、MRI去髓鞘斑、患者強烈希望早期改善。

視神經炎是由於某種原因導致視神經發炎而引起視功能下降的疾病。在排除感染性和非感染性(中毒性、遺傳性、壓迫性)視神經病變後,大多數為特發性,認為由自體免疫機制引起。
好發年齡為15~45歲,女性較多,表現為單眼急性視神經病變。視功能障礙在數天至2週內進展,隨後在5週內顯示恢復趨勢。
| 病型 | 特徵 |
|---|---|
| 特發性(自體免疫機轉) | 最常見。基本上為單相病程 |
| 抗AQP4抗體陽性(NMOSD相關) | 約佔特發性病例的10%。類固醇抗性,男女比1:9 |
| 抗MOG抗體陽性(MOGAD) | 雙側、視乳頭水腫、長節段病變。對類固醇有反應但易復發 |
| MS相關 | 高達75%的MS患者一生中至少經歷一次ON |
| CRION | 類固醇依賴、復發性。2003年Kidd等人提出5) |
| 感染性 | 梅毒、病毒等。使用類固醇前必須排除 |
初診時檢測抗AQP4抗體,陰性則按特發性處理。
日本年發生率為成人每10萬人1.6例。好發年齡15-45歲,女性約佔70%。全球盛行率估計為每10萬人1-5例。
與多發性硬化(MS)的關聯非常密切,特發性視神經炎發病後15年內轉化為MS的累積機率為50%。若初次發病時腦部MRI無脫髓鞘病變,轉化率僅為25%,但若存在1個或以上病變,則可達78%。
兒童的好發年齡為9~10歲,年齡越小越容易出現雙眼性和嚴重的視力障礙,尤其5歲以下更為顯著。兒童轉化為MS的比例,安達等人報告約為30%,溝田等人報告為16%。
MOGAD的年發生率估計為每百萬人1.6~4.8例。1)
特發性視神經炎約50%在15年內轉化為MS。但初次發病時腦部MRI無脫髓鞘病變者轉化率僅為25%。發病後應透過腦部MRI進行風險評估,並與神經內科協作進行追蹤觀察。
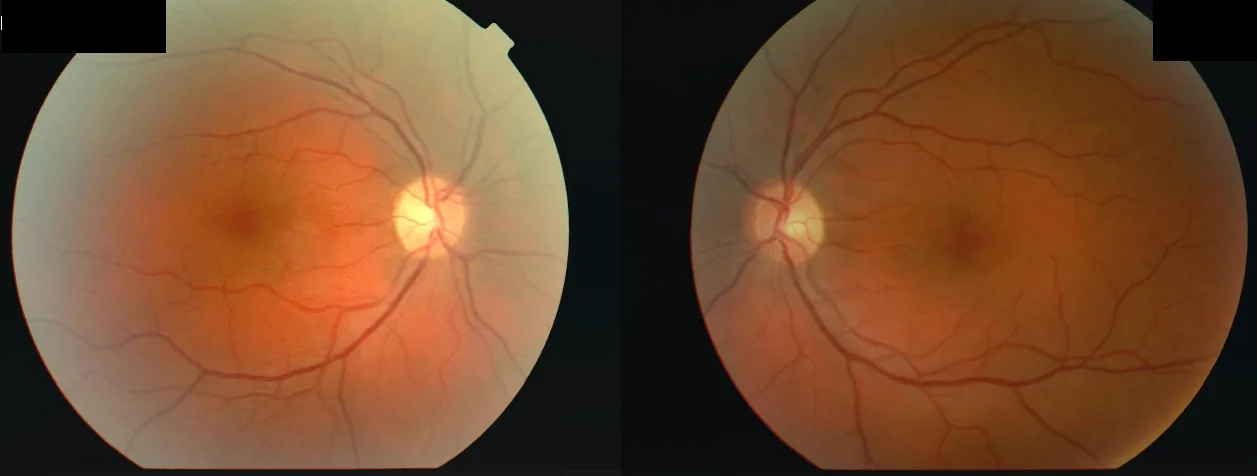
呈急性發病模式,以下症狀具有特徵性:
出現以下徵象時懷疑非典型視神經炎,進行詳細病因檢查。
| 特徵 | MOG-ON | AQP4-ON | MS-ON | CRION |
|---|---|---|---|---|
| 性別比(男:女) | 1:1 | 1:7~9 | 1:3 | 1:1.7~2.3 |
| 雙眼性 | 31%~84% | 13%~82% | 極為罕見 | 有 |
| 視乳頭水腫 | 45%~92% | 7%~52% | 11%~14% | 輕度 |
| 眼痛 | 73%~92% | 28%~50% | 10%~46% | 有 |
| 最低視力 | 中度至重度 | 中度至重度 | 輕度至中度 | 多樣 |
| 恢復 | 良好 | 可能不良 | 良好 | 類固醇依賴 |
出處: Jeyakumar N, et al. Eye. 20241)
兒童視神經炎較成人更常表現為伴有視盤充血、腫脹的典型視乳頭炎,而非球後視神經炎。炎症不僅限於視盤,而是累及整個視神經。雙眼受累佔50%~75%,前部視神經炎型佔50%~75%。
Uhthoff徵是指體溫升高時出現一過性視力障礙的現象。患者在洗澡或運動後自覺視力下降或視物模糊。症狀在數分鐘內出現,1小時內消失。此徵象多見於多發性硬化相關的視神經炎,但其他視神經病變也有報告,並非多發性硬化特有。
抗AQP4抗體陽性視神經炎是一種難治性亞型,約佔特發性視神經炎的10%。與普通視神經炎相比,發病時視力更差,對類固醇治療反應不佳,復發更頻繁,且易轉為雙眼受累。診斷必須檢測血清抗AQP4抗體。
在懷疑自體免疫機制的特發性病例中,微膠細胞等發炎相關細胞浸潤視神經並引起發炎。反覆發炎會導致神經纖維累積性損傷,進而發展為視神經萎縮。
有假說認為病毒感染可觸發自體免疫反應,部分患者腦脊髓液中可檢測到麻疹、水痘、流感等病毒抗體。在兒童中,已知與伴有發燒、頭痛的急性瀰散性腦脊髓炎(ADEM)相關。
據報導,疫苗接種和感染可觸發MOGAD發病,推測機制包括旁觀者激活等導致免疫耐受破壞。1)
有COVID-19感染後或疫苗接種後發生視神經炎的報導。從疫苗接種到視神經炎發病的中位時間為18天,55例中14例MOG-IgG陽性。11)
視神經炎是臨床診斷。根據急性單眼視力下降、眼球運動痛、RAPD陽性、視野缺損的組合進行診斷。
典型ON和非典型ON的MRI表現區別如下。
| 特徵 | 典型ON(MS相關) | 非典型ON |
|---|---|---|
| 顯影模式 | 短節段顯影 | 長節段顯影(≥1/2) |
| 病變部位 | 前部(球後視神經) | 向後延伸(視交叉和視束) |
| 視神經鞘 | 無顯影增強 | 視神經鞘和眼眶脂肪顯影增強 |
| 特徵 | NMOSD-ON | MOG-ON | MS-ON |
|---|---|---|---|
| 受累模式 | 雙側 | 雙側 | 單眼 |
| 好發部位 | 顱內和視交叉 | 球後(前方) | 球後和管內 |
| 病變長度 | 長範圍 | 長範圍 | 短節段 |
| 視神經鞘增強 | 罕見 | 50%陽性 | 無報告 |
來源: Jeyakumar 20241); Cacciaguerra & Flanagan4)
測量視乳頭周圍視網膜神經纖維層(pRNFL)厚度。急性期可見pRNFL增厚(MOG-ON中位數164μm vs MS-ON 103μm)。慢性期出現pRNFL變薄,復發次數與pRNFL減少相關。pRNFL低於50μm閾值時,視野平均偏差顯著惡化。1)
可見P100潛時延長。該發現反映脫髓鞘。
若病程不典型,則檢測以下項目。
評估視神經炎是否為MS的首發症狀。通過證明中樞神經系統炎症性脫髓鞘病變的時間和空間多發性,並排除其他疾病來診斷。如果腦室周圍、皮質/近皮質、幕下和脊髓四個區域中至少兩個區域存在T2高信號病變,則可證明空間多發性。
| 分類 | 主要鑑別疾病 | 鑑別要點 |
|---|---|---|
| 脫髓鞘性 | MS相關視神經炎、NMO | 抗體檢測、MRI |
| 免疫介導性 | CRION、類肉瘤病、SLE | 類固醇依賴性、全身表現 |
| 感染性 | 梅毒、疱疹、結核 | 使用類固醇前必須排除 |
| 遺傳性 | Leber遺傳性視神經病變 | 年輕男性、雙眼、無痛→基因檢測 |
| 藥物性 | 乙胺丁醇、利奈唑胺 | MRI無顯影增強 |
| 血管性 | 非動脈炎性前部缺血性視神經病變 | 老年人、通常無痛、視盤部分蒼白水腫 |
| 兒童 | 急性瀰散性腦脊髓炎 | 伴有發燒、頭痛、意識障礙 |
有報告指出,診斷為球後視神經炎的病例實際上是眼窩淋巴瘤引起的壓迫性視神經病變。若出現非典型特徵,不應輕易使用類固醇,而應進行詳細檢查。9)
通常,成人進行的FA(螢光眼底造影)、CFF和動態視野檢查不適用於兒童;診斷依據眼底所見和頭部MRI。
在典型ON中,僅在視神經的短節段出現顯影增強。相反,非典型ON表現為視神經的長節段顯影增強(超過長度的一半)、向後延伸(至視交叉和視束)以及視神經鞘的顯影增強。這些MRI所見直接關係到病因的鑑別診斷。
特發性視神經炎的視力預後良好。超過90%的視神經炎病例通過觀察或全身類固醇給藥後視力改善。根據ONTT的長期結果,發病1年後的視力達到0.5以上者佔93%,達到1.0以上者佔70%以上。
對於矯正視力相對較好的特發性視神經炎,可口服甲鈷胺1500μg/日(仿單外使用)進行觀察。
典型ON
第一線治療:類固醇脈衝療法(甲基培尼皮質醇1000mg/日靜脈滴注×3天)。仿單外使用。
脈衝後:開始口服培尼皮質醇0.5mg/kg/日,然後每3-4天減量5-10mg。
首次無效時:間隔4-5天後進行第二次脈衝。
效果:縮短恢復期,但發病1年後的最終視力無顯著差異。
積極適應症:雙眼發病、高度視功能障礙、唯一功能眼、復發、MRI去髓鞘斑、患者強烈希望早期改善。
抗AQP4抗體陽性ON
急性期:類固醇脈衝療法(首選)。
無效時:間隔3-4天再次脈衝→仍無效→考慮血漿置換。
血漿置換:單純血漿置換 > 雙重膜過濾血漿置換 > 免疫吸附療法(按療效排序)。1療程5-6次。
維持療法:潑尼松龍5-10mg/日 + 硫唑嘌呤50-100mg/日。
注意:與特發性ON不同,口服類固醇預防復發很重要。
抗MOG抗體陽性ON(MOGAD)
急性期:類固醇脈衝療法高度有效。完全恢復50%,部分恢復44%。13)
復發傾向:類固醇依賴性很強,口服潑尼松龍減量期間(特別是低於10mg/日或停藥後2個月內)70%復發。14)
維持療法:IVIg(≥1g/kg/4週可顯著減少復發)。15) 利妥昔單抗可能不如AQP4-ON有效。
治療開始時機:通常在第二次發作後開始(因為>50%為單相性)。
CRION(慢性復發性炎症性視神經病)
急性期:甲基潑尼龍靜脈注射1mg/kg×3-5天。
中間期:口服潑尼松1mg/kg,逐漸減至最小有效劑量。
長期維持:硫唑嘌呤、甲氨蝶呤、環磷酰胺、黴酚酸酯是候選藥物。IVIG也是選擇之一。
注意:停藥會導致復發,因此需要長期持續治療。
標準劑量(1mg/kg/天)的口服潑尼松龍單藥治療在ONTT中與安慰劑或靜脈類固醇相比復發率更高,因此不推薦。
甲潑尼龍30mg/kg/天×3天。視力預後通常良好。
積極進行類固醇治療。如果對類固醇脈衝反應不佳,可選擇大劑量免疫球蛋白靜脈滴注或血漿置換療法。
合併MS的病例在視力改善後考慮預防復發的治療。與神經內科協作,考慮疾病修飾藥物(干擾素β、醋酸格拉替雷、芬戈莫德、那他珠單抗等)。
根據ONTT的結果,類固醇脈衝療法可縮短恢復時間,但對發病一年後的最終視力無顯著影響。特發性視神經炎中,93%未經治療的患者視力恢復至0.5以上。但抗AQP4抗體陽性病例對類固醇耐藥,需要包括早期血漿置換在內的積極治療。
由於CRION是一種停藥後復發的疾病,即使在症狀緩解後,通常也需要長期免疫抑制治療。在確定類固醇的最小有效劑量後,聯合使用非類固醇免疫抑制劑,並個體化設計治療方案。
在懷疑自體免疫機制的特發性病例中,微膠質細胞等發炎相關細胞浸潤視神經並引起發炎。
反覆經歷視神經發炎會導致神經纖維累積性損傷,進而發展為視神經萎縮。
抗AQP4抗體與補體結合,攻擊視神經內的膠質細胞——星狀膠質細胞,從而發病。視神經和視交叉的星狀膠質細胞高表達AQP4,容易成為攻擊目標。
MOG-IgG(主要是IgG1亞類)靶向CNS髓鞘表面的MOG。補體途徑的激活和抗體依賴性細胞吞噬參與脫髓鞘。然而,與AQP4-IgG相比,補體激活較弱。在MOGAD中,CD4陽性T細胞和巨噬細胞為主,而在MS中,CD8陽性T細胞佔優勢。1)4)
儘管MOG不在視網膜中表現,但MOG-ON會導致視網膜神經節細胞損傷。麩胺酸毒性和視神經乳頭血腦屏障的脆弱性被認為是其機轉。1)
IL-6增加血腦屏障通透性並促進漿母細胞分化的機轉也受到關注。
CRION最初被提出作為涵蓋類固醇反應性和復發性視神經炎的症候群。5) 隨後對CRION隊列的抗體檢測發現,高達22%為AQP4-IgG陽性,高達25%為MOG-IgG陽性。6)7)8) 因此,CRION被認為是一種包含MOG抗體相關視神經炎和AQP4抗體相關視神經炎等異質性病因的症候群診斷。
病毒感染觸發自體免疫反應的假說已被提出。有報導在一些ON患者的腦脊髓液中檢測到水痘帶狀皰疹病毒和單純皰疹病毒的DNA。在MOGAD中,疫苗接種或感染導致的免疫耐受破壞(旁觀者激活、分子模仿)被認為是可能的機轉。1)
針對AQP4陽性NMOSD,已出現具有1級證據的生物製劑。4)
這兩種藥物對AQP4陽性NMOSD均有確鑿證據,但對MOGAD的適應症尚未確立。
薩特利珠單抗(NCT05271409)和羅扎諾利昔單抗(NCT05063162)的第三期隨機對照試驗正在進行中。托珠單抗(IL-6受體抗體)的仿單外使用已被報導可預防復發長達29個月。1)
已有COVID-19感染後出現脫髓鞘性視神經炎的病例報導。Jossy等人(2022)報告了感染恢復期發生視神經炎的病例,所有患者經類固醇脈衝治療後視力恢復。10)
COVID-19疫苗接種後發生視神經炎的報導逐漸增多,從接種到發病的中位時間為18天。55例中14例MOG-IgG陽性,無AQP4-IgG陽性病例。11)也有SARS-CoV-2感染後出現MOG抗體相關視神經炎的病例報導。12)
隨著MOG-IgG和AQP4-IgG抗體檢測的普及,部分既往診斷為CRION的病例正被重新分類為MOGAD或NMOSD。未來,基於抗體譜的疾病概念重新定義有望推進。