典型的ON
第一選択: ステロイドパルス療法(メチルプレドニゾロン1,000mg/日点滴静注×3日間)。保険適用外。
パルス後: プレドニゾロン0.5mg/kg/日から内服開始し、3〜4日ごとに5〜10mgずつ漸減する。
1回目無効時: 中4〜5日で2回目パルスを施行する。
効果: 回復期間を短縮するが、発症1年後の最終視力に有意差はない。
積極的適応: 両眼発症・高度視機能障害・唯一機能眼・再発例・MRI脱髄斑あり・患者が強く早期改善を望む場合。

視神経炎は、何らかの原因で視神経が炎症を起こして視機能が低下する疾患である。感染性・非感染性(中毒性・遺伝性・圧迫性)の視神経症を除外した上で、自己免疫機序が原因と思われる特発性が大半を占める。
好発年齢は15〜45歳で女性に多く、単眼性の急性視神経症として発症する。数日から2週間程度まで視機能障害が進行し、その後5週間以内に回復傾向を示す。
| 病型 | 特徴 |
|---|---|
| 特発性(自己免疫機序) | 最多。基本的に単相性 |
| 抗AQP4抗体陽性(NMOSD関連) | 特発性の約10%。ステロイド抵抗性、男女比1:9 |
| 抗MOG抗体陽性(MOGAD) | 両側性・乳頭腫脹・長範囲病変。ステロイド応答性だが再発傾向 |
| MS関連 | MS患者の最大75%が生涯に1回以上ON経験 |
| CRION | ステロイド依存性・再発性。2003年Kiddらが提唱5) |
| 感染性 | 梅毒・ウイルス等。ステロイド前に除外必須 |
初診時に抗AQP4抗体を測定し、陰性の場合に特発性として扱う。
日本の年間発症率は成人10万人あたり1.6人。好発年齢は15〜45歳で女性が約7割を占める。世界的な有病率はおよそ10万人あたり1〜5人と推定されている。
MSとの関連は非常に深く、特発性視神経炎発症後15年間のMS移行累積確率は50%である。初回発症時の脳MRIで脱髄病変がなければ移行率は25%にとどまるが、病変が1つ以上あれば78%に達する。
小児では好発年齢が9〜10歳とされ、幼少なほど両眼性・重篤な視力障害を呈する。特に5歳以下で顕著である。小児MSへの移行率は安達ら約30%、溝田ら16%と報告されている。
MOGADの年間発症率は100万人あたり1.6〜4.8と推定される。1)
特発性視神経炎の約50%が15年以内にMSに移行するとされる。ただし、初回発症時の脳MRIで脱髄病変がなければ移行率は25%にとどまる。発症後は脳MRIによるリスク評価を行い、神経内科と連携した経過観察が重要である。
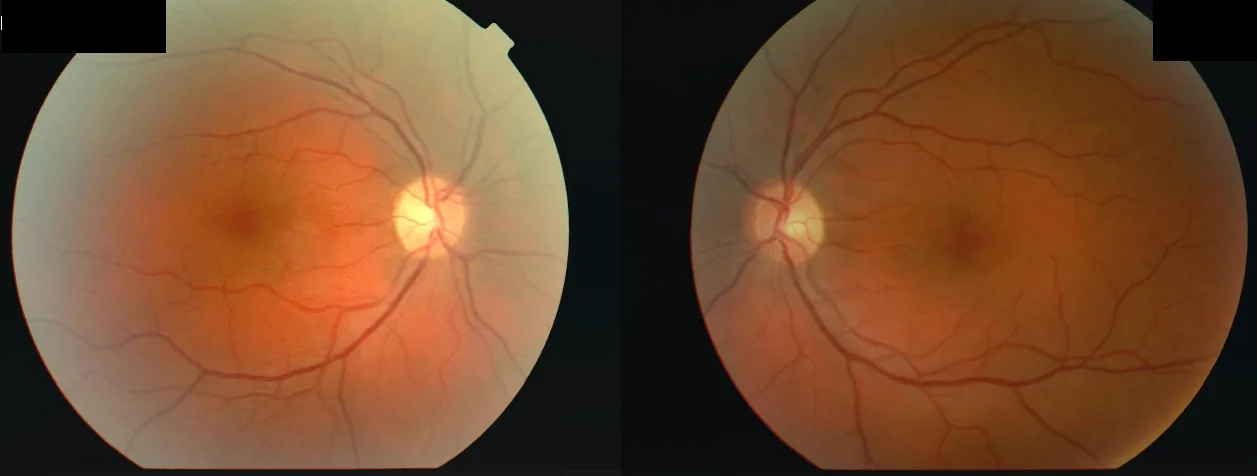
急性発症パターンを呈し、以下の症状が特徴的である。
以下の徴候がある場合は非定型視神経炎を疑い、詳細な原因検索を行う。
| 特徴 | MOG-ON | AQP4-ON | MS-ON | CRION |
|---|---|---|---|---|
| 男女比 | 1:1 | 1:7〜9 | 1:3 | 1:1.7〜2.3 |
| 両眼性 | 31〜84% | 13〜82% | 極めて稀 | あり |
| 乳頭腫脹 | 45〜92% | 7〜52% | 11〜14% | 軽度 |
| 眼痛 | 73〜92% | 28〜50% | 10〜46% | あり |
| 最低時視力 | 中等度〜重度 | 中等度〜重度 | 軽度〜中等度 | 多様 |
| 回復 | 良好 | 不良な場合あり | 良好 | ステロイド依存 |
出典: Jeyakumar N, et al. Eye. 20241)
小児視神経炎では成人でみられる球後視神経炎より、視神経乳頭の発赤・腫脹を伴う典型的な乳頭炎を呈することが多い。炎症の部位は乳頭のみの腫脹ではなく視神経全長に及ぶ。両眼性が50〜75%、前部視神経炎型が50〜75%を占める。
抗AQP4抗体陽性視神経炎は特発性視神経炎の約10%を占める難治性の病型である。通常の視神経炎に比べ発症時の視力がより不良で、ステロイド治療への反応が悪く、再発が多い。両眼性に移行しやすい点も異なる。診断には血清抗AQP4抗体の測定が必須である。
自己免疫機序が疑われる特発性では、ミクログリアなどの炎症関連細胞が視神経内に浸潤して炎症を引き起こす。繰り返し炎症を起こすと神経線維にダメージが蓄積し、視神経萎縮へ移行する。
ウイルス感染が自己免疫反応の引き金となる仮説が提唱されており、一部の患者の髄液中に麻疹・水痘・インフルエンザなどのウイルス抗体が検出される。小児では発熱・頭痛を伴うADEM(急性散在性脳脊髄炎)との関連が知られている。
MOGADの発症契機としてワクチン接種・感染が報告されており、バイスタンダー活性化などの免疫寛容破綻機序が推定されている。1)
COVID-19感染後・ワクチン接種後のON発症報告がある。ワクチン接種からON発症中央値は18日で、55例中14例でMOG-IgG陽性であった。11)
視神経炎は臨床診断である。急性片眼性視力低下、眼球運動痛、RAPD陽性、視野欠損の組み合わせで診断する。
定型ONと非定型ONではMRI所見が以下の点で異なる。
| 特徴 | 定型ON(MS関連) | 非定型ON |
|---|---|---|
| 造影パターン | 短分節の造影増強 | 長大な造影増強(1/2以上) |
| 病変部位 | 前方(球後視神経) | 後方(視交叉・視索)にも及ぶ |
| 視神経鞘 | 造影増強なし | 視神経鞘・眼窩脂肪の造影増強 |
NMOSD-ON・MOG-ON・MS-ONの画像的特徴の比較:
| 特徴 | NMOSD-ON | MOG-ON | MS-ON |
|---|---|---|---|
| 罹患パターン | 両側性 | 両側性 | 片眼性 |
| 好発部位 | 頭蓋内・視交叉 | 球後(前方) | 球後・管内 |
| 病変の長さ | 長範囲 | 長範囲 | 短い分節 |
| 視神経鞘増強 | 稀 | 50%で陽性 | 報告なし |
出典: Jeyakumar 20241); Cacciaguerra & Flanagan4)
乳頭周囲網膜神経線維層(pRNFL)厚を測定する。急性期はpRNFL肥厚(MOG-ON中央値164μm vs MS-ON 103μm)を認める。慢性期にはpRNFL菲薄化が生じ、再発数とpRNFL減少が相関する。pRNFL 50μm閾値以下では視野mean deviationが有意に悪化する。1)
P100潜時の延長を認める。脱髄を反映する所見である。
非典型的な経過を示す場合は以下を測定する。
視神経炎がMSの初発症状である可能性を評価する。中枢神経の炎症性脱髄病変の時間的および空間的多発性を証明し、他の疾患を除外することで診断する。脳室周囲・皮質直下・テント下・脊髄の4領域のうち2領域以上にT2高信号病変があれば空間的多発性を証明できる。
| 分類 | 主な鑑別疾患 | 鑑別のポイント |
|---|---|---|
| 脱髄性 | MS関連視神経炎、NMO | 抗体検査・MRI |
| 免疫介在性 | CRION、サルコイドーシス、SLE | ステロイド依存性、全身所見 |
| 感染性 | 梅毒、ヘルペス、結核 | ステロイド前に除外必須 |
| 遺伝性 | Leber遺伝性視神経症 | 若年男性・両眼性・無痛→遺伝子検査 |
| 薬剤性 | エタンブトール、リネゾリド | MRIで造影効果なし |
| 血管性 | 非動脈炎性前部虚血性視神経症 | 高齢者、通常無痛、乳頭部分蒼白浮腫 |
| 小児 | ADEM | 発熱・頭痛・意識障害を伴う |
球後視神経炎と診断された症例が眼窩リンパ腫による圧迫性視神経症であった報告があり、非定型の特徴がある場合は安易にステロイドを投与せず精査を行うべきである。9)
通常、成人で施行されるFA(蛍光眼底造影)・CFF・動的視野は小児には適しておらず、眼底所見と頭部MRIで診断する。
定型ONでは視神経の短い分節のみに造影増強を認める。一方、非定型ONでは視神経の長大な造影増強(長さの1/2以上)、後方への進展(視交叉・視索)、視神経鞘の造影増強といった所見を呈する。これらのMRI所見は原因疾患の鑑別に直結する。
特発性視神経炎の視機能予後は良好である。9割以上の視神経炎で経過観察もしくはステロイドの全身投与により視力は改善する。ONTTの長期成績では、発症1年後の視力が0.5以上となるものが93%、1.0以上となるものが70%以上である。
矯正視力の比較的よい特発性視神経炎では、メコバラミン1,500μg/日の内服(保険適用外)で経過をみてもよい。
典型的ON
第一選択: ステロイドパルス療法(メチルプレドニゾロン1,000mg/日点滴静注×3日間)。保険適用外。
パルス後: プレドニゾロン0.5mg/kg/日から内服開始し、3〜4日ごとに5〜10mgずつ漸減する。
1回目無効時: 中4〜5日で2回目パルスを施行する。
効果: 回復期間を短縮するが、発症1年後の最終視力に有意差はない。
積極的適応: 両眼発症・高度視機能障害・唯一機能眼・再発例・MRI脱髄斑あり・患者が強く早期改善を望む場合。
抗AQP4抗体陽性ON
急性期: ステロイドパルス療法(第一選択)。
無効時: 中3〜4日で再パルス→なお無効→血漿交換療法を考慮。
血漿交換: 単純血漿療法 > 二重膜濾過血漿交換療法 > 免疫吸着療法(効果の順)。1クール5〜6回。
維持療法: プレドニゾロン5〜10mg/日+アザチオプリン50〜100mg/日。
注意: 特発性ONと異なりステロイド内服による再発予防が重要。
抗MOG抗体陽性ON(MOGAD)
急性期: ステロイドパルス療法が高度に有効。完全回復50%、部分回復44%。13)
再発傾向: ステロイド依存性が強く、経口プレドニゾロン減量中(特に10mg/日未満または中止後2か月以内)に70%が再発。14)
維持療法: IVIg(≥1g/kg/4週間で有意に再発減少)。15) リツキシマブはAQP4-ONより効果が劣る可能性がある。
治療開始時期: 通常2回目の発作後に開始(単相性が50%以上のため)。
CRION(慢性再発性炎症性視神経症)
急性期: メチルプレドニゾロン静注 1mg/kg×3〜5日間。
中間期: 経口プレドニゾン1mg/kgから最小有効量まで漸減。
長期維持: アザチオプリン、メトトレキサート、シクロホスファミド、ミコフェノール酸モフェチルが候補。IVIGも選択肢。
注意: 治療中止で再発するため長期継続が必要。
標準用量(1mg/kg/日)の経口プレドニゾロン単独療法はONTTにおいてプラセボや静脈内ステロイドと比較して再発率が高かったため、推奨されない。
メチルプレドニゾロン30mg/kg/日×3日間を施行する。視力予後は一般的に良好である。
積極的にステロイド療法を行う。ステロイドパルスに反応が乏しい場合は免疫グロブリン大量点滴静注や血漿交換療法が選択肢となる。
MS合併例では視力改善後に再発予防のための治療を考慮する。神経内科と連携のうえ疾患修飾薬(インターフェロンβ、グラチラマー酢酸塩、フィンゴリモド、ナタリズマブ等)を検討する。
ONTTの結果では、ステロイドパルス療法は回復速度を短縮するが、発症1年後の最終的な視力には有意差を認めなかった。特発性視神経炎では無治療でも93%が0.5以上の視力に回復する。ただし抗AQP4抗体陽性例はステロイド抵抗性のため、早期の血漿交換療法を含む積極的治療が求められる。
CRIONは治療中止で再発する疾患であるため、症状の寛解後も長期的な免疫抑制療法の継続が必要となる場合が多い。ステロイドの最小有効量を特定した上で非ステロイド性免疫抑制薬を併用し、治療レジメンを個別に設計する。
自己免疫機序が疑われる特発性では、ミクログリアなどの炎症関連細胞が視神経内に浸潤して炎症を引き起こす。
繰り返し視神経の炎症を経験すると、神経線維への蓄積的ダメージにより視神経萎縮へ移行する。
抗AQP4抗体が補体と結合し、視神経内のグリア細胞であるアストロサイトを攻撃することにより発症する。視神経および視交叉のアストロサイトはAQP4を多く発現しており、標的となりやすい。
MOG-IgG(主にIgG1サブクラス)はCNS髄鞘表面のMOGを標的とする。補体経路の活性化と抗体依存性細胞貪食が脱髄に関与する。ただし補体活性化はAQP4-IgGと比較して弱い。MOGADではCD4陽性T細胞とマクロファージが主体であるのに対し、MSではCD8陽性T細胞が優勢である。1)4)
MOGは網膜に発現しないにもかかわらず、MOG-ONでは網膜神経節細胞の障害が生じる。この機序としてグルタミン酸毒性や視神経乳頭の血液脳関門の脆弱性が提唱されている。1)
IL-6が血液脳関門の透過性を増大させ形質芽球分化を促進する機序も注目されている。
CRIONは元来、ステロイド反応性で再発傾向のある視神経炎を包括する症候群として提唱された。5) その後のCRIONコホートの抗体検査で、最大22%がAQP4-IgG陽性、最大25%がMOG-IgG陽性であることが判明した。6)7)8) このことから、CRIONはMOG抗体関連視神経炎やAQP4抗体関連視神経炎を含む異質な病因群を包含する症候群的診断と考えられる。
ウイルス感染が自己免疫反応の引き金となるという仮説が提唱されている。一部のON患者の髄液中に水痘帯状疱疹ウイルスや単純ヘルペスウイルスのDNAが検出されたとの報告がある。MOGADではワクチン接種・感染による免疫寛容破綻(バイスタンダー活性化・分子模倣)が想定されている。1)
AQP4陽性NMOSDに対してLevel 1エビデンスを有する生物学的製剤が登場している。4)
これらはいずれもAQP4陽性NMOSDに対するエビデンスが確立されているが、MOGADに対する適応は未確立である。
サトラリズマブ(NCT05271409)、ロザノリキシズマブ(NCT05063162)のPhase 3 RCTが進行中である。トシリズマブ(IL-6受容体抗体)のoff-label使用では、最大29か月間の再発予防効果が報告されている。1)
COVID-19感染後に脱髄性視神経炎を発症する症例が報告されている。Jossyら(2022)は感染回復期に視神経炎を発症した症例を報告し、全例がステロイドパルス療法で視力回復を得た。10)
COVID-19ワクチン接種後のON発症報告が集積されており、接種からON発症中央値は18日。55例中14例でMOG-IgG陽性であり、AQP4-IgG陽性例はなかった。11) SARS-CoV-2感染後にMOG抗体関連視神経炎が発症した症例も報告されている。12)
MOG-IgGおよびAQP4-IgGの抗体検査の普及に伴い、従来CRIONと診断されていた症例の一部がMOGADやNMOSDに再分類される動向がある。今後、抗体プロファイルに基づく疾患概念の再定義が進むと考えられる。