非動脈炎性前部虚血性視神経症(NAION)

視神経症
1. 視神経症とは
Section titled “1. 視神経症とは”視神経症(optic neuropathy)は、視神経に何らかの障害が生じて視機能が低下する疾患群の総称である。視力低下・視野欠損・色覚異常・コントラスト感度低下のいずれか、または複数を呈する2)。
視神経は網膜神経節細胞(RGC)の軸索約120万本から構成される。眼球内で視神経乳頭として束ねられ、視神経管を経て視交叉に至る。視神経乳頭から視交叉前までの障害が「前部視路障害」であり、臨床的に問題となる視神経症の大半がこの部位に相当する2)。視交叉以降(視索・視放線・後頭葉)の障害は「後部視路障害」であり、視神経症ではなく「視路障害」として扱われる。
視神経は4区分に分けられる。眼球内部(乳頭部、約1 mm)は虚血性・炎症性視神経症が好発する。眼窩内部(約25 mm)は圧迫性・炎症性が多い。管内部(視神経管、約5〜8 mm)は外傷性や骨性圧迫が起きやすい。頭蓋内部(約10 mm)は下垂体腺腫や頭蓋咽頭腫による圧迫が多い。視神経乳頭を直接観察できる「前部視神経症」と、眼底が正常に見える「球後視神経症」の区別も重要である。球後視神経症では眼底に乳頭変化がないため、視力低下の原因として見落とされやすい。
視神経乳頭の血流は短後毛様動脈(SPC動脈)が主として担っている。SPC動脈は眼動脈の終枝であり、視神経乳頭前層部・篩状板・篩状板後部に血流を供給する。この部分の循環障害がNAIONおよびAAIONの主要な病態基盤となる3)。視神経内部は血液脳関門によって保護されているが、この保護機構が炎症性視神経炎や自己免疫疾患では破綻する2)。
病態の共通経路と視神経萎縮
Section titled “病態の共通経路と視神経萎縮”原因が異なっても、最終的には網膜神経節細胞および視神経軸索のダメージ→アポトーシス→視神経萎縮という共通経路をたどる。視神経萎縮(optic atrophy)は視神経症の終末像であり、乳頭の蒼白化として認識される。萎縮が確立すると視機能の回復は著しく限定的となる2)。
視神経軸索は直径0.2〜10 μmの有髄・無髄線維の混合体であり、p細胞(輝度・コントラスト担当)とm細胞(動き・輪郭担当)に大別される。視神経症では特にATP消費の激しいp細胞が障害されやすく、中毒性・栄養性視神経症での中心暗点の発生機序と関連する2)。
主要な視神経症の年間発症率(成人10万人あたり)を概観する。NAIONは2.3〜10.2(米国)と最多である3)。特発性視神経炎は1.6(日本成人)とされ13)、LHON(レーベル遺伝性視神経症)は日本の年間新規発症者が約117人(2014年調査)で希少疾患に相当する14)。AAION/GCAの推定年間発症率は50歳以上で10万人あたり0.36とされ、北欧系白人に多い(ノルウェーで10万人あたり約30人)。GCAの視覚合併症は10〜30%(最大70%の報告もある)に生じ、AAIONはその60〜90%を占める1)。MOGADの年間発症率は100万人あたり1.6〜4.8と推定される6)。
視神経症の分類体系
Section titled “視神経症の分類体系”視神経症は複数の視点から分類される。臨床的に最も使いやすい分類を以下に示す。
発症様式による分類
原因による分類
- 虚血性:NAION・AAION・PION
- 炎症性(視神経炎):特発性・MS関連・NMOSD関連・MOGAD関連・感染性
- 圧迫性:腫瘍・嚢胞・動脈瘤・甲状腺眼症
- 中毒性:エタンブトール・アミオダロン・アルコール等
- 栄養性:ビタミンB12/B1/葉酸/銅欠乏
- 遺伝性:LHON・ADOA・Wolfram症候群
- 外傷性:視神経管骨折・直接損傷
- 放射線性:遅発性虚血変性
局在による分類
視神経症の診断フレームワーク
Section titled “視神経症の診断フレームワーク”視神経症の診断は5つのステップで進める。
Step 1: 視神経機能障害の確認 RAPD・視力・色覚・視野を用いて視神経機能障害を客観的に確認する。
Step 2: 病変部位の局在 前部(乳頭変化あり)か球後(乳頭正常)か、眼窩内か管内か頭蓋内か。視野欠損パターンで局在を推定する。
Step 3: 片眼か両眼か・急性か慢性か 鑑別疾患の大幅な絞り込みが可能となる。
Step 4: 危険な病型の除外 GCA(ESR・CRP)、圧迫性(MRI)、感染性(梅毒・真菌)を優先して除外する。
Step 5: 特異的検査 病型に応じて抗AQP4抗体・抗MOG抗体・mtDNA検査・栄養検査を追加する。
2. 視神経炎との違い(概念の整理)
Section titled “2. 視神経炎との違い(概念の整理)”「視神経炎」と「視神経症」は臨床現場でしばしば混同されるが、下位概念と上位概念の関係にある。
非炎症性視神経症(虚血性・圧迫性・中毒性・遺伝性)を視神経炎と混同すると、ステロイドの誤投与が生じる危険がある。特に浸潤型アスペルギルス症はステロイドが禁忌であり2)、LHON急性期にステロイドを投与しても無効であるだけでなく、遅れた確定診断につながる。
視神経炎の主な臨床的特徴
Section titled “視神経炎の主な臨床的特徴”視神経炎(炎症性)には以下の特徴が非炎症性との鑑別に役立つ。
- 急性発症:数日〜2週間で進行し、その後5週間以内に回復傾向を示す。
- 眼球運動痛:約50%に認められる。虚血性・圧迫性・中毒性では通常ない。
- 好発年齢:15〜45歳(虚血性は通常50歳以上)。
- MRI所見:視神経に一致した造影効果(ガドリニウム増強T1)が典型的。
- 自然回復:特発性・MS関連では90%以上が1年後に視力0.5以上に回復(ONTT研究)4)。
- MS移行リスク:初回発症15年後に脳MRI病変なし→25%、あり→78%でMSに至る4)。
鑑別が難しい状況
Section titled “鑑別が難しい状況”以下では視神経炎と非炎症性視神経症の鑑別が困難になる。
- 50歳以上女性の急性片眼性視力低下:NAION vs. AQP4抗体陽性視神経炎(NMOSD)
- 若年者の急性両眼性視力低下:LHON vs. 両眼同時発症視神経炎 vs. 中毒性視神経症
- 乳頭腫脹を伴う片眼性視力低下:NAION vs. 前部視神経炎 vs. 乳頭血管炎
AQP4抗体陽性視神経炎は特発性視神経炎の約10%を占めるステロイド抵抗性の難治性疾患であり、通常の視神経炎よりも年齢が高めで女性(男女比1:9)が多い5)。AQP4抗体は視神経内のアストロサイトに発現するアクアポリン4チャネルを標的とし、補体依存性の細胞傷害を引き起こす5)。AQP4抗体陽性例と陰性例では治療戦略が根本的に異なるため、ステロイドパルス前に抗体検査をオーダーする。測定法はELISA法よりもcell-based assay(CBA)法の感度・特異度が高く、CBAが推奨される5)。
視神経炎においてステロイドパルスを施行する前には、感染症(B型肝炎・梅毒・HIV・真菌)を必ず除外しなければならない2)。B型肝炎ウイルスキャリアへの大量ステロイド投与は劇症肝炎を引き起こす危険がある。梅毒性視神経炎は抗菌薬をステロイドに優先して用いる。
3. 緊急度が高い病型
Section titled “3. 緊急度が高い病型”視神経症のうち特に緊急対応を要する病型を下表に示す。
| 病型 | 緊急度 | 見逃した場合の影響 |
|---|---|---|
| 動脈炎性前部虚血性視神経症(AAION/GCA) | 最緊急 | 僚眼失明(未治療では65%が10日以内に発症)1) |
| 急性圧迫性視神経症(腫瘍・嚢胞・血腫) | 緊急 | 進行性視神経萎縮・不可逆性視力障害 |
| 鼻性視神経症(浸潤型アスペルギルス症) | 緊急 | 死亡率94%の報告あり2) |
| 外傷性視神経症(視神経管骨折) | 緊急 | 早期治療で視機能温存の可能性 |
| 後部虚血性視神経症(PION) | 緊急 | 手術後・大量失血後に発症、不可逆性が多い |
GCA緊急対応フロー
Section titled “GCA緊急対応フロー”一過性黒内障(amaurosis fugax)は恒久的視力喪失の約30%に前駆症状として出現し、平均8.5日前に認められる1)。この時点でGCAを疑い積極的にステロイドを開始することが二次予防として極めて重要である。
4. 鑑別の入口
Section titled “4. 鑑別の入口”視神経症の鑑別は「急性か慢性か」「片眼か両眼か」「痛みの有無」「乳頭所見」の4軸で系統的に整理する。
急性か慢性か
Section titled “急性か慢性か”急性(数時間〜数日で最大障害に達する)
- NAION:起床時に気付く突然の視力低下が典型的
- AAION:急激な片眼視力低下、重度(視力20/200未満が60%以上)1)
- 外傷性:外傷直後〜数時間以内
亜急性(数日〜数週間)
慢性(月〜年単位で緩徐に進行)
- ADOA(常染色体優性視神経萎縮症):学童期発症の両眼性緩徐進行
- 慢性圧迫性:下垂体腺腫・眼窩腫瘍などによる
- 中毒性・栄養性:長期曝露・栄養不足で亜急性〜慢性に進行
片眼か両眼か
Section titled “片眼か両眼か”片眼性に偏る疾患
- NAION:原則として片眼性(両眼同時発症は極めてまれ)
- AAION:片眼性に始まり、未治療では65%が10日以内に僚眼へ波及1)
- 特発性視神経炎・MS関連:典型的に片眼性
- 圧迫性・外傷性・放射線性:片眼性が多い
両眼性に偏る疾患
- LHON:最初は片眼、数週〜数カ月で両眼化(最終的にほぼ100%両眼性)
- ADOA:両眼対称性で発症
- 中毒性・栄養性:両眼性が原則(片眼が完全正常なら中毒性は除外を考慮)2)
- NMOSD/AQP4-IgG陽性:重症・両眼性・再発性。60〜69%で少なくとも片眼に20/200以下の永続的障害5)
- MOGAD:両眼性発症が頻繁(MS関連・特発性では極めてまれ)6)
| 痛みあり | 痛みなし(無痛性) |
|---|---|
| 特発性視神経炎(眼球運動痛約50%)13) | NAION(眼球痛なし、頭痛・顎跛行はGCA全身症状) |
| MS関連視神経炎 | AAION(眼球痛なし、顎跛行・頭痛あり) |
| NMOSD関連(眼窩周囲痛) | LHON・ADOA(無痛性)14) |
| MOGAD(頭痛合併が多い)6) | 中毒性・栄養性(眼球運動痛なし) |
| 外傷性(受傷による痛み) | 圧迫性(通常無痛だが眼窩痛合併あり) |
乳頭所見による分類
Section titled “乳頭所見による分類”5. 診察と検査
Section titled “5. 診察と検査”必須の眼科的評価
Section titled “必須の眼科的評価”視神経症が疑われる場合、下記の評価を系統的に行う。
視力・色覚 矯正視力は障害の程度と経過評価の基本である。色覚(Ishihara・Farnsworth-Munsell 100 hue)は視神経症で早期から障害されやすく、視力が比較的保たれていても色覚異常が先行することがある。中毒性・栄養性視神経症では赤色感覚の鈍化が初期兆候となる2)。ADOA(常染色体優性視神経萎縮症)では後天性第三色覚異常(青黄色覚異常)が特徴的であり、Farnsworth-Munsell 100 hueテストで第三色覚異常軸を示す2)。
RAPDはスウィングライト法(交互照射法)で評価し、視神経機能障害の客観的指標となる。詐病や機能性視覚障害との鑑別にも役立つ2)。
OCT(光干渉断層計)
Section titled “OCT(光干渉断層計)”OCTは視神経症の病期評価と経過観察に不可欠な検査である。
| 評価指標 | 急性期所見 | 慢性期所見 |
|---|---|---|
| pRNFL(乳頭周囲RNFL厚) | 乳頭浮腫で肥厚(偽陽性注意) | 視神経萎縮で菲薄化 |
| GCL-IPL(神経節細胞+内網状層厚) | 変化少ない | 網膜神経節細胞障害を反映して菲薄化 |
| 視神経乳頭形状 | 陥凹が消失・縮小 | 萎縮後に固定 |
pRNFL菲薄化のパターンと病型鑑別
OCTのpRNFL菲薄化パターンは発症後数週〜数カ月以降から病型鑑別に有用である。
- 全周性高度菲薄化:NMOSD(AQP4抗体陽性型)が最重症。全周で高度に菲薄化する。
- 耳側優位菲薄化(papillomacular bundle):中毒性・栄養性・LHON・ADOA。中心暗点と対応。
- 上方または下方の扇状菲薄化:NAION。上方または下方の束状欠損に対応。
- MOGAD vs. MS関連:MOG-ON後のpRNFL菲薄化はMS関連より高度6)。
- 緑内障との鑑別:緑内障では乳頭形状変化(陥凹拡大)が先行し、GCL菲薄化パターンも異なる。
視野検査(ハンフリー視野計)
Section titled “視野検査(ハンフリー視野計)”視野欠損パターンは障害部位の解剖学的推定に直結する。
| 視野欠損パターン | 主に疑う疾患 | 解剖学的対応 |
|---|---|---|
| 中心暗点・盲点中心暗点 | 中毒性・栄養性・LHON・ADOA・特発性視神経炎2) | 乳頭黄斑線維束(PMB)障害 |
| 水平性欠損(下耳側〜下方) | NAION(束状線維欠損)3) | 乳頭部上半または下半の虚血 |
| 両耳側半盲 | 視交叉圧迫(下垂体腺腫・頭蓋咽頭腫) | 視交叉中央交叉線維 |
| 同名半盲(同側) | 視交叉後(視索・視放線・後頭葉)病変 | 中枢視路 |
| 接合部暗点 | 視交叉前端部病変、鼻性視神経症の一型 | 乳頭黄斑線維束+対側上耳側 |
| 全般的感度低下 | NMOSD関連・重症視神経炎後5) | 広範な視神経線維障害 |
| Mariotte盲点拡大(視力正常) | 乳頭ドルーゼン・乳頭血管炎・視神経周囲炎 | 乳頭周囲のみ |

血液・髄液検査
Section titled “血液・髄液検査”急性視神経症の初期評価として推奨される検査を示す。
| 検査項目 | 目的 | 臨床的意義 |
|---|---|---|
| ESR・CRP・血小板 | GCA(AAION)の除外 | 最優先。CRPのほうがESRより特異度が高い1) |
| 抗AQP4抗体(cell-based assay) | NMOSD診断 | ELISA法はCBA法より感度・特異度が低い5) |
| 抗MOG抗体(cell-based assay) | MOGAD診断 | 生来のMOG分子を認識するCBAが必須6) |
| 梅毒反応(TPHA・RPR)・HIV | 感染性視神経炎の除外 | ステロイド前に必ず確認 |
| ビタミンB12・B1・葉酸・銅 | 栄養性視神経症の評価 | 肥満外科手術後・ヴィーガン食で特に重要 |
| ミトコンドリア遺伝子(mt11778・mt14484・mt3460) | LHON診断 | 3変異で全症例の95%以上をカバー14) |
| β-Dグルカン・真菌培養 | 浸潤型アスペルギルス症疑い | 浸潤型では上昇しやすい2) |
| ACE・リゾチーム・胸部CT | サルコイドーシス除外 | — |
| ANA・dsDNA・ANCA | 全身性自己免疫疾患(SLE・血管炎)関連 | — |
髄液検査の適応 感染性髄膜炎・脳炎疑い、NMOSD/MOGADの診断補助(CSF細胞増多・IgG index上昇)、MS診断補助(髄液オリゴクローナルバンド)が適応となる。NMOSDでは最大50 cells/μL以上の顕著な細胞増多を来すことがある6)。
| 検査 | 主な評価内容 | 特記事項 |
|---|---|---|
| 眼窩MRI(脂肪抑制T2/造影T1) | 視神経炎症・浮腫・腫瘤・造影効果 | 視神経炎では造影効果あり。LHON急性期は造影なし14) |
| 頭部MRI(FLAIR) | 脱髄病変(MS・NMOSD)・頭蓋内病変 | MS診断のMcDonald基準で使用 |
| CT(骨条件) | 視神経管骨折(外傷)・副鼻腔病変・石灰化(ドルーゼン) | 外傷・鼻性疾患で必須 |
| 頭部超音波(カラードプラ) | GCA診断のハロー徴候 | 感度68%、特異度91%(両側陽性で100%)1) |
| PET-CT(FDG) | GCA大血管病変の評価 | 感度92%、特異度85%(GAPS試験)1) |
| 眼窩超音波 | 視神経乳頭ドルーゼンの石灰化確認 | — |
急性視神経症では原則として眼窩MRIが必要である。圧迫性病変の除外が最優先であり、視神経に一致した造影増強(炎症性)か、圧排・変形(圧迫性)かで治療方針が大きく変わる2)。造影MRIで視神経炎症所見がなければ中毒性・遺伝性・栄養性を考慮する。LHON急性期には炎症所見はなく、蛍光眼底造影でも乳頭からの蛍光漏出を認めない点が炎症性視神経炎との重要な鑑別点である14)。MRI禁忌の場合はCTで副鼻腔・眼窩・視神経管の評価を行う。
視覚誘発電位(VEP)の活用
Section titled “視覚誘発電位(VEP)の活用”視覚誘発電位(VEP)は脱髄性視神経炎のマーカーとして有用である。P100潜時の延長(正常130 ms以内)は脱髄を示唆し、MS関連・特発性視神経炎では回復後も延長が残存することが多い13)。振幅の減少は軸索障害(中毒性・虚血性)で顕著に認められる。中毒性視神経症ではP100潜時の遅延はなく、振幅のみ減少する点が脱髄性との鑑別に役立つ13)。フリッカー値(CFF: critical flicker frequency)の低下も視神経症の機能障害を反映し、NMOSD関連視神経炎では顕著な低下を示す13)。
6. 原因別の特徴
Section titled “6. 原因別の特徴”主要な視神経症を原因別に分類し、各病型の特徴をまとめる。
6-1. 虚血性視神経症
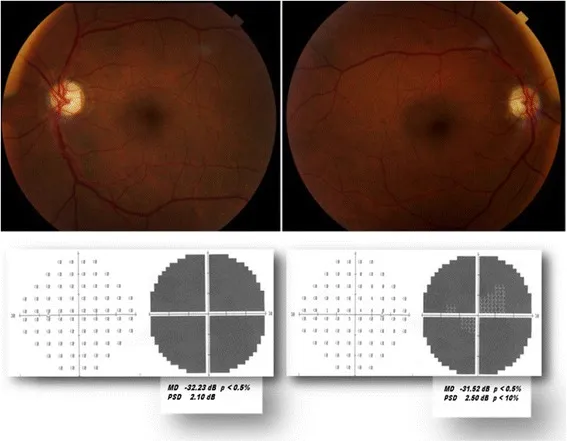
Section titled “6-1. 虚血性視神経症”非動脈炎性前部虚血性視神経症(NAION)
Section titled “非動脈炎性前部虚血性視神経症(NAION)”NAIONは成人の急性視神経症の中で最も多い病型であり、50歳以上に多く発症する3)。短後毛様動脈(SPC動脈)の急性循環不全により視神経乳頭部に虚血性梗塞が生じる。
- 疫学:米国での年間発症率は10万人あたり2.3〜10.23)。50歳以上が大半だが、50歳未満での発症も増加傾向にある。
- リスク因子:高血圧・糖尿病・高脂血症・睡眠時無呼吸症候群・disc at risk(C/D比0.2未満の小乳頭)。disc at riskは僚眼の約80%に認められる3)。
- 症状:無痛性・急性の片眼性視力低下で起床時に気付くことが多い。RAPDが病側で陽性。
- 乳頭所見:発赤腫脹(下方優位の扇状)。出血を伴うこともある。
- 視野:水平性線維束欠損(下耳側欠損が典型)。
- 治療:急性期に有効な治療法は確立されていない。血管危険因子の管理、睡眠時無呼吸症候群の治療が再発予防の中心。
- 近年の注目点:セマグルチド(GLP-1受容体作動薬)使用者でのNAIONリスク上昇が2024年の観察研究で報告された。ただし因果関係は確立しておらず、処方判断では糖尿病・肥満治療上の利益との比較が必要である7)。
動脈炎性前部虚血性視神経症(AAION/GCA)
Section titled “動脈炎性前部虚血性視神経症(AAION/GCA)”AAIONは前部虚血性視神経症全体の5〜10%を占めるが、最緊急の視神経症である1)。視神経乳頭を栄養する短後毛様動脈の血管炎が本態であり、原疾患の90%以上が巨細胞性動脈炎(GCA)である。
- 疫学:50歳以上(特に75歳以上)の高齢女性に多い(男女比1:3)1)。日本での発症率は10万人あたり1.47人と欧米に比べて極めて低い。
- 症状:急激な片眼重度視力低下(60%以上で視力20/200未満、20%以上で光覚なし)1)。一過性黒内障を約30%が先行して経験する。
- 全身症状:頭痛(65〜90%)・顎跛行(11〜45%)・頭皮圧痛・発熱・PMR様症状。
- 乳頭所見:チョーク様蒼白腫脹(pallid swelling)が特徴的。
- 検査:ESR・CRP高値(80%以上で亢進)1)。側頭動脈生検(感度・特異度95%以上)1)。
- 治療:高用量ステロイド(mPSL 500〜1,000 mg点滴3日間→プレドニゾロン経口漸減)1)。トシリズマブ(IL-6受容体拮抗薬)がステロイド節減に有効(GiACTA試験・RCTエビデンス)1)。
- 予後:罹患眼の視力回復はほぼ期待できないが、ステロイド治療は僚眼発症の予防に有効。
6-2. 炎症性視神経炎
Section titled “6-2. 炎症性視神経炎”特発性視神経炎
Section titled “特発性視神経炎”自己免疫機序による視神経の炎症性疾患であり、視神経炎の大半を占める13)。好発年齢は15〜45歳で女性が約70%を占め、日本の年間発症率は成人10万人あたり1.6人である13)。
- 症状:急性片眼性視力低下と眼球運動痛(約50%)。数日〜2週間進行し、5週間以内に自然回復傾向を示す。
- 視野:中心暗点・盲点中心暗点が多い。
- MRI:視神経に一致した造影増強(ガドリニウム)。
- 予後:90%以上が1年後に視力0.5以上に回復(ONTT研究)4)。
- 治療:mPSL 1,000 mg/日×3日間のステロイドパルス療法が回復を早める。ステロイド経口単独療法は再発率上昇のため施行しない(ONTT研究)4)。
- MS移行リスク:初回発症後15年間の累積発症率50%。脳MRI病変なし→25%、あり→78%4)。
MS関連視神経炎
Section titled “MS関連視神経炎”MSの初発症状として約30%に出現し、MS患者の生涯に1回以上の視神経炎経験は最大75%に上る8)。片眼性・眼球運動痛あり・球後病変が多い(眼底正常65%)。脳MRIの脱髄病変(T2/FLAIR高信号)が診断のkey。McDonald基準(2017年版・2024年改訂)による診断確定後は疾患修飾療法(DMT:インターフェロンβ・ナタリズマブ・フィンゴリモド・抗CD20薬等)で再発を予防する。
NMOSD(視神経脊髄炎スペクトラム障害)関連視神経炎
Section titled “NMOSD(視神経脊髄炎スペクトラム障害)関連視神経炎”AQP4-IgG陽性。女性(男女比1:9)・中年・アジア系に好発し、MS関連視神経炎より重症・両眼性・再発性である5)。少なくとも片眼で20/200以下の永続的視力障害をきたす割合が60〜69%に達する5)。眼窩MRIでは視神経の長大病変(視交叉関与が多い)を示す。治療は急性期ステロイドパルス→血漿交換療法→再発予防免疫療法(エクリズマブ・リツキシマブ・サトラリズマブ)5)。
MOGAD(MOG抗体関連疾患)関連視神経炎
Section titled “MOGAD(MOG抗体関連疾患)関連視神経炎”MOG-IgG陽性。年間発症率は100万人あたり1.6〜4.86)。両眼性発症が頻繁で乳頭腫脹が強く、前部病変優位である。MRIでは乳頭部腫脹・長範囲視神経病変・視神経周囲炎(optic perineuritis)が特徴的6)。MS-ON:AQP4-ON:MOG-ONの性差比較では男女比が3:1 / 7〜9:1 / 1:1と異なる6)。ステロイド応答性だが早期減量で再発しやすく、慎重な漸減が必要6)。
6-3. 圧迫性視神経症
Section titled “6-3. 圧迫性視神経症”腫瘍・動脈瘤・血腫・膿瘍・嚢胞・肥大した外眼筋などが視神経を圧迫して生じる。圧迫部位によって症状・視野欠損パターンが大きく異なる。
- 眼窩先端部:甲状腺眼症(甲状腺視神経症は甲状腺眼症の3〜8.6%に合併し、70%が両眼性)、眼窩腫瘍(良性では特発性眼窩炎症20%・多形腺腫13%・血管腫13%が上位。悪性では悪性リンパ腫が最多)9)。
- 視交叉部:下垂体腺腫(成人で最多、両耳側半盲)、頭蓋咽頭腫(小児で最多)。
- 鼻性視神経症(特記):副鼻腔真菌症(アスペルギルス・ムコール)の浸潤型は死亡率94%の報告がある2)。ステロイドが一時奏功するため球後視神経炎と誤診されやすく、知らずにステロイドを継続すると致命的となる。CT/MRIでの骨破壊像が診断の要であり、耳鼻科と緊急連携する。
治療の原則は原因病変の外科的除去である。圧迫解除が早いほど視機能の回復が期待でき、視神経萎縮が確立した後では回復は限定的となる。
6-4. 中毒性視神経症
Section titled “6-4. 中毒性視神経症”化学物質の曝露により前部視路が障害される疾患群である2)。両眼性・無痛性が原則であり、片眼が完全正常なら中毒性視神経症を除外すべきとされる2)。
- 原因物質:タバコ・アルコール・シンナー(薬剤:エタンブトール〈最も有名〉・アミオダロン・リネゾリド・シスプラチン・免疫抑制薬等)。
- 視野:特徴的に中心盲暗点または中心暗点(p細胞優位の障害)2)。
- 色覚:赤色感覚の鈍化が初期兆候。
- 眼底:初期は正常または軽度発赤→慢性期に乳頭耳側蒼白化・乳頭黄斑線維束欠損。
- RAPD:両眼対称性のため原則陰性。
- VEP:振幅の減少があり、P100潜時の遅延はない(潜時遅延は脱髄性視神経炎の特徴)13)。
- エタンブトール:用量依存性(15 mg/kgを超えると発症リスク上昇)。投与前のベースライン視機能検査と定期モニタリングが不可欠。
- 治療:原因物質の中止が基本。特効薬はない。
6-5. 栄養性視神経症
Section titled “6-5. 栄養性視神経症”ビタミンB群(B12・B1・B2・B9)および銅の欠乏による両眼対称性・進行性の視神経障害である。中毒性視神経症と同じスペクトラムに位置するが、栄養欠乏を原因とする点で区別される。現代のリスクは肥満外科手術後(生涯にわたるモニタリング必須)・ヴィーガン食・アルコール依存症である。症状・視野・眼底所見は中毒性と類似(中心暗点・無痛性・乳頭耳側蒼白化)。早期の栄養補充で回復が期待できるが、慢性例では不可逆的な障害が残る。
6-6. 遺伝性視神経症
Section titled “6-6. 遺伝性視神経症”LHON(レーベル遺伝性視神経症)
Section titled “LHON(レーベル遺伝性視神経症)”ミトコンドリアDNA(mtDNA)の点変異を原因とし、母系遺伝する急性ないし亜急性の視神経症である14)。3大変異(mt3460・mt11778・mt14484)が全症例の95%以上を占め、mt11778がアジアでは全症例の約90%を占める14)。
- 疫学:有病率1/31,000〜1/68,000。浸透率2.5〜17.5%で保因者の大半は発症しない14)。日本では年間新規発症者が約117人(2014年調査)。指定難病。
- 症状:若年男性に好発(男女比約93:7)。亜急性・無痛性の両眼性中心暗点(片眼先行後、数週〜数カ月で両眼化)。
- 急性期眼底:視神経乳頭の発赤・腫脹と乳頭近傍毛細血管の拡張・蛇行。蛍光眼底造影で乳頭からの蛍光漏出を認めない(炎症性視神経炎との重要鑑別)14)。
- 対光反射:他の視神経疾患に比べて保たれるか、障害されても軽微14)。
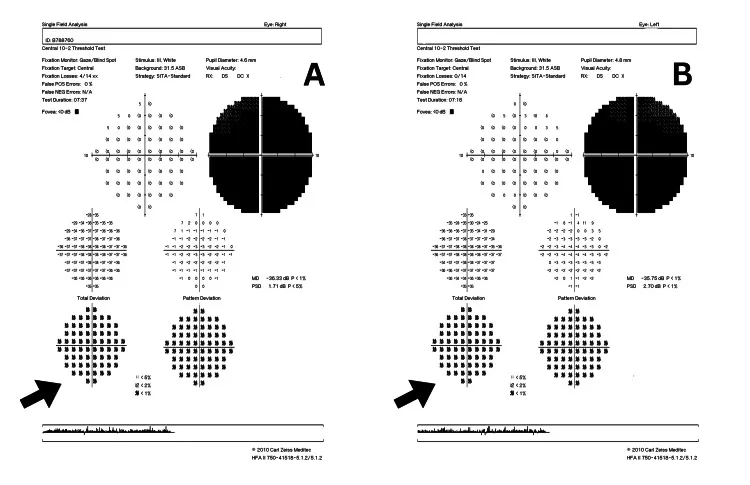
- 最終視力:mt11778では0.01前後が多い。mt14484は自然回復率が最も高い14)。
- 治療:イデベノン900 mg/日(欧州EMA承認)。LEROS試験ではCRR(有意義な視力回復)が46.0%(プラセボ対照)10)。ウェールズコホート試験では27カ月時点でCRR 86%を達成10)。遺伝子治療も第III相試験で有効性を示している11)。禁煙指導が発症・重症化予防に重要。
ADOA(常染色体優性視神経萎縮症)
Section titled “ADOA(常染色体優性視神経萎縮症)”OPA1遺伝子変異を主因とする最頻度の遺伝性視神経症。学童期に両眼性の原因不明の視力発達障害として発見される。後天性第三色覚異常(青黄色覚異常)が特徴的。OCTでは耳側〜下側象限優位なRNFL菲薄化を示す2)。現時点で有効な治療はなく、ロービジョンケアと遺伝カウンセリングが主体となる。
6-7. 外傷性視神経症
Section titled “6-7. 外傷性視神経症”頭部・眼窩への鈍的外傷後に生じる視神経損傷であり、視神経管内での間接外力による損傷が多い。受傷直後から急性の視力低下を来す。CTの骨条件で視神経管骨折を確認する。高用量ステロイドまたは視神経管減圧術の適応を検討するが、いずれもエビデンスは限定的である。
6-8. 放射線性視神経症
Section titled “6-8. 放射線性視神経症”頭頸部腫瘍・眼窩腫瘍への放射線治療後の遅発性虚血性障害である。血管内皮障害を主体とした機序で視機能が失われる。発症は照射後3カ月〜9年で、10〜20カ月に多く平均約18カ月とされる12)。総線量50Gy超または単回線量10Gy超でリスクが高まる。通常無痛性で予後不良である。確立した治療はなく、ステロイド全身投与・抗凝固療法・高圧酸素療法の効果は限定的である12)。MRIでは視神経に一致した造影増強が確認できる。
6-9. その他の特殊な視神経症
Section titled “6-9. その他の特殊な視神経症”後部虚血性視神経症(PION) 眼窩内後部または管内部の視神経虚血。大量出血・低血圧・脊椎手術・心臓手術後に発症する術後PIGNが代表的である。眼底所見は正常(乳頭変化なし)で急激な視力低下をきたす。対光反射はRAPD陽性となる。有効な治療法は確立されていない。
視神経网膜炎(neuroretinitis) 視神経乳頭浮腫と網膜の星芒状白斑(star figure)が特徴的な症候群。Bartonella henselae(ネコひっかき病)・梅毒・Leber特発性星芒状視神経網膜症などが原因。星芒状白斑は浮腫液が黄斑部でHenle線維層に沿って沈着したものであり、乳頭浮腫が消退する数週間後に出現する。自然寛解傾向があるが、感染症は原因に対する特異的治療を行う。
乳頭血管炎(papillophlebitis) 若年〜壮年者に生じる、視機能障害を伴わない片眼性乳頭浮腫と網膜静脈拡張蛇行を示す症候群。Mariotte盲点の拡大を認めるが矯正視力は正常。眼窩MRIは正常。予後良好で治療不要であるが、うっ血乳頭・視神経炎・虚血性視神経症との鑑別が重要である2)。
免疫チェックポイント阻害薬関連視神経症 がん免疫療法(ニボルマブ・ペムブロリズマブ等)の免疫関連有害事象(irAE)として視神経症が稀に生じる。ステロイドパルス療法で治療し、がん治療との継続可否をオンコロジストと協議する。
視神経症ワンライナーまとめ表
Section titled “視神経症ワンライナーまとめ表”| 疾患 | 側性 | 痛み | 乳頭所見 | 視野 | キーポイント |
|---|---|---|---|---|---|
| NAION | 片眼 | なし | 発赤腫脹(下方) | 水平束状欠損 | 起床時発症、disc at risk3) |
| AAION/GCA | 片眼→両眼 | なし(頭痛・顎跛行) | 蒼白腫脹 | 多様(重度) | 最緊急、ESR/CRP上昇1) |
| 特発性視神経炎 | 片眼 | あり(50%) | 腫脹または正常 | 中心暗点 | 若年女性、MS移行リスク13) |
| NMOSD関連 | 両眼化しやすい | あり | 腫脹または正常 | 多様(高度) | AQP4抗体陽性、難治性5) |
| MOGAD関連 | 両眼が多い | あり(頭痛) | 高度腫脹 | 多様 | MOG抗体、perineuritis6) |
| 圧迫性 | 片眼/両眼 | なし | 正常または萎縮 | 多様 | MRI必須9) |
| 中毒性 | 両眼 | なし | 正常→耳側蒼白 | 中心盲暗点 | 原因物質を問診2) |
| 栄養性 | 両眼 | なし | 正常→耳側蒼白 | 中心暗点 | B12/銅欠乏 |
| LHON | 両眼(片眼先行) | なし | 発赤/毛細血管拡張 | 中心暗点 | 若年男性、蛍光漏出なし14) |
| ADOA | 両眼 | なし | 蒼白 | 中心暗点 | 学童期、青黄色覚異常2) |
| 外傷性 | 片眼 | あり(外傷) | 正常 | 多様 | 視神経管骨折CT確認 |
| 放射線性 | 片眼/両眼 | なし | 正常→萎縮 | 多様 | 平均18カ月12) |
7. 治療の考え方
Section titled “7. 治療の考え方”視神経症の治療は原因に依存し、病型ごとに根本的に異なる。共通原則を下記に示す。
緊急処置が必要な状況
Section titled “緊急処置が必要な状況”- GCA/AAION:高用量ステロイド全身投与(当日開始)。検査結果を待たない1)。
- 急性圧迫性:手術的減圧(耳鼻科・脳外科との緊急連携)。浸潤型アスペルギルス症ではステロイドを中止し抗真菌薬に切り替える2)。
- 外傷性:視神経管減圧術の適応検討。
炎症性(視神経炎)の治療
Section titled “炎症性(視神経炎)の治療”ステロイドパルス療法(mPSL 1,000 mg/日×3日間)が急性期の回復速度を早める4)。経口ステロイド単独は特発性視神経炎において再発リスクを上昇させるため施行しない(ONTT研究)4)。NMOSD急性期はステロイドパルス→反応不十分例に血漿交換療法→再発予防免疫療法という段階的治療を行う5)。MOGAD視神経炎はステロイド応答性だが早期減量で再発するため慎重な漸減が必要6)。
虚血性(NAION)の治療
Section titled “虚血性(NAION)の治療”急性期に有効な治療法は確立されていない。血管危険因子(高血圧・糖尿病・高脂血症・睡眠時無呼吸症候群)の管理が主体であり、対側眼の発症予防が治療目標となる。セマグルチド(GLP-1受容体作動薬)についてはNAIONとの関連を示す観察研究があり、既往やリスクがある患者では注意深い説明と経過観察が望ましい7)。
遺伝性(LHON)の治療
Section titled “遺伝性(LHON)の治療”イデベノン900 mg/日は欧州EMAで承認されており、LEROS試験においてCRR 46%を達成した(プラセボ対照比較)10)。ウェールズコホートでは27カ月時点でのCRR 86%と実臨床での良好な成績が報告されている10)。遺伝子治療(レナドジーン・ノルパルボベク)が第III相試験で有効性を示し、今後の適応拡大が期待される11)。禁煙指導(喫煙は発症リスク因子)と適切なロービジョンケアが必須である14)。
中毒性・栄養性の治療
Section titled “中毒性・栄養性の治療”原因物質の中止または欠乏栄養素の補充が基本である。早期の介入で視機能回復が期待できるが、慢性例では不可逆的障害が残ることがある。エタンブトール視神経症は用量依存性のため、投与前のベースライン視機能検査と定期モニタリング(視力・色覚・視野)が不可欠である。
圧迫性の治療
Section titled “圧迫性の治療”原因病変の外科的除去が原則である。甲状腺視神経症では緊急または待機的な眼窩減圧術を行う。視神経萎縮が進行した後では外科的除去後の視力回復は限定的となるため、早期診断・早期治療が重要である。
| 病型 | 視力予後 | 回復の可否 |
|---|---|---|
| 特発性視神経炎 | 90%以上が1年後0.5以上4) | 回復良好 |
| NAION | 1/3改善、1/3不変、1/3悪化 | 部分回復 |
| AAION/GCA | 罹患眼の回復はほぼ期待できない | 僚眼予防が目標1) |
| NMOSD関連 | 重篤。少なくとも片眼が20/200以下60〜69%5) | 再発予防が重要 |
| LHON(mt11778) | 最終視力0.01前後が多い | 自然回復は一部のみ14) |
| LHON(mt14484) | 自然回復率が最も高い変異型 | 回復例あり14) |
| ADOA | 緩徐進行、重篤な失明には至らないことが多い | 進行抑制なし |
| 圧迫性 | 早期除去で回復可能 | 萎縮進行前が勝負 |
| 中毒性・栄養性 | 早期中止・補充で回復 | 慢性例では不可逆 |
| 放射線性 | 急性・高度で不可逆的な視力低下が多い12) | 治療法確立なし |
原因疾患の迅速な同定である。GCA疑いの場合は検査結果を待たずにステロイドを当日開始し、僚眼失明を予防する1)。圧迫性の場合は原因病変の外科的除去が視機能温存の唯一の方法であり、診断の遅れが不可逆的視神経萎縮につながる。炎症性(視神経炎)ではステロイドパルスが回復を早めるが、病型によって追加治療戦略が大きく異なる。特に抗AQP4抗体陽性の場合はステロイド単独では再発を繰り返すため、早期に再発予防免疫療法を導入することが視機能温存の鍵となる5)。
両者は「急性〜亜急性の無痛性視力低下」という初期症状が類似し、特にLHON急性期には乳頭腫脹を伴うため混同されやすい。最重要鑑別点は蛍光眼底造影による乳頭からの蛍光漏出の有無である。炎症性視神経炎では造影効果と蛍光漏出を認めるが、LHON急性期では蛍光漏出がない14)。また視神経炎には眼球運動痛が約50%に認められるが、LHONは無痛性である。ミトコンドリア遺伝子検査(mt11778・mt14484・mt3460)により確定診断が可能であり、外注検査で実施できる14)。LHON患者にステロイドを投与しても無効であるだけでなく、確定診断の遅れを招くため、若年男性の急性両眼性視力低下ではLHONを鑑別に含めることが必須である。
8. 関連記事(視神経症)
Section titled “8. 関連記事(視神経症)”鑑別すべき視神経疾患・腫瘍
Section titled “鑑別すべき視神経疾患・腫瘍”- Piccus R, Hansen MS, Hamann S, et al. An update on the clinical approach to giant cell arteritis. Eye 2023.
- Biousse V, Newman NJ. Diagnosis and clinical features of common optic neuropathies. Lancet Neurol 2016;15:1355–67.
- Salvetat ML, Pellegrini F, Spadea L, et al. Non-Arteritic Anterior Ischemic Optic Neuropathy (NA-AION): A Comprehensive Overview. Vision 2023;7:72.
- Beck RW, Gal RL. The Optic Neuritis Treatment Trial: a report on the visual function at 15 years. Ophthalmology 2008;115:1079–82.
- Wingerchuk DM, Banwell B, Bennett JL, et al. International consensus diagnostic criteria for neuromyelitis optica spectrum disorders. Neurology 2015;85:177–89.
- Jeyakumar N, Lerch M, Dale RC, Ramanathan S. MOG antibody-associated optic neuritis. Eye 2024.
- Hathaway JT, Shah MP, Hathaway DB, et al. Risk of nonarteritic anterior ischemic optic neuropathy in patients prescribed semaglutide. JAMA Ophthalmol. 2024;142:740-741. PMID: 38958939. doi:10.1001/jamaophthalmol.2024.2514.
- Thompson AJ, Banwell BL, Barkhof F, et al. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald criteria. Lancet Neurol 2018;17:162–73.
- Biousse V, Newman NJ. Compressive Optic Neuropathies. J Neuroophthalmol 2015;35 Suppl 1:S67–S74.
- Sanders FWB, Votruba M. Outcomes of idebenone therapy for Leber hereditary optic neuropathy in a cohort of patients from Wales. Eye 2025.
- Newman NJ, et al. Hereditary optic neuropathy: advances in treatment. Eye 2024.
- Danesh-Meyer HV. Radiation-induced optic neuropathy. J Clin Neurosci 2008;15:95–100.
- Toosy AT, Mason DF, Miller DH. Optic neuritis. Lancet Neurol 2014;13:83–99.
- Carelli V, Ross-Cisneros FN, Sadun AA. Mitochondrial dysfunction as a cause of optic neuropathies. Prog Retin Eye Res 2004;23:53–89.
