表在型

視神経乳頭ドルーゼン
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 視神経乳頭ドルーゼンとは
Section titled “1. 視神経乳頭ドルーゼンとは”視神経乳頭ドルーゼン(optic disc drusen; ODD)は、視神経乳頭(optic nerve head)内に蓄積した石灰化沈着物である。ムコタンパク質・ムコ多糖類からなる屈折性の石灰化物で構成され、細胞外物質の石灰化凝集体が軸索輸送(axoplasmic transport)の障害の結果として視神経乳頭に沈着・蓄積したものと考えられている2)。視神経乳頭表面に粒が見える表在型と、表面から視認できない埋没型の2型が存在する。
ODDは先天性疾患だが、幼児期には外見上目立たないことが多い。健診や他疾患を契機に眼底検査を施行して発見されることが大半である。有病率は検査法により異なり、検眼鏡では0.37%程度、眼底写真では0.12%程度である一方、enhanced depth imaging(EDI)を用いたspectral-domain OCTでは2.21%と報告されている4)。性差はなく、70%以上の症例で両眼性に生じるが左右非対称が多い2)。
ODDは「偽乳頭浮腫(pseudopapilledema)」の代表的な原因であり、特に埋没型はうっ血乳頭との鑑別に苦慮することがある。かつては良性の静的疾患と考えられていたが、近年では視野異常が70%以上に認められ緩徐ながら進行することが明らかとなっており、慢性進行性の視神経疾患としての認識が広まっている。
ODDの病変は視神経乳頭内に限局し、加齢黄斑変性の前駆病変であるBruch膜上の網膜ドルーゼンとは発生部位・組成・臨床的意義のすべてが異なる。関連疾患として、網膜色素変性症・網膜色素線条(angioid streaks)・アッシャー症候群・ヌーナン症候群・アラジール症候群が挙げられる。
不完全浸透を伴う常染色体優性遺伝が疑われている。家族にODDがある場合は眼科受診を推奨する。両眼性の割合が高いことも特徴である。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”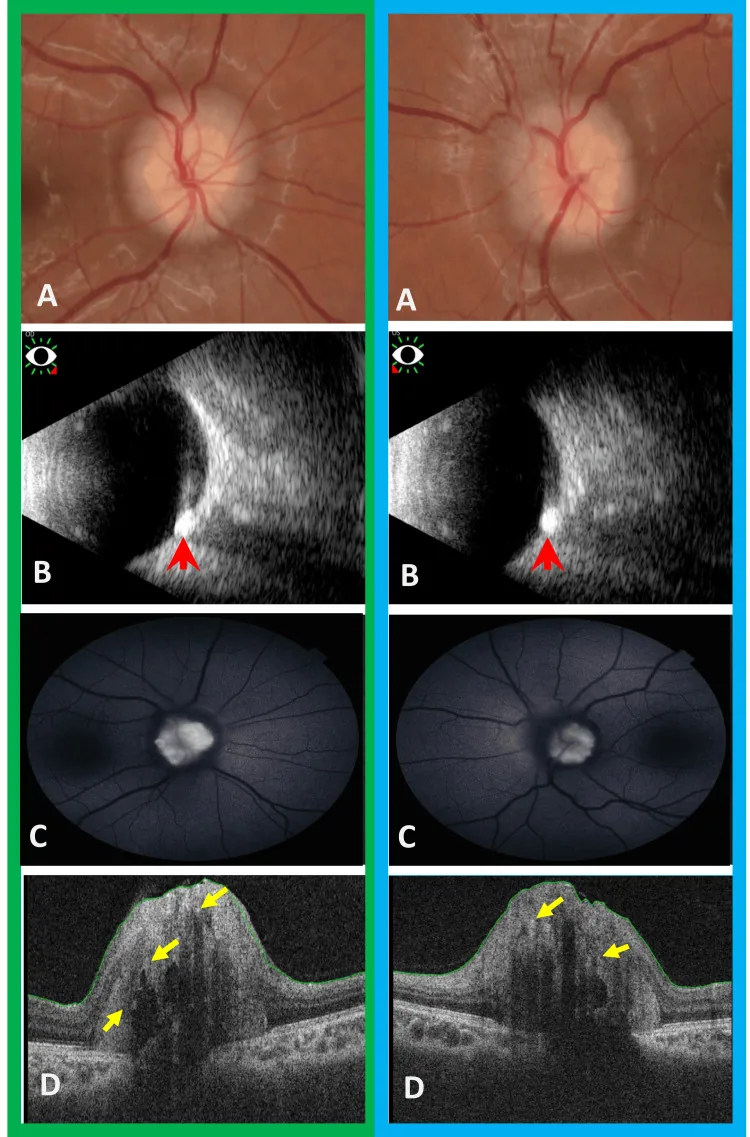
ODDの経過は通常無症状である。視野異常は緩徐に進行するため、多くの場合、患者自身は視野欠損を自覚しない。
- 一過性視覚消失:患者の約9%に認められる2)
- 視野異常:盲点拡大・弓状暗点・周辺性陥凹のパターンをとり、視神経線維走行に沿って出現する2)
- 突然の視力低下:まれにNA-AIONやCNVM合併時に急激な視力低下を自覚することがある(治療法の項参照)
視野異常(70%以上に出現)
Section titled “視野異常(70%以上に出現)”視野異常は以下の形態をとる。
- 視神経線維束欠損:神経線維走行に沿った弓状の視野欠損
- Mariotte盲点拡大:生理的盲点の拡大
- 周辺視野狭窄:求心性に進行する視野狭窄
- 水平半盲:まれだが報告がある
| パターン | 特徴 |
|---|---|
| 盲点拡大 | 最も一般的 |
| 弓状暗点 | 視神経線維走行に沿う |
| 周辺視野狭窄 | 進行例で出現 |
いずれも緩徐に進行するため、初診時にすでに視野異常が存在していても自覚症状がないことが多い。視野欠損の頻度は表在型で73%程度、埋没型で36%程度と報告されており、ドルーゼンの体積が大きいほど視野障害が強くなる傾向がある5)。年約1.6%の割合で視野狭窄が進行する。視野障害の主要因はドルーゼンによる視神経線維への直接圧迫(direct axonal compression)である2)。
表在型と埋没型の分類
Section titled “表在型と埋没型の分類”埋没型
外観:乳頭表面から視認できない。乳頭が全体的に隆起してみえる
診断:眼底検査だけでは判断困難。自発蛍光・CT・Bモードエコー・OCTによる確認が必要
鑑別:うっ血乳頭との鑑別が最重要課題
視野障害:表在型より高率に生じる
- lumpy-bumpy外観:視神経が凹凸のある外観を呈する
- 乳頭陥凹の消失:陥凹を欠き、隆起している
- 表在型では乳頭表面に白色のドルーゼンを認める
- 乳頭辺縁の不鮮明化(埋没型で特に顕著)
- 血管の異常:蛇行した血管走行や視神経毛様体シャント血管を認めることがある
- RAPD陽性:神経障害が非対称な場合に出現する
- 自発性静脈拍動:しばしば認められる
- 鼻側乳頭:ドルーゼンの最も一般的な発生部位は鼻側境界である
- 乳頭充血や網膜出血・白斑はみられない(うっ血乳頭との重要な鑑別点)
ODDには以下の疾患・病態との合併が報告されている。
- 網膜色素変性症:視機能低下を来す合併疾患
- 網膜色素線条(angioid streaks):脈絡膜新生血管のリスクとなる
- 小乳頭:乳頭ドルーゼンは小乳頭の合併が多いとされる
- 乳頭周囲CNVM:まれに合併し、急激な視力低下を生じうる
- NA-AION:突然の視野欠損・視力低下を自覚する場合に考慮する
突然の視野欠損・視力低下を自覚する場合には、視神経乳頭内虚血が原因と考えられる。この機序は虚血性視神経症(NAION)様の機序に類似しており、急性期の精査が必要である。
通常は良好な視力予後である。ただし年約1.6%の視野狭窄の進行があり、まれにNA-AIONやCNVM合併時に急激な視力低下をきたすことがある。定期的な検査が重要である。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”発症機序(軸索輸送障害仮説)
Section titled “発症機序(軸索輸送障害仮説)”ODDの形成機序として、軸索輸送障害を背景とした石灰化が広く受け入れられている7)。
- 視神経乳頭の篩状板前方で軸索内輸送が阻害される
- ミトコンドリアなどの細胞内小器官が視神経乳頭内に蓄積する
- ムコ多糖類・リン酸カルシウムなどの物質が沈着する
- これらが石灰化してドルーゼンを形成する
この過程は幼児期から始まり、年齢とともに石灰化が進行する。幼児期には埋没型として存在し、青年期〜成人期に表在型として可視化されることが多い。
解剖学的リスク因子
Section titled “解剖学的リスク因子”- 小乳頭(狭い強膜管・crowded OD):視神経線維が密集した状態で篩状板を通過するため、軸索輸送障害が生じやすい。乳頭ドルーゼンに小乳頭の合併が多いことは、この機序を支持している2)
- 乳頭陥凹の欠如:ODDに特徴的な解剖学的所見であり、病態と関連する
遺伝的素因と関連疾患
Section titled “遺伝的素因と関連疾患”両眼性が多く、家族内発症の報告もある。不完全浸透を伴う常染色体優性遺伝のパターンが示唆されているが、特定の遺伝子変異はまだ確定されていない。遺伝的素因が小乳頭形成や軸索輸送の脆弱性に関与している可能性がある。
関連疾患として以下が挙げられる。
- 網膜色素変性症
- 網膜色素線条(angioid streaks)
- アッシャー症候群(Usher syndrome)
- ヌーナン症候群(Noonan syndrome)
- アラジール症候群(Alagille syndrome)
4. 診断と検査方法
Section titled “4. 診断と検査方法”ODDの診断は複数の検査を組み合わせて行う。特に埋没型の診断と、うっ血乳頭との鑑別が実臨床での重要課題である。Optic Disc Drusen Studies(ODDS)Consortium はEDI-OCTによるODD診断のコンセンサス基準(篩状板前方の信号低下領域、内部のhyperreflective focusなど)を策定しており、現在の標準診断アプローチとして広く参照されている。
眼底検査・眼底写真
Section titled “眼底検査・眼底写真”視神経乳頭の陥凹欠如と隆起が基本所見である。表在型では乳頭表面の白色粒子で診断できる。
無赤色光眼底撮影
Section titled “無赤色光眼底撮影”無赤色光(グリーンフィルター)を用いて眼底写真を撮影すると、ドルーゼンがキラキラと輝いて観察される。表在型の確認に有用である。
各種画像検査
Section titled “各種画像検査”眼底自発蛍光(FAF)
OCT(EDI-OCT)
所見:視神経乳頭内の低反射卵形構造として同定される
意義:埋没型ドルーゼンに対して従来のOCTやBモードエコーよりも高い検出感度を示し、現在最も鋭敏な診断モダリティと位置付けられている
RNFL評価:早期の網膜神経線維層菲薄化の検出に有用。視野欠損の局在とRNFL欠損の分布が一致する3)
超音波検査(Bモード/Aモード)
所見:石灰化部位の高輝度エコー(高振幅スパイク)を検出する
特徴:ゲインを低下させても信号が維持される
意義:非侵襲的で繰り返し施行可能。CTが困難な場合(小児など)の代替手段として有用
- 蛍光眼底造影(FA):ODDでは原則として乳頭からの色素漏出を認めない。これに対し、うっ血乳頭や視神経乳頭浮腫では蛍光漏出が生じる。乳頭周囲の染色のみで漏出がないことが、偽乳頭浮腫(ODD)を示唆する所見である。FA初期の毛細血管拡張と後期漏出がある場合はCNVM合併を示唆する
- CT:MRIよりドルーゼン検出に優れる。視神経乳頭部をスライスすると石灰化が高吸収域として描出される。うっ血乳頭との鑑別において最も確実な画像検査の一つ
- PHOMS評価:OCTでの乳頭周囲視神経線維層の過反射隆起(peripapillary hyperreflective ovoid mass-like structure)の評価は偽乳頭浮腫の診断精度向上に寄与する
うっ血乳頭との鑑別(最重要)
Section titled “うっ血乳頭との鑑別(最重要)”| 所見 | 真の乳頭浮腫 | ODD(偽乳頭浮腫) |
|---|---|---|
| 充血 | あり | なし |
| 毛細血管拡張 | あり | なし |
| 出血 | あり | なし/まれ |
| 血管走行追跡 | 不明瞭 | 明瞭に追える |
ODDは緑内障の鑑別診断としても重要である。
5. 標準的な治療法
Section titled “5. 標準的な治療法”現時点では、ODDそのものを縮小・除去する確立された治療法は存在しない。診療の主体は以下の2つである。
- 合併症に対する管理・治療
- 定期的な視野モニタリングによる進行把握
経過観察・モニタリング
Section titled “経過観察・モニタリング”定期的な視野検査と画像評価が管理の核心である。
- 視野検査:Humphrey視野計などによる自動視野検査を定期的に施行し、視野欠損の進行を把握する
- OCT-RNFL:網膜神経線維層厚の経時的計測により、視神経線維の菲薄化(不可逆的な神経脱落)を早期に検出する
- 眼底写真:乳頭所見の変化を記録・比較する
受診間隔は疾患の重症度・視野異常の程度によって異なるが、定期的な通院が不可欠である。視野欠損に対する有効な治療法は確立されておらず、一部の症例では眼圧降下薬が検討されることがある。
CNVM合併時の治療
Section titled “CNVM合併時の治療”Markanらの症例報告では、ODDに伴う乳頭周囲CNVM合併の10代前半男児例にマルチモーダルイメージングが実施された。左眼BCVAは6/60で、他院で視神経炎と誤診されステロイド治療が施行されていた。抗VEGF3回投与で網膜下滲出液が消退し、3か月後にBCVA 6/9まで改善した。
CNVM合併時の治療選択肢は以下の通り。
- 抗VEGF療法:症例報告にて有効性が示されている
- 光線力学療法(PDT):選択肢の一つとして報告がある
- レーザー光凝固:従来からの選択肢
合併症への対応
Section titled “合併症への対応”| 合併症 | 対応 |
|---|---|
| 突然の視力低下・視野欠損 | 乳頭内虚血(NAION様機序)を考慮し、虚血性視神経症に準じた緊急精査 |
| 網膜色素変性症の合併 | 網膜電図(ERG)追加・網膜機能の評価 |
| 網膜色素線条の合併 | 脈絡膜新生血管の監視(FA・OCTアンギオグラフィーなど) |
| 乳頭周囲CNVM | 抗VEGF療法・PDT・レーザー光凝固の検討 |
ドルーゼン自体への有効な治療はない。合併症(CNVMなど)への対処が主体である。定期的な視野検査と乳頭形態変化の観察が重要である。急な視力低下・視野異常がある場合は速やかに受診する。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”軸索輸送障害と石灰化の過程
Section titled “軸索輸送障害と石灰化の過程”ODDの形成は、視神経乳頭の解剖学的特性と軸索輸送障害が組み合わさった結果として生じる。先天的に小さい・混雑した視神経乳頭(crowded optic disc)が形成の前提条件である2)。
視神経は篩状板を通過して眼球外に出る際、すべての網膜神経節細胞の軸索がこの狭い孔(強膜管)を通過する。小さな強膜管を持つ個体では、神経線維がより密に詰め込まれた状態になる。
- 輸送障害の発生:密集した軸索環境では、軸索内輸送(材料・エネルギーの神経線維内輸送)が篩状板前方で阻害されやすい
- 細胞内物質の蓄積:輸送が停滞すると、ミトコンドリアや小胞体などの細胞内小器官、ムコ多糖類が乳頭内に蓄積する
- 石灰化の進行:蓄積した物質にリン酸カルシウムが沈着し、徐々に石灰化してドルーゼンを形成する7)
視野障害の発生機序
Section titled “視野障害の発生機序”加齢とともにドルーゼンが増大すると、視神経線維への機械的圧迫が生じ、視野障害が進行する2)。視野障害の発生機序は以下の通りである。
- 機械的圧迫:ドルーゼンによる視神経線維への直接圧迫
- 虚血:視神経乳頭の血流障害
- 軸索流障害:軸索輸送の慢性的な阻害
ドルーゼンの大きさや局在と視野変化は必ずしも一致しない。CNVM(乳頭周囲脈絡膜新生血管膜)の発生機序は、ODD部位における脈絡膜血管への影響と乳頭周囲の血管構造障害と推察されている。
この石灰化過程は出生直後から始まると考えられており、幼児期には乳頭内に石灰化がまだ小さく埋没しているため外見上目立たない。青年期から成人期にかけて石灰化が進み、乳頭表面に露出して表在型として視認されるようになる。乳頭陥凹の欠如は、乳頭内のドルーゼン形成により解剖学的なスペースが圧迫されているためと解釈されており、ODDに特徴的な眼底所見の一つである。
慢性進行性の視神経障害として
Section titled “慢性進行性の視神経障害として”かつてODDは静的な良性病変と考えられていたが、視野異常が70%以上に認められ緩徐に進行することから、現在は慢性進行性の視神経疾患として位置づけられている。継続的な軸索圧迫・局所虚血が視神経線維の緩徐な脱落を引き起こすと考えられており、長期的な視野モニタリングの重要性が増している。
7. 最新の研究と今後の展望(研究段階の報告)
Section titled “7. 最新の研究と今後の展望(研究段階の報告)”EDI-OCTによる非侵襲的評価と埋没型検出精度の向上
Section titled “EDI-OCTによる非侵襲的評価と埋没型検出精度の向上”Enhanced depth imaging OCT(EDI-OCT)を用いた乳頭内ドルーゼンの可視化・形状評価は近年急速に発展している1)。ドルーゼンの深度・体積・数の定量化が可能となりつつあり、将来的には進行モニタリングのツールになることが期待されている。OCTの普及により埋没型ドルーゼンの検出精度も向上しており、PHOMS(乳頭周囲視神経線維層の過反射隆起)概念の導入によって偽乳頭浮腫の診断精度がさらに向上しつつある6)。
マルチモーダルイメージングによる包括的評価
Section titled “マルチモーダルイメージングによる包括的評価”眼底自発蛍光・OCT・OCT-A・FA・超音波(USG)を組み合わせたマルチモーダルイメージングが、ODD関連合併症の包括的評価に有用である。特にOCT-Aは乳頭周囲の異常血管膜(CNVM)の検出に有用であり、FA単独では見逃される症例の把握に貢献する。
国際的な用語・分類統一への動き
Section titled “国際的な用語・分類統一への動き”ODDの診断基準や用語は施設・国によって異なる部分があった。国際的なコンセンサス形成(ODDS Consortium等)が進んでおり、診断基準の統一化が今後の研究の精度向上に貢献すると考えられている。
抗VEGF療法の有効性
Section titled “抗VEGF療法の有効性”ODDに伴うCNVMへの抗VEGF療法の有効性が症例報告で示されており、知見の蓄積が期待される。症例数が少なく長期成績は不明だが、治療選択肢として検討されている。
視野欠損の進行予測因子
Section titled “視野欠損の進行予測因子”ODDの自然史における視野欠損の進行速度・進行予測因子については、長期前向き研究が不足している。ドルーゼンの大きさ・部位・数と視野予後の関連を検討する研究が今後の重要課題である5)。
NA-AION様急性視神経虚血との関連
Section titled “NA-AION様急性視神経虚血との関連”ODD(特に50歳未満)に合併する急性視神経虚血は非動脈炎性前部虚血性視神経症(NA-AION)様の病態を示すことが報告されている2)。乳頭内の構造的狭窄が虚血発症リスクを高める可能性が示唆されており、リスク因子の解明と予防戦略の確立が今後の課題となっている。
通常無症状のため定期的な眼科検診が基本となる。すでに診断されている場合は主治医の指示する間隔で視野検査を受けることが重要である。突然の視力低下・視野の急激な変化・閃光・光視症などを自覚した場合は速やかに眼科を受診する。
8. 参考文献
Section titled “8. 参考文献”-
Malmqvist L, Bursztyn L, Costello F, et al. The Optic Disc Drusen Studies Consortium recommendations for diagnosis of optic disc drusen using optical coherence tomography. J Neuroophthalmol. 2018;38(3):299-307. PMID: 29095768.
-
Costello F, Rothenbuehler SP, Sibony PA, Hamann S; Optic Disc Drusen Studies Consortium. Diagnosing optic disc drusen in the modern imaging era: a practical approach. Neuroophthalmology. 2020;45(1):1-16. PMID: 33762782; PMCID: PMC7946029.
-
Wandji BN, Dugauquier A, Ehongo A. Visual field defects and retinal nerve fiber layer damage in buried optic disc drusen: a new insight. Int J Ophthalmol. 2022;15(10):1641-1649. PMID: 36262850; PMCID: PMC9522567.
-
Mukriyani H, Malmqvist L, Subhi Y, Hamann S. Prevalence of optic disc drusen: a systematic review, meta-analysis and forecasting study. Acta Ophthalmol. 2024;102(1):15-24. PMID: 37144704.
-
Lee KM, Woo SJ, Hwang JM. Factors associated with visual field defects of optic disc drusen. PLoS One. 2018;13(4):e0196001. PMID: 29708976; PMCID: PMC5927402.
-
Sibony PA, Kupersmith MJ, Kardon RH. Optical Coherence Tomography Neuro-Toolbox for the Diagnosis and Management of Papilledema, Optic Disc Edema, and Pseudopapilledema. J Neuroophthalmol. 2021;41(1):77-92. doi:10.1097/WNO.0000000000001078. PMID:32909979; PMCID:PMC7882012.
-
Liu X, Yan Y. Advances in origin, evolution, and pathogenesis of optic disc drusen: a narrative review. Indian J Ophthalmol. 2025;73(5):637-647. PMID: 40272291; PMCID: PMC12121874.
