視神経周囲炎(OPN)
視神経周囲炎
1. 視神経周囲炎とは
Section titled “1. 視神経周囲炎とは”視神経周囲炎(Optic Perineuritis; OPN)は、視神経の髄膜(鞘)に炎症が限局する眼窩炎症性疾患の一種である。1883年にEdmunds & Lawfordが病理標本で視神経周囲の炎症浸潤を初めて報告した。
OPNには概念的に二つの捉え方がある。古典的な概念では、梅毒・サルコイドーシスによる髄膜炎を起因とする両側性の乳頭浮腫を指す。新しい概念では、視神経髄鞘に限局した炎症でMRIにリング状高信号を呈し、Mariotte盲点拡大以外の視機能低下がないものを指す。
分類は以下の通りである。
- 一次性(特発性)OPN:基礎疾患が同定できないもの。大多数を占める。
- 二次性OPN:全身性炎症・感染症・悪性腫瘍などの基礎疾患に随伴するもの。
発症平均年齢は40〜60歳(報告範囲15〜85歳)で、女性にやや多い傾向があるが確定的な性差は未確立である。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”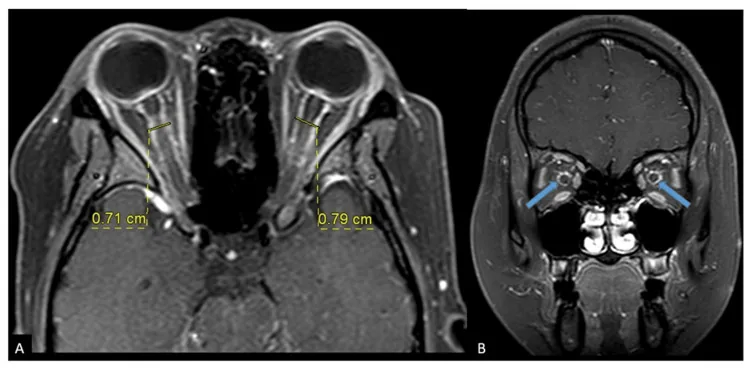
- 眼痛・眼球運動時痛:最も多い自覚症状。典型的なONより重度で持続的なことが多い。
- 視力低下:無症状から重度まで多様。霧視、暗点(「しみ」「斑点」)を訴えることがある。
- 発症経過:数週間単位で緩徐に進行する(ONの数日単位より遅い)。
- 眼窩症状:まれに眼球突出・眼球運動制限を呈する。
- 視神経乳頭浮腫:大部分の患者に認められる。正常乳頭を呈する症例もある。
- 中心視力:比較的保たれやすい。ただし症例によっては高度低下(NPL〜CF)に至る。
- 色覚・RAPD:異常の頻度は低い、または軽微である。
- 視野欠損:弓状暗点・傍中心暗点・中心暗点・周辺残存・水平半盲・Mariotte盲点拡大など多彩なパターンを呈する。
- 眼窩徴候:眼瞼下垂・眼筋麻痺・眼球突出がみられることがある。
- 片側性が多いが両側性の報告もある。1)5)7)
- 結節性多発動脈炎(PAN)合併例では発作性交代性失明を呈した報告がある。5)
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”OPNの大多数は特発性である。二次性OPNでは以下のような原疾患が同定される。
全身性炎症疾患
Section titled “全身性炎症疾患”- サルコイドーシス:古典的OPNの主要原因の一つ
- IgG4関連疾患
- 多発血管炎性肉芽腫症(GPA)
- 巨細胞性動脈炎
- ベーチェット病・SLE
- 炎症性腸疾患(クローン病含む)8)
- 結節性多発動脈炎(PAN)5)
- 結核2)7)・梅毒・HSV・VZV・COVID-191)
自己免疫・抗体関連
Section titled “自己免疫・抗体関連”- 白血病・リンパ腫(原発性・転移性)3)
薬剤性・医原性
Section titled “薬剤性・医原性”- 免疫チェックポイント阻害薬(ニボルマブ):irAEとして発症しうる。4)
- フローダイバーター留置後6)
TB-IRIS
Section titled “TB-IRIS”- 抗結核治療中の免疫再構築症候群(TB-IRIS)7)
特発性OPNとされた場合でも、基礎疾患が潜在している可能性があるため全身評価が推奨される。梅毒血清反応・ACE(サルコイドーシス除外)・ANCA・IgG4・MOG抗体・AQP4抗体・ESR・CRP・胸部X線が主な検査項目となる。基礎疾患が見つかれば原疾患の治療が再発予防にもつながる。
4. 診断と検査方法
Section titled “4. 診断と検査方法”MRIが診断の要である。ガドリニウム造影・脂肪抑制T1強調画像で以下の所見を確認する。
- tram-track sign(路面電車の線路状増強):軸位断で視神経鞘が二重線状に増強される所見。
- doughnut sign(ドーナツ状増強):冠状断で視神経周囲が環状に増強される所見。STIR冠状断も有用である。6)
ONとの鑑別においては、ONでは視神経自体が増強するのに対し、OPNでは視神経鞘周囲が増強する点が重要である。ただし、tram-track signはOPN特異的ではなく、視神経鞘髄膜腫・サルコイドーシス・白血病でも出現しうる。CTは軟部組織解像度が劣るため診断には不十分である。
OPNとONの主な鑑別点を以下に示す。
典型的視神経炎(ON)
眼科・神経生理検査
Section titled “眼科・神経生理検査”- 視力・視野検査:Humphrey・Goldmann視野計で多彩な欠損パターンを評価する。
- 色覚(Ishihara)・瞳孔検査(RAPD):頻度は低いが評価する。
- 光干渉断層計(OCT):急性期の網膜神経線維層肥厚、慢性期の菲薄化を確認できる。1)7)
血液・髄液検査
Section titled “血液・髄液検査”- OPN特異的な検査は存在しない。以下の検査で鑑別・原因精査を行う。
- 梅毒血清反応・ACE・ANCA・IgG4・MOG抗体・AQP4抗体
- ESR・CRP
- 基礎疾患が特定されない場合は、CNS感染症・悪性腫瘍除外のため腰椎穿刺を行う。古典的OPNでは髄液の細胞増多が認められることがある。
- 脱髄性視神経炎・MOG-ON・AQP4-ON
- 眼窩炎症性症候群(特発性・IgG4関連・サルコイドーシス)
- 感染症(結核・梅毒・ライム病・バルトネラ症)
- 腫瘍(髄膜腫・白血病・リンパ腫・転移)
- 後部強膜炎・ぶどう膜炎に伴う二次性乳頭浮腫
- うっ血乳頭・虚血性視神経症・糖尿病乳頭症・乳頭血管炎
5. 標準的な治療法
Section titled “5. 標準的な治療法”治療の基本方針は原疾患の治療と経過観察である。原疾患の治療が奏効すれば、通常視機能低下は生じない。
全身性副腎皮質ステロイド療法
Section titled “全身性副腎皮質ステロイド療法”高用量ステロイドが第一選択である。治療開始後数時間〜1日以内に症状が緩和するONより迅速な反応が特徴的である。
- 急性期(ステロイドパルス療法):メチルプレドニゾロン1,000mg/日 静脈内投与×3日間4)5)6)7)
- 維持期:経口プレドニゾロン(1mg/kg/日から緩徐に減量)7)
用量と再発率の関係は重要な臨床的事項である。
| 経口プレドニゾロン用量 | 再発率 |
|---|---|
| 低用量(30〜40mg/日) | 高用量群より再発率が高い |
| 高用量(60〜80mg/日) | 低用量群より再発率が低い |
二次性OPNの原疾患治療
Section titled “二次性OPNの原疾患治療”- 結核合併例:抗結核薬(オフロキサシン・イソニアジド・リファンピシン・ピラジナミド)+デキサメタゾン(CNS TB治療レジメン)2)
- PAN合併例:シクロホスファミド静脈内投与(1,000mg×7回)+高用量ステロイド+アザチオプリン 150mg5)
- 悪性腫瘍合併例:化学療法(髄腔内メトトレキサートなど)3)
- 免疫チェックポイント阻害薬関連例:原因薬の中止+ステロイド4)
難治例・その他の選択肢
Section titled “難治例・その他の選択肢”- 放射線療法・免疫抑制剤(アザチオプリン):ステロイド抵抗例に用いる。
- インドメタシン:Purvinらの症例で奏効の報告がある。
- 自然寛解の可能性:視機能が保持され疼痛が軽度の場合、経過観察も選択肢となる。文献上7例以上の自然寛解例が確認されている。8)
フォローアップ
Section titled “フォローアップ”定期的に視力・視野・色覚・瞳孔・眼底を評価する。症状が持続しなければ画像再検査は通常不要だが、再燃モニタリングが重要である。
OPNではステロイド減量時の再燃が多く、急激な中止は避けるべきである。経口プレドニゾロンでは低用量(30〜40mg/日)群が高用量(60〜80mg/日)群より再発率が高いことが知られており、緩徐な漸減が推奨される。自然寛解例も文献上報告されているが、それは視機能が保持されかつ疼痛が軽度の選択された症例に限る。
視機能が保持されており眼痛が軽度な症例では、経過観察で自然寛解に至った報告がある。文献上6例以上の自然寛解例が確認されており、クローン病合併例でも2週間での疼痛消失・3か月での完全寛解が報告されている。8)ただし視力低下が進行している場合や基礎疾患が疑われる場合は積極的治療が必要であり、自己判断で経過観察を選択することは危険である。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”OPNの本態は視神経周囲髄膜における免疫介在性炎症である。
病理学的変化
Section titled “病理学的変化”- 視神経周囲髄膜の肥厚・炎症浸潤(多形核白血球→リンパ球浸潤)→線維化
- 肉芽腫性炎症や局所壊死を示す症例もある
- 視力障害を伴う症例では、視神経の脱髄や梗塞を引き起こす血管炎変化を認める
- 炎症は主に神経鞘内に限局するが、視神経軸索も様々な程度で影響を受ける
原疾患別の発症機序
Section titled “原疾患別の発症機序”MOGAD関連OPNではMOG-IgG抗体による体液性機序が中心である。表面ミエリンへの自己抗体結合が補体活性化・細胞傷害を引き起こす。COVID-19後MOGADではサイトカインストームによる血液脳関門(BBB)の破綻が低力価抗体(1:20)のCNS侵入を可能にすると考えられている。IL-1β・IL-6・TNF・IFN-1の放出と脳微小血管内皮細胞のアポトーシスが病態に関与する。1)
TB-IRIS関連OPNでは抗結核治療による免疫再構築の過程で、結核菌(MTB)に対するTh1優位の過剰免疫応答が視神経周囲に炎症を惹起する。7)
IBD関連OPNでは全身性炎症性サイトカインの上方制御と抗原交差反応性が関与するとされる。8)
免疫チェックポイント阻害薬関連OPNではPD-1阻害による免疫チェックポイントの解除が免疫関連有害事象(irAE)として視神経周囲炎症を惹起する。4)
7. 最新の研究と今後の展望(研究段階の報告)
Section titled “7. 最新の研究と今後の展望(研究段階の報告)”MOGAD関連OPN
Section titled “MOGAD関連OPN”MOGADがOPNの重要な原因として認識されつつある。サルコイドーシスと並ぶ主要鑑別疾患として位置づけられる。
Leitãoら(2023)はCOVID-19重症感染後に両側性MOGAD-OPNを発症した56歳男性を報告した。MOG-IgG 1:20(低力価)陽性、ESR 42mm/h・CRP 8.2mg/dLと炎症反応上昇を認めた。メチルプレドニゾロン1,000mg×3日のステロイドパルス療法で視野が改善し、6か月後にはMOG抗体が陰性化した。1)
免疫チェックポイント阻害薬(ICI)関連OPN
Section titled “免疫チェックポイント阻害薬(ICI)関連OPN”irAEとしてのOPN症例が報告されており、ステロイド治療抵抗性を示す可能性が示唆されている。
Takadaら(2021)は非小細胞肺癌に対するニボルマブ治療7サイクル目後に右眼視力低下(20/2000)を呈した54歳男性を報告した。MRIでtram-track sign・doughnut signを確認しOPNと診断した。ステロイドパルス療法を2回施行したが視野改善は乏しかった。irAEとしてのOPN初報告例である。4)
フローダイバーター留置後OPN
Section titled “フローダイバーター留置後OPN”血管内治療後の新たな合併症としてOPNが報告されている。
Tanakaら(2022)は内頸動脈傍眼動脈瘤に対するフローダイバーター留置後にOPNを発症した2症例(49歳・57歳女性)を報告した。術後に視野障害が出現し、MRI STIR冠状断でdoughnut signを確認した。ステロイドパルス療法で改善を得た。術前STIR冠状断評価の重要性が強調された。6)
自然寛解の可能性
Section titled “自然寛解の可能性”従来「全例治療必須」とされてきたOPNだが、一部の症例では経過観察も選択肢となりうる。
Pickelら(2022)はクローン病合併の28歳女性における右眼視神経周囲炎の自然寛解例を報告した。視力 20/20を保持した状態で無治療経過観察を選択し、2週間で疼痛消失・3か月で完全寛解を達成した。文献レビューで6例の自然寛解例が確認され、視機能保持かつ軽度疼痛例では経過観察が選択肢になり得ると結論された。8)
トシリズマブ
Section titled “トシリズマブ”難治性OPNに対する静脈内トシリズマブ投与の有効性が報告されている(文献言及のみ)。8)
8. 参考文献
Section titled “8. 参考文献”-
Leitão M, Davila Siliezar P, Laylani N, Lee AG. Myelin oligodendrocyte glycoprotein antibody disorder (MOGAD) optic perineuritis following severe COVID-19 infection. Am J Ophthalmol Case Rep. 2023;32:101952.
-
Ismail MA, Shariffudin NS, Bt Abd Jalil NF, Yew TC, Wan Hitam WH. Concurrent tuberculous optic neuritis and optic perineuritis in a patient with human immunodeficiency virus (HIV). Cureus. 2024;16(3):e55867. doi:10.7759/cureus.55867.
-
Khan RR, Mahmood A, Kahlon S, Benyahia SA. Optic Perineuritis Secondary to CNS Involvement of Lymphoma. Cureus. 2024;16(12):e75818. doi:10.7759/cureus.75818. PMID:39822410; PMCID:PMC11735239.
-
Takada K, Fujiwara K, Ando E, Onishi K, Kuribayashi T, Mitsumune S, et al. Optic Perineuritis Associated with Nivolumab Treatment for Non-Small Cell Lung Cancer. Case reports in oncology. 2021;14(2):792-796. doi:10.1159/000516275. PMID:34248541; PMCID:PMC8255753.
-
Droger SM, Hensen JH, van Rooij LC. Optic perineuritis in polyarthritis nodosa. BMJ Case Rep. 2021;14(7). doi:10.1136/bcr-2020-237988. PMID:34289998. PMCID:PMC8296769.
-
Tanaka Y, Nagatsuka H, Miki Y, Tetsuo Y, Yabuzaki H, Nakayama S, et al. Two patients of visual disturbance and optic perineuritis after placement of a flow diverter. Radiology case reports. 2022;17(5):1487-1490. doi:10.1016/j.radcr.2022.01.085. PMID:35265246; PMCID:PMC8899115.
-
Fatimah-Halwani I, Wahab Z, Masnon NA, Wan Hitam WH, Shatriah I, Haron J. Bilateral Optic Perineuritis in Tuberculosis-Immune Reconstitution Inflammatory Syndrome. Cureus. 2022;14(8):e27600. doi:10.7759/cureus.27600. PMID:36059337; PMCID:PMC9435306.
-
Pickel L, Micieli JA. Spontaneous resolution of optic perineuritis in a patient with Crohn’s disease. Case Rep Ophthalmol. 2022;13:470-475. doi:10.1159/000525157.
