表浅型
外观:视盘表面可见白色至黄白色颗粒
眼底自发荧光表现:眼底自发荧光(FAF)显示高荧光
诊断:眼底检查可直接观察到,诊断相对容易
病程:婴儿期表现为埋没型,随着年龄增长钙化进展并暴露于表面

视神经乳头玻璃膜疣(ODD)是积聚在视神经乳头内的钙化沉积物。它们由含黏蛋白和黏多糖的屈光性钙化物构成,被认为是轴浆运输障碍导致细胞外物质钙化聚集体在视神经乳头沉积所致2)。分为两种类型:表浅型,乳头表面可见颗粒;埋藏型,表面不可见。
ODD是先天性疾病,但幼儿期常不明显。多数在体检或因其他疾病进行眼底检查时偶然发现。患病率因检查方法而异:检眼镜检查约0.37%,眼底照相约0.12%,而使用增强深度成像(EDI)的频域OCT报告为2.21%4)。无性别差异,70%以上病例为双眼发病,但常不对称2)。
ODD是假性视乳头水肿的常见原因,尤其是埋藏型与视乳头水肿的鉴别有时很困难。过去被认为是良性静止性疾病,但近年研究发现70%以上患者出现视野异常且缓慢进展,因此被重新认识为慢性进行性视神经疾病。
ODD病变局限于视神经乳头内,与年龄相关性黄斑变性前驱病变Bruch膜上的视网膜玻璃膜疣在发生部位、组成和临床意义上完全不同。相关疾病包括视网膜色素变性、血管样条纹、Usher综合征、Noonan综合征和Alagille综合征。
怀疑为常染色体显性遗传,伴不完全外显率。如果家族中有ODD患者,建议进行眼科检查。双眼发病比例高也是其特征。
ODD的病程通常无症状。视野异常缓慢进展,因此多数情况下患者自身并未察觉视野缺损。
视野异常表现为以下形态。
| 模式 | 特征 |
|---|---|
| 盲点扩大 | 最常见 |
| 弓形暗点 | 沿视神经纤维走行 |
| 周边视野狭窄 | 出现在进展期 |
所有这些都缓慢进展,因此即使在初诊时已存在视野异常,患者也常无自觉症状。视野缺损的发生率在表浅型约为73%,在埋藏型约为36%,且玻璃疣体积越大,视野损害越严重5)。视野狭窄以每年约1.6%的速度进展。视野损害的主要原因是玻璃疣对视神经纤维的直接轴突压迫2)。
表浅型
外观:视盘表面可见白色至黄白色颗粒
眼底自发荧光表现:眼底自发荧光(FAF)显示高荧光
诊断:眼底检查可直接观察到,诊断相对容易
病程:婴儿期表现为埋没型,随着年龄增长钙化进展并暴露于表面
埋没型
ODD已被报道与以下疾病/状况相关。
如果出现突然的视野缺损或视力下降,考虑由视盘缺血引起。其机制类似于缺血性视神经病变(NAION),需要紧急检查。
通常视力预后良好。但每年约有1.6%的视野狭窄进展,罕见情况下合并NA-AION或CNVM时可导致突然视力下降。定期检查很重要。
作为ODD的形成机制,基于轴浆运输障碍的钙化被广泛接受7)。
这一过程从幼儿期开始,随着年龄增长钙化逐渐进展。幼儿期常以埋藏型存在,青年期至成年期多表现为表面型而可见。
多为双眼发病,有家族内发病的报告。提示为不完全外显的常染色体显性遗传模式,但尚未确定特定基因突变。遗传易感性可能与小视盘形成或轴浆运输脆弱性有关。
相关疾病包括以下:
ODD的诊断需要结合多种检查。特别是埋没型玻璃膜疣的诊断以及与视乳头水肿的鉴别是临床实践中的重要课题。视盘玻璃膜疣研究(ODDS)联盟制定了基于EDI-OCT的ODD诊断共识标准(包括筛板前信号缺失区域、内部高反射灶等),目前被广泛参考作为标准诊断方法。
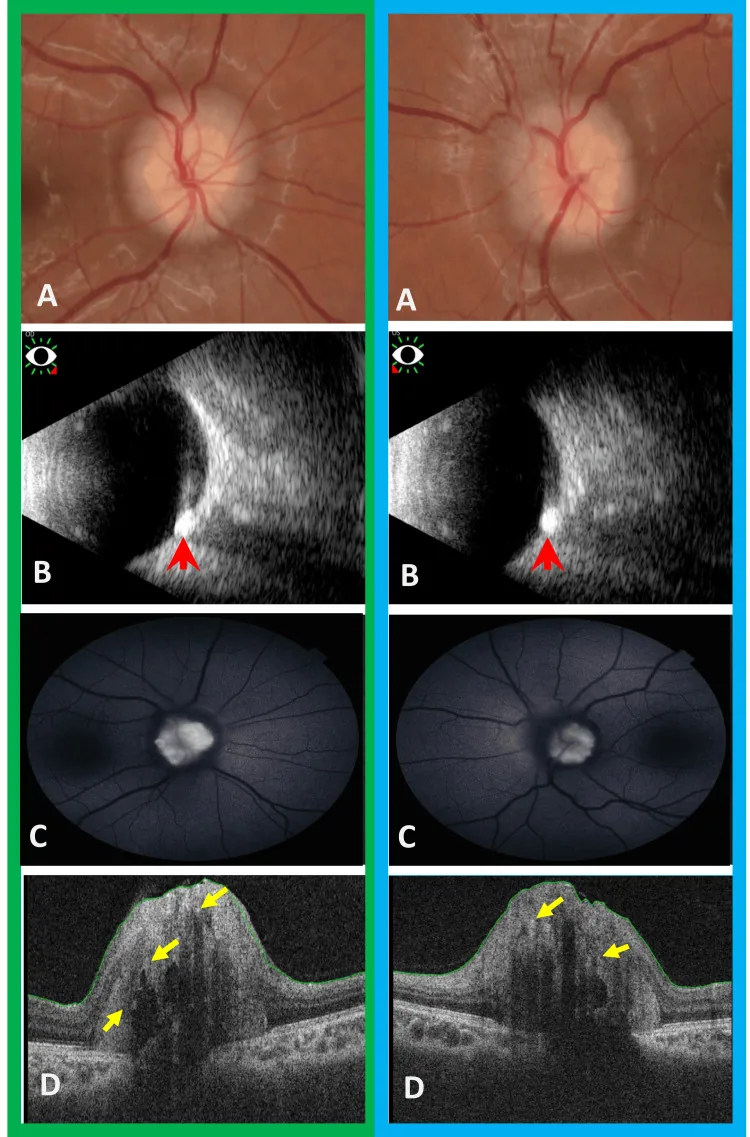
基本所见为视盘凹陷消失和隆起。表浅型可通过视盘表面的白色颗粒进行诊断。
使用无赤光(绿色滤光片)拍摄眼底照片时,玻璃膜疣会呈现闪闪发光的亮白色。这对于确认表浅型玻璃膜疣很有用。
眼底自发荧光(FAF)
表浅型:表现为高荧光,清晰可见
埋没型:可检测到自发荧光,有助于发现眼底检查无法看到的埋没型玻璃膜疣
鉴别诊断:由于淤血乳头无自发荧光,因此直接有助于鉴别。
OCT(EDI-OCT)
所见:被识别为视神经乳头内的低反射卵形结构。
意义:对埋没型玻璃疣的检测灵敏度高于传统OCT或B型超声,目前被认为是最灵敏的诊断方式。
RNFL评估:有助于早期检测视网膜神经纤维层变薄。视野缺损的定位与RNFL缺损的分布一致3)。
超声检查(B型/A型)
所见:检测钙化部位的高强度回声(高振幅尖峰)。
特征:即使降低增益,信号仍能维持。
意义:无创且可重复进行。在CT困难时(如儿童)可作为替代手段。
| 表现 | 真性视乳头水肿 | ODD(假性视乳头水肿) |
|---|---|---|
| 充血 | 有 | 无 |
| 毛细血管扩张 | 有 | 无 |
| 出血 | 有 | 无/罕见 |
| 血管走行追踪 | 不清晰 | 清晰可追踪 |
ODD在青光眼的鉴别诊断中也很重要。
埋藏型仅通过眼底检查无法看到,因此眼底自发荧光(FAF)是首选。如果发现与玻璃膜疣部位一致的自发荧光,即可作为诊断依据。CT显示钙化、B型超声和EDI-OCT有助于确诊。荧光眼底造影显示视盘无染料渗漏也是与视盘水肿鉴别的重要发现。
目前,尚无确切的治疗方法可以缩小或消除ODD本身。诊疗主要围绕以下两点:
定期视野检查和影像评估是管理的核心。
就诊间隔取决于疾病严重程度和视野异常程度,但定期随访至关重要。视野缺损尚无有效的治疗方法;部分病例可考虑使用降眼压药物。
Markan等人的病例报告中,对一名合并ODD相关视乳头周围CNVM的10岁出头男孩进行了多模态成像。左眼BCVA为6/60,曾在其他医院被误诊为视神经炎并接受激素治疗。三次抗VEGF注射后,视网膜下渗出消退,3个月后BCVA改善至6/9。
合并CNVM的治疗选择如下:
| 并发症 | 处理 |
|---|---|
| 突然视力下降或视野缺损 | 考虑视乳头内缺血(类似NAION机制),按照缺血性视神经病变进行紧急检查 |
| 合并视网膜色素变性 | 加做视网膜电图(ERG),评估视网膜功能 |
| 合并血管样条纹 | 监测脉络膜新生血管(荧光血管造影、OCT血管成像等) |
| 视乳头周围CNVM | 考虑抗VEGF治疗、PDT或激光光凝 |
玻璃膜疣本身没有有效的治疗方法。主要处理并发症(如CNVM)。定期进行视野检查和视乳头形态变化观察很重要。如果出现突然视力下降或视野异常,请立即就医。
ODD的形成是视盘解剖学特征与轴突运输障碍相结合的结果。先天性小且拥挤的视盘(crowded optic disc)是形成的前提条件2)。
视神经通过筛板穿出眼球时,所有视网膜神经节细胞的轴突都通过这个狭窄的孔(巩膜管)。具有小巩膜管的个体,神经纤维会更为密集地排列。
随着年龄增长,玻璃膜疣增大,对视神经纤维产生机械压迫,导致视野缺损进展2)。视野缺损的发生机制如下。
玻璃膜疣的大小和位置与视野变化并不总是一致。CNVM(视盘周围脉络膜新生血管膜)的发生机制推测与ODD部位对脉络膜血管的影响以及视盘周围血管结构破坏有关。
这一钙化过程被认为从出生后不久开始。在幼儿期,钙化灶较小且埋没在视盘内,外观上不明显。从青春期到成年期,钙化进展,玻璃膜疣暴露于视盘表面,成为表浅型而可见。视杯凹陷的缺失被解释为由于视盘内玻璃膜疣形成导致解剖空间受压,是ODD特征性的眼底表现之一。
ODD曾被认为是一种静态良性病变,但由于70%以上的患者出现视野异常且缓慢进展,现在被视为一种慢性进行性视神经疾病。持续的轴突压迫和局部缺血被认为会导致视神经纤维的缓慢丢失,因此长期视野监测的重要性日益增加。
使用增强深度成像OCT(EDI-OCT)对视盘玻璃疣进行可视化和形态评估近年来发展迅速1)。玻璃疣的深度、体积和数量的量化正在成为可能,有望成为未来进展监测的工具。OCT的普及也提高了埋藏型玻璃疣的检测精度,PHOMS(视盘周围高反射卵形团块样结构)概念的引入进一步提高了假性视盘水肿的诊断准确性6)。
结合眼底自发荧光、OCT、OCT-A、FA和超声(USG)的多模态成像对于ODD相关并发症的综合评估非常有用。特别是OCT-A有助于检测视盘周围脉络膜新生血管膜(CNVM),有助于发现仅通过FA可能遗漏的病例。
ODD的诊断标准和术语因机构和国家的不同而有所差异。国际共识形成(如ODDS联盟)正在推进,诊断标准的统一被认为有助于提高未来研究的准确性。
病例报告显示抗VEGF疗法对ODD相关的CNVM有效,期待更多证据的积累。尽管病例数较少且长期结果未知,但正在考虑作为治疗选择。
关于ODD自然病程中视野缺损的进展速度和预测因素,长期前瞻性研究尚不足。探讨玻璃疣的大小、位置、数量与视野预后关系的研究是未来的重要课题5)。
据报道,与ODD(尤其是50岁以下患者)并发的急性视神经缺血表现出非动脉炎性前部缺血性视神经病变(NA-AION)样病理状态2)。有研究表明,视盘内的结构性狭窄可能增加缺血发作的风险,阐明风险因素和建立预防策略是未来的课题。
通常无症状,因此定期眼科检查是基础。如果已经确诊,按照主治医生指示的间隔进行视野检查非常重要。如果自觉突然视力下降、视野急剧变化、闪光或闪光感,请立即就诊眼科。
Malmqvist L, Bursztyn L, Costello F, et al. The Optic Disc Drusen Studies Consortium recommendations for diagnosis of optic disc drusen using optical coherence tomography. J Neuroophthalmol. 2018;38(3):299-307. PMID: 29095768.
Costello F, Rothenbuehler SP, Sibony PA, Hamann S; Optic Disc Drusen Studies Consortium. Diagnosing optic disc drusen in the modern imaging era: a practical approach. Neuroophthalmology. 2020;45(1):1-16. PMID: 33762782; PMCID: PMC7946029.
Wandji BN, Dugauquier A, Ehongo A. Visual field defects and retinal nerve fiber layer damage in buried optic disc drusen: a new insight. Int J Ophthalmol. 2022;15(10):1641-1649. PMID: 36262850; PMCID: PMC9522567.
Mukriyani H, Malmqvist L, Subhi Y, Hamann S. Prevalence of optic disc drusen: a systematic review, meta-analysis and forecasting study. Acta Ophthalmol. 2024;102(1):15-24. PMID: 37144704.
Lee KM, Woo SJ, Hwang JM. Factors associated with visual field defects of optic disc drusen. PLoS One. 2018;13(4):e0196001. PMID: 29708976; PMCID: PMC5927402.
Sibony PA, Kupersmith MJ, Kardon RH. Optical Coherence Tomography Neuro-Toolbox for the Diagnosis and Management of Papilledema, Optic Disc Edema, and Pseudopapilledema. J Neuroophthalmol. 2021;41(1):77-92. doi:10.1097/WNO.0000000000001078. PMID:32909979; PMCID:PMC7882012.
Liu X, Yan Y. Advances in origin, evolution, and pathogenesis of optic disc drusen: a narrative review. Indian J Ophthalmol. 2025;73(5):637-647. PMID: 40272291; PMCID: PMC12121874.