ดรูเซนของจานประสาทตา (ODD ) คือตะกอนหินปูนที่สะสมภายในจานประสาทตา ซึ่งเป็นสาเหตุทั่วไปของภาวะ papilledema เทียมแบ่งเป็น 2 ชนิด: ชนิดผิวเผิน (เห็นเม็ดสีขาวบนผิวของจานประสาทตา ) และชนิดฝังลึก (มองไม่เห็นจากผิว)
ความชุก 0.34–2.4% ไม่แตกต่างระหว่างเพศ เกิดสองข้างในมากกว่า 70% ของผู้ป่วยแต่มักไม่สมมาตร
สงสัยการถ่ายทอดทางพันธุกรรมแบบ autosomal dominant แบบไม่สมบูรณ์ และถือเป็นโรคแต่กำเนิด
มักไม่มีอาการ แต่ความผิดปกติของลานตาเกิดขึ้นในมากกว่า 70% ของผู้ป่วย และเป็นโรคเส้นประสาทตา เรื้อรังที่ดำเนินไปอย่างช้าๆ ในอัตราประมาณ 1.6% ต่อปี
ในชนิดฝังลึก การแยกจาก papilledema คั่งเลือดเป็นสิ่งสำคัญที่สุด โดยอาศัย autofluorescence, OCT , อัลตราซาวนด์ และ CT
ไม่มีการรักษาที่แน่ชัด การดูแลมุ่งเน้นที่การจัดการภาวะแทรกซ้อน (เช่น NA-AION และ CNV M) และการติดตามลานตาเป็นระยะ
ดรูเซนของจานประสาทตา (ODD ) คือตะกอนหินปูนที่สะสมภายในหัวประสาทตา ประกอบด้วยสารหินปูนหักเหแสงจากมิวโคโปรตีนและมิวโคโพลีแซ็กคาไรด์ เชื่อว่าเป็นก้อนหินปูนของสารนอกเซลล์ที่ตกตะกอนและสะสมในจานประสาทตา อันเป็นผลจากความผิดปกติของการขนส่งตามแนวแอกซอน 2) มี 2 ชนิด: ชนิดผิวเผิน (เห็นเม็ดบนผิวของจานประสาทตา ) และชนิดฝังลึก (มองไม่เห็นจากผิว)
ODD เป็นโรคแต่กำเนิด แต่มักไม่เด่นชัดทางสายตาในวัยเด็ก ส่วนใหญ่พบเมื่อตรวจอวัยวะรับภาพในการตรวจสุขภาพหรือเนื่องจากโรคอื่น ความชุกแตกต่างกันตามวิธีการตรวจ: ประมาณ 0.37% ด้วยกล้องตรวจตา ประมาณ 0.12% ด้วยการถ่ายภาพอวัยวะรับภาพ ในขณะที่ด้วย spectral-domain OCT ที่ใช้ enhanced depth imaging (EDI) รายงานไว้ที่ 2.21% 4) ไม่แตกต่างระหว่างเพศ เกิดสองข้างในมากกว่า 70% ของผู้ป่วยแต่มักไม่สมมาตร 2)
ODD เป็นสาเหตุทั่วไปของ «papilledema เทียม» และโดยเฉพาะชนิดฝังลึกมักแยกจาก papilledema คั่งเลือดได้ยาก เดิมเคยถือว่าเป็นโรคไม่ร้ายแรงที่คงที่ แต่การศึกษาล่าสุดแสดงให้เห็นว่าความผิดปกติของลานตาเกิดขึ้นในมากกว่า 70% ของผู้ป่วยและดำเนินไปอย่างช้าๆ จึงได้รับการยอมรับว่าเป็น โรคเส้นประสาทตา เรื้อรังที่ดำเนินไป
รอยโรคของ ODD จำกัดอยู่ภายในจานประสาทตา และแตกต่างอย่างสิ้นเชิงจากดรูเซน จอประสาทตา บนเยื่อบรูค ซึ่งเป็นรอยโรคก่อนเกิดจอประสาทตา เสื่อมตามอายุ ในด้านตำแหน่งที่เกิด องค์ประกอบ และความสำคัญทางคลินิก โรคที่เกี่ยวข้อง ได้แก่ จอประสาทตา อักเสบชนิดรงควัตถุ เส้นเลือดเปราะ (angioid streaks) กลุ่มอาการอัชเชอร์ กลุ่มอาการนูนัน และกลุ่มอาการอาลาจิลล์
Q
ดรูเซนจานประสาทตาและดรูเซนจอประสาทตาเป็นสิ่งเดียวกันหรือไม่?
A
ชื่อคล้ายกันแต่เป็นโรคคนละชนิดกัน ดรูเซน จานประสาทตา (ODD ) คือตะกอนหินปูนภายในจานประสาทตา และแตกต่างอย่างสิ้นเชิงจากดรูเซน จอประสาทตา บนเยื่อบรูค ซึ่งเป็นรอยโรคก่อนเกิดจอประสาทตา เสื่อมตามอายุ ในด้านตำแหน่งที่เกิด องค์ประกอบ และความสำคัญทางคลินิก ODD เป็นโรคเส้นประสาทตา ที่มีมาแต่กำเนิด และไม่เกี่ยวข้องกับจอประสาทตา เสื่อมตามอายุ
Q
ดรูเซนจานประสาทตาถ่ายทอดทางพันธุกรรมหรือไม่?
A
สงสัยว่าเป็นการถ่ายทอดแบบออโตโซมอลโดมิแนนต์ที่มีการแทรกซึมไม่สมบูรณ์ หากมีประวัติครอบครัวเป็น ODD แนะนำให้พบจักษุแพทย์ ลักษณะเด่นอีกอย่างคืออัตราการเป็นสองตาสูง
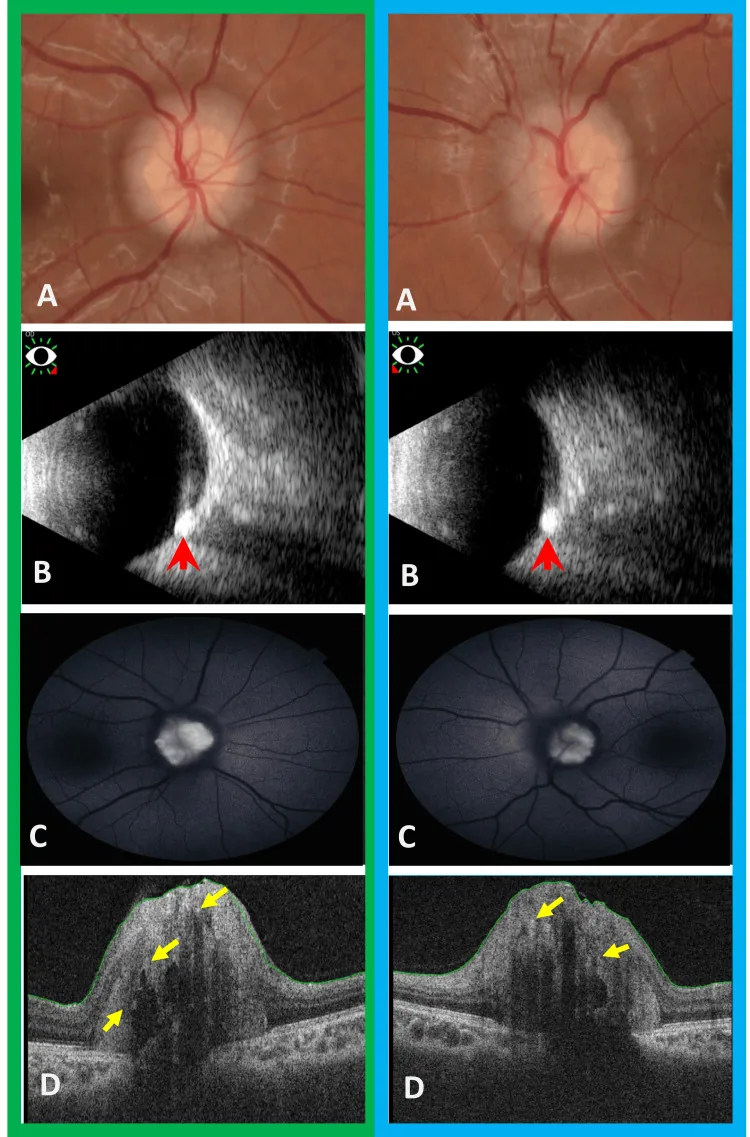
ภาพ multimodal ของดรูเซนจานประสาทตาทั้งสองข้าง แสดงความไม่สม่ำเสมอของผิวจานประสาทตา คลื่นเสียงความถี่สูงสะท้อนสูง และดรูเซนที่ถูกฝังใน OCT Alkhayat MI, et al. Chiari Malformation Type I With Concurrent Bilateral Optic Disc Drusen: Is Follow-up Necessary?. Cureus. 2024. Figure 2. PM
CI D: PMC11298954. License: CC BY.
พบดรูเซน สีขาวผิวไม่สม่ำเสมอบนจานประสาทตา ทั้งสองข้าง คลื่นเสียงความถี่สูงแสดงการสะท้อนสูงและเงาด้านหลัง OCT แสดงโพรงสะท้อนต่ำและจุดสะท้อนสูงที่สอดคล้องกับดรูเซน ที่ถูกฝัง แสดงผลการตรวจทางคลินิกและการวินิจฉัยหลัก
โดยทั่วไปแล้ว ODD จะไม่มีอาการ ความผิดปกติของลานตาดำเนินไปอย่างช้าๆ ดังนั้นในหลายกรณีผู้ป่วยไม่รู้สึกถึงข้อบกพร่องของลานตา
การสูญเสียการมองเห็น ชั่วคราว : พบในผู้ป่วยประมาณ 9% 2) ความผิดปกติของลานตา : มีรูปแบบเช่น จุดบอดขยายใหญ่ จุดบอดรูปโค้ง และลานตาส่วนปลายหดตัว เกิดขึ้นตามแนวเส้นใยประสาทตา 2) การมองเห็น ลดลงอย่างกะทันหันการมองเห็น ลดลงเฉียบพลันเมื่อมี NA-AION หรือ CNV M (ดูหัวข้อ วิธีการรักษามาตรฐาน )
ความผิดปกติของลานตามีรูปแบบดังต่อไปนี้
ความบกพร่องของมัดใยประสาทตา : ความบกพร่องของลานสายตา แบบโค้งตามแนวเส้นใยประสาทการขยายของจุดบอด Mariotte : การขยายของจุดบอดทางสรีรวิทยาการตีบของลานสายตาส่วนปลาย : การตีบของลานสายตาแบบเข้าสู่ศูนย์กลางที่ดำเนินไปเรื่อยๆตาบอดครึ่งซีกแนวนอน : พบได้น้อยแต่มีรายงาน
รูปแบบ ลักษณะ การขยายของจุดบอด พบบ่อยที่สุด จุดบอดรูปโค้ง ตามแนวเส้นใยประสาทตา การตีบของลานสายตาส่วนปลาย พบในกรณีที่ดำเนินไปมาก
เนื่องจากทั้งหมดดำเนินไปอย่างช้าๆ จึงมักไม่มีอาการให้รู้สึกได้แม้ว่าจะมีความบกพร่องของลานสายตา อยู่แล้วในการตรวจครั้งแรก ความถี่ของความบกพร่องของลานสายตา รายงานว่าประมาณ 73% ในชนิดตื้น และประมาณ 36% ในชนิดฝัง และยิ่งปริมาตรของดรูเซน มากเท่าใด ความรุนแรงของการสูญเสียลานสายตาก็จะยิ่งมากขึ้น5) การตีบของลานสายตาดำเนินไปในอัตราประมาณ 1.6% ต่อปี สาเหตุหลักของการสูญเสียลานสายตาคือการกดทับโดยตรงต่อแอกซอนของเส้นประสาทตา จากดรูเซน 2)
ชนิดตื้น
ลักษณะภายนอก : พบอนุภาคสีขาวถึงขาวเหลืองบนพื้นผิวของหัวประสาทตา
ผลการตรวจ autofluorescence จอประสาทตา : แสดงการเรืองแสงมากเกินไป (hyperfluorescence) ในการตรวจ autofluorescence จอประสาทตา (FAF )
การวินิจฉัย : การวินิจฉัยค่อนข้างง่ายเนื่องจากสามารถมองเห็นได้โดยตรงจากการตรวจจอประสาทตา
การดำเนินโรค : ในวัยเด็กจะอยู่ในรูปแบบที่ฝังอยู่ และเมื่ออายุมากขึ้น การกลายเป็นหินปูนจะดำเนินไปและโผล่ขึ้นมาบนพื้นผิว
ชนิดฝังอยู่
ลักษณะภายนอก : ไม่สามารถมองเห็นได้จากพื้นผิวของหัวประสาทตา หัวประสาทตาทั้งหมดดูนูนขึ้น
การวินิจฉัย : ยากที่จะระบุได้จากการตรวจจอประสาทตา เพียงอย่างเดียว จำเป็นต้องยืนยันด้วย autofluorescence, CT, อัลตราซาวนด์ B-mode และ OCT
การแยกโรค : การแยกจากภาวะ papilledema เป็นสิ่งที่สำคัญที่สุด
ความผิดปกติของลานสายตา : เกิดขึ้นบ่อยกว่าชนิดผิวเผิน
ลักษณะขรุขระ (lumpy-bumpy) : เส้นประสาทตา มีลักษณะไม่เรียบการหายไปของรอยบุ๋มหัวประสาทตา : ขาดรอยบุ๋มและนูนขึ้นในชนิดผิวเผิน พบ drusen สีขาวบนพื้นผิวของหัวประสาทตา
ขอบหัวประสาทตาไม่ชัดเจน (เด่นชัดโดยเฉพาะในชนิดฝังอยู่)
ความผิดปกติของหลอดเลือด : อาจพบหลอดเลือดคดเคี้ยวหรือหลอดเลือด shunt cilioretinalRAPD บวกการเต้นของหลอดเลือดดำเอง : มักพบหัวประสาทตาด้านจมูก : ตำแหน่งที่พบบ่อยที่สุดของดรูเซน คือขอบด้านจมูกไม่พบภาวะคั่งของหัวประสาทตา เลือดออกในจอตา หรือจุดขาว (จุดสำคัญในการแยกจากภาวะหัวประสาทตาบวม)
ODD มีรายงานร่วมกับโรคและภาวะต่อไปนี้
จอประสาทตา เสื่อมชนิดสี (retinitis pigmentosa)รอยเส้นแองจิออยด์ (angioid streaks) : เสี่ยงต่อการเกิดเส้นเลือดใหม่ในคอรอยด์ หัวประสาทตาเล็ก : ดรูเซน ของหัวประสาทตามักพบร่วมกับหัวประสาทตาเล็กCNV M รอบหัวประสาทตาการมองเห็น ลดลงอย่างเฉียบพลันNA-AION : พิจารณาเมื่อมีข้อบกพร่องของลานสายตาหรือการมองเห็น ลดลงอย่างเฉียบพลัน
เมื่อมีข้อบกพร่องของลานสายตาหรือการมองเห็น ลดลงอย่างเฉียบพลัน สาเหตุเชื่อว่าเกิดจากภาวะขาดเลือดภายในหัวประสาทตา กลไกนี้คล้ายกับโรคเส้นประสาทตา ขาดเลือด (NAION ) และจำเป็นต้องตรวจอย่างเร่งด่วนในระยะเฉียบพลัน
Q
ดรูเซนของหัวประสาทตาทำให้ตาบอดหรือไม่?
A
โดยทั่วไปการพยากรณ์โรคทางสายตาดี อย่างไรก็ตาม มีการลุกลามของการแคบลงของลานสายตาประมาณ 1.6% ต่อปี และในบางกรณีอาจเกิดการมองเห็น ลดลงอย่างเฉียบพลันเมื่อมี NA-AION หรือ CNV M ร่วมด้วย การตรวจเป็นประจำมีความสำคัญ
ในฐานะกลไกการเกิด ODD การกลายเป็นปูนบนพื้นฐานของความผิดปกติของการขนส่งตามแนวแกนเป็นที่ยอมรับอย่างกว้างขวาง 7)
การขนส่งภายในแอกซอนถูกขัดขวางบริเวณด้านหน้าของลามินาคริบโรซา ของจานประสาทตา
ออร์แกเนลล์ภายในเซลล์ เช่น ไมโทคอนเดรีย สะสมภายในจานประสาทตา
สารต่างๆ เช่น มิวโคโพลีแซ็กคาไรด์ และแคลเซียมฟอสเฟต ตกตะกอน
สารเหล่านี้กลายเป็นปูนกลายเป็นดรูเซน
กระบวนการนี้เริ่มต้นตั้งแต่วัยเด็กตอนต้น และการกลายเป็นปูนจะดำเนินไปตามอายุ ในวัยเด็ก ดรูเซน จะอยู่ในรูปแบบที่ฝังอยู่ และมักจะมองเห็นเป็นดรูเซน ผิวเผินในวัยรุ่นถึงผู้ใหญ่
จานประสาทตา เล็ก (ช่องตาขาว แคบ / จานประสาทตา แออัด)ลามินาคริบโรซา ในสภาพที่หนาแน่น ทำให้เกิดความผิดปกติของการขนส่งตามแนวแกนได้ง่าย การที่จานประสาทตา เล็กร่วมกับดรูเซน จานประสาทตา บ่อยครั้งสนับสนุนกลไกนี้ 2) การไม่มีรอยบุ๋มจานประสาทตา : เป็นลักษณะทางกายวิภาคที่จำเพาะของ ODD และสัมพันธ์กับพยาธิสภาพ
มักเป็นทั้งสองข้าง และมีรายงานการเกิดในครอบครัว มีการเสนอรูปแบบการถ่ายทอดทางพันธุกรรมแบบออโตโซมอลโดมิแนนต์ที่มีการแทรกซึมไม่สมบูรณ์ แต่ยังไม่มีการระบุการกลายพันธุ์ของยีนที่จำเพาะ ปัจจัยทางพันธุกรรมอาจเกี่ยวข้องกับการเกิดจานประสาทตา เล็กหรือความเปราะบางของการขนส่งตามแนวแกน
โรคที่เกี่ยวข้องได้แก่:
จอประสาทตา เสื่อมชนิดรงควัตถุ (Retinitis pigmentosa)รอยเส้นแองจอยด์ (Angioid streaks)
กลุ่มอาการอัชเชอร์ (Usher syndrome)กลุ่มอาการนูนัน (Noonan syndrome)กลุ่มอาการอลาจิลล์ (Alagille syndrome)
ไม่มีวิธีป้องกันดรูเซนของจานประสาทตา ได้โดยตรง หากมีประวัติครอบครัวเป็น ODD แนะนำให้ตรวจตาเป็นประจำ หากได้รับการวินิจฉัยแล้ว การติดตามความคืบหน้าตั้งแต่เนิ่นๆ ด้วยการตรวจลานสายตา เป็นประจำเป็นสิ่งสำคัญ หากสังเกตเห็นการมองเห็น ลดลงอย่างกะทันหันหรือความผิดปกติของลานสายตา ควรไปพบจักษุแพทย์ทันที
การวินิจฉัย ODD ทำได้โดยการตรวจหลายอย่างร่วมกัน โดยเฉพาะการวินิจฉัยชนิดฝังลึกและการแยกจากภาวะ papilledema เป็นความท้าทายทางคลินิกที่สำคัญ กลุ่มศึกษา Drusen จานประสาทตา (ODD S) ได้กำหนดเกณฑ์ฉันทามติสำหรับการวินิจฉัย ODD ด้วย EDI-OCT (เช่น บริเวณสัญญาณลดลงด้านหน้า lamina cribrosa, จุดสะท้อนแสงสูง ภายใน) ซึ่งปัจจุบันใช้กันอย่างแพร่หลายเป็นแนวทางการวินิจฉัยมาตรฐาน
ลักษณะพื้นฐานคือการไม่มีแอ่งและนูนของจานประสาทตา ในชนิดตื้น สามารถวินิจฉัยได้จากเม็ดสีขาวบนผิวจานประสาทตา
เมื่อถ่ายภาพอวัยวะรับภาพด้วยแสงไม่แดง (ฟิลเตอร์สีเขียว) ดรูเซน จะปรากฏเป็นประกายแวววาว มีประโยชน์ในการยืนยันชนิดตื้น
การเรืองแสงเองของอวัยวะรับภาพ (FAF)
ชนิดตื้น : ปรากฏชัดเจนเป็นบริเวณเรืองแสงมากเกินไป
ชนิดฝังลึก : สามารถตรวจพบการเรืองแสงเองได้ มีประโยชน์ในการค้นหาชนิดฝังลึกที่ไม่เห็นในการตรวจอวัยวะรับภาพ
การวินิจฉัยแยกโรค : Papilledema ไม่มีการเรืองแสงเอง ดังนั้นจึงมีประโยชน์โดยตรงในการวินิจฉัยแยกโรค
OCT (EDI-OCT)
ผลการตรวจ : ระบุเป็นโครงสร้างรูปไข่สะท้อนแสงต่ำภายในจานประสาทตา
ความสำคัญ : แสดงความไวในการตรวจจับสูงกว่า OCT ทั่วไปและ B-mode echo สำหรับ drusen ที่ถูกฝัง และปัจจุบันถือเป็นวิธีการวินิจฉัยที่ไวที่สุด
การประเมิน RNFL : มีประโยชน์ในการตรวจหาการบางลงของชั้นเส้นใยประสาทจอประสาทตา ตั้งแต่ระยะแรก ตำแหน่งของความบกพร่องของลานสายตา สอดคล้องกับการกระจายของความบกพร่องของ RNFL 3)
การตรวจอัลตราซาวนด์ (B-mode/A-mode)
ผลการตรวจ : ตรวจพบสัญญาณสะท้อนความเข้มสูง (ยอดแอมพลิจูดสูง) ในบริเวณที่มีหินปูน
ลักษณะ : สัญญาณยังคงอยู่แม้จะลดเกนลง
ความสำคัญ : ไม่รุกรานและสามารถทำซ้ำได้ มีประโยชน์เป็นทางเลือกเมื่อ CT ทำได้ยาก (เช่น ในเด็ก)
การตรวจหลอดเลือดด้วยฟลูออเรสซีน (FA ) : ใน ODD โดยหลักการแล้วไม่มีการรั่วของสีจากจานประสาทตา ในทางตรงกันข้าม ใน papilledema และจานประสาทตา บวม จะมีการรั่วของฟลูออเรสซีน การย้อมสีรอบจานประสาทตา เพียงอย่างเดียวโดยไม่มีการรั่วเป็นสิ่งที่บ่งชี้ถึง pseudopapilledema (ODD ) หากมีการขยายตัวของเส้นเลือดฝอยในระยะแรกและการรั่วในระยะหลัง แสดงว่ามี CNV M ร่วมด้วยCT : เหนือกว่า MRI ในการตรวจหา drusen เมื่อตัดผ่านจานประสาทตา หินปูนจะปรากฏเป็นบริเวณความหนาแน่นสูง หนึ่งในการตรวจภาพที่เชื่อถือได้มากที่สุดในการแยกความแตกต่างจาก papilledemaการประเมิน PHOMS : การประเมินโครงสร้างคล้ายก้อนรูปไข่สะท้อนแสงสูงรอบจานประสาทตา (peripapillary hyperreflective ovoid mass-like structure) ใน OCT ช่วยเพิ่มความแม่นยำในการวินิจฉัย pseudopapilledema
จานประสาทตา : จุดสำคัญในการวินิจฉัยแยกโรค
การวินิจฉัยแยกโรคทำได้โดยการรวมสิ่งต่อไปนี้
การเรืองแสงเอง (FAF ) : ODD → บวก / ภาวะหัวประสาทตาบวมจากเลือดคั่ง → ปกติลบ
การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) : ODD → ไม่มีการรั่ว / ภาวะหัวประสาทตาบวมจากเลือดคั่ง → มีการรั่ว
CT หรืออัลตราซาวนด์ B-mode : ODD → มีหินปูน / ภาวะหัวประสาทตาบวมจากเลือดคั่ง → ไม่มีหินปูน
ผลตรวจอวัยวะภายในลูกตา : ODD → ไม่มีเลือดคั่ง ไม่มีการขยายของเส้นเลือดฝอย ไม่มีเลือดออก / ภาวะหัวประสาทตาบวมจากเลือดคั่ง → มีเลือดคั่ง มีการขยายของเส้นเลือดฝอย มีเลือดออกแบบรูปเปลวไฟ
การติดตามผล : ODD → ไม่มีการเปลี่ยนแปลงรูปร่างของหัวประสาทตา / ภาวะหัวประสาทตาบวมจากเลือดคั่ง → มีการเปลี่ยนแปลงที่ดำเนินไป
การไม่พบการเปลี่ยนแปลงระหว่างการติดตามผลเป็นหลักฐานสำคัญในการยืนยันภาวะหัวประสาทตาบวมเทียม (ODD )
ลักษณะที่พบ ภาวะหัวประสาทตาบวมจริง ODD (ภาวะหัวประสาทตาบวมเทียม )เลือดคั่ง มี ไม่มี การขยายของเส้นเลือดฝอย มี ไม่มี เลือดออก มี ไม่มี/พบน้อย การติดตามเส้นทางเดินของหลอดเลือด ไม่ชัดเจน สามารถติดตามได้ชัดเจน
ODD มีความสำคัญในการวินิจฉัยแยกโรคต้อหิน ด้วย
Q
จะวินิจฉัยดรูเซนของจานประสาทตาแบบฝังได้อย่างไร?
A
เนื่องจากชนิดฝังไม่สามารถมองเห็นได้ด้วยการตรวจอวัยวะภายในตาเพียงอย่างเดียว การถ่ายภาพเรืองแสงอัตโนมัติของจอตา (FAF ) จึงเป็นทางเลือกแรก การพบการเรืองแสงอัตโนมัติที่สอดคล้องกับตำแหน่งของดรูเซน เป็นพื้นฐานในการวินิจฉัย เพื่อยืนยัน การใช้ CT เพื่อแสดงหินปูน อัลตราซาวนด์โหมด B และ EDI-OCT มีประโยชน์ การไม่มีการรั่วของสีจากจานประสาทตา ในการตรวจหลอดเลือดด้วยฟลูออเรสซีน ก็เป็นข้อค้นพบสำคัญในการแยกจากภาวะคั่งของจานประสาทตา
Q
ในการตรวจสุขภาพเด็ก มีการบอกว่า "จานประสาทตาบวม" มีความเป็นไปได้ที่จะเป็นดรูเซนหรือไม่?
A
ในเด็กที่มีลักษณะบวมของจานประสาทตา ทั้งสองข้าง ODD อยู่ในรายการวินิจฉัยแยกโรค การตรวจหาหินปูนด้วยอัลตราซาวนด์โหมด B หรือ OCT เป็นสิ่งสำคัญเพื่อแยกจากภาวะบวมของจานประสาทตา ที่แท้จริง หากจำเป็น ให้พิจารณาการตรวจทางระบบประสาทเพิ่มเติม
ในปัจจุบัน ยังไม่มีการรักษาที่พิสูจน์แล้วว่าสามารถทำให้ ODD เล็กลงหรือหายไปได้ การดูแลหลักเน้นที่สองประการต่อไปนี้:
การจัดการและรักษาภาวะแทรกซ้อน การติดตามลานสายตาเป็นระยะ เพื่อประเมินความก้าวหน้า
การตรวจลานสายตา เป็นระยะและการประเมินภาพเป็นหัวใจสำคัญของการจัดการ
การตรวจลานสายตา การตรวจลานสายตา อัตโนมัติเป็นระยะด้วยเครื่อง Humphrey perimeter และอื่นๆ เพื่อประเมินความก้าวหน้าของข้อบกพร่องลานสายตาOCT -RNFL ชั้นเส้นใยประสาทจอประสาทตา ตามเวลาเพื่อตรวจหาการบางลงของเส้นใยประสาท (การสูญเสียเส้นประสาทที่ไม่สามารถกลับคืนได้) ตั้งแต่ระยะแรกภาพถ่ายจอตา : บันทึกและเปรียบเทียบการเปลี่ยนแปลงของลักษณะหัวประสาทตา
ช่วงเวลาการนัดตรวจแตกต่างกันไปตามความรุนแรงของโรคและระดับของข้อบกพร่องลานสายตา แต่การมาตรวจเป็นระยะเป็นสิ่งจำเป็น ยังไม่มีการรักษาที่มีประสิทธิภาพที่ได้รับการยอมรับสำหรับข้อบกพร่องลานสายตา และในบางกรณีอาจพิจารณาใช้ยาลดความดันลูกตา
ในรายงานผู้ป่วยโดย Markan และคณะ ได้ทำการถ่ายภาพหลายรูปแบบในเด็กชายวัยรุ่นตอนต้นที่มี CNV M รอบหัวประสาทตาที่เกี่ยวข้องกับ ODD ค่า BCVA ของตาซ้ายคือ 6/60 และเขาได้รับการวินิจฉัยผิดว่าเป็น optic neuritis ที่โรงพยาบาลอื่นและได้รับการรักษาด้วยสเตียรอยด์ หลังจากให้ anti-VEGF 3 ครั้ง น้ำใต้จอประสาทตา หายไป และ BCVA ดีขึ้นเป็น 6/9 หลังจาก 3 เดือน
ทางเลือกการรักษาสำหรับ CNV M ร่วมมีดังนี้:
การรักษาด้วย anti-VEGF : มีรายงานผู้ป่วยแสดงประสิทธิผลการรักษาด้วยแสงไดนามิก (PDT )การจี้ด้วยเลเซอร์ : ทางเลือกดั้งเดิม
ภาวะแทรกซ้อน การจัดการ การมองเห็น ลดลงอย่างกะทันหันหรือข้อบกพร่องของลานสายตาพิจารณาภาวะขาดเลือดภายในหัวประสาทตา (กลไกคล้าย NAION ) และตรวจสอบอย่างเร่งด่วนเช่นเดียวกับโรคเส้นประสาทตา ขาดเลือด ภาวะแทรกซ้อนของจอประสาทตา เสื่อมชนิดเม็ดสี เพิ่มการตรวจคลื่นไฟฟ้าจอประสาทตา (ERG ) และประเมินการทำงานของจอประสาทตา ภาวะแทรกซ้อนของรอยเส้นสีจอประสาทตา เฝ้าระวังเส้นเลือดใหม่ในคอรอยด์ (ด้วยการตรวจฟลูออเรสซีน แองจิโอกราฟฟี, OCT แองจิโอกราฟฟี ฯลฯ) เส้นเลือดใหม่ในคอรอยด์ รอบหัวประสาทตาพิจารณาการรักษาด้วยยาต้าน VEGF , การรักษาด้วยแสงไดนามิก , การจี้ด้วยเลเซอร์
ไม่มีการรักษาที่พิสูจน์แล้วสำหรับดรูเซน เอง ข้อบกพร่องของลานสายตาอาจดำเนินไปอย่างช้าๆ ดังนั้นการติดตามลานสายตาในระยะยาวจึงเป็นสิ่งจำเป็น
หากมีการมองเห็น ลดลงเฉียบพลันหรือการขยายตัวของข้อบกพร่องลานสายตาอย่างรวดเร็ว ควรสงสัยภาวะขาดเลือดภายในหัวประสาทตาหรือเส้นเลือดใหม่ในคอรอยด์ และตรวจสอบทันที
หากวินิจฉัยภาวะหัวประสาทตาบวมเทียม จาก ODD ผิดว่าเป็นภาวะหัวประสาทตาบวมจริง อาจมีความเสี่ยงที่จะทำการตรวจทางระบบประสาทที่ไม่จำเป็น
หากแยกผิดจากโรคประสาทตาอักเสบ อาจให้การรักษาด้วยสเตียรอยด์ แต่สเตียรอยด์ ไม่ได้ผลสำหรับ ODD เอง และอาจทำให้กรณีที่มีเส้นเลือดใหม่ในคอรอยด์ แย่ลง
Q
เมื่อวินิจฉัยว่ามีดรูเซน จำเป็นต้องรักษาหรือไม่?
A
ไม่มีการรักษาที่ได้ผลสำหรับดรูเซน เอง การจัดการส่วนใหญ่เป็นการจัดการกับภาวะแทรกซ้อน (เช่น เส้นเลือดใหม่ในคอรอยด์ ) การตรวจลานสายตา เป็นประจำและการสังเกตการเปลี่ยนแปลงของรูปร่างหัวประสาทตาเป็นสิ่งสำคัญ หากมีการมองเห็น ลดลงกะทันหันหรือความผิดปกติของลานสายตา ควรรีบไปพบแพทย์
การเกิด ODD เป็นผลมาจากการรวมกันของลักษณะทางกายวิภาคของหัวประสาทตาและความผิดปกติของการขนส่งตามแนวแอกซอน หัวประสาทตาที่มีขนาดเล็กและแออัดแต่กำเนิดเป็นปัจจัยพื้นฐานที่จำเป็นสำหรับการเกิด 2)
เมื่อเส้นประสาทตา ผ่านแผ่นลามินาคริบโรซา เพื่อออกจากลูกตา แอกซอนทั้งหมดของเซลล์ปมประสาทจอประสาทตา จะผ่านรูแคบนี้ (ช่องตาขาว ) ในบุคคลที่มีช่องตาขาว เล็ก เส้นใยประสาทจะถูกอัดแน่นมากขึ้น
การเกิดความผิดปกติของการขนส่ง : ในสภาพแวดล้อมที่แอกซอนหนาแน่น การขนส่งภายในแอกซอน (การขนส่งวัสดุและพลังงานภายในเส้นใยประสาท) จะถูกขัดขวางได้ง่ายที่ด้านหน้าของแผ่นลามินาคริบโรซา การสะสมของสารภายในเซลล์ : เมื่อการขนส่งหยุดชะงัก ออร์แกเนลล์ภายในเซลล์ เช่น ไมโทคอนเดรียและเอนโดพลาสมิกเรติคูลัม รวมถึงมิวโคโพลีแซ็กคาไรด์ จะสะสมภายในหัวประสาทตาการดำเนินไปของการกลายเป็นหินปูน : แคลเซียมฟอสเฟตจะจับตัวบนสารที่สะสม และค่อยๆ กลายเป็นหินปูนก่อตัวเป็นดรูเซน 7)
เมื่ออายุมากขึ้น ดรูเซน จะมีขนาดใหญ่ขึ้น ทำให้เกิดการกดทับทางกลต่อเส้นใยประสาทตา และความบกพร่องของลานสายตา จะดำเนินไป 2) กลไกการเกิดความบกพร่องของลานสายตา มีดังนี้
การกดทับทางกล : ดรูเซน กดทับโดยตรงต่อเส้นใยประสาทตาภาวะขาดเลือด : ความผิดปกติของการไหลเวียนเลือดที่หัวประสาทตาความผิดปกติของการไหลตามแอกซอน : การขัดขวางการขนส่งตามแนวแอกซอนแบบเรื้อรัง
ขนาดและตำแหน่งของดรูเซน ไม่จำเป็นต้องสอดคล้องกับการเปลี่ยนแปลงของลานสายตา กลไกการเกิด CNV M (เยื่อเส้นเลือดใหม่คอรอยด์ รอบหัวประสาทตา) สันนิษฐานว่าเป็นผลกระทบต่อหลอดเลือดคอรอยด์ บริเวณ ODD และความเสียหายของโครงสร้างหลอดเลือดรอบหัวประสาทตา
เชื่อว่ากระบวนการกลายเป็นหินปูนนี้เริ่มต้นทันทีหลังคลอด และในวัยเด็กตอนต้น หินปูนภายในหัวประสาทตายังเล็กและถูกฝังอยู่ จึงไม่เด่นชัดภายนอก ตั้งแต่วัยรุ่นถึงวัยผู้ใหญ่ การกลายเป็นหินปูนดำเนินไป และดรูเซน จะโผล่ขึ้นมาบนผิวหัวประสาทตา กลายเป็นชนิดตื้นที่มองเห็นได้ การไม่มีแอ่งหัวประสาทตาถูกตีความว่าเป็นผลจากการกดทับพื้นที่ทางกายวิภาคโดยการเกิดดรูเซน ภายในหัวประสาทตา และเป็นหนึ่งในลักษณะเฉพาะของจอประสาทตา ใน ODD
ก่อนหน้านี้ ODD ถูกมองว่าเป็นรอยโรคที่ไม่ร้ายแรงและคงที่ แต่เนื่องจากพบความผิดปกติของลานตาในผู้ป่วยมากกว่า 70% และดำเนินไปอย่างช้าๆ ปัจจุบันจึงถูกจัดเป็นโรคเส้นประสาทตา เรื้อรังที่ดำเนินไป เชื่อว่าการกดทับแอกซอนอย่างต่อเนื่องและภาวะขาดเลือดเฉพาะที่ทำให้เส้นใยประสาทตาสูญเสียอย่างช้าๆ ซึ่งเพิ่มความสำคัญของการติดตามลานตาในระยะยาว
การถ่ายภาพ OCT แบบเพิ่มความลึก (EDI-OCT ) เพื่อการมองเห็น และประเมินรูปร่างของดรูเซน จานประสาทตา ได้พัฒนาอย่างรวดเร็วในช่วงไม่กี่ปีที่ผ่านมา 1) การวัดปริมาณความลึก ปริมาตร และจำนวนของดรูเซน กำลังเป็นไปได้ และคาดว่าจะกลายเป็นเครื่องมือติดตามการดำเนินโรคในอนาคต การแพร่หลายของ OCT ช่วยเพิ่มความแม่นยำในการตรวจพบดรูเซน ชนิดถูกฝัง และการนำแนวคิด PHOMS (ส่วนนูนสะท้อนแสงสูงรอบจานประสาทตา ) มาใช้ช่วยเพิ่มความแม่นยำในการวินิจฉัยภาวะ papilledema เทียม 6)
การถ่ายภาพหลายรูปแบบที่รวมการเรืองแสงอัตโนมัติของจอตา, OCT , OCT -A, การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน และอัลตราซาวนด์ มีประโยชน์ในการประเมินภาวะแทรกซ้อนที่เกี่ยวข้องกับ ODD อย่างครอบคลุม โดยเฉพาะอย่างยิ่ง OCT -A มีประโยชน์ในการตรวจหาเยื่อหุ้มเส้นเลือดใหม่คอรอยด์ รอบจานประสาทตา (CNV M) ที่อาจพลาดไปหากใช้การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน เพียงอย่างเดียว
เกณฑ์การวินิจฉัยและคำศัพท์ของ ODD แตกต่างกันไปตามสถานพยาบาลและประเทศ กำลังมีการพัฒนาฉันทามติระหว่างประเทศ (เช่น ODD S Consortium) และการกำหนดมาตรฐานเกณฑ์การวินิจฉัยคาดว่าจะช่วยเพิ่มความแม่นยำของการวิจัยในอนาคต
รายงานผู้ป่วยได้แสดงให้เห็นถึงประสิทธิผลของการรักษาด้วย Anti-VEGF สำหรับ CNV M ที่เกี่ยวข้องกับ ODD และคาดว่าจะมีการสะสมความรู้เพิ่มเติม แม้ว่าจำนวนผู้ป่วยจะน้อยและผลลัพธ์ระยะยาวยังไม่ทราบ แต่กำลังถูกพิจารณาเป็นทางเลือกในการรักษา
การศึกษาระยะยาวยังขาดข้อมูลเกี่ยวกับอัตราการดำเนินของข้อบกพร่องลานตาและปัจจัยทำนายในประวัติธรรมชาติของ ODD การศึกษาที่ตรวจสอบความสัมพันธ์ระหว่างขนาด ตำแหน่ง และจำนวนของดรูเซน กับการพยากรณ์โรคทางสายตาเป็นประเด็นสำคัญในอนาคต 5)
มีรายงานว่าภาวะขาดเลือดของเส้นประสาทตา เฉียบพลันที่เกิดร่วมกับ ODD (โดยเฉพาะในผู้ที่มีอายุต่ำกว่า 50 ปี) แสดงลักษณะทางพยาธิวิทยาคล้ายกับภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่หลอดเลือดแดงอักเสบ (NA-AION) 2) มีข้อเสนอแนะว่าการตีบแคบของโครงสร้างภายในหัวประสาทตาอาจเพิ่มความเสี่ยงต่อการเกิดภาวะขาดเลือด และการอธิบายปัจจัยเสี่ยงและการกำหนดกลยุทธ์การป้องกันเป็นความท้าทายในอนาคต
Q
ควรไปพบจักษุแพทย์เมื่อใดสำหรับภาวะดรูเซนของเส้นประสาทตา?
A
เนื่องจากมักไม่มีอาการ การตรวจตาเป็นประจำจึงเป็นพื้นฐาน หากได้รับการวินิจฉัยแล้ว สิ่งสำคัญคือต้องตรวจลานสายตาตามช่วงเวลาที่แพทย์ผู้รักษากำหนด หากสังเกตเห็นการมองเห็น ลดลงอย่างกะทันหัน การเปลี่ยนแปลงของลานสายตาอย่างรวดเร็ว แสงวาบ หรือภาพแสง ควรรีบไปพบจักษุแพทย์ทันที
Malmqvist L, Bursztyn L, Costello F, et al. The Optic Disc Drusen Studies Consortium recommendations for diagnosis of optic disc drusen using optical coherence tomography. J Neuroophthalmol. 2018;38(3):299-307. PMID: 29095768.
Costello F, Rothenbuehler SP, Sibony PA, Hamann S; Optic Disc Drusen Studies Consortium. Diagnosing optic disc drusen in the modern imaging era: a practical approach. Neuroophthalmology. 2020;45(1):1-16. PMID: 33762782; PMCI D: PMC7946029.
Wandji BN, Dugauquier A, Ehongo A. Visual field defects and retinal nerve fiber layer damage in buried optic disc drusen: a new insight. Int J Ophthalmol. 2022;15(10):1641-1649. PMID: 36262850; PMCI D: PMC9522567.
Mukriyani H, Malmqvist L, Subhi Y, Hamann S. Prevalence of optic disc drusen: a systematic review, meta-analysis and forecasting study. Acta Ophthalmol. 2024;102(1):15-24. PMID: 37144704.
Lee KM, Woo SJ, Hwang JM. Factors associated with visual field defects of optic disc drusen. PLoS One. 2018;13(4):e0196001. PMID: 29708976; PMCI D: PMC5927402.
Sibony PA, Kupersmith MJ, Kardon RH. Optical Coherence Tomography Neuro-Toolbox for the Diagnosis and Management of Papilledema, Optic Disc Edema, and Pseudopapilledema. J Neuroophthalmol. 2021;41(1):77-92. doi:10.1097/WNO.0000000000001078. PMID:32909979; PMCI D:PMC7882012.
Liu X, Yan Y. Advances in origin, evolution, and pathogenesis of optic disc drusen: a narrative review. Indian J Ophthalmol. 2025;73(5):637-647. PMID: 40272291; PMCI D: PMC12121874.