เส้นเลือดใหม่ในคอรอยด์ (choroidal neovascularization) คือการเจริญเติบโตผิดปกติของหลอดเลือดจากคอรอยด์ ผ่านเยื่อบรูค (Bruch’s membrane) เกิดในโรคต่างๆ เช่น จอประสาทตา เสื่อมชนิดเปียกที่สัมพันธ์กับอายุ, โรคหลอดเลือดคอรอยด์ โป่งพอง (polypoidal choroidal vasculopathy), และจอประสาทตา เสื่อมจากสายตาสั้น
OCT angiography (OCTA ) แสดงภาพหลอดเลือดขนาดเล็กของจอประสาทตา และคอรอยด์ โดยไม่ต้องใช้สารทึบรังสี มีประโยชน์ในการวินิจฉัยชนิดของเส้นเลือดใหม่ในคอรอยด์เส้นเลือดใหม่ในคอรอยด์แบ่งตามเนื้อเยื่อวิทยาเป็น 3 ชนิด: ชนิดที่ 1 (ใต้ RPE ), ชนิดที่ 2 (เหนือ RPE ), และชนิดที่ 3 (ในจอประสาทตา , RAP )
ในโรคหลอดเลือดคอรอยด์ โป่งพอง (PCV ) อัตราการตรวจพบเครือข่ายเส้นเลือดใหม่แบบแยกแขนง (BNN) ด้วย OCTA เกือบ 100% แต่อัตราการตรวจพบตัวโปลิปเองประมาณ 79% 7)
ต้องระวังสิ่งแปลกปลอม (artifacts) เช่น ข้อผิดพลาดจากการฉายภาพและการแบ่งชั้น และใช้ร่วมกับ B-scan OCT เสมอ
การรักษาด้วย anti-VEGF เป็นทางเลือกแรกสำหรับทุกชนิด ในโรคหลอดเลือดคอรอยด์ โป่งพอง อาจพิจารณา PDT เพียงอย่างเดียวหรือร่วมกับ anti-VEGF ขึ้นอยู่กับระดับการมองเห็น
เส้นเลือดใหม่ในคอรอยด์ (CNV) คือการเจริญเติบโตผิดปกติของหลอดเลือดจากคอรอยด์ ผ่านเยื่อบรูค ไปยังจอประสาทตา ปัจจุบันเรียกอีกอย่างว่า “เส้นเลือดใหม่ในจุดรับภาพ (MNV)”
สาเหตุหลัก ได้แก่ จอประสาทตา เสื่อมชนิดเปียกที่สัมพันธ์กับอายุ, โรคหลอดเลือดคอรอยด์ โป่งพอง, จอประสาทตา เสื่อมจากสายตาสั้น , จอประสาทตา อักเสบชนิดเซรุ่มส่วนกลางเรื้อรัง, ม่านตาอักเสบ , และการบาดเจ็บ ทุกชนิดมีการเพิ่มการผลิต vascular endothelial growth factor (VEGF) เป็นวิถีทางสุดท้ายร่วมกัน
OCT angiography (OCTA ) เป็นการตรวจแบบไม่รุกรานที่แสดงการไหลเวียนเลือดโดยใช้ความคมชัดจากการเคลื่อนที่ (motion contrast) จากการเปลี่ยนแปลงสัญญาณ (decorrelation) ระหว่างการสแกน B-scan ซ้ำๆ โดยไม่ต้องใช้สารทึบรังสี ด้วยการแบ่งชั้น (segmentation) สามารถแสดงโครงสร้างหลอดเลือดขนาดเล็กรอบคอรอยด์ และ RPE ด้วยความละเอียดเชิงลึก การรวม OCT และ OCTA ทำให้สามารถอธิบายเส้นเลือดใหม่ในจุดรับภาพทั้งสามชนิดในสามมิติในระดับเนื้อเยื่อวิทยา 8)
Q
OCTA มีหลักการอย่างไรในการแสดงภาพหลอดเลือด?
A
บริเวณเดียวกันถูกสแกนซ้ำๆ ในช่วงเวลาสั้นๆ เนื้อเยื่อที่อยู่นิ่ง (จอประสาทตา และคอรอยด์ ) ไม่เปลี่ยนแปลง ในขณะที่บริเวณที่มีการไหลเวียนเลือดจะมีการเปลี่ยนแปลงสัญญาณ สัญญาณ “decorrelation” นี้ถูกใช้เป็นความคมชัดจากการเคลื่อนที่เพื่อสร้างภาพ โดยไม่ต้องใช้สารทึบรังสี ทำให้ภาระต่อผู้ป่วยน้อยลง และเหมาะสำหรับการตรวจซ้ำ
เมื่อเกิดเส้นเลือดใหม่ในคอรอยด์ (choroidal neovascularization) จะมีอาการต่อไปนี้เกิดขึ้นแบบเฉียบพลันถึงกึ่งเฉียบพลัน
การมองเห็น ลดลงอย่างรวดเร็วจอประสาทตา ส่วนกลาง (macula)ภาพบิดเบี้ยว (metamorphopsia)จอประสาทตา นูนหรือบวมน้ำจุดบอดกลาง (central scotoma)การมองเห็น ส่วนกลาง
เส้นเลือดใหม่ในคอรอยด์มีชนิดแตกต่างกันตามตำแหน่งและความสัมพันธ์ของชั้นต่างๆ การวินิจฉัยทำโดยใช้ OCT และการตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (slit-lamp)
เส้นเลือดใหม่ในคอรอยด์ชนิดที่ 1 (Type 1 MNV) : อยู่ใต้ชั้น retinal pigment epithelium (RPE ) ใน OCT พบ RPE ไม่สม่ำเสมอ นูนขึ้น และมีการสะท้อนแสงปานกลาง การตรวจ fluorescein angiography (FA ) พบลักษณะแบบ occult (ซ่อนเร้น)เส้นเลือดใหม่ในคอรอยด์ชนิดที่ 2 (Type 2 MNV) : ทะลุ RPE และขยายเข้าไปในช่องใต้จอประสาทตา ใน OCT พบเป็นก้อนสะท้อนแสงปานกลางเหนือ RPE การตรวจ FA พบลักษณะแบบ classic (คลาสสิก)เส้นเลือดใหม่ในคอรอยด์ชนิดที่ 3 (Type 3 MNV / RAP ) : เส้นเลือดใหม่เกิดขึ้นภายในจอประสาทตา (retinal angiomatous proliferation) มักมีเลือดออกในจอประสาทตา แบบจุดเล็กๆ ร่วมด้วยโรคหลอดเลือดคอรอยด์ แบบ polyp (PCV ) : พบรอยโรคยกตัวสีส้มแดงที่จอตา ใน OCT พบ RPE ยกตัวอย่างรวดเร็วและ double layer sign (โครงสร้างสองชั้นของ RPE และเยื่อ Bruch) เป็นลักษณะเฉพาะ
การเกิดเส้นเลือดใหม่ในคอรอยด์มีหลายปัจจัย
อายุและพันธุกรรม : การสะสมของผลิตภัณฑ์เมตาบอลิซึม (drusen) ในเยื่อ Bruch ความเครียดออกซิเดชันที่เพิ่มขึ้นตามอายุจอประสาทตา เสื่อมตามอายุ (AMD )สายตาสั้น มากPXE ) เส้นเลือดใหม่ในคอรอยด์จาก angioid streaks เกิดขึ้นมากกว่า 70% ของผู้ป่วย และการเป็นสองตาพบประมาณ 90%5) .จอประสาทตา ชั้นคอรอยด์ อักเสบเรื้อรังชนิดเซรุ่มส่วนกลางคอรอยด์ ชนิดที่ 1 นอกจากนี้ยังมีรายงาน pachychoroid CNVM ภายหลังจอประสาทตา ชั้นคอรอยด์ อักเสบชนิดเซรุ่มส่วนกลาง2) .โรคคอรอยด์ อักเสบชนิดจุดภายใน (PIC ) : เส้นเลือดใหม่คอรอยด์ เกิดตามมาจากแผลเป็นอักเสบ3) .โรคจอประสาทตา ชั้นคอรอยด์ อักเสบชนิดมีน้ำและเลือดออกบริเวณรอบจุดรับภาพ (PEHCR ) : อาจมีเส้นเลือดใหม่คอรอยด์ ร่วมด้วย ซึ่งเป็นความท้าทายในการวินิจฉัยและรักษา1) .ภาวะหินปูนเกาะที่ตาขาว และคอรอยด์ (SCC ) : แม้พบได้น้อย แต่มีรายงานผู้ป่วยที่มีเส้นเลือดใหม่คอรอยด์ ร่วมกับรอยโรค SCC 4) .
Q
เส้นเลือดใหม่คอรอยด์สามารถเกิดขึ้นในโรคอื่นนอกเหนือจากจอประสาทตาเสื่อมตามอายุได้หรือไม่?
A
เส้นเลือดใหม่คอรอยด์ เกิดขึ้นในโรคต่างๆ เช่น สายตาสั้น มาก PXE PIC จอประสาทตา ชั้นคอรอยด์ อักเสบเรื้อรังชนิดเซรุ่มส่วนกลาง การบาดเจ็บ ม่านตาอักเสบ PEHCR SCC เป็นต้น โดยเฉพาะใน PXE เส้นเลือดใหม่คอรอยด์ เกิดขึ้นในอัตราสูงบนพื้นหลังของ striae angioid มักเป็นทั้งสองตาและดื้อต่อการรักษา5) การระบุโรคที่เป็นสาเหตุมีความสำคัญต่อการกำหนดแผนการรักษา
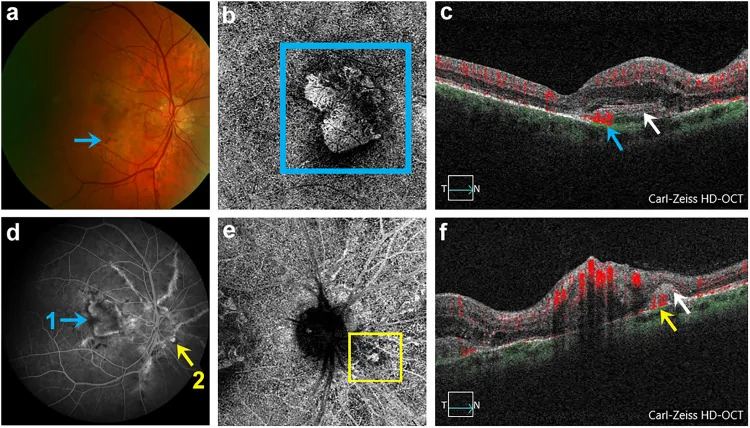
ภาพผลการตรวจหลอดเลือดด้วย Optical Coherence Tomography Angiography ของเส้นเลือดใหม่คอรอยด์ Adnan Kilani; Denise Vogt; Armin Wolf; Efstathios Vounotrypidis. The role of multimodal imaging in characterization and monitoring of choroidal neovascularization secondary to angioid streaks. Eur J Ophthalmol. 2025 Jan 27; 35(1):306-313 Figure 3. PM
CI D: PMC11697489. License: CC BY.
ตาขวาที่มี angioid streaks (AS), CNV 2 ตำแหน่ง (จอตาและใกล้หัวประสาทตา) และ drusen หัวประสาทตา (ONHD) ของผู้ป่วยหมายเลข 3 (a) จอตาที่มี AS, ONHD, CNV จอตา และเลือดออกในจอตา (ลูกศรสีน้ำเงิน) (b) OCTA ของ CNV จอตาที่ตรวจพบในการแบ่งส่วนเรตินาชั้นนอก-คอริโอแคปิลลาริส (ORCC) (สี่เหลี่ยมสีน้ำเงิน) (c) B-scan ที่สอดคล้องของ CNV จอตาที่มีการลงทะเบียนการไหลเวียนเลือด (ลูกศรสีน้ำเงิน) (d) FA เผยให้เห็น CNV จอตา (กำหนดเป็น 1, ลูกศรสีน้ำเงิน) และ CNV ใกล้หัวประสาทตา (กำหนดเป็น 2, ลูกศรสีเหลือง) (e) การแสดง SD-OCTA ของ CNV ใกล้หัวประสาทตาที่ตรวจพบในการแบ่งส่วน ORCC (สี่เหลี่ยมสีเหลือง) (f) B-scan ที่สอดคล้องของ CNV ใกล้หัวประสาทตาที่มีการลงทะเบียนการไหลเวียนเลือด (ลูกศรสีเหลือง) และสารสะท้อนแสงสูงใต้จอตา (SHRM) (ลูกศรสีขาว)
การประเมินภาพหลายรูปแบบเป็นพื้นฐานสำหรับการวินิจฉัยเส้นเลือดใหม่ในคอรอยด์ OCTA มีบทบาทสำคัญ แต่บางครั้งอาจไม่เพียงพอหากใช้เพียงอย่างเดียว
OCTA สามารถใช้ได้ทั้งกับ SD-OCT (โดเมนสเปกตรัม) และ SS-OCT (แหล่งกำเนิดแสงแบบกวาด) หลังการถ่ายภาพ การประมวลผลการแบ่งส่วนจะแสดงการไหลเวียนเลือดในชั้นจอตาแต่ละชั้น รอบ RPE และคอรอยด์ เป็นภาพ en face
เส้นเลือดใหม่ในคอรอยด์ชนิดที่ 1
ตำแหน่ง : ระหว่าง RPE และเยื่อบรูค (ใต้ RPE )
ลักษณะ OCTA : เครือข่ายหลอดเลือดรูปพัดทะเล (sea-fan) หรือรูปปะการัง (coral-like) ใน en face OCTA จะเห็นที่ชั้น RPE ถึงคอริโอแคปิลลาริส 8)
หลอดเลือดใหม่ชนิดจอประสาทตา ชนิดที่ 1 แบบพาคิคอรอยด์ (Pachychoroid type 1 MNV) : แสดงโครงสร้างหลอดเลือดที่โตเต็มที่และแบนราบ โดยเห็นได้ชัดเจนบน OCTA SIRE เป็นตัวบ่งชี้ทางชีวภาพ ที่มีประโยชน์ 6) สามารถตรวจพบสัญญาณชั้นคู่ (double layer sign) ได้จาก OCT 8)
หลอดเลือดใหม่คอรอยด์ชนิดที่ 2
ตำแหน่ง : ทะลุผ่าน RPE และขยายเข้าไปในช่องใต้จอประสาทตา
ลักษณะทาง OCTA : ปรากฏเป็นรอยโรคสะท้อนแสงสูงเหนือ RPE บางครั้งอาจแสดงห่วงหลอดเลือดหรือรูปแบบคล้ายล้อ
ผลการตรวจ FA ที่สอดคล้อง : สอดคล้องกับหลอดเลือดใหม่คอรอยด์ ชนิดคลาสสิก (classic CNV) โดยแสดงการเรืองแสงเกินขอบเขตชัดเจนตั้งแต่ระยะแรก
หลอดเลือดใหม่คอรอยด์ชนิดที่ 3 (RAP)
ตำแหน่ง : การเจริญของหลอดเลือดแบบแองจิโอมาโตซัสในจอประสาทตา (retinal angiomatous proliferation)
ลักษณะทาง OCTA : หลอดเลือดผิดปกติจะถูกแสดงในชั้นในของจอประสาทตา มักมองเห็นได้ชัดเจน สัญญาณการไหลเวียนเลือดต่อเนื่องจนถึงสัญญาณ bump (bump sign) เป็นลักษณะเฉพาะ 8)
ลักษณะทางคลินิก : มักมีเลือดออกในจอประสาทตา แบบจุดและจอประสาทตา บวมน้ำแบบถุงน้ำเล็กๆ ร่วมด้วย และดำเนินโรคเร็ว
โรคหลอดเลือดคอรอยด์ แบบโพลิป (PCV ) ถือเป็นชนิดย่อยของหลอดเลือดใหม่คอรอยด์ ชนิดที่ 1 ประกอบด้วยเครือข่ายหลอดเลือดใหม่แบบแตกแขนง (BNN) และรอยโรคโพลิปที่ส่วนปลาย
อัตราการตรวจพบ BNN : ตรวจพบได้เกือบ 100% โดย OCTA 7) อัตราการตรวจพบโพลิป : ประมาณ 79% เท่านั้นใน OCTA 7) การไม่เห็นภาพเกิดจากความสูงของโพลิปที่เพิ่มขึ้น การเต้นเป็นจังหวะ และการบดบังจากเลือดออกใต้จอประสาทตา 7) การจำแนกทางสัณฐานวิทยาของ BNN : แบ่งเป็น 4 ชนิด: ชนิดต้นไม้ตาย (dead-tree), ชนิดพุ่มปะการัง (coral-bush), ชนิดต่อเชื่อม (anastomosis) และชนิดคล้ายเทียม (pseudopod-like) 7) การจำแนกโครงสร้างของ BNN (การจำแนกของ Huang) : 3 ชนิด: ชนิดลำต้น (trunk), ชนิดโกลเมอรูลัส (glomeruli) และชนิดแท่ง (stick) 7) การเปรียบเทียบกับ ICGA : มีรายงานว่า OCTA มีความไว 97% เทียบกับ ICGA 66% ในการตรวจหาเส้นเลือดใหม่ในคอรอยด์ชนิด pachychoroid 6)
ลักษณะของวิธีการตรวจแต่ละวิธีแสดงไว้ด้านล่าง
การตรวจ ข้อดี ข้อจำกัด FA ตรวจจับการรั่วซึม, การจำแนกแบบคลาสสิก/ซ่อนเร้น ต้องใช้สารทึบรังสี (รุกล้ำ) ICGA ดีเยี่ยมในการแสดงภาพโพลิป ต้องใช้สารทึบรังสี (รุกล้ำ) OCTA ไม่รุกล้ำ, ความละเอียดเชิงลึก อัตราการตรวจพบโพลิปประมาณ 79%
OCTA มีสิ่งแปลกปลอม (artifact) เฉพาะที่อาจทำให้เกิดผลบวกลวงและผลลบลวงได้ สิ่งสำคัญแสดงไว้ด้านล่าง
สิ่งแปลกปลอม สาเหตุ การจัดการ การฉายภาพ สัญญาณเท็จจากการไหลเวียนเลือดชั้นตื้นถูกฉายลงสู่ชั้นลึก ยืนยันด้วยภาพตัดขวาง B-scan การแบ่งชั้น การบิดเบือนขอบเขตชั้นเนื่องจากการยื่นออกมาของเส้นเลือดใหม่คอรอยด์ ปรับการแบ่งชั้นด้วยตนเอง การเคลื่อนไหว การเคลื่อนตำแหน่งเนื่องจากการเคลื่อนไหวของลูกตาหรือร่างกาย การแนะนำให้จ้องและยึดศีรษะอย่างเคร่งครัด
แม้ในเส้นเลือดใหม่คอรอยด์ ที่เกิดร่วมกับการกลายเป็นปูนของตาขาวและคอรอยด์ OCTA ก็สามารถแสดงโครงข่ายเส้นเลือดใหม่ได้ 4) แม้จะเป็นโรคที่พบได้ยาก แต่การยืนยันด้วยภาพมีความสัมพันธ์โดยตรงกับการตัดสินใจแผนการรักษา
Q
เป็นไปได้หรือไม่ที่เส้นเลือดใหม่ในคอรอยด์จะไม่เห็นใน OCTA?
A
ผลลบลวงอาจเกิดขึ้นได้เนื่องจากสิ่งรบกวนจากการฉายภาพและข้อผิดพลาดในการแบ่งส่วน นอกจากนี้ อัตราการตรวจพบติ่งเนื้อในโรคโพลิปอยด์คอรอยด์ วาสคูโลพาทีอยู่ที่ประมาณ 79% เท่านั้น 7) และการถ่ายภาพทำได้ยากหากมีเลือดออกใต้จอประสาทตา จำนวนมาก ต้องตีความ OCTA ร่วมกับการตรวจ OCT แบบ B-scan เสมอ
Q
OCTA สามารถแทนที่การตรวจฟลูออเรสซีนแองจิโอกราฟี (FA) หรืออินโดไซยานีนกรีนแองจิโอกราฟี (ICGA) ได้หรือไม่?
A
ในการตรวจหาเส้นเลือดใหม่ชนิดที่ 2 (BNN) OCTA มีความไวเท่ากับหรือสูงกว่า ICGA 6) แต่ FA และ ICGA ยังคงมีประโยชน์ในบางสถานการณ์เพื่อประเมินการรั่วซึมและยืนยันติ่งเนื้อ โดยเฉพาะในโรคโพลิปอยด์คอรอยด์ วาสคูโลพาทีและการประเมินผลการรักษา แนะนำให้ใช้การถ่ายภาพหลายรูปแบบร่วมกัน
การฉีดยาต้าน VEGF เข้าแก้วตาเป็นการรักษาทางเลือกแรกสำหรับเส้นเลือดใหม่ในคอรอยด์ทุกชนิด
จอประสาทตา เสื่อมตามอายุชนิดเปียกทั่วไป (เส้นเลือดใหม่ในคอรอยด์ใต้รอยบุ๋ม)ยาต้าน VEGF เพียงอย่างเดียว 8) โรคโพลิปอยด์คอรอยด์ วาสคูโลพาที : หากสายตาดี ≥ 0.6 ให้ใช้ยาต้าน VEGF เพียงอย่างเดียว หากสายตาดี ≤ 0.5 การรักษาด้วยแสงไดนามิก (PDT ) เพียงอย่างเดียวหรือร่วมกับยาต้าน VEGF เป็นทางเลือก 8) ในช่วงไม่กี่ปีที่ผ่านมา แนวโน้มการรักษาโรคโพลิปอยด์คอรอยด์ วาสคูโลพาทีเปลี่ยนจากการใช้ PDT ไปสู่การใช้ยาต้าน VEGF เพียงอย่างเดียว 6) เส้นเลือดใหม่ในคอรอยด์ที่เกี่ยวข้องกับ PXE : ยาต้าน VEGF ช่วยให้สายตาดีขึ้นในระยะสั้น แต่ความถี่ในการฉีดมักสูง (ระยะห่างเฉลี่ย 4.4 เดือน เทียบกับ 7.2 เดือนในจอประสาทตา เสื่อมตามอายุทั่วไป) 5) ทำให้การจัดการระยะยาวเป็นความท้าทายเส้นเลือดใหม่ในคอรอยด์ที่เกี่ยวข้องกับ SCC : การให้รานิบิซูแมบ แบบ PRN (3-9 ครั้งใน 6 ปี) มีรายงานว่าทำให้สายตาดีถึง 20/25 4) PEHCR ยาต้าน VEGF มีประโยชน์ โดยมีการฉีดเฉลี่ย 7.7 ครั้ง 1)
พิจารณาในโรคโพลิปอยด์คอรอยด์ วาสคูโลพาทีชนิดแนวตั้ง (กรณีสายตาไม่ดี) หรือกรณีที่ดื้อต่อยาต้าน VEGF ฉีดเวอร์เทพออร์ฟินทางหลอดเลือดดำ จากนั้นฉายเลเซอร์ความยาวคลื่น 689 นาโนเมตร
มีบางกรณีที่ดื้อต่อการรักษาด้วย anti-VEGF มาตรฐาน เช่น หลอดเลือดคอรอยด์ ใหม่ที่เกี่ยวข้องกับ PIC มีรายงานผู้ป่วยที่ไม่ตอบสนองอย่างสมบูรณ์ต่อ Aflibercept แต่รอยโรคถูกควบคุมได้หลังจากให้ Faricimab (ยาที่ยับยั้ง VEGF-A และ Ang-2 แบบคู่) ขนาด 6 มก. จำนวน 6 ครั้ง 3)
การตอบสนองต่อการรักษาแตกต่างกันตามชนิดของหลอดเลือดคอรอยด์ ใหม่ ชนิดที่ 3 (RAP ) ดำเนินโรคเร็วและต้องได้รับการแทรกแซงตั้งแต่เนิ่นๆ
การฉีด anti-VEGF จำเป็นต้องมีการติดตามผลอย่างสม่ำเสมอและการให้ยาต่อเนื่อง การหยุดยาเองอาจทำให้เกิดการกลับเป็นซ้ำหรืออาการแย่ลง
หลังการรักษาด้วย PDT สำหรับโรคหลอดเลือดคอรอยด์ โพลิปอยด์ อาจเกิดการมองเห็น ลดลงชั่วคราวหรือไวต่อแสง มากขึ้น
หลอดเลือดคอรอยด์ ใหม่ที่เกี่ยวข้องกับโรคทางพันธุกรรม เช่น PXE มักดื้อต่อการรักษาและอาจต้องให้ยาความถี่สูงในระยะยาว 5)
Q
การตอบสนองต่อการรักษาแตกต่างกันตามชนิดของหลอดเลือดคอรอยด์ใหม่หรือไม่?
A
ทุกชนิดรักษาด้วย anti-VEGF เป็นการรักษาพื้นฐาน แต่มีการตอบสนองที่แตกต่างกัน หลอดเลือดใหม่จอประสาทตา ชนิดที่ 1 (รวมถึงชนิด pachychoroid) ค่อนข้างควบคุมได้ง่ายกว่า ในขณะที่โรคหลอดเลือดคอรอยด์ โพลิปอยด์จะพิจารณาใช้ PDT ร่วมด้วยตามระดับการมองเห็น ชนิดที่ 3 (RAP ) ดำเนินโรคเร็วและมักต้องได้รับการรักษาอย่างเข้มข้น กรณีที่มีโรคพื้นฐานเช่น PXE หรือ PIC อาจดื้อต่อการรักษามากขึ้น 5)
วิถีทางร่วมของหลอดเลือดคอรอยด์ ใหม่คือความผิดปกติของเยื่อบรูชและการผลิต VEGF ที่เพิ่มขึ้น
เมื่ออายุมากขึ้นหรือมีความโน้มเอียงทางพันธุกรรม การสะสมของผลิตภัณฑ์เมตาบอลิซึม (ดรูเซน ) บนเยื่อบรูชจะขัดขวางการขนส่งสารระหว่าง RPE และชั้นหลอดเลือดฝอยคอรอยด์ ทำให้เกิดภาวะขาดออกซิเจนเฉพาะที่ กระตุ้นให้ RPE ผลิต VEGF ซึ่งส่งเสริมการเคลื่อนที่และการเพิ่มจำนวนของเซลล์บุผนังหลอดเลือด เริ่มต้นกระบวนการสร้างหลอดเลือดใหม่
หลอดเลือดคอรอยด์ ใหม่ที่เกี่ยวข้องกับโรคทางพันธุกรรมมีกลไกเฉพาะ
กลุ่มอาการ Cowden (การกลายพันธุ์ PTEN) : การสูญเสียการทำงานของ PTEN ทำให้สัญญาณ PI3K/Akt/VEGF ถูกกระตุ้นอย่างต่อเนื่อง 5) ซึ่งอาจเป็นกลไกระดับโมเลกุลของการดื้อต่อการรักษาด้วย anti-VEGFPXE (การกลายพันธุ์ ABCC 6)FA แสดงให้เห็นความสัมพันธ์กับจอประสาทตา เสื่อมรุนแรง 5) ซึ่งส่งผลต่อความรุนแรงของหลอดเลือดคอรอยด์ ใหม่
ในแนวคิดของ pachychoroid neovasculopathy คอรอยด์ ที่หนาผิดปกติจะกดทับและทำให้ชั้นหลอดเลือดฝอยคอรอยด์ ขาดเลือด ทำให้เกิดภาวะเครียดออกซิเดชัน เรื้อรังต่อ RPE และเป็นแหล่งเพาะพันธุ์ของหลอดเลือดใหม่จอประสาทตา ชนิดที่ 1
การแบ่งส่วนอัตโนมัติโดยใช้การเรียนรู้เชิงลึกกำลังถูกวิจัยเพื่อปรับปรุงความแม่นยำและความสามารถในการทำซ้ำของการตรวจหาเส้นเลือดใหม่ในคอรอยด์ การปรับปรุงเทคนิคการกำจัดสิ่งรบกวนจากการฉายภาพ (PR-OCTA ) ก็กำลังดำเนินไป
ด้วยการแพร่หลายของ OCTA แนวคิดทางพยาธิวิทยาอิสระของเส้นเลือดใหม่ในจอประสาทตา ชนิดที่ 1 บนพื้นหลังคอรอยด์หนา กำลังถูกสร้างขึ้น 6) การตรวจสอบความสำคัญทางคลินิกของตัวบ่งชี้ทางชีวภาพ ใหม่ เช่น SIRE ยังคงดำเนินต่อไป
การถกเถียงยังคงดำเนินต่อไปว่าติ่งเนื้อใน Polypoidal Choroidal Vasculopathy เป็นโป่งพองที่แท้จริงหรือไม่ 6) การกำหนดมาตรฐานสากลของระบบการตั้งชื่อและการจำแนกเป็นปัญหาที่ยังไม่ได้รับการแก้ไข ซึ่งสำคัญต่อการรวมกลยุทธ์การรักษา
Faricimab ซึ่งยับยั้ง VEGF-A และ Ang-2 พร้อมกัน กำลังถูกศึกษาเพื่อประยุกต์ใช้กับเส้นเลือดใหม่ในคอรอยด์ที่ดื้อต่อการรักษาด้วยยาต้าน VEGF ชนิดเดี่ยวที่มีอยู่ 3) ผ่านกลไกการออกฤทธิ์ใหม่ในการทำให้หลอดเลือดคงตัว คาดว่าจะยืดระยะเวลาการฉีดและประสิทธิภาพในกรณีที่ดื้อต่อการรักษา
Elwood KF, et al. PEHCR : Diagnostic and Therapeutic Challenges. Medicina. 2023;59(9):1507.
Garg A, Khaleel H, Wahab C, Yan P. Acquired Focal Choroidal Excavation Secondary to Pachychoroid Choroidal Neovascular Membrane After Central Serous Chorioretinopathy. J Vitreoretin Dis. 2023;7(4):340-343. doi:10.1177/24741264231163395. PMID:37927310; PMCI D:PMC10621713.
Rezaei K, et al. Atypical choroidal neovascular membrane. Am J Ophthalmol Case Rep. 2024;36:102191.
Battaglia Parodi M, et al. CNV complicating sclerochoroidal calcifications. Am J Ophthalmol Case Rep. 2021;24:101235.
Wu F, Mukai S. Refractory CNV in PXE and Cowden Syndrome. J VitreoRetinal Dis. 2023;7(1):70-73.
Cheung CMG, et al. Polypoidal Choroidal Vasculopathy. Eye. 2024;38:S1-S22.
Sen P, Manayath G, Shroff D, Salloju V, Dhar P. Polypoidal Choroidal Vasculopathy: An Update on Diagnosis and Treatment. Clin Ophthalmol. 2023;17:53-70. doi:10.2147/OPTH.S385827. PMID:36636621; PMCI D:PMC9831529.
AAO . Age-Related Macular Degeneration Preferred Practice Pattern. Ophthalmology. 2024.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต