Polypoidal choroidal vasculopathy (PCV ) เป็นโรคที่มีพื้นฐานจากเครือข่ายหลอดเลือดคอรอยด์ ที่ผิดปกติแบบแตกแขนง และจัดอยู่ในกลุ่ม pachychoroid spectrum 5, 8)
พบได้ 22-62% ของจอประสาทตา เสื่อมชนิดเปียกที่สัมพันธ์กับอายุ (nAMD ) ในชาวเอเชีย และมีรายงานว่าประมาณครึ่งหนึ่งของ nAMD เป็น PCV 5, 11)
เมื่อเทียบกับ nAMD ทั่วไป มักมีเลือดออกมากกว่าและของเหลวในจอประสาทตา (IRF) น้อยกว่า และมีแนวโน้มเกิดเลือดออกใต้จอประสาทตา (SMH) ปริมาณมาก 5)
การตรวจหลอดเลือดด้วยสีอินโดไซยานีนกรีน (ICGA ) เป็นมาตรฐานทองคำ และการตรวจพบรอยโรคแบบ polyp เป็นการวินิจฉัยที่แน่นอน 5, 7)
ในกรณีที่สายตาดี (≥0.6) แนะนำให้รักษาด้วยยา anti-VEGF เพียงอย่างเดียว ส่วนกรณีที่สายตา ≤0.5 แนะนำให้ใช้ PDT เพียงอย่างเดียวหรือร่วมกับ anti-VEGF 9, 10)
Aflibercept มีอัตราการหายของ polyp อย่างสมบูรณ์ 40-50% สูงกว่า ranibizumab (20-30%) และเป็นยาทางเลือกแรกในปัจจุบัน 9)
หลังจากตอบสนองต่อการรักษา ต้องระวังเลือดออกใต้จอประสาทตา อย่างกะทันหันจากการแตกของ polyp
Polypoidal choroidal vasculopathy (PCV ) เป็นโรคที่มีลักษณะเฉพาะคือเครือข่ายหลอดเลือดคอรอยด์ ที่ผิดปกติแบบแตกแขนง (branching vascular network; BVN) และการขยายตัวของหลอดเลือดแบบ polyp ที่ปลายทาง 5) เป็นชนิดย่อยของจอประสาทตา เสื่อมที่สัมพันธ์กับอายุ (AMD ) ซึ่งแสดงการขยายตัวของหลอดเลือดคอรอยด์ แบบ polyp ในการตรวจหลอดเลือดด้วยสีอินโดไซยานีนกรีน (ICGA ) ทำให้เกิดรอยโรคทรงกลมสีส้มแดงใต้เยื่อบุผิวรับแสง (RPE ) และทำให้เกิดการลอกตัวของเยื่อบุผิวรับแสง (PED ) แบบมีน้ำหรือเลือด
รายงานครั้งแรกในทศวรรษ 1980 ในชื่อ “idiopathic hemorrhagic RPE detachment” 5) ปัจจุบันจัดอยู่ในกลุ่ม pachychoroid spectrum ซึ่งเป็นสเปกตรัมต่อเนื่องกับ central serous chorioretinopathy (CSC ) และ pachychoroid neovasculopathy (PNV ) 5, 6) มีการชี้ให้เห็นว่าแนวคิดของโรคนี้อาจเปลี่ยนแปลงเพิ่มเติมในอนาคต
มักเกิดในผู้ชายอายุ 50–65 ปี โดยรวมในชาวเอเชีย พบได้ 22–62% ของผู้ป่วย nAMD ชนิด渗出 5) และมีรายงานว่าประมาณครึ่งหนึ่งของ AMD ชนิด渗出เป็น PCV 11) ในชาวคอเคเซียนตะวันตก พบเพียงประมาณ 10–20% 5) คาดว่าประชากรโลกอายุมากกว่า 65 ปีจะเกิน 1.5 พันล้านคนภายในปี 2050 ส่งผลให้ผู้ป่วย nAMD และ PCV เพิ่มขึ้น 5)
Q
โรคโพลิปอยด์ คอรอยดัล วาสคูโลพาที (PCV) เป็นโรคเดียวกับจอประสาทตาเสื่อมตามอายุ (AMD) หรือไม่?
A
PCV มักถูกจัดเป็นชนิดย่อยของ nAMD แต่มีความแตกต่างในด้านพยาธิวิทยา การตอบสนองต่อการรักษา และพื้นฐานทางพันธุกรรม มีแนวโน้มเลือดออกมากกว่าและมีของเหลวในจอประสาทตา ชั้นใน (IRF) น้อยกว่าเมื่อเทียบกับ nAMD ปัจจุบันยังคงมีการถกเถียงว่าควรถือเป็นโรคอิสระในสเปกตรัมคอรอยด์หนา หรือไม่ 5, 6)
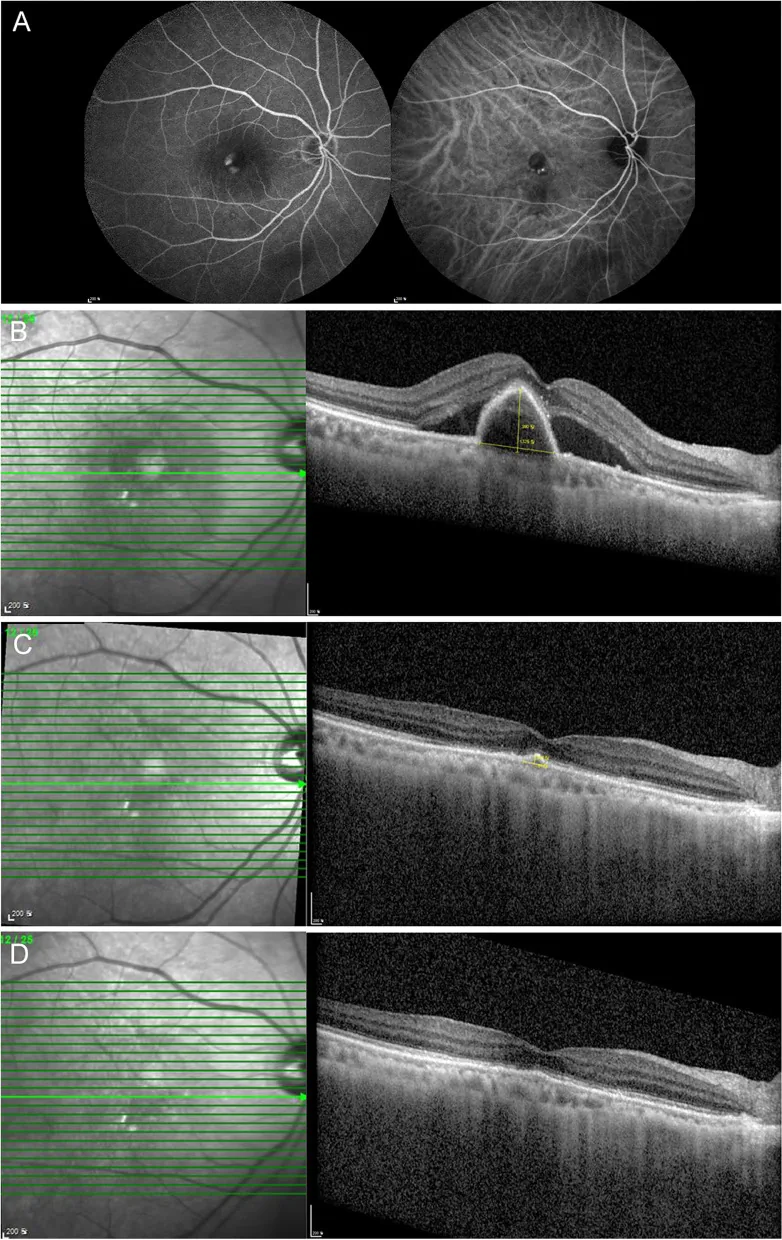
ผลการตรวจ angiography และการดำเนินของจอประสาทตาชั้น pigment epithelium หลุดลอกชนิด serous ใน OCT ใน PCV Nam SW, et al. Response to brolucizumab treatment for refractory serous pigment epithelial detachment secondary to polypoidal choroidal vasculopathy. BMC Ophthalmol. 2022. Figure 2. PM
CI D: PMC9749193. License: CC BY.
A แสดง fluorescein angiography และ indocyanine green angiography ของเส้นเลือดใหม่
คอรอยด์ ชนิด polypoidal ส่วน B, C และ D แสดงภาพ
OCT การดีขึ้นของ
จอประสาทตา ชั้น pigment epithelium หลุดลอกชนิด serous (
PED ) และ
ของเหลวใต้จอประสาทตา (SRF) ตามการรักษา ซึ่งสอดคล้องกับ
PED ชนิด serous ที่กล่าวถึงในหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก”
การมองเห็น ลดลงการมองเห็น ลดลงอย่างเฉียบพลันและรวดเร็ว 5) ภาพบิดเบี้ยว (metamorphopsia)จอประสาทตา จุดบอดกลาง (central scotoma)จอประสาทตา ผู้ป่วยจะรู้สึกมีจุดมืดตรงกลางลานสายตาการมองเห็น แย่ลงอย่างกะทันหันจอประสาทตา (SMH) จำนวนมาก มีลักษณะการเปลี่ยนแปลงแบบเลือดออกมาก และรายงานว่าประมาณ 10% ของผู้ป่วยเกิด SMH ภายใน 5 ปี 5)
เมื่อเทียบกับ nAMD ทั่วไป PCV มีเลือดออกมากกว่าในขณะที่มีของเหลวในจอประสาทตา ชั้นใน (IRF) น้อยกว่า นอกจากนี้ยังมีลักษณะเด่นคือ PED ชนิด serous และเลือดออกใต้จอประสาทตา บ่อย
การตรวจจอประสาทตา พบ รอยโรคยกตัวสีส้มแดง ที่เป็นลักษณะเฉพาะ สังเกตเป็นเส้นเลือดโป่งพองแบบ polypoidal ใต้ retinal pigment epithelium (RPE ) มักพบร่วมกับ PED ชนิดเลือดออกหรือ PED ชนิด serosanguinous
ลักษณะของ PCV
รอยโรคทรงกลมสีส้มแดง : การขยายตัวของหลอดเลือดแบบโพลิปใต้ RPE สังเกตเป็นรอยโรคทรงกลมสีส้มแดงด้วยกล้องตรวจตา
การหลุดลอกของเยื่อบุผิวเม็ดสีแบบเลือดออก : การนูนสูงชันเนื่องจากเลือดออกมากใต้ RPE มักมี IRF น้อย
การหลุดลอกของเยื่อบุผิวเม็ดสีแบบเซรุ่ม-เลือด : การหลุดลอกของ RPE ที่มีทั้งเซรุ่มและเลือดปนกัน
การเปรียบเทียบกับ nAMD
PCV ICGA การอุดตันโพลิปเป็นเป้าหมายการรักษา
nAMD ทั่วไป : หลอดเลือดใหม่คอรอยด์ (CNV ) เป็นหลัก, IRF มาก, เลือดออกน้อย เห็นชัดใน FA
ผล OCT ให้ข้อมูลสำคัญในการวินิจฉัย PCV 5)
สัญญาณสองชั้น : ผลที่แสดงโครงสร้างสองชั้นของ RPE และเยื่อบรูค พบในบริเวณเครือข่ายหลอดเลือดผิดปกติ ความไว 59% 5) การนูนสูงชันของ RPE : มีลักษณะการนูนสูงชันของ RPE ตรงกับรอยโรคโพลิปสัญญาณฮีมาโตคริต : ภาพการแยกของเหลวและเลือดภายใน PED แบบเลือดออกโบลา (PED รูปนิ้วหัวแม่มือ) : การนูนสูงชันกลมคล้ายโพลิปใต้ RPE เกณฑ์ APOIS : การรวมผล OCT ทำให้ AUC 0.90 ในการแยกจาก nAMD 5, 12)
เป็นที่ทราบว่าหลายกรณีมีคอรอยด์หนา และความสัมพันธ์กับสเปกตรัมพาคิคอรอยด์ เป็นที่สนใจ
ICGA คอรอยด์ แบบโพลิปอยด์ที่มีลักษณะเฉพาะ และโครงข่ายหลอดเลือดผิดปกติ (หลอดเลือดแบบร่างแห) การตรวจพบรอยโรคโพลิปเป็นการวินิจฉัยที่แน่ชัด 5, 7) การตรวจหลอดเลือดด้วยฟลูออเรสซีน (FA ) : บริเวณที่ตรงกับรอยโรคโพลิปจะแสดงการเรืองแสงมากเกินไปค่อนข้างเร็ว ในระยะหลังมักแสดงจุดบกพร่องแบบหน้าต่าง (window defect) ที่สอดคล้องกับรอยโรคฝ่อ
OCTA สามารถแสดงภาพหลอดเลือดได้โดยไม่ต้องรุกราน และ BVN (โครงข่ายหลอดเลือดผิดปกติ) มักแสดงได้ชัดเจนกว่า ICGA 5) มีรายงานการจำแนก BNN ออกเป็น 3 ชนิด โดยมีความไวในการตรวจหา PCV 82.6% และความจำเพาะ 100% 5) อย่างไรก็ตาม การตรวจหารอยโรคโพลิปยังมีข้อจำกัดและไม่ดีเท่า ICGA การวินิจฉัยชนิดของ PCV หรือการเจริญของหลอดเลือดในจอประสาทตา แบบแองจิโอมาโตซัส (RAP ) ด้วย OCTA เพียงอย่างเดียวยังเป็นความท้าทาย ดังนั้นการวินิจฉัยด้วยภาพหลายรูปแบบจึงมีความสำคัญ
โรคหลอดเลือดคอรอยด์ โพลิปอยด์เป็นชนิดพิเศษของเส้นเลือดใหม่คอรอยด์ ชนิดที่ 1 (CNV ) ที่อยู่ใต้ชั้น RPE 5, 8) พื้นฐานทางพยาธิวิทยาที่สำคัญคือ ภาวะคอรอยด์หนา (pachychoroid) ซึ่งมีลักษณะการขยายตัวของชั้นฮาลเลอร์ (ชั้นหลอดเลือดคอรอยด์ ชั้นนอก) และการบางลงของชั้นแซทเลอร์และเยื่อเส้นเลือดฝอยคอรอยด์ ร่วมด้วย 5)
การคั่งของเลือดในหลอดเลือดดำวอร์ติโคส : การคั่งของเลือดในหลอดเลือดดำคอรอยด์ ทำให้ชั้นฮาลเลอร์ขยายตัว ในประมาณ 90% ของกรณีพบการเชื่อมต่อระหว่างหลอดเลือดพาคีที่ขยายตัวกับหลอดเลือดดำวอร์ติโคส 5) ภาวะขาดเลือดและการอุดตันของเยื่อเส้นเลือดฝอยคอรอยด์ : ภาวะขาดเลือดในระดับเส้นเลือดฝอยคอรอยด์ กระตุ้นให้เกิดการสร้างกลุ่มเส้นเลือดใหม่ (BVN) 5) ความเสียหายต่อ RPE และเยื่อบรูค : การคั่งของเลือดในคอรอยด์ เรื้อรังทำให้ RPE และเยื่อบรูค เสียหาย ร่วมกับกิจกรรมของโปรตีเอสที่เพิ่มขึ้น นำไปสู่การเกิดรอยโรคแบบโพลิปอยด์ 5)
มีรายงานความสัมพันธ์กับความหลากหลายของยีน CF H (คอมพลีเมนต์ แฟกเตอร์ H) และ ARMS 2/HTRA1 5) มียีนที่ไวต่อโรคบางส่วนร่วมกับ nAMD ทั่วไป แต่ในชนิดที่ไม่ใช่พาคีคอรอยด์ (PCV ที่ขับเคลื่อนโดยดรูเซน ความหนาคอรอยด์ ปกติ) ความสัมพันธ์กับ ARMS 2/HTRA1 จะแข็งแรงกว่า 5, 8) SNP ของยีน ANGP T2 และการกลายพันธุ์แบบมิสเซนส์ของยีน FGD6 ก็ถูกเสนอว่ามีความสัมพันธ์กับการเกิด PCV 5)
ประมาณครึ่งหนึ่งของดวงตาที่เป็น PCV มีความหนาคอรอยด์ ปกติ 5) ชนิดพาคีคอรอยด์ มีแนวโน้มอายุน้อยกว่า มีลักษณะคล้าย CSC หลายอย่าง ร่วมกับภาวะหลอดเลือดคอรอยด์ รั่วซึมมากเกินไป และอาจดื้อต่อการรักษาด้วย anti-VEGF ชนิดไม่พาคีคอรอยด์ เป็นชนิดที่ขับเคลื่อนโดยดรูเซน (ลักษณะคล้าย AMD ) และมีความสัมพันธ์กับ ARMS 2/HTRA1 ที่แข็งแรงกว่า 5, 8)
การขาดการไหลเวียนเลือดในแผ่นเส้นเลือดฝอยคอรอยด์ (CCF D) เพิ่มขึ้นไม่เพียงแต่ในตาที่เป็น PCV แต่ยังรวมถึงตาข้างปกติด้วย ซึ่งบ่งชี้ว่าภาวะคอรอยด์หนา อาจเป็นปัจจัยโน้มเอียงทั่วร่างกาย ไม่ใช่เฉพาะที่ 5)
PCV ทุติยภูมิหลังคอรอยด์ อักเสบRPE และเยื่อบรูค จากคอรอยด์ อักเสบจากวัณโรคอาจเป็นพื้นดินที่เอื้ออำนวย มีรายงานผู้ป่วยที่เกิด PCV ประมาณ 20 ปีหลังการอักเสบ และการมองเห็น ดีขึ้นจาก 6/9 เป็น 6/6 หลังได้รับ aflibercept 3 ครั้ง 1) การดำเนินโรคเร็วหลังวัคซีน COVID-19 : มีรายงานผู้ป่วย (ชายอายุ 79 ปี) ที่มีอาการปรากฏ 16 ชั่วโมงหลังเข็มที่สาม และดำเนินไปอย่างรวดเร็วเป็นเลือดออกใต้จอประสาทตา จำนวนมากภายใน 2 สัปดาห์ 4)
ไม่มีวิธีการป้องกันปฐมภูมิที่ชัดเจนที่เกี่ยวข้องกับวิถีชีวิตสำหรับโรคหลอดเลือดคอรอยด์ แบบโพลิปอยด์ หากคุณรู้สึกว่าภาพบิดเบี้ยว หรือมืดลงบริเวณศูนย์กลางลานสายตาหลังอายุ 50 ปี ให้พบจักษุแพทย์ทันที การตรวจอวัยวะภายในตาเป็นประจำช่วยในการตรวจพบแต่เนิ่นๆ การสูบบุหรี่เป็นปัจจัยเสี่ยงทั่วไปสำหรับจอประสาทตา เสื่อมตามอายุ ดังนั้นจึงแนะนำให้เลิกสูบบุหรี่
PCV ประกอบด้วยรอยโรคแบบโพลิปและเครือข่ายหลอดเลือดผิดปกติ ตามเกณฑ์การวินิจฉัยปัจจุบัน จำแนกได้ดังนี้
กรณียืนยัน : พบรอยโรคยกตัวสีส้มแดงในการตรวจอวัยวะภายในตา และตรวจพบรอยโรคแบบโพลิปใน ICGA 7) ผลการตรวจที่น่าสงสัย : พบเฉพาะเครือข่ายหลอดเลือดผิดปกติใน ICGA พบจอประสาทตาลอก ตัวแบบมีเลือดออกหรือมีน้ำใต้ชั้นเยื่อบุผิวเม็ดสีซ้ำๆ
เกณฑ์การวินิจฉัยที่อิงจาก ICGA ซึ่งกำหนดโดยกลุ่มศึกษา EVEREST ถูกใช้อย่างแพร่หลายในระดับนานาชาติ 7, 10) วินิจฉัย PCV หากเข้าเกณฑ์ข้อใดข้อหนึ่งต่อไปนี้
พบรอยโรคทรงกลมสีส้มแดงในการตรวจอวัยวะภายในตา
พบรอยโรคเรืองแสงมากแบบเป็นก้อนกลม (โพลิป) ใน ICGA
ตรวจพบเครือข่ายหลอดเลือดผิดปกติแบบแตกแขนง (BVN) ในการตรวจ ICGA
ICGA เป็นมาตรฐานทองคำในการวินิจฉัย PCV 5, 7) มีความโดดเด่นในการมองเห็น หลอดเลือดคอรอยด์ และเนื่องจากคุณสมบัติความยาวคลื่นยาวของ ICG ทำให้สามารถมองเห็นโครงสร้างหลอดเลือดได้แม้ผ่านเลือด ของเหลว และไขมันใต้ RPE 5) ระบุรอยโรคโพลิปอยด์ที่เรืองแสงเร็วและ BVN
ลักษณะเฉพาะของการตรวจแต่ละวิธีแสดงไว้ด้านล่าง
วิธีการตรวจ ผลการตรวจหลัก ข้อสังเกตพิเศษ ICGA BVN และโพลิป มาตรฐานทองคำ5, 7) OCT สัญญาณสองชั้นและโบลา เกณฑ์ APOIS AUC 0.905, 12) OCTA การจำแนก BNN3 และความไว 82.6% ไม่รุกราน5) FA การเรืองแสงมากเกินไปในระยะแรก / ข้อบกพร่องแบบหน้าต่าง มีประโยชน์ในการแสดงภาพ CNV
สำหรับการแยก PCV ด้วย OCT เพียงอย่างเดียว มีรายงาน AUC 0.90 ตามเกณฑ์ APOIS (APOIS PCV workgroup) 5, 12) เครื่องหมายสองชั้นมีประโยชน์สำหรับการคัดกรองในสถานที่ที่ไม่ทำ ICGA แต่ความไวเพียง 59% 5) ในสถานการณ์ที่ไม่มี ICGA การรวม OCT และ OCTA อาจเป็นทางเลือก แต่ ICGA ยังคงสำคัญสำหรับการตัดสินใจรักษา (เช่น การเพิ่ม PDT )
AMD ทั่วไป (type 1/2 CNV )ICGA เป็นจุดแยกโรคจอประสาทตา อักเสบชนิดเซรุ่มส่วนกลาง (CSC )คอรอยด์ และการมีเส้นเลือดใหม่มีประโยชน์โป่งพองของหลอดเลือดแดงจอตา : ต้องแยกจาก PED ชนิดเลือดออก
Q
สามารถวินิจฉัย PCV โดยไม่ต้องทำ ICGA ได้หรือไม่?
A
แม้ว่าความก้าวหน้าของ OCT และ OCTA จะทำให้การวินิจฉัยโดยไม่พึ่ง ICGA เป็นไปได้มากขึ้น แต่ในปัจจุบัน ICGA ยังคงเป็นมาตรฐานทองคำ แม้ว่าเกณฑ์ APOIS จะแสดงความสามารถในการแยกโรคสูงด้วย AUC 0.90 แต่ ICGA ยังคงเป็นการตรวจที่สำคัญสำหรับการตัดสินใจรักษา (เช่น การเพิ่ม PDT ) 5, 12)
แนวทางการรักษาปี 2012 โดยคณะทำงานศึกษาของกระทรวงสาธารณสุข แรงงาน และสวัสดิการ แนะนำให้เลือกการรักษาตามระดับสายตา
กรณีสายตาดี (0.6 ขึ้นไป) : พิจารณาการรักษาด้วยยาต้าน VEGF เพียงอย่างเดียวการมองเห็น 0.5 หรือต่ำกว่าการรักษาด้วยแสงไดนามิก (PDT ) เพียงอย่างเดียว หรือร่วมกับยาต้าน VEGF
ใน PCV การถดถอยของรอยโรคแบบ polyp มีความสัมพันธ์กับการกลับเป็นซ้ำหลังการรักษา Ranibizumab มีอัตราการถดถอยของ polyp อย่างสมบูรณ์ 20-30% ในขณะที่ aflibercept สูงกว่าคือ 40-50% ดังนั้นในช่วงไม่กี่ปีที่ผ่านมา การใช้ยายับยั้ง VEGF เพียงอย่างเดียวโดยไม่คำนึงถึงการมองเห็น จึงเพิ่มขึ้น 9)
การฉีดยาต้าน VEGF เข้าในน้ำวุ้นตา เป็นการรักษาทางเลือกแรกสำหรับ PCV 5, 9)
Aflibercept แสดงอัตราการอุดตันของ polyp ที่สูงกว่า ranibizumab ในการทดลอง PLANET พบว่า aflibercept เพียงอย่างเดียวไม่ด้อยกว่า aflibercept ร่วมกับ PDT (ผลลัพธ์ 1 ปี) 9) อัตราการอุดตันของ polyp สูงถึงมากกว่า 85% ในกลุ่มที่ได้รับยาเดี่ยว 3, 9)
Vella และคณะ (2021) รายงานว่า การให้ aflibercept หนึ่งครั้งในผู้ป่วย PCV ที่ไม่ตอบสนองต่อ ranibizumab หกครั้ง ส่งผลให้ของเหลวใต้จอประสาทตา (SRF) หายไปอย่างสมบูรณ์ 3)
PDT มีประสิทธิภาพโดยเฉพาะในการอุดตัน polyp ตัวอย่างใบสั่งยาดังนี้
Verteporfin : 6 มก./ตร.ม. ของพื้นที่ผิวกาย ให้ทางหลอดเลือดดำในเวลา 10 นาทีการฉายเลเซอร์: 15 นาทีหลังจากเริ่มฉีด, 689 นาโนเมตร, 600 มิลลิวัตต์/ตร.ซม., นาน 83 วินาที
ขนาดการฉาย: เส้นผ่านศูนย์กลางรอยโรคที่ใหญ่ที่สุดจากภาพถ่าย + 1000 ไมโครเมตร
ต้องหลีกเลี่ยงแสงแดดโดยตรงเป็นเวลา 2 วันหลังการรักษา
ในการรักษาแบบผสม PDT + ยายับยั้ง VEGF สามารถให้ยายับยั้ง VEGF ก่อน PDT (ภายใน 1 สัปดาห์) และในวันเดียวกับ PDT (ภายใต้การป้องกันแสง)
ชื่อการทดลอง การรักษา ผลลัพธ์หลัก EVEREST I PDT ร่วมกับ ranibizumabอัตราการอุดตันของโพลิป 77.8%10) EVEREST II PDT ร่วมกับ ranibizumab+9.6 ตัวอักษร เทียบกับยาเดี่ยว10) PLANET Aflibercept เดี่ยว พิสูจน์ความไม่ด้อยกว่า PDT 9)
ในการศึกษา EVEREST I อัตราการอุดตันของรอยโรคคือ 77.8% ด้วย PDT ร่วมกับ ranibizumab หรือ PDT เพียงอย่างเดียว ในขณะที่ ranibizumab เพียงอย่างเดียวอยู่ที่ 26.7%10) ในการศึกษา EVEREST II (RCT) กลุ่ม PDT ร่วมกับ ranibizumab แสดงการมองเห็น ดีขึ้น 9.6 ตัวอักษรเมื่อเทียบกับกลุ่ม ranibizumab เพียงอย่างเดียวที่สัปดาห์ที่ 2410)
เป็นทางเลือกที่มีการรุกรานน้อยกว่า PDT โดยมีรายงานประสิทธิภาพของเลเซอร์ไมโครพัลส์ 577 นาโนเมตร
Jafar และคณะ (2024) รายงานผู้ป่วย PCV ที่ได้รับการรักษาด้วยเลเซอร์ ไมโครพัลส์ 577 นาโนเมตร (รอบการทำงาน 5%, 400 mW, 200 μm, 200 ms) และ SRF หายไปอย่างสมบูรณ์หลังจาก 12 สัปดาห์ การมองเห็น ดีขึ้นจาก 20/60 เป็น 20/252)
ในกรณีที่มี SMH จำนวนมาก อาจจำเป็นต้องผ่าตัดน้ำวุ้นตา เพื่อนำก้อนเลือดออก5)
Sasajima และคณะ (2022) ได้ทำการผ่าตัดวุ้นตา โดยใช้ tissue plasminogen activator (tPA 12.5 ไมโครกรัม/0.05 มล.) + แก๊ส SF6 1.2 มล. ในผู้ป่วย PCV (ชายอายุ 79 ปี) ที่ดำเนินโรคอย่างรวดเร็วหลังได้รับวัคซีน COVID-19 เข็มที่สาม ในวันที่ 13 หลังผ่าตัด พบว่า SMH และ SRF ลดลง 4)
ใน PCV ต้องระวังเลือดออกใต้จอประสาทตา ที่เกิดจากการแตกของโปลิป แม้ว่าจะไม่มีการเปลี่ยนแปลงแบบ exudative หลังการรักษาที่ได้ผล ก็อาจเกิดเลือดออกใต้จอประสาทตา อย่างกะทันหันได้ สิ่งสำคัญคือต้องแนะนำให้ผู้ป่วยไปพบแพทย์ตั้งแต่เนิ่นๆ หากมีการเปลี่ยนแปลงใดๆ
หากไม่สามารถอุดโปลิปได้ด้วย anti-VEGF เพียงอย่างเดียว ให้พิจารณาใช้ร่วมกับ PDT
PDT มีความเสี่ยงต่อผลข้างเคียง เช่น การฝ่อของคอรอยด์ ดังนั้นควรพิจารณาข้อบ่งชี้อย่างรอบคอบหลังทำ PDT หลีกเลี่ยงการสัมผัสแสงแดดโดยตรงและแสงจ้าเป็นเวลา 2 วัน (ป้องกันปฏิกิริยาไวต่อแสง ) เมื่อออกนอกบ้าน ให้สวมแขนยาว ถุงมือ และแว่นกันแดดเพื่อปกป้องผิวหนังและดวงตาการรักษาด้วย anti-VEGF จำเป็นต้องให้ยาในขนาดคงไว้ และควรระวังการกลับเป็นซ้ำเมื่อยืดระยะห่างระหว่างการให้ยา
Q
ควรเลือก Aflibercept หรือ Ranibizumab?
A
Aflibercept มีอัตราการยุบตัวของโปลิปสมบูรณ์ 40-50% สูงกว่า ranibizumab (20-30%) การทดลอง PLANET ยังพิสูจน์ว่า PDT ไม่ด้อยกว่า aflibercept เพียงอย่างเดียว และปัจจุบันแนะนำให้ใช้ aflibercept เป็น anti-VEGF ทางเลือกแรกสำหรับ PCV 3, 9)
PCV เป็นโรคที่เป็นตัวแทนของ Pachychoroid Spectrum (PSD) 5, 6) PSD ประกอบด้วย Pachychoroid pigment epitheliopathy, Pachychoroid neovascularization (PNV ), Central serous chorioretinopathy (CSC ) และ Peripapillary pachychoroid syndrome (PPS ) 5) เมื่อเร็วๆ นี้ Peripheral exudative hemorrhagic chorioretinopathy (PEHCR ) ก็ถูกเพิ่มเข้าไปใน Pachychoroid Spectrum และถูกจัดให้เป็นฟีโนไทป์ส่วนปลายของ PCV 5, 13) PCV เป็นชนิดพิเศษของ type 1 CNV ที่อยู่ใต้ RPE ซึ่งเครือข่ายหลอดเลือดผิดปกติก่อตัวขึ้นบนพื้นฐานของภาวะขาดเลือดของแผ่นเส้นเลือดฝอยคอรอยด์
หลอดเลือดคอรอยด์ ขนาดใหญ่ที่ขยายตัว (Pachychoroid vessel) ในชั้น Haller เป็นศูนย์กลางของพยาธิวิทยา 5) พบการเชื่อมต่อระหว่าง vortex vein บนและล่างในประมาณ 90% ของดวงตา PSD ทำให้เกิดการหายไปของ horizontal watershed zone 5) การคั่งของ vortex vein นี้ทำให้เกิดการขยายตัวของชั้น Haller → การบางลงของชั้น Sattler และแผ่นเส้นเลือดฝอยคอรอยด์ → ภาวะขาดเลือดในระดับเส้นเลือดฝอย → การสร้าง complex หลอดเลือดใหม่ 5)
ภาวะเลือดคั่งในคอรอยด์ เรื้อรังทำให้เกิดการเปลี่ยนแปลงต่อไปนี้อย่างค่อยเป็นค่อยไป
ความผิดปกติของเมแทบอลิซึมและการทำงานผิดปกติของ RPE
การทำลายโครงสร้างของเยื่อบรูค เนื่องจากการเพิ่มขึ้นของกิจกรรมโปรตีเอส 5)
การสร้างเครือข่ายหลอดเลือดแตกแขนงผิดปกติ (BVN)
การปรากฏของรอยโรคขยายตัวคล้ายโพลิป
คอรอยด์ ไม่มีโครงข่ายเส้นเลือดฝอยเหมือนจอประสาทตา จึงสัมผัสโดยตรงกับการไหลเวียนเลือดแบบเป็นจังหวะ ดังนั้นปลายของ CNV จึงมีแนวโน้มที่จะขยายตัวและเกิดเป็นโพลิป 5) นอกจากนี้ ข้อบกพร่องของการไหลเวียนเลือดในแผ่นเส้นเลือดฝอยคอรอยด์ (CCF D) เพิ่มขึ้นไม่เพียงแต่ในตาที่เป็น PCV แต่ยังรวมถึงตาข้างปกติด้วย ซึ่งบ่งชี้ว่า pachychoroid อาจทำหน้าที่เป็นปัจจัยโน้มนำทางระบบของทั้งสองตา 5)
PCV ชนิด pachychoroid มักเกิดในอายุน้อยกว่า มีลักษณะคล้าย CSC หลายอย่าง ร่วมกับภาวะหลอดเลือดคอรอยด์ รั่วซึมมากเกิน (CVH) และอาจดื้อต่อการรักษาด้วย anti-VEGF 5, 8) ในทางตรงกันข้าม ชนิด non-pachychoroid (PCV ที่เกิดจาก drusen) แสดงลักษณะคล้าย AMD และสัมพันธ์อย่างมากกับอัลลีลเสี่ยง ARMS 2/HTRA1 5, 8) เนื่องจากทั้งสองชนิดมีแนวทางทางคลินิกและการตอบสนองต่อการรักษาที่แตกต่างกัน จึงจำเป็นต้องมีกลยุทธ์การรักษาเฉพาะบุคคล
ความเสียหายโดยตรงต่อ RPE และเยื่อบรูค จากการอักเสบสามารถเป็นพื้นฐานให้เกิด PCV ได้ 1) ในกรณีที่ PCV เกิดขึ้น 20 ปีหลังจากคอรอยด์ อักเสบจากวัณโรค การสะสมของความเสียหายของเนื้อเยื่อจากการอักเสบเรื้อรังคาดว่ามีส่วนเกี่ยวข้องกับการเกิด PCV 1)
Brolucizumab (แอนติบอดีสายเดี่ยวที่มีความสัมพันธ์สูงต่อ VEGF-A) แสดงให้เห็นถึงการพัฒนาการมองเห็น ที่ไม่ด้อยกว่าและผลลัพธ์ทางกายวิภาคที่เหนือกว่าเมื่อเทียบกับยาต้าน VEGF ที่มีอยู่ 5) ร่วมกับ faricimab (ตัวยับยั้งคู่ VEGF-A/Ang-2) ถือเป็นยาที่มีศักยภาพในการยืดระยะเวลาการรักษา (treat-and-extend; T&E) 6) ทั้งสองชนิดยังอยู่ในระยะรอการสะสมข้อมูลระยะยาว
PDS ซึ่งเป็นอุปกรณ์ปลดปล่อยยาต้าน VEGF อย่างต่อเนื่อง กำลังได้รับการพัฒนาเป็นทางเลือกแทนการฉีดเข้าแก้วตาแบบบ่อยครั้ง 5) อาจช่วยลดภาระการรักษาในผู้ป่วย nAMD รวมถึง PCV
T&E เป็นวิธีการยืดระยะเวลาการรักษาหลังจากให้ยาในขนาดคงที่ในช่วงแรก ตามความเสี่ยงของการกลับเป็นซ้ำของแต่ละบุคคล 6) ได้รับความสนใจในการประยุกต์ใช้กับผู้ป่วย PCV แต่ยังไม่มีการกำหนดโปรโตคอลที่เหมาะสมที่สุด
การวินิจฉัยด้วย AI โดยอาศัยผล OCT (เกณฑ์ APOIS) แสดงความสามารถในการแยกแยะ nAMD -PCV ด้วย AUC 0.90 5, 12) ในการทดลอง TIGER กำลังมีการศึกษาระบบใหม่สำหรับการประเมินการวินิจฉัยและการตอบสนองต่อการรักษาโดยใช้ OCTA และ AI 5)
ด้วยการแพร่หลายของแนวคิดสเปกตรัม pachychoroid การถกเถียงยังคงดำเนินต่อไปว่า PCV ควรถูกมองว่าเป็นชนิดย่อยของ nAMD หรือโรคอิสระ 6, 8) การศึกษาแสดงให้เห็นว่า PCV ชนิด pachychoroid และชนิด non-pachychoroid (drusen-driven) แตกต่างกันในความหนาของคอรอยด์ การตอบสนองต่อการรักษา และการพยากรณ์โรคระยะยาว 14) ดังนั้น การปรับปรุงกลยุทธ์การรักษาโดยการแยกความแตกต่างระหว่างทั้งสองและตัดสินใจเป็นรายบุคคลระหว่างการให้ยาต้าน VEGF เพียงอย่างเดียวหรือร่วมกับ PDT จึงเป็นความท้าทายหลักในอนาคต
การพยากรณ์โรคของ PCV สัมพันธ์อย่างใกล้ชิดกับระดับการหดตัวของรอยโรค polypoidal อัตราการหดตัวสมบูรณ์ของ polyp ด้วย aflibercept อยู่ที่ 40-50% ซึ่งสูงกว่า 20-30% ด้วย ranibizumab 9) ในกรณีที่ polyp หดตัวสมบูรณ์ ความเสี่ยงของการกลับเป็นซ้ำจะลดลง แต่ในกรณีที่หดตัวไม่สมบูรณ์ มักเกิดการสะสมของของเหลวเพิ่มขึ้นอีก ดังนั้นจึงจำเป็นต้องมีการประเมินภาพเป็นระยะ
แม้หลังการรักษาได้ผลและการเปลี่ยนแปลงแบบ exudative หายไป ก็อาจเกิดเลือดออกใต้จอประสาทตา จำนวนมาก (SMH) จากการแตกของ polyp ได้ อุบัติการณ์ของ SMH ใน 5 ปีรายงานประมาณ 10% 5) และผู้ป่วยควรได้รับคำแนะนำให้ไปพบแพทย์ทันทีเมื่อมีอาการทางสายตาเปลี่ยนแปลงอย่างกะทันหัน เลือดออกใต้รอยบุ๋มจอประสาทตา จำนวนมากทำให้การพยากรณ์การมองเห็น ไม่ดี และอาจต้องได้รับการผ่าตัด เช่น การเปลี่ยนแก๊สร่วมกับ tPA
PCV ชนิด pachychoroid มักดื้อต่อการรักษาด้วย anti-VEGF และมักจำเป็นต้องใช้ PDT ร่วมด้วย 5, 8) ในขณะที่ชนิด non-pachychoroid (drusen-driven) มักมีแนวทางการดำเนินโรคแบบเรื้อรังคล้าย AMD และจำเป็นต้องได้รับการรักษาแบบ maintenance ในระยะยาว 5, 8) ทั้งสองชนิดย่อยมีการกลับเป็นซ้ำบ่อย ดังนั้นจึงสำคัญที่จะต้องติดตามผลด้วย OCT และ ICGA อย่างสม่ำเสมอแม้หลังการรักษาสิ้นสุดลง
Mohankumar A, Mohan S, Rajan M. Polypoidal choroidal vasculopathy 20 years after resolution of tubercular choroiditis. Digit J Ophthalmol. 2023;29.
Jafar SM, Hussein ZR, Yasir MB. A case of treating polypoidal choroidal vasculopathy subretinal fluid by subthreshold micropulse laser. Am J Ophthalmol Case Rep. 2024;36:102225.
Vella G, Sacconi R, Borrelli E, Bandello F, Querques G. Polypoidal choroidal vasculopathy in a patient with early-onset large colloid drusen. Am J Ophthalmol Case Rep. 2021;22:101085.
Sasajima H, Zako M, Maeda R, Ueta Y. Rapid progression of polypoidal choroidal vasculopathy following third BNT162b2 mRNA vaccination. Case Rep Ophthalmol. 2022;13:459-464.
Sen P, Manayath G, Shroff D, Salloju V, Dhar P. Polypoidal choroidal vasculopathy: an update on diagnosis and treatment. Clin Ophthalmol. 2023;17:53-70.
Cheung CMG, Dansingani KK, Koizumi H, et al. Pachychoroid disease: review and update. Eye (Lond). 2025;39(5):819-834. doi:10.1038/s41433-024-03253-4.
Koh AH, Chen LJ, Chen SJ, et al. Polypoidal choroidal vasculopathy: evidence-based guidelines for clinical diagnosis and treatment. Retina. 2013;33:686-716.
Cheung CMG, Lai TYY, Ruamviboonsuk P, et al. Polypoidal choroidal vasculopathy: definition, pathogenesis, diagnosis, and management. Ophthalmology. 2018;125:708-724.
Lee WK, Iida T, Ogura Y, et al. Efficacy and safety of intravitreal aflibercept for polypoidal choroidal vasculopathy in the PLANET study: a randomized clinical trial. JAMA Ophthalmol. 2018;136:786-793.
Lim TH, Lai TYY, Takahashi K, et al. Comparison of ranibizumab with or without verteporfin photodynamic therapy for polypoidal choroidal vasculopathy: the EVEREST II randomized clinical trial. JAMA Ophthalmol. 2020;138:935-942.
Chaikitmongkol V, Cheung CM, Koizumi H, et al. Latest developments in polypoidal choroidal vasculopathy: epidemiology, etiology, diagnosis, and treatment. Asia-Pac J Ophthalmol. 2020;9:260-272.
Chong Teo KY, Sadda SR, Cheung CMG, et al. Non-ICGA treatment criteria for suboptimal anti-VEGF response for polypoidal choroidal vasculopathy: APOIS PCV workgroup report 2. Ophthalmol Retin. 2021;5:945-953.
Dansingani KK, Balaratnasingam C, Nishi K, et al. Understanding aneurysmal type 1 neovascularization (polypoidal choroidal vasculopathy): a lesson in the taxonomy of ‘expanded spectra’ — a review. Prog Retin Eye Res. 2018;65:89-117.
Miyake M, Tsujikawa A, Yamashiro K, et al. Pachychoroid neovasculopathy and age-related macular degeneration. Sci Rep. 2015;5:16204.