การเพิ่มจำนวนหลอดเลือดจอตา (RAP ) เป็นชนิดพิเศษของจอประสาทตา เสื่อมตามอายุ (AMD ) โดยมีลักษณะเฉพาะคือเส้นเลือดใหม่ (MNV ชนิดที่ 3) ที่มีต้นกำเนิดจากข่ายหลอดเลือดฝอยชั้นลึกในจอตา
ในยุโรปและอเมริกา คิดเป็น 15-20% ของ AMD ชนิดเนโอวาสคิวลาร์ แต่ในญี่ปุ่นพบค่อนข้างน้อยประมาณ 5%
มักเกิดในผู้หญิงสูงอายุ และอัตราการเกิดในตาทั้งสองข้างสูงมาก ดังนั้นจึงจำเป็นต้องตรวจตาอีกข้างเป็นประจำเมื่อตาข้างหนึ่งเป็นโรค
ดรูเซน ชนิดอ่อนหลายจุดที่ขั้วหลังและดรูเซน เทียมแบบร่างแห (RP D) มีความสำคัญในฐานะรอยโรคก่อนเกิดการฉีดยา anti-VEGF เข้าแก้วตาเป็นทางเลือกแรก และการทำ PDT เพียงอย่างเดียวสำหรับ MNV ชนิดที่ 3 ปัจจุบันไม่แนะนำ 1)
เมื่อเทียบกับ AMD ชนิดเนโอวาสคิวลาร์อื่นๆ ดำเนินโรคเร็วและมักดื้อต่อการรักษา จึงจำเป็นต้องจัดการในระยะยาว
อัตราการกลับเป็นซ้ำสูงแม้หลังตอบสนองต่อการรักษา และเกิดรอยโรคฝ่อได้ง่ายในระยะยาว ดังนั้นการพยากรณ์โรคทางสายตาไม่ดี
ภาวะหลอดเลือดขยายตัวแบบแองจิโอมาโตซัสของจอตา (retinal angiomatous proliferation; RAP ) เป็นชนิดย่อยพิเศษของจอประสาทตา เสื่อมตามอายุ (AMD ) แตกต่างจาก AMD อื่นที่มีหลอดเลือดใหม่เกิดจากคอรอยด์ ใน RAP หลอดเลือดใหม่เกิดจากข่ายเส้นเลือดฝอยชั้นลึกของจอตา (deep retinal capillary plexus) และเมื่อดำเนินโรค จะเชื่อมต่อกับหลอดเลือดใหม่ของคอรอยด์
ในปี 2001 Yannuzzi และคณะได้เสนอแนวคิดโรคอิสระนี้ และเริ่มแรกจำแนกเป็น 3 ระยะ (ระยะ 1-3) 3) ต่อมาในปี 2010 Yannuzzi เองได้เพิ่มระยะที่ 4 ทำให้เป็นการจำแนก 4 ระยะ ในทางกลับกัน Freund และคณะเสนอชื่อเรียกที่เป็นหนึ่งเดียวว่า “เนโอวาสคิวลาไรเซชันชนิดที่ 3” และเห็นว่าการจำแนกระยะไม่จำเป็น 4)
ในแนวทางปฏิบัติทางคลินิกของญี่ปุ่นสำหรับ AMD ชนิดเนโอวาสคิวลาร์ (2024) หลอดเลือดใหม่ในจุดรับภาพเรียกรวมว่า “หลอดเลือดใหม่ของจุดรับภาพ (macular neovascularization; MNV)” และ RAP ถูกจำแนกอย่างเป็นทางการเป็น “MNV ชนิดที่ 3” 1) เนื่องจากคำดั้งเดิม “หลอดเลือดใหม่ของคอรอยด์ (CNV )” ไม่รวมหลอดเลือดใหม่ที่เกิดจากจอตา ปัจจุบันจึงมีการเปลี่ยนไปใช้ MNV
แต่เดิม หลอดเลือดใหม่ในจุดรับภาพเรียกว่า “หลอดเลือดใหม่ของคอรอยด์ (choroidal neovascularization; CNV )” แต่เนื่องจากรวมถึงหลอดเลือดใหม่ที่เกิดจากจอตา คำว่า “หลอดเลือดใหม่ของจุดรับภาพ (macular neovascularization; MNV)” จึงถูกใช้ในระดับนานาชาติตั้งแต่ปี 2020 1) MNV ชนิดที่ 3 ที่สอดคล้องกับ RAP เป็นหลอดเลือดใหม่ที่เกิดจากหลอดเลือดจอตา และแตกต่างอย่างชัดเจนในแหล่งกำเนิดจาก MNV ชนิดที่ 1 และชนิดที่ 2 ซึ่งมาจากคอรอยด์
ในยุโรปและอเมริกา RAP คิดเป็น 15-20% ของผู้ป่วย AMD ชนิดเนโอวาสคิวลาร์ ในญี่ปุ่น ความถี่ต่ำในคนเอเชียประมาณ 5% มีลักษณะเฉพาะคือมักเกิดในผู้หญิงสูงอายุ และอายุที่เริ่มเป็นมัก 70 ปีขึ้นไป
อัตราการเกิดโรคในตาทั้งสองข้างสูงมาก และเมื่อเกิดในตาข้างเดียว ความเสี่ยงในการเกิดในตาอีกข้างจะเพิ่มขึ้นอย่างมีนัยสำคัญ ดังนั้น การติดตามตาข้างที่แข็งแรงจึงมีความสำคัญทางคลินิกอย่างยิ่ง เมื่อเปรียบเทียบกับชนิดย่อยอื่นของ AMD การดำเนินโรคจะรวดเร็ว และอัตราการกลับเป็นซ้ำสูงแม้จะได้รับการรักษา ในระยะยาว มักเกิดรอยโรคฝ่อ และชนิดย่อยนี้ได้รับการยอมรับว่ามีการพยากรณ์ทางการมองเห็น ที่ไม่ดีในกลุ่ม AMD
Q
RAP เป็นโรคเดียวกับจอประสาทตาเสื่อมตามอายุหรือไม่?
A
RAP ถูกจัดเป็นชนิดย่อยพิเศษของจอประสาทตา เสื่อมตามอายุ (AMD ) แตกต่างจาก AMD ชนิดเส้นเลือดใหม่งอกทั่วไปในเรื่องต้นกำเนิดของเส้นเลือดใหม่ ซึ่งเส้นเลือดใหม่เกิดจากข่ายเส้นเลือดฝอยชั้นลึกในจอประสาทตา ไม่ใช่จากคอรอยด์ และนี่คือความแตกต่างที่สำคัญ ในการจำแนกประเภทระหว่างประเทศปัจจุบัน เรียกว่า “MNV ชนิดที่ 3” 1) วิธีการรักษาเหมือนกัน แต่การพยากรณ์โรคแตกต่างกันเนื่องจากการดื้อต่อการรักษาและอัตราการเกิดในตาทั้งสองข้างสูง
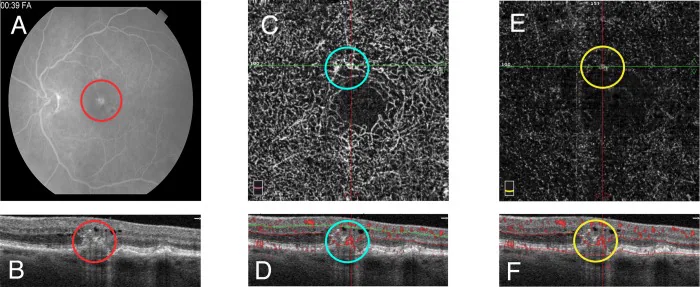
ภาพหลายรูปแบบของรอยโรคหลอดเลือดคล้ายเนื้องอกในจอประสาทตา Fayed AE, et al. Projection resolved optical coherence tomography angiography to distinguish flow signal in retinal angiomatous proliferation from flow artifact. PLoS One. 2019. Figure 1. PM
CI D: PMC6519823. License: CC BY.
A แสดงการเรืองแสงมากเกินไปในการถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน , B แสดงรอยโรคสะท้อนแสงสูงภายในจอประสาทตา ใน OCT , C และ D แสดงโครงสร้างหลอดเลือดผิดปกติและสัญญาณการไหลเวียนเลือดในข่ายเส้นเลือดฝอยชั้นลึกใน OCTA ซึ่งสอดคล้องกับรอยโรคหลอดเลือดคล้ายเนื้องอกในจอประสาทตา ที่กล่าวถึงในหัวข้อ “2. อาการหลักและผลการตรวจทางคลินิก”
อาการที่ผู้ป่วยรู้สึกต่อไปนี้ปรากฏตั้งแต่ระยะต้นถึงระยะกลาง
ภาพบิดเบี้ยว (เห็นสิ่งของผิดรูป)จอประสาทตา บวมน้ำหรือมีสารน้ำรั่วในบริเวณจุดรับภาพ พบได้บ่อยเป็นอาการเริ่มแรกจุดบอดกลาง ภาพการมองเห็น ลดลงจอประสาทตา หรือเส้นเลือดใหม่งอกมาก
การดำเนินของอาการค่อนข้างรวดเร็ว และเมื่อเทียบกับชนิดย่อยอื่นของ AMD มักทำให้การมองเห็น ลดลงอย่างรุนแรงตั้งแต่ระยะแรก เมื่อมีการบวมน้ำแบบถุงน้ำในจอประสาทตา อย่างชัดเจน อาจเกิดการมองเห็น ลดลงอย่างฉับพลัน ดังนั้น การวินิจฉัยและการรักษาตั้งแต่เนิ่นๆ จึงมีความสำคัญต่อการรักษาการทำงานของการมองเห็น
ลักษณะพื้นฐานที่เด่นคือการรวมกลุ่มของดรูเซน ชนิดอ่อนหลายจุดในขั้วหลังของลูกตา และดรูเซน เทียมแบบร่างแห (reticular pseudodrusen; RP D) RP D คือสิ่งสะสมรูปร่างแหถึงจุดซึ่งอยู่บนชั้นเยื่อบุผิวเม็ดสีจอประสาทตา (RPE ) และถือเป็นรอยโรคก่อนเกิด RAP 1)
ในช่วงที่โรคมีการดำเนินงาน จะพบผลการตรวจดังต่อไปนี้
เลือดออกในชั้นผิวของจอตาและเลือดออกในชั้นในของจอตา : มีเลือดออกเล็กน้อยถึงปานกลางที่ขั้วหลัง โดยเฉพาะในระยะที่ 1 จะพบเลือดออกในชั้นผิวเล็กน้อยรอบๆ หลอดเลือดใหม่ที่ปรากฏเป็นจุดแดงแบบปุ่มอาการบวมน้ำที่จุดรับภาพแบบถุงน้ำ : เป็นลักษณะเฉพาะของ RAP มักปรากฏเร็วและรุนแรงกว่าเมื่อเทียบกับชนิดย่อยอื่นของ AMD ของเหลวใต้จอตาและจอตาลอกแบบมีน้ำใต้จอตา : ปรากฏในระยะที่ 2 ขึ้นไปการลอกของชั้นเยื่อบุเม็ดสี (PED ) : เกิดในกรณีที่ลุกลาม (ระยะที่ 3 ขึ้นไป) มีลักษณะเป็น PED แบบเส้นใยหลอดเลือดหรือ PED แบบดรูเซน
ลักษณะทางคลินิกตามการแบ่งระยะของ RAP (การแบ่ง 4 ระยะของ Yannuzzi) แสดงไว้ด้านล่าง 3)
ระยะที่ 1
หลอดเลือดใหม่ในชั้นในจอตา : ปรากฏเป็นจุดแดงแบบปุ่มภายในข่ายเส้นเลือดฝอยชั้นลึก
เลือดออกในชั้นผิวของจอตา : เลือดออกในชั้นผิวเล็กน้อยรอบรอยโรค
อาการบวมน้ำแบบถุงน้ำ : อาการบวมน้ำแบบถุงน้ำรอบรอยโรค
ผลการตรวจ FA : แสดงจุดเรืองแสงเกินปกติแบบปุ่มเล็ก (hot spot)
ผลการตรวจ IA : พบ hot spot และการเชื่อมต่อของหลอดเลือดจอตากับจอตา (RRA) ในประมาณ 30% ของกรณี
ผลการตรวจ OCT : พบ PED แบบดรูเซน (PED ที่สอดคล้องกับดรูเซน อ่อน) และอาการบวมน้ำในชั้นในจอตา
ระยะที่ 2
หลอดเลือดใหม่ใต้จอตา : ระยะที่หลอดเลือดใหม่ในชั้นในจอตาลุกลามเข้าไปในช่องใต้จอตา
จอตาลอกแบบมีน้ำใต้จอตา : จอตาลอกแบบมีน้ำใต้จอตาปรากฏในบริเวณจุดรับภาพ
เลือดออก : นอกจากเลือดออกในจอประสาทตา และชั้นผิวแล้ว อาจพบเลือดออกใต้จอประสาทตา ได้
จอประสาทตา บวมน้ำชนิดถุงน้ำ (cystoid macular edema)การมองเห็น แย่ลง
ระยะที่ 3
ร่วมกับการลอกตัวของเยื่อบุผิวเม็ดสี (PED ) : ระยะที่เพิ่ม PED เข้าไปในผลการตรวจของระยะที่ 2
ผลการตรวจ FA : การเรืองแสงมากเกินไปบริเวณศูนย์กลางของ PED สอดคล้องกับรอยโรค RAP ในการตรวจ OCT
สัญญาณ bump : ก้อนสะท้อนแสงคล้ายการฉีกขาดของ RPE ที่ตำแหน่ง PED
ระยะที่ 4
การเชื่อมต่อระหว่างจอประสาทตา และคอรอยด์ (RCA) : ระยะสุดท้ายที่เส้นเลือดใหม่จากจอประสาทตา และคอรอยด์ เชื่อมต่อกัน
ผลการตรวจ IA : IA มีประโยชน์ในการตรวจหา RCA และ RRA การเรืองแสงมากเกินไปจะปรากฏเป็นจุดร้อน
การเกิดแผลเป็น : การเกิดแผลเป็นรูปจานนำไปสู่การสูญเสียการมองเห็น ส่วนกลางอย่างถาวร
MNV ชนิดที่ 3 สังเกตได้ยากด้วยกล้องตรวจตา หรือการถ่ายภาพจอประสาทตา ดังนั้นการยืนยันด้วยภาพจึงจำเป็น 1) ต่อไปนี้เป็นสรุปวิธีการตรวจทางภาพหลักและผลการตรวจ
การตรวจ ผลการตรวจที่จำเพาะ FA จุดร้อน (การเรืองแสงมากเกินไปแบบก้อนกลม), การรั่วซึมมากในระยะท้าย IA (ICGA ) hot spot, การเห็น RRA และ RCA OCT bump sign, IRF, SRF, PED , จอประสาทตา บวมแบบถุงน้ำ OCTA การมองเห็น หลอดเลือดใหม่ในจอตาและใต้จอตาแบบไม่รุกล้ำ
OCT RAP และประเมินผลการรักษา bump sign คือรอยโรคยกตัวเล็กๆ เหนือ RPE โดยตรง ถือเป็นลักษณะที่ค่อนข้างจำเพาะสำหรับ MNV ชนิดที่ 3 OCT พบจอประสาทตา บวมแบบถุงน้ำตั้งแต่ระยะแรก และเมื่อระยะดำเนินไปจะเกิด PED 1)
ในภาพ B-scan ของ OCTA RPE ไปใต้ RPE ได้ 1) เนื่องจาก RAP เกิดจากหลอดเลือดใหม่ในจอตา ในกลุ่ม AMD หลอดเลือดผิดปกติจะมองเห็นได้ง่ายเป็นพิเศษด้วย OCTA ในผู้สูงอายุที่ยากต่อการตรวจ angiography ซ้ำๆ การประเมินรอยโรคแบบไม่รุกล้ำด้วย OCTA มีประโยชน์ 10)
ของเหลวในจอตา (IRF) และของเหลวใต้จอตา (SRF) ใช้เป็นตัวบ่งชี้กิจกรรมของโรค เนื่องจากรอยโรค MNV ชนิดที่ 3 ไม่จำเป็นต้องเกิดที่โฟเวียเสมอไป จึงแนะนำให้สแกนทั่วจอประสาทตา หรือทั่วรอยโรคเพื่อประเมินของเหลวอย่างแม่นยำ 1)
Q
OCT เห็นอะไรบ้าง?
A
ใน OCT การสะท้อนเป็นก้อนเหนือ RPE ที่เรียกว่า “bump sign” เป็นลักษณะเด่น นอกจากนี้ยังพบจอประสาทตา บวมแบบถุงน้ำ ของเหลวในจอตา (IRF) ของเหลวใต้จอตา (SRF) และจอประสาทตาลอก ตัว (PED ) ในภาพ B-scan OCTA จะเห็นสัญญาณการไหลเวียนเลือดต่อเนื่องจากหลอดเลือดจอตาชั้นผิวไปยัง bump sign 1) การมีหรือไม่มี IRF และ SRF ใช้เป็นตัวบ่งชี้ในการประเมินกิจกรรม
ปัจจัยเสี่ยงหลักของ RAP มีดังนี้
อายุที่มากขึ้น : เป็นปัจจัยเสี่ยงที่สำคัญที่สุด ยิ่งอายุมาก ความเสี่ยงในการเกิดโรคยิ่งสูงเพศ : พบในผู้หญิงบ่อยกว่าดรูเซน ชนิดอ่อนที่ขั้วหลัง (Soft drusen)ดรูเซน ชนิดอ่อนขนาดใหญ่ (เส้นผ่านศูนย์กลาง ≥125 ไมครอน) หลายจุดในบริเวณจอประสาทตา ส่วนกลางเป็นสิ่งบ่งชี้ก่อนเกิดโรคที่สำคัญสำหรับการดำเนินของโรคจอประสาทตา เสื่อมตามอายุ 1) ดรูเซน เทียมแบบร่างแห (Reticular pseudodrusen: RP D)RAP RP D แตกต่างจากดรูเซน ทั่วไป (ซึ่งอยู่ใต้ชั้น RPE ) เนื่องจากเป็นตะกอนแบบร่างแหถึงจุดที่อยู่เหนือชั้น RPE และเป็นที่รู้จักอย่างกว้างขวางว่าเป็นปัจจัยเสี่ยงต่อการดำเนินไปเป็น MNV ชนิดที่ 3 และ AMD ชนิดฝ่อ 1) ความโน้มเอียงทางพันธุกรรม : ความหลากหลายของยีน ARMS 2 และความหลากหลายของยีน CF H (Complement Factor H) เกี่ยวข้องกับความไวต่อ AMD โดยรวม 11) การศึกษาเชื่อมโยงทั่วทั้งจีโนมขนาดใหญ่ยืนยันว่าตำแหน่งยีนเหล่านี้เป็นปัจจัยกำหนดหลักของความเสี่ยงต่อ AMD การสูบบุหรี่ : เป็นปัจจัยเสี่ยงต่อ AMD โดยรวม และเป็นปัจจัยเสี่ยงที่ปรับเปลี่ยนได้ที่สำคัญที่สุด การศึกษา Funagata, Hisayama และ Nagahama ที่ดำเนินการในประชากรญี่ปุ่นทั้งหมดรายงานความสัมพันธ์ระหว่างการสูบบุหรี่กับ AMD และการศึกษา Hisayama ระบุว่านิสัยการสูบบุหรี่เพิ่มความเสี่ยงต่อ AMD ระยะปลายถึง 4 เท่า 12)
อัตราการเกิดโรคในตาทั้งสองข้างสูงก็เป็นลักษณะสำคัญเช่นกัน เมื่อตาข้างหนึ่งเป็นโรค การติดตามตาอีกข้างอย่างสม่ำเสมอเป็นสิ่งจำเป็น หากตาอีกข้างมีดรูเซน ชนิดอ่อนหรือ RP D ร่วมด้วย ความเสี่ยงในการเกิดโรคจะยิ่งสูงขึ้น จึงจำเป็นต้องตรวจอย่างละเอียดในช่วงเวลาสั้นๆ
ในเรื่องอัตราส่วนเพศ AMD ชนิดเส้นเลือดใหม่โดยรวมพบในผู้ชายมากกว่า (ชาย:หญิง = 3:1) ในขณะที่ RAP มีลักษณะเฉพาะคือเกิดในผู้หญิงมากกว่า อายุที่เริ่มป่วยเท่ากับหรือสูงกว่า AMD โดยรวมเล็กน้อย โดยส่วนใหญ่อายุ 70 ปีขึ้นไป
เพื่อชะลอการดำเนินของจอประสาทตา เสื่อมตามอายุ แนะนำให้รับประทานอาหารเสริมตามใบสั่ง AREDS2 อย่างต่อเนื่อง โดยเฉพาะอย่างยิ่งส่วนประกอบประกอบด้วยลูทีน 10 มก., ซีแซนทีน 2 มก., วิตามินซี 500 มก., วิตามินอี 400 IU, สังกะสี 25 มก. และทองแดง 2 มก. 1) การสูบบุหรี่เพิ่มความเสี่ยงต่อ AMD อย่างมีนัยสำคัญ ดังนั้นการเลิกบุหรี่จึงสำคัญ แนะนำให้รับประทานอาหารที่มีปลาที่มีกรดไขมันไม่อิ่มตัวเชิงซ้อนโอเมก้า 3 สายยาวสูง และผักใบเขียวเข้ม ให้เราตรวจตาเป็นประจำและติดตามตนเองด้วยตาราง Amsler ต่อไป
Q
หากเกิดโรคในตาข้างเดียว ตาอีกข้างจะเกิดโรคด้วยหรือไม่?
A
RAP เป็นโรคที่มีอัตราการเกิดโรคในตาทั้งสองข้างสูงมาก แม้จะเริ่มเป็นข้างเดียว ความเสี่ยงที่ตาอีกข้างจะเป็นโรคก็สูงกว่าเมื่อเทียบกับชนิดย่อยอื่นของ AMD การตรวจตาอีกข้างอย่างละเอียดเป็นประจำเป็นสิ่งจำเป็นตั้งแต่เริ่มเป็นข้างเดียว
เนื่องจาก MNV ชนิดที่ 3 สังเกตได้ยากด้วยกล้องตรวจตา หรือการถ่ายภาพจอประสาทตา การวินิจฉัยที่แน่นอนจำเป็นต้องมีการประเมินอย่างเป็นระบบโดยรวมการตรวจภาพหลายวิธี 1)
ขั้นตอนการวินิจฉัยมีดังนี้:
ข้อสงสัยทางคลินิก : ในผู้ป่วยสูงอายุที่มีดรูเซน ชนิดอ่อนจำนวนมากในตาทั้งสองข้าง และมีเลือดออกในจอประสาทตา บริเวณขั้วหลัง ให้สงสัย MNV ชนิดที่ 3การตรวจ OCT จอประสาทตา บวมน้ำแบบถุงน้ำตั้งแต่ระยะแรก และหากพบ bump sign (ก้อนสะท้อนแสงคล้ายการฉีกขาดของ RPE ) จะบ่งชี้อย่างมาก การมี PED บ่งบอกถึงการดำเนินโรคการตรวจ OCT Aจอประสาทตา ชั้นผิวไปยัง bump sign เป็นการตรวจที่ไม่รุกรานและมีประโยชน์โดยเฉพาะในผู้สูงอายุที่ยากต่อการตรวจ angiographyการตรวจ FA /ICGA : FA แสดงการเรืองแสงมากเกินแบบก้อน (hot spot) และการรั่วของสารเรืองแสงจำนวนมากในระยะท้าย ICGA แสดง hot spot เป็น RRA/RCA ซึ่งช่วยในการกำหนดระยะของโรค
การประเมินกิจกรรมของโรคใช้ OCT เป็นหลักในการตรวจหา IRF, SRF และของเหลวใต้ RPE แบบไม่รุกราน 1) การแยก PED ชนิดเซรุ่มและชนิดเลือดออกทำได้โดยดูความสว่างของเนื้อหาใน OCT หากความสว่างปานกลางคือดรูเซน หากต่ำคือเซรุ่ม
MacTel type 2 ทำให้เกิดรอยโรคที่จุดรับภาพคล้ายกับ RAP และอาจมีเส้นเลือดใหม่ใต้จอประสาทตา ร่วมด้วย ดังนั้นการแยกโรคจึงสำคัญ 5)
จุดที่ใช้แยก RAP (MNV ชนิดที่ 3)MacTel type 2อายุที่เริ่มเป็น สูงอายุ (มัก >70 ปี) วัยกลางคน (50-60 ปี) ลักษณะพื้นหลัง ดรูเซน ชนิดอ่อนจำนวนมากและ RP Dความโปร่งใสของจอประสาทตา ลดลงทางด้านขมับของรอยบุ๋ม OCT bump sign, PED , ภาวะบวมน้ำแบบถุงน้ำ (cystoid edema) ข้อบกพร่องของ ellipsoid zone, โพรงจอตา (retinal cavity) โดยไม่มีความหนา ความเร็วในการดำเนินโรค เร็ว (ส่วนใหญ่มีการรั่วซึมและเลือดออก) ช้า (ส่วนใหญ่มีการฝ่อของจอตา)
ใน MacTel type 2 ลักษณะเด่นคือ venule มุมฉาก (right-angled venule) ที่โค้งเป็นมุมฉากและถูกดึงเข้าไปในชั้นลึกของจอตา และคราบผลึก (crystalline deposits) ภาพ red free (โดยเฉพาะ confocal blue light reflectance) จะแสดงบริเวณจุดรับภาพ (macula) มีการสะท้อนแสงสูงเป็นรูปวงแหวนหรือวงรีแนวนอน ซึ่งพบได้ตั้งแต่ระยะแรก จึงมีประโยชน์ในการวินิจฉัย 5) นอกจากนี้ OCT ยังแสดงโพรงจอตา (retinal cavity) โดยไม่มีความหนาของจอตา ซึ่งเป็นลักษณะเฉพาะ และเมื่อดำเนินโรคอาจเกิดรูพรุนชั้นนอกหรือรูที่จุดรับภาพ (macular hole) ได้ 5)
ในทางตรงกันข้าม RAP จะมี hot spot ใน IA และการรวมกลุ่มของ drusen แบบอ่อน (soft drusen) และใน OCT จะมี bump sign และ macular edema แบบ cystoid เป็นหลัก ซึ่งแตกต่างจาก MacTel อย่างชัดเจน MacTel มีการฝ่อของจอตาเป็นหลักและดำเนินโรคช้า ในขณะที่ RAP มักดำเนินโรคเร็วโดยมีการรั่วซึมและเลือดออกเด่นชัด
PCV แสดงรอยโรคแบบ polyp (hyperfluorescence แบบ nodular) และเครือข่ายหลอดเลือดแตกแขนง (branching vascular network) ใน IA และใน OCT มีลักษณะเด่นคือ RPE โป่งสูงชันร่วมกับโพรงสะท้อนต่ำภายใน 1) ในภาพถ่ายจอตา จะเห็นรอยโรคยกตัวสีส้มแดง ใน RAP hot spot ใน IA เป็นหลัก และ macular edema แบบ cystoid เด่นชัด ซึ่งใช้แยกจากกัน PCV มักมีการหนาตัวของคอรอยด์ (pachychoroid) ในขณะที่ RAP มีพื้นหลังเป็น drusen แบบอ่อนและ RP D รวมกลุ่มกัน
ใน AMD ทั่วไป หลอดเลือดใหม่เกิดจากคอรอยด์ เป็นหลัก MNV type 1 อยู่ใต้ RPE และแสดง double layer sign ใน OCT MNV type 2 อยู่เหนือ RPE (ใต้จอตา) และตรวจพบเป็นก้อนสะท้อนปานกลางใต้จอตาใน OCT 1) ใน RAP หลอดเลือดใหม่เกิดจากจอตาและอยู่ในชั้นจอตา จึงทำให้เกิด macular edema แบบ cystoid ตั้งแต่ระยะแรกและมี bump sign ซึ่งใช้แยกจากกัน นอกจากนี้ RAP มักเป็นทั้งสองข้างและมักมี drusen แบบอ่อนจำนวนมาก
การรักษาทางเลือกแรกสำหรับ AMD ชนิด neovascular คือการฉีดยา anti-VEGF เข้าแก้วตา 1) สำหรับ MNV type 3 ยา anti-VEGF ทุกชนิดแสดงให้เห็นถึงการฟื้นฟูการมองเห็น
ปัจจุบัน ยาต้าน VEGF ที่ใช้ได้สำหรับ AMD ชนิด neovascular มีดังนี้ 1)
Ranibizumab (Lucentis/Ranibizumab BS) : ในการทดลอง MARINA กลุ่ม sham สูญเสียการมองเห็น 14.9 ตัวอักษรใน 24 เดือน ในขณะที่กลุ่มที่ได้รับ ranibizumab รายเดือนดีขึ้น 6.6 ตัวอักษร 14) การทดลอง ANCHOR ก็แสดงให้เห็นความเหนือกว่า PDT เช่นกัน 15) Aflibercept 2 มก. (Eylea) : ในการทดลอง VIEW 1/2 การฉีดทุก 8 สัปดาห์หลังจาก 3 ครั้งแรก แสดงให้เห็นว่าไม่ด้อยกว่า ranibizumab รายเดือนในการรักษาระดับการมองเห็น 6) Brolucizumab 6 มก. (Beovu) : ในการทดลอง HAWK/HARRIER การฉีดทุก 8–12 สัปดาห์หลังจาก 3 ครั้งแรก แสดงให้เห็นว่าไม่ด้อยกว่าในการปรับปรุงการมองเห็น และเหนือกว่าในการลดความหนาของจอประสาทตา ส่วนกลางเมื่อเทียบกับ aflibercept 7) Faricimab (Vabysmo) : แอนติบอดีแบบคู่เป้าหมายที่ยับยั้ง VEGF และ angiopoietin-2 ในการทดลอง TENAYA/LUCERNE การฉีดทุก 8–16 สัปดาห์หลังจาก 4 ครั้งแรก แสดงให้เห็นว่าไม่ด้อยกว่า aflibercept 8)
ระยะเริ่มต้น (induction phase) ประกอบด้วยการฉีดเดือนละครั้ง โดยปกติ 3 ครั้งติดต่อกัน (4 ครั้งสำหรับ faricimab) เพื่อปรับปรุงการมองเห็น 1)
ระยะบำรุงรักษา (maintenance phase) มีตัวเลือกการให้ยาดังนี้:
การให้ยาแบบคงที่ (fixed dosing) : วิธีการที่ใช้ในการทดลองทางคลินิก ฉีดตามช่วงเวลาที่กำหนด (เช่น ทุก 8 สัปดาห์)การให้ยาตามความจำเป็น (PRN) : ติดตามทุกเดือนและฉีดเฉพาะเมื่อมีกิจกรรมของโรค อย่างไรก็ตาม รายงานระบุว่าการมองเห็น แย่ลงในระยะยาวด้วยวิธี PRN 1, 13) วิธี treat-and-extend (T&E) : ขยายระยะห่างระหว่างการฉีดทีละน้อยตามกิจกรรมของโรค ปัจจุบันเป็นวิธีการบำรุงรักษาที่แนะนำมากที่สุด การวิเคราะห์อภิมานแสดงให้เห็นว่าวิธีนี้คงการปรับปรุงการมองเห็น ได้เทียบเท่าการฉีดรายเดือน โดยให้ผลการมองเห็น ดีกว่า PRN 1)
ในการทดลอง ALTAIR ในผู้ป่วยญี่ปุ่น วิธี T&E ด้วย aflibercept (ปรับช่วงห่าง 2 หรือ 4 สัปดาห์) คงการปรับปรุงการมองเห็น และความหนาของจอประสาทตา ได้นาน 96 สัปดาห์ 9) ไม่มีฉันทามติว่าควรทำ T&E ต่อไปนานเท่าใด การตัดสินใจขึ้นอยู่กับสภาพทางการแพทย์และสังคมของผู้ป่วย 1)
OCT เป็นเครื่องมือหลักในการประเมินประสิทธิภาพการรักษา การมีหรือกลับมาของของเหลวรอบๆ หลอดเลือดใหม่คอรอยด์ (ของเหลวในจอประสาทตา ใต้จอประสาทตา หรือใต้ RPE ) ถือเป็นสัญญาณของกิจกรรม 1) เนื่องจากหลอดเลือดใหม่ชนิดที่ 3 ไม่ได้จำกัดอยู่ที่รอยบุ๋มจอตา เสมอไป จึงแนะนำให้สแกนทั่วทั้งจอตา หรือรอยโรคทั้งหมดเพื่อประเมิน
เมื่อการรักษาได้ผลไม่ดี (กรณีดื้อต่อการรักษา) หรือประสิทธิภาพลดลง (เกิดการดื้อยา) การเปลี่ยนไปใช้ยาต้าน VEGF ตัวอื่นอาจได้ผล 1) RAP เป็นรูปแบบโรคที่มักแสดงการดื้อต่อการรักษา ดังนั้นการเปลี่ยนยาเร็วเมื่อตอบสนองไม่ดีจึงเป็นสิ่งสำคัญ การเปลี่ยนยาอาจพิจารณาเพื่อลดภาระการรักษาได้เช่นกัน
ปัจจุบันไม่แนะนำให้ใช้ PDT เพียงอย่างเดียวสำหรับ MNV ชนิดที่ 3 1) ในกรณีที่ดื้อต่อยาต้าน VEGF อาจพิจารณาใช้ PDT ร่วมด้วย แต่ในระยะยาว PDT อาจทำให้จอประสาทตา ฝ่อแย่ลง ควรหลีกเลี่ยงในกรณีที่คอรอยด์ บางหรือมีจอประสาทตา ฝ่ออยู่แล้ว 1)
ใบสั่งยาเมื่อใช้ PDT ร่วมมีดังนี้:
เวอร์เทพออร์ฟิน (วิซูดายน์) : 6 มก./ตร.ม. ของพื้นที่ผิวกาย ให้ทางหลอดเลือดดำเป็นเวลา 10 นาทีการฉายเลเซอร์ : 15 นาทีหลังจากเริ่มฉีด (689 นาโนเมตร, 600 มิลลิวัตต์/ตร.ซม., เป็นเวลา 83 วินาที)ขนาดจุดฉาย : เส้นผ่านศูนย์กลางรอยโรคสูงสุดจากผลการตรวจหลอดเลือด + 1000 ไมโครเมตรช่วงเวลาการให้ยาต้าน VEGF ร่วม : ภายใน 1 สัปดาห์ก่อน PDT หรือในวันเดียวกับ PDT (ภายใต้การป้องกันแสง)การดูแลหลังทำหัตถการ : หลีกเลี่ยงการสัมผัสแสงแดดโดยตรงเป็นเวลา 2 วันหลังการรักษา
ปัจจุบันไม่สามารถรักษา AMD ชนิดเส้นเลือดงอกใหม่ให้หายขาดได้ และหากไม่ได้รับการรักษาและการจัดการระยะยาวที่เหมาะสม จะเกิดการสูญเสียการมองเห็น แบบถาวร 1) RAP ต้องการการดูแลเป็นพิเศษในระยะยาวในประเด็นต่อไปนี้:
แม้ว่ากิจกรรมของ MNV จะสงบลงแล้ว ก็อาจกลับมาเป็นซ้ำได้ในระยะยาว
การมีน้ำใต้จอประสาทตา ซ้ำๆ ทำให้เกิดการเปลี่ยนแปลงแบบฝ่อหรือพังผืด ในระยะยาว จอประสาทตา ฝ่อ (geographic atrophy) เกิดขึ้นได้ง่ายการมองเห็น แบบถาวร
MNV ยังเกิดขึ้นในตาข้างตรงข้ามด้วยอัตราที่สูง
ในกรณีที่การทำงานของการมองเห็น ลดลงอย่างรุนแรง ควรพิจารณานำการดูแลผู้มีสายตาเลือนราง โดยใช้แว่นขยายหรือเครื่องอ่านขยายมาใช้อย่างจริงจัง เนื่องจากไม่สามารถรักษา AMD ชนิดเส้นเลือดงอกใหม่ให้หายขาดได้ จึงควรแบ่งปันแผนการจัดการที่ยั่งยืนกับผู้ป่วย โดยคำนึงถึงสถานการณ์ทางสังคมของผู้ป่วยและสภาพของตาข้างตรงข้าม 1)
Q
ต้องฉีดกี่ครั้ง?
A
แม้จะมีความแตกต่างระหว่างบุคคลมาก หลังจากให้ 3 ครั้งติดต่อกัน (4 ครั้งสำหรับ faricimab) ในระยะเริ่มต้น ช่วงเวลาการฉีดจะถูกปรับด้วยวิธี treat-and-extend 1) RAP มักจะดื้อต่อการรักษามากกว่าชนิดย่อยอื่นของ AMD และอาจต้องฉีดหลายครั้ง ในการทดลอง ALTAIR ในชาวญี่ปุ่น ยืนยันการคงประสิทธิภาพการรักษาเป็นเวลา 96 สัปดาห์ 9) ด้วยยาใหม่เช่น faricimab สามารถรักษาระยะห่างได้ถึง 16 สัปดาห์ ลดภาระการรักษา 8)
แก่นแท้ของ RAP คือเส้นเลือดใหม่ภายในจอประสาทตา ที่เกิดจากข่ายเส้นเลือดฝอยชั้นลึกของจอประสาทตา นี่คือพื้นฐานที่ทำให้ถูกเรียกว่า “MNV ชนิดที่ 3” และกลไกการเกิดแตกต่างโดยพื้นฐานจาก MNV ชนิดที่ 1 และ 2 ซึ่งเกิดจากคอรอยด์ 1)
การจัดตำแหน่งของ MNV ชนิดที่ 3 ในการจำแนก MNV มีดังนี้:
MNV ชนิดที่ 1 : เส้นเลือดใหม่จากคอรอยด์ ใต้ RPE (ตรงกับ occult CNV )MNV ชนิดที่ 2 : เส้นเลือดใหม่จากคอรอยด์ เหนือ RPE (ในช่องใต้จอประสาทตา ) (ตรงกับ classic CNV )MNV ชนิดที่ 3 : เส้นเลือดใหม่ที่เกิดจากหลอดเลือดจอประสาทตา (RAP ) 1)
การสะสมของดรูเซน ชนิดอ่อน (soft drusen) และ RP D (retinal pseudodrusen) มีความสำคัญในฐานะรอยโรคก่อนเกิด RP D แตกต่างจากดรูเซน ทั่วไป (สิ่งสะสมใต้ RPE ) เนื่องจากเป็นสิ่งสะสมรูปสามเหลี่ยมที่อยู่เหนือ RPE ในการตรวจ OCT จะเห็นเป็นส่วนยื่นจากผิว RPE เข้าสู่จอประสาทตา และบางส่วนอาจเลยผ่านโซน ellipsoid ไปจนถึงเยื่อลิมิตันภายนอก RP D มีความสัมพันธ์อย่างใกล้ชิดกับ AMD ชนิดฝ่อและ MNV ชนิดที่ 3 (RAP ) และถือเป็นปัจจัยทำนายการเกิด RAP ที่สำคัญทางคลินิก 1)
จากพื้นหลังของการสะสมของ RP D และดรูเซน ชนิดอ่อน ความผิดปกติของ RPE และเซลล์รับแสง จะดำเนินไป ภายใต้ภาวะขาดออกซิเจนเรื้อรัง ปัจจัยส่งเสริมการสร้างเส้นเลือดใหม่ เช่น VEGF จะถูกผลิตและสะสม กระตุ้นให้เกิดการแตกหน่อของเส้นเลือดใหม่จากข่ายเส้นเลือดฝอยชั้นลึก เส้นเลือดใหม่จะดำเนินไปเป็นระยะๆ ดังนี้
ระยะที่ 1 : การสร้างเส้นเลือดใหม่ภายในข่ายเส้นเลือดฝอยชั้นลึก (neovascularization ภายในจอประสาทตา )ระยะที่ 2 : การขยายไปยังช่องใต้จอประสาทตา ระยะที่ 3 : ร่วมกับการลอกตัวของเยื่อบุผิวสีระยะที่ 4 : การเกิด anastomosis กับเส้นเลือดใหม่คอรอยด์ (retinal-choroidal anastomosis)
ในรายงานต้นฉบับของ Yannuzzi และคณะในปี 2001 ได้เสนอแบบจำลองการดำเนินโรคจากด้านจอประสาทตา ไปทางคอรอยด์ 3) อย่างไรก็ตาม ในช่วงไม่กี่ปีที่ผ่านมา ด้วยความก้าวหน้าของ OCT ก็มีรายงานรูปแบบที่เส้นเลือดใหม่เกิดขึ้นจากด้านคอรอยด์ และเชื่อมต่อกับเส้นเลือดจอประสาทตา Freund และคณะเรียกเส้นเลือดใหม่ที่ทำให้เกิด retinal-choroidal anastomosis ว่า “neovascularization ชนิดที่ 3” และมีจุดยืนว่าไม่จำเป็นต้องมีการจำแนกระยะ 4)
ปัจจุบัน มีสามเส้นทางที่ถูกสันนิษฐาน
เส้นเลือดจอประสาทตา → ชั้นนอกของจอประสาทตา → RPE → คอรอยด์ (เส้นทางคลาสสิก)
เส้นเลือดใหม่คอรอยด์ → RPE → จอประสาทตา (เส้นทางย้อนกลับ)
การดำเนินโรคสองทิศทางจากทั้งสองด้าน
ไม่ว่าจะเป็นเส้นทางใด ความเสียหายต่อ RPE และเซลล์รับแสง เป็นจุดเริ่มต้นของการเพิ่มการผลิต VEGF เมื่อ retinal-choroidal anastomosis สมบูรณ์ การดื้อต่อการรักษาจะเพิ่มขึ้นและการดำเนินไปสู่พังผืดจะเร่งขึ้น ดังนั้นจึงเป็นสิ่งสำคัญที่จะยับยั้งการทำงานของเส้นเลือดใหม่ให้เร็วที่สุดเท่าที่จะเป็นไปได้
ในผลลัพธ์ 2 ปีจากการทดลอง TENAYA และ LUCERNE (รายงานของ Khanani และคณะ 2024) ฟาริซิแมบ (แอนติบอดีแบบสองจำเพาะต่อต้าน VEGF/Ang-2) แสดงความไม่ด้อยกว่าในผลลัพธ์ทางสายตาและกายวิภาคเมื่อเทียบกับอะฟลิเบอร์เซปต์ 2 มก. และผู้ป่วยประมาณครึ่งหนึ่งบรรลุการให้ยาเพื่อรักษาระดับด้วยช่วงห่างสูงสุด 16 สัปดาห์ 8) การยับยั้ง Ang-2 คาดว่าจะให้ผลเสริมฤทธิ์ในการทำให้หลอดเลือดคงตัวและยับยั้งการรั่วซึม
อะฟลิเบอร์เซปต์ 8 มก. (สูตรขนาดสูง) มีความเข้มข้นสูงกว่าสูตร 2 มก. ที่มีอยู่ และในการทดลอง PULSAR กำลังพิจารณาการให้ยาเพื่อรักษาระดับด้วยช่วงห่างสูงสุด 16-20 สัปดาห์ 2) ในรูปแบบโรคเช่น RAP ที่ต้องฉีดหลายครั้ง การยืดช่วงห่างการให้ยาคาดว่าจะช่วยลดภาระการรักษา
OCTA กำลังถูกนำมาใช้ในทางคลินิกอย่างรวดเร็วในฐานะวิธีการที่ไม่รุกรานเพื่อประเมินกิจกรรมของเส้นเลือดใหม่ในจอประสาทตา 10) เนื่องจาก RAP มีเส้นเลือดใหม่ภายในจอประสาทตา จึงเหมาะสำหรับการถ่ายภาพด้วย OCTA และคาดว่าจะเป็นทางเลือกเมื่อการตรวจด้วยสารทึบแสงซ้ำๆ เป็นเรื่องยากในผู้สูงอายุ ในอนาคต การพัฒนาอัลกอริทึมการตัดสินใจรักษาโดยอาศัยการวิเคราะห์เชิงปริมาณของ OCTA เป็นความท้าทาย
การวิจัยเกี่ยวกับการแบ่งชั้นความเสี่ยงตามความหลากหลายทางพันธุกรรมของ ARMS 2 และ CF H และกลยุทธ์การรักษาเฉพาะบุคคลกำลังดำเนินอยู่ 11) การเลือกการรักษาและการแทรกแซงป้องกันตามโปรไฟล์ทางพันธุกรรมถือเป็นความท้าทายในอนาคต กำลังมีการสำรวจความเป็นไปได้ในการปรับปรุงพยากรณ์โรคทางสายตาโดยการระบุผู้ป่วยที่มีความเสี่ยงทางพันธุกรรมสูงในระยะ AMD ระยะกลางและแทรกแซงตั้งแต่เนิ่นๆ
ใน AMD ชนิดเส้นเลือดใหม่รวมถึง RAP การตกเลือดใต้จอประสาทตา จำนวนมากอาจทำให้การมองเห็น ลดลงอย่างรวดเร็ว ในระยะแรก การฉีดแก๊สเข้าในน้ำวุ้นตา (ฉีด SF6 หรือ C3F8 0.3-0.5 มล. ร่วมกับการนอนคว่ำ) หรือการตัดน้ำวุ้นตา เพื่อย้ายก้อนเลือดอาจมีประสิทธิภาพในการฟื้นฟูการมองเห็น การใช้เนื้อเยื่อพลาสมิโนเจนแอคติเวเตอร์ (tPA) ร่วมด้วยก็ได้มีการทดลอง แต่ข้อบ่งชี้จำเป็นต้องศึกษาเพิ่มเติม 1)
日本網膜硝子体学会新生血管型加齢黄斑変性診療ガイドライン作成ワーキンググループ. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024;128(9):680-695.
Flaxel CJ, Adelman RA, Bailey ST, et al. Age-Related Macular Degeneration Preferred Practice Pattern. Ophthalmology. 2024;131(1):P1-P49.
Yannuzzi LA, Negrão S, Iida T, et al. Retinal angiomatous proliferation in age-related macular degeneration. Retina. 2001;21(5):416-434.
Freund KB, Ho IV, Barbazetto IA, et al. Type 3 neovascularization: the expanded spectrum of retinal angiomatous proliferation. Retina. 2008;28(2):201-211.
飯田知弘ほか(黄斑部毛細血管拡張症2型診療ガイドライン作成ワーキンググループ). 黄斑部毛細血管拡張症2型診療ガイドライン(第1版). 日眼会誌. 2022;126(4):463-470.
Heier JS, Brown DM, Chong V, et al. Intravitreal aflibercept (VEGF trap-eye) in wet age-related macular degeneration: VIEW 1 and VIEW 2 study results. Ophthalmology. 2012;119(12):2537-2548.
Dugel PU, Koh A, Ogura Y, et al. HAWK and HARRIER: phase 3, multicenter, randomized, double-masked trials of brolucizumab for neovascular age-related macular degeneration. Ophthalmology. 2020;127(1):72-84.
Khanani AM, Kotecha A, Chang A, et al. TENAYA and LUCERNE: 2-year results of faricimab for neovascular age-related macular degeneration. Ophthalmology. 2024;131(7):914-926.
Ohji M, Takahashi K, Okada AA, et al. Efficacy and safety of intravitreal aflibercept treat-and-extend regimens in exudative age-related macular degeneration: 52- and 96-week findings from ALTAIR. Adv Ther. 2020;37(3):1173-1187.
Spaide RF, Fujimoto JG, Waheed NK , et al. Optical coherence tomography angiography. Prog Retin Eye Res. 2018;64:1-55.
Fritsche LG, Igl W, Bailey JN, et al. A large genome-wide association study of age-related macular degeneration highlights contributions of rare and common variants. Nat Genet. 2016;48(2):134-143.
Klein R, Klein BE, Knudtson MD, et al. Fifteen-year cumulative incidence of age-related macular degeneration: the Beaver Dam Eye Study. Ophthalmology. 2007;114(2):253-262.
Martin DF, Maguire MG, Fine SL, et al. Ranibizumab and bevacizumab for treatment of neovascular age-related macular degeneration: two-year results. Ophthalmology. 2012;119(7):1388-1398.
Rosenfeld PJ, Brown DM, Heier JS, et al. Ranibizumab for neovascular age-related macular degeneration. N Engl J Med. 2006;355:1419-1431.
Brown DM, Kaiser PK, Michels M, et al. Ranibizumab versus verteporfin for neovascular age-related macular degeneration. N Engl J Med. 2006;355:1432-1444.