第1期

视网膜血管瘤样增生(RAP)
一目了然的要点
Section titled “一目了然的要点”1. 什么是视网膜血管瘤样增生(RAP)?
Section titled “1. 什么是视网膜血管瘤样增生(RAP)?”视网膜血管瘤样增生(RAP)是年龄相关性黄斑变性(AMD)的一种特殊亚型。与其他源于脉络膜血管的AMD不同,RAP的新生血管起源于视网膜深层毛细血管丛,随着进展可与脉络膜新生血管吻合。
2001年Yannuzzi等人将其作为独立疾病概念提出,最初分为1~3期 3)。随后在2010年,Yannuzzi本人增加了第4期,报告了四期分期。另一方面,Freund等人提出了统一的命名“3型新生血管”,并认为分期没有必要 4)。
在日本新生血管性AMD诊疗指南(2024年)中,将黄斑部新生血管统称为“黄斑新生血管(MNV)”,并将RAP正式分类为“3型MNV” 1)。由于传统的“脉络膜新生血管(CNV)”一词不包括视网膜来源的新生血管,目前正逐步向MNV过渡。
传统上,黄斑部新生血管被称为“脉络膜新生血管(CNV)”,但由于也包括视网膜来源的新生血管,自2020年起国际上使用“黄斑新生血管(MNV)”这一术语 1)。对应于RAP的3型MNV起源于视网膜血管,与脉络膜来源的1型和2型MNV在起源上明显不同。
在欧美,新生血管性AMD患者中RAP占15-20%。在日本,亚洲人中的频率较低,约为5%。其特征是好发于老年女性,发病年龄多在70岁以上。
双眼发病率极高,单眼发病时对侧眼的发病风险显著升高。因此,临床随访对侧眼极为重要。与其他AMD亚型相比,进展更快,即使治疗反应良好,复发率也高。长期病程中易出现萎缩病灶,被认为是AMD中视力预后不良的亚型。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”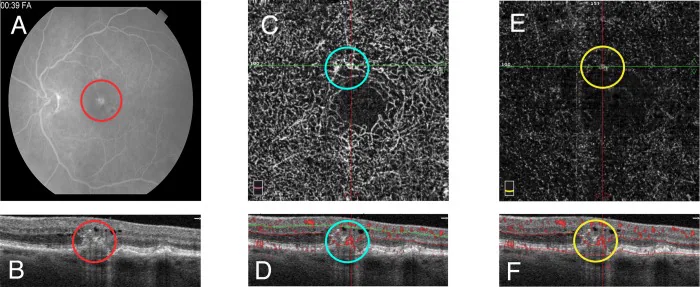
早期至中期出现以下自觉症状。
症状进展相对较快,与其他AMD亚型相比,早期即易出现严重视力下降。当囊样黄斑水肿显著时,可能出现急剧视力下降,因此早期就诊和诊断对维持视功能至关重要。
临床所见(医生检查确认的所见)
Section titled “临床所见(医生检查确认的所见)”后极部多发性软性玻璃膜疣聚集和网状假性玻璃膜疣(RPD)是特征性基础所见。RPD是位于视网膜色素上皮(RPE)上的网状至点状沉积物,被认为是RAP的前驱病变1)。
活动期可见以下所见。
- 视网膜表层出血和视网膜内出血:后极部有少量至中等量出血。特别是在第1期,新生血管周围可见少量表层出血,新生血管表现为结节状红点。
- 囊样黄斑水肿:RAP的特征性表现,与其他AMD亚型相比,更严重且更早出现。
- 视网膜下渗出液和浆液性视网膜脱离:第2期及以后出现。
- 色素上皮脱离(PED):在进展期(第3期及以后)合并出现。表现为纤维血管性PED或玻璃膜疣样PED。
基于RAP分期分类(Yannuzzi 4期分类)的临床发现如下所示3)。
第2期
第3期
第4期
影像学检查所见
Section titled “影像学检查所见”3型MNV在检眼镜或眼底照片下难以观察,必须通过影像学检查确认1)。主要检查方法和所见总结如下。
| 检查 | 特征性所见 |
|---|---|
| FA | 热点(结节状强荧光),后期荧光素渗漏明显 |
| IA(ICGA) | 热点、RRA/RCA显示 |
| OCT | bump征、IRF、SRF、PED、囊样黄斑水肿 |
| OCTA | 无创显示视网膜内和视网膜下新生血管 |
OCT是RAP分期和治疗效果评估的主要手段。bump征是RPE正上方的小隆起性病变,被认为是3型MNV相对特异的征象。OCT在发病早期即可见囊样黄斑水肿,随着病程进展可并发PED1)。
OCTA的B扫描图像可以捕捉到与视网膜表层血管吻合的视网膜内新生血管延伸至视网膜下或穿透RPE至RPE下的图像1)。由于RAP在视网膜内产生新生血管,因此在AMD中尤其容易通过OCTA显示异常血管。对于难以重复进行造影检查的老年患者,OCTA的无创病灶评估非常有用10)。
IRF(视网膜内液)和SRF(视网膜下液)被用作疾病活动性的判断指标。由于3型MNV的病灶不一定发生在中心凹,因此建议扫描整个黄斑或整个病变区域以准确评估液体1)。
3. 原因和风险因素
Section titled “3. 原因和风险因素”RAP的主要风险因素如下所示。
- 年龄:最大的风险因素。年龄越大,发病风险越高。
- 性别:女性好发。
- 后极部软性玻璃膜疣:黄斑部出现多个大型软性玻璃膜疣(长径≥125μm)是AMD进展的重要前驱表现1)。
- 网状假性玻璃膜疣(RPD):被认为是与RAP发病最密切相关的前驱病变。RPD不同于通常的玻璃膜疣(位于RPE下),是位于RPE上的网状至点状沉积物,广泛被认为是3型MNV和萎缩型AMD进展的风险因素1)。
- 遗传易感性:ARMS2基因多态性和CFH(补体H因子)基因多态性与AMD的整体易感性有关11)。大规模全基因组关联分析已证实这些基因座是AMD发病风险的主要决定因素。
- 吸烟:是AMD整体的风险因素,也是最重要的可改变危险因素。在针对日本人群的Funagata研究、Hisayama研究和Nagahama研究中,均报告了吸烟与AMD的关联,Hisayama研究指出吸烟习惯使晚期AMD的发病风险增加4倍12)。
双眼发病率高也是重要特征,一旦发现单眼发病,必须定期随访对侧眼。如果对侧眼也出现软性玻璃膜疣或RPD,发病风险会进一步升高,因此需要缩短间隔进行精密检查。
关于性别比例,新生血管型AMD整体男性较多(男:女=3:1),而RAP则女性发病较多。发病年龄与AMD整体相同或略高,70岁以上占大多数。
RAP的双眼发病率极高。即使只有单眼发病,对侧眼同样发病的风险也高于其他AMD亚型。从单眼发病时起,就必须定期对侧眼进行精密检查。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”3型MNV难以通过检眼镜或眼底照片观察,因此确诊需要结合多种影像检查进行系统评估1)。
诊断步骤如下。
- 临床怀疑:双眼多发软性玻璃膜疣的老年患者,后极部出现视网膜内出血时,应怀疑3型MNV。
- OCT检查:发病早期出现囊样黄斑水肿,若出现bump sign(RPE断裂样团块反射)则强烈提示。合并PED提示病情进展。
- OCTA检查:B扫描图像中确认从视网膜表层血管向bump sign的连续血流信号。无创,尤其适用于难以进行造影检查的老年患者。
- FA/ICGA检查:FA显示结节状强荧光(热点)和晚期明显荧光渗漏。ICGA显示RRA/RCA作为热点,有助于确定病期。
活动性评估以OCT为主,无创判断IRF、SRF和sub-RPE fluid的存在1)。浆液性PED与出血性PED的鉴别通过OCT内容物亮度进行:中亮度为玻璃膜疣,低亮度为浆液性。
与黄斑部毛细血管扩张症2型(MacTel type 2)的鉴别
Section titled “与黄斑部毛细血管扩张症2型(MacTel type 2)的鉴别”MacTel 2型与RAP一样在黄斑部产生病变,并可合并视网膜下新生血管,因此鉴别很重要5)。
| 鉴别点 | RAP(3型MNV) | MacTel type 2 |
|---|---|---|
| 发病年龄 | 老年(70岁以上多见) | 中老年(50~60岁) |
| 背景所见 | 多发软性玻璃膜疣和RPD | 中心凹颞侧视网膜透明度降低 |
| OCT | bump征、PED、囊样水肿 | 椭圆体带缺损、视网膜空腔(无增厚) |
| 进展速度 | 快(以渗出/出血为主) | 缓慢(以视网膜萎缩为主) |
MacTel 2型的特征性表现是直角小静脉(向视网膜深层方向直角弯曲并被牵拉的小静脉)和晶状体蛋白样沉积物。无赤光图像(尤其是共焦蓝光反射)显示黄斑区呈环形或水平椭圆形高反射,在疾病早期即可出现,对诊断有用5)。OCT上特征性表现为无视网膜增厚的视网膜内空腔,进展时可形成外层板层孔或黄斑孔5)。
而RAP在IA上表现为热点伴软性玻璃膜疣聚集,OCT上以bump征和囊样黄斑水肿为主,可与MacTel明确区分。MacTel以视网膜萎缩为主,进展缓慢;而RAP以渗出/出血为主,进展迅速。
与息肉状脉络膜血管病变(PCV)的鉴别
Section titled “与息肉状脉络膜血管病变(PCV)的鉴别”PCV在IA上表现为息肉状病灶(结节状强荧光)和异常血管网(分支状血管网),OCT上特征性表现为内部低反射腔的陡峭RPE隆起1)。眼底照片可见橙红色隆起病灶。RAP以IA上的热点为主,囊样黄斑水肿突出,可资鉴别。PCV常伴有脉络膜增厚(厚脉络膜表现),而RAP的背景表现为软性玻璃膜疣和RPD聚集。
与典型AMD(1型和2型MNV)的鉴别
Section titled “与典型AMD(1型和2型MNV)的鉴别”典型AMD以脉络膜来源的新生血管为主。1型MNV位于RPE下,OCT上表现为双层征。2型MNV位于RPE上(视网膜下腔),OCT上表现为视网膜下中等反射团块1)。RAP因新生血管来源于视网膜血管且位于视网膜内,早期即出现囊样黄斑水肿并伴有bump征,可与之区分。此外,RAP常双眼发病,且多伴有软性玻璃膜疣多发。
5. 标准治疗方法
Section titled “5. 标准治疗方法”玻璃体腔内抗VEGF药物注射(一线治疗)
Section titled “玻璃体腔内抗VEGF药物注射(一线治疗)”新生血管性AMD的一线治疗是玻璃体腔内抗VEGF药物注射1)。对于3型MNV,所有抗VEGF药物也显示出视力改善效果。
目前,可用于新生血管性AMD的抗VEGF药物如下1)。
- 雷珠单抗(Lucentis/雷珠单抗BS):MARINA试验中,24个月时假注射组视力下降14.9个字母,而雷珠单抗每月注射组视力改善6.6个字母14)。ANCHOR试验也显示其优于PDT15)。
- 阿柏西普2mg(Eylea):VIEW 1/2试验中,初始3次注射后每8周注射一次,在维持视力方面非劣效于雷珠单抗每月注射6)。
- 布罗珠单抗6mg(Beovu):HAWK/HARRIER试验中,初始3次注射后每8-12周注射一次,在视力改善方面非劣效于阿柏西普,且在减少中心视网膜厚度方面显示出优效性7)。
- 法瑞西单抗(Vabysmo):针对VEGF和血管生成素-2的双特异性抗体。TENAYA/LUCERNE试验中,初始4次注射后每8-16周注射一次,非劣效于阿柏西普8)。
导入期:每月注射1次,通常连续3次(法瑞西单抗为4次),以改善视力1)。
维持期的给药方法包括以下选择。
- 固定给药法:临床试验中使用的方法。按固定间隔(如每8周)给药。
- 按需给药法(PRN):每月随访,仅在观察到疾病活动时给药。但长期报告显示PRN法可能导致视力恶化1, 13)。
- 治疗并延长间隔法(T&E):根据疾病活动逐步延长给药间隔的方法,是目前最推荐的维持疗法。荟萃分析显示,该方法可维持与每月注射相当的视力改善,且视力结果优于PRN法1)。
针对日本患者的ALTAIR试验报告,阿柏西普的T&E法(以2周或4周为增量调整间隔)在96周内维持了视力和视网膜厚度的改善9)。关于T&E法应持续多久尚无共识,需根据患者病情和社会状况判断1)。
治疗中的疾病活动性评估
Section titled “治疗中的疾病活动性评估”OCT是评估治疗效果的主要工具。MNV周围液体(IRF、SRF、sub-RPE fluid)的存在或复发提示活动性1)。由于3型MNV的视网膜内新生血管不一定局限于中心凹,建议扫描整个黄斑或整个病变区域进行评估。
当治疗中效果不佳(治疗抵抗病例)或效果减弱(获得耐药性)时,换用其他抗VEGF药物可能有效1)。RAP是容易表现出治疗抵抗性的病变类型,因此在反应不良时早期换药很重要。有时也会考虑换药以减轻治疗负担。
光动力疗法(PDT)
Section titled “光动力疗法(PDT)”目前不推荐对3型MNV单独使用PDT1)。对于抗VEGF药物抵抗的病例,可考虑联合PDT,但长期来看PDT可能加重黄斑萎缩。对于脉络膜较薄或已有黄斑萎缩的病例,最好避免使用PDT1)。
联合使用PDT时的处方如下。
- 维替泊芬(维速达尔):6 mg/体表面积(m²),静脉输注10分钟
- 激光照射:输注开始后15分钟照射(689 nm,600 mW/cm²,83秒)
- 照射范围:基于造影所见病变最大直径+1,000 μm的光斑大小
- 抗VEGF药物联合时机:PDT前1周内或PDT当天(避光下)给药
- 术后管理:治疗后2天内需避免直射阳光
新生血管性AMD目前无法完全治愈,如果不进行适当的治疗和长期管理,会导致不可逆的视力下降1)。RAP尤其需要在以下方面长期注意。
- 即使MNV活动性稳定,长期过程中也可能复发
- 反复渗出会导致萎缩性变化和纤维性瘢痕。长期过程中容易发生视网膜萎缩(地图状萎缩),这是不可逆视力下降的主要原因
- 对侧眼也高概率发生MNV
当出现严重视功能下降时,应积极考虑引入放大镜、放大阅读器等低视力康复。由于新生血管性AMD无法完全治愈,建议与患者共同制定可持续的管理计划,同时考虑患者的社会状况和对侧眼的状态1)。
个体差异很大,但导入期连续给药3次(法瑞西单抗为4次)后,采用treat-and-extend法调整给药间隔1)。RAP比其他AMD亚型更易出现治疗抵抗,可能需要多次注射。针对日本人的ALTAIR试验证实了96周长期维持治疗效果9)。法瑞西单抗等新药可维持最长16周的给药间隔,有望减轻治疗负担8)。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”新生血管的起源
Section titled “新生血管的起源”RAP的本质是起源于视网膜深层毛细血管丛的视网膜内新生血管。这是其被命名为“3型MNV”的依据,与起源于脉络膜的1型和2型MNV在发病机制上根本不同1)。
MNV分类中3型MNV的定位如下:
前驱病变与RAP形成的过程
Section titled “前驱病变与RAP形成的过程”软性玻璃膜疣的聚集和网状假性玻璃膜疣(RPD)是重要的前驱病变。RPD与通常的玻璃膜疣(位于RPE下方的沉积物)不同,是位于RPE上方的三角锥状沉积物。在OCT上表现为从RPE层向视网膜内突出的形状,有些可越过椭圆体带达到外界膜。RPD与萎缩型AMD和3型MNV(RAP)密切相关,作为RAP发病的预测因子在临床上受到重视1)。
在RPD和软性玻璃膜疣积累的背景下,RPE和感光细胞的功能障碍逐渐进展。在慢性低氧环境下,包括VEGF在内的促血管生成因子产生并积累,诱导从深层毛细血管丛发出新生血管芽。新生血管按以下过程逐步进展。
- 第1阶段:深层毛细血管丛内的新生血管形成(视网膜内新生血管)
- 第2阶段:向视网膜下腔扩展
- 第3阶段:合并色素上皮脱离
- 第4阶段:与脉络膜新生血管形成吻合(视网膜-脉络膜血管吻合)
关于发病途径的讨论
Section titled “关于发病途径的讨论”在2001年Yannuzzi等人的原始报告中,提出了从视网膜侧向脉络膜方向进展的模型3)。然而近年来,随着OCT的进步,也有报道称新生血管从脉络膜侧发生并与视网膜血管吻合。Freund等人将形成视网膜-脉络膜血管吻合的新生血管称为“3型新生血管”,并认为分期是不必要的4)。
目前,假设有以下三种途径。
- 视网膜血管→视网膜外层→RPE→脉络膜(经典途径)
- 脉络膜新生血管→RPE→视网膜(逆行途径)
- 双向进展
在任何途径中,RPE和感光细胞的损伤都是VEGF产生增加的起点。一旦视网膜-脉络膜吻合完成,治疗抵抗性进一步增加,向纤维瘢痕的进展加速,因此尽可能在早期阶段抑制新生血管活动至关重要。
7. 最新研究与未来展望(研究阶段的报告)
Section titled “7. 最新研究与未来展望(研究阶段的报告)”法瑞西单抗的长期结果
Section titled “法瑞西单抗的长期结果”TENAYA和LUCERNE试验的2年结果(Khanani等人,2024年报告)显示,法瑞西单抗(抗VEGF/抗Ang-2双特异性抗体)在视力和解剖学结局方面与阿柏西普2mg相比保持非劣效性,约半数患者实现了长达16周间隔的维持给药8)。通过抑制Ang-2,预期可产生血管稳定和渗出抑制的协同效应。
阿柏西普8mg高剂量制剂
Section titled “阿柏西普8mg高剂量制剂”阿柏西普8mg(高剂量制剂)比现有的2mg制剂浓度更高,在PULSAR试验中正在探讨长达16-20周间隔的维持给药2)。对于像RAP这样需要多次注射的疾病类型,延长给药间隔有望大大减轻治疗负担。
OCTA随访的进展
Section titled “OCTA随访的进展”OCTA作为一种无创评估视网膜新生血管活动性的方法,正在迅速进入临床应用10)。RAP由于新生血管存在于视网膜内,适合用OCTA显示,在老年患者难以进行重复造影检查时,有望作为替代手段。未来的挑战是开发基于OCTA定量分析的治疗决策算法。
基因个体化治疗与预防策略
Section titled “基因个体化治疗与预防策略”基于ARMS2和CFH基因多态性的发病风险分层和个体化治疗策略的研究正在推进11)。根据基因图谱选择治疗和进行预防干预被认为是未来的课题。正在探索在中期AMD阶段识别高遗传风险患者并早期治疗干预以改善视力预后的可能性。
黄斑下血肿的外科干预
Section titled “黄斑下血肿的外科干预”在包括RAP在内的新生血管性AMD中,大量黄斑下出血可导致急剧视力下降。在早期阶段,玻璃体内注气术(注入SF6或C3F8 0.3-0.5mL并保持俯卧位)或玻璃体切除术伴血肿移位可能对视力改善有效。也有尝试联合使用组织型纤溶酶原激活剂(tPA),但适应症仍需进一步研究1)。
8. 参考文献
Section titled “8. 参考文献”- 日本網膜硝子体学会新生血管型加齢黄斑変性診療ガイドライン作成ワーキンググループ. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024;128(9):680-695.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Age-Related Macular Degeneration Preferred Practice Pattern. Ophthalmology. 2024;131(1):P1-P49.
- Yannuzzi LA, Negrão S, Iida T, et al. Retinal angiomatous proliferation in age-related macular degeneration. Retina. 2001;21(5):416-434.
- Freund KB, Ho IV, Barbazetto IA, et al. Type 3 neovascularization: the expanded spectrum of retinal angiomatous proliferation. Retina. 2008;28(2):201-211.
- 飯田知弘ほか(黄斑部毛細血管拡張症2型診療ガイドライン作成ワーキンググループ). 黄斑部毛細血管拡張症2型診療ガイドライン(第1版). 日眼会誌. 2022;126(4):463-470.
- Heier JS, Brown DM, Chong V, et al. Intravitreal aflibercept (VEGF trap-eye) in wet age-related macular degeneration: VIEW 1 and VIEW 2 study results. Ophthalmology. 2012;119(12):2537-2548.
- Dugel PU, Koh A, Ogura Y, et al. HAWK and HARRIER: phase 3, multicenter, randomized, double-masked trials of brolucizumab for neovascular age-related macular degeneration. Ophthalmology. 2020;127(1):72-84.
- Khanani AM, Kotecha A, Chang A, et al. TENAYA and LUCERNE: 2-year results of faricimab for neovascular age-related macular degeneration. Ophthalmology. 2024;131(7):914-926.
- Ohji M, Takahashi K, Okada AA, et al. Efficacy and safety of intravitreal aflibercept treat-and-extend regimens in exudative age-related macular degeneration: 52- and 96-week findings from ALTAIR. Adv Ther. 2020;37(3):1173-1187.
- Spaide RF, Fujimoto JG, Waheed NK, et al. Optical coherence tomography angiography. Prog Retin Eye Res. 2018;64:1-55.
- Fritsche LG, Igl W, Bailey JN, et al. A large genome-wide association study of age-related macular degeneration highlights contributions of rare and common variants. Nat Genet. 2016;48(2):134-143.
- Klein R, Klein BE, Knudtson MD, et al. Fifteen-year cumulative incidence of age-related macular degeneration: the Beaver Dam Eye Study. Ophthalmology. 2007;114(2):253-262.
- Martin DF, Maguire MG, Fine SL, et al. Ranibizumab and bevacizumab for treatment of neovascular age-related macular degeneration: two-year results. Ophthalmology. 2012;119(7):1388-1398.
- Rosenfeld PJ, Brown DM, Heier JS, et al. Ranibizumab for neovascular age-related macular degeneration. N Engl J Med. 2006;355:1419-1431.
- Brown DM, Kaiser PK, Michels M, et al. Ranibizumab versus verteporfin for neovascular age-related macular degeneration. N Engl J Med. 2006;355:1432-1444.
