
视野扭曲或缺失的可能原因总结
一目了然的要点
Section titled “一目了然的要点”1. 视野变形或缺损是什么?
Section titled “1. 视野变形或缺损是什么?”“东西变形”、“直线看起来弯曲”、“视野部分缺失或变暗”等症状可由多种原因引起,包括黄斑疾病、视网膜疾病、青光眼、视神经疾病和脑部疾病。这些症状大致分为两种病理状态。
视物变形是指物体的形状、大小或直线看起来变形的症状。主要原因是黄斑(视网膜中心部分)的结构性变化,典型表现为方格或直线看起来呈波浪状。
视野缺损是指视野的一部分看不见(感觉变暗或缺失)的症状。可由多种疾病引起,包括青光眼、视网膜脱离、视网膜血管阻塞、视神经疾病和脑部疾病。
年龄相关性黄斑变性(AMD)的患病率在久山町研究中报告为晚期1.6%(渗出型1.5%,萎缩型0.1%),在长滨研究中前驱病变占22.8%。AMD多见于50岁以上人群和男性(男:女=3:1),双眼受累占40%。另一方面,青光眼的患病率在40岁以上人群中约为5% 1),是日本主要致盲原因之一。
准确掌握症状的类型和发作方式,并在适当的时间就诊眼科是保护视力的关键。养成每只眼睛分别检查的习惯有助于早期发现。
2. 引起视物变形(扭曲)的疾病
Section titled “2. 引起视物变形(扭曲)的疾病”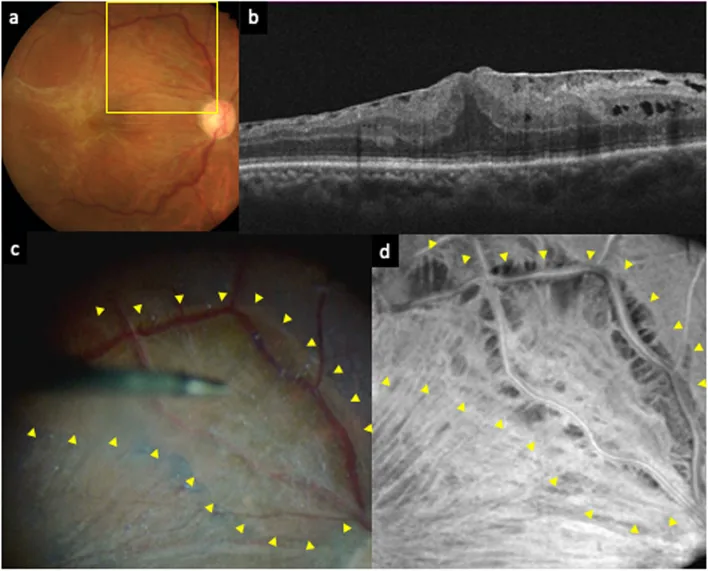
视物变形通常由黄斑(眼睛中心部分)的结构性变化引起。典型症状包括直线或格子看起来呈波浪状,以及中心视野变暗(中心暗点)。
| 疾病 | 好发年龄/性别 | 主要特征 | 紧急程度 |
|---|---|---|---|
| 黄斑前膜 | 中老年人 | 视物变形、大视症。Gass分级0~2级。OCT确诊。 | 低至中(观察→手术) |
| 年龄相关性黄斑变性(AMD) | 50岁以上,男性居多 | 首发症状为视物变形和中心暗点。进展后视力≤0.1。 | 中至高(早期治疗很重要) |
| 黄斑裂孔 | 中老年女性 | 中心凹全层缺损→中心暗点和视物变形 | 中(有手术指征) |
| 中心性浆液性脉络膜视网膜病变(CSC) | 青中年男性 | 压力或类固醇使用为诱因。也可出现小视症2) | 低至中(多可自然缓解) |
| 糖尿病性黄斑水肿(DME) | 糖尿病患者 | 黄斑部水肿导致视物变形和视力下降3) | 中至高(治疗干预可防止恶化) |
视网膜前膜(黄斑前膜)的详细说明
Section titled “视网膜前膜(黄斑前膜)的详细说明”视网膜前膜在特发性病例中由视网膜胶质细胞在内界膜上增殖形成纤维组织所致。也可继发于炎症、视网膜脱离、外伤或视网膜血管肿瘤。症状包括视力下降和视物变形,有时伴有大视症。Gass分级从0级(玻璃纸样黄斑病变:透明,无视网膜变形)到2级(灰色不透明膜,明显皱褶)。OCT检查确认视网膜前膜和视网膜厚度增加是确诊的依据。当存在视力障碍、明显视网膜增厚或严重视物变形时,可行玻璃体切除术联合视网膜前膜剥离。术后视力与术前视力密切相关,恢复可能需要较长时间(一年以上)。
年龄相关性黄斑变性(AMD)的分类
Section titled “年龄相关性黄斑变性(AMD)的分类”AMD从前驱病变(软性玻璃膜疣、视网膜色素上皮异常)进展,分为萎缩型(地图状萎缩)和渗出型(脉络膜新生血管:CNV)。渗出型中,息肉状脉络膜血管病变(PCV)是日本人中常见的特殊亚型。渗出型AMD以视物变形和中心暗点起病,若不治疗,约90%的患者视力降至0.1以下。大量出血病例可能出现突然的严重视力下降。
3. 引起视野缺损(缺失)的疾病
Section titled “3. 引起视野缺损(缺失)的疾病”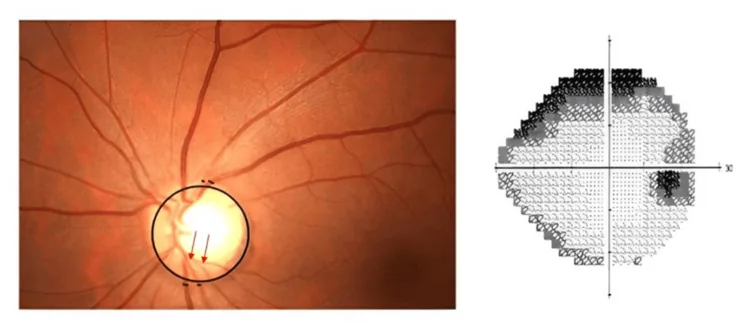
视野缺损表现为视野部分变暗、缺失或像有帘子遮挡等症状。原因多种多样,从缓慢进展的青光眼到突然发作的紧急疾病如视网膜脱离和视网膜动脉阻塞。
| 疾病 | 视野缺损模式 | 紧急程度 |
|---|---|---|
| 青光眼 | 弓形暗点、旁中心暗点。中心视力保持到末期 1) | 低至中(慢性进展,需要定期管理) |
| 视网膜脱离(孔源性) | 帘幕状视野缺损。从一侧扩展。 | 紧急(可能需要当天手术) |
| 视网膜静脉阻塞(分支型) | 扇形视野缺损(与阻塞静脉区域一致)4) | 中至高(早期治疗影响预后) |
| 视网膜动脉阻塞 | 突然无痛性视力丧失及广泛视野缺损5) | 紧急(发病后数小时是关键) |
| 双侧视野缺损 | 以垂直线为界的偏盲(同侧偏盲)→ 怀疑脑部疾病6) | 紧急(与神经内科/神经外科协作) |
青光眼视野缺损的特征
Section titled “青光眼视野缺损的特征”青光眼中,视神经纤维的变性和脱落导致相应视野出现弓形暗点和旁中心暗点。早期至中期中心视力保持正常,因此患者往往难以察觉,当意识到时通常已有相当程度的视野丧失1)。根据多治见研究,40岁以上日本人的原发性开角型青光眼患病率约为3.9%1),定期测量眼压和眼底检查对早期发现至关重要。
视网膜脱离的视野缺损
Section titled “视网膜脱离的视野缺损”在孔源性视网膜脱离中,视网膜下液从裂孔扩散时,会出现从一侧扩大的帘幕状或幕状视野缺损9)。发病前常先有闪光感和飞蚊症的急剧增加。当视野缺损累及黄斑部(中心区域)时,视力显著下降,因此在此之前进行紧急手术对视力预后至关重要。
脑部疾病引起的视野缺损
Section titled “脑部疾病引起的视野缺损”双侧视野对称性缺损的“同侧偏盲”提示视放射或枕叶等脑部病变。可能由脑梗死、脑肿瘤或颅内出血引起6),需要与神经内科和神经外科迅速协作。
4. 突然的视野变化(闪光暗点/一过性黑蒙)
Section titled “4. 突然的视野变化(闪光暗点/一过性黑蒙)”突然的暂时性视野变化,从可自行消退的偏头痛相关闪光暗点,到需要紧急检查的一过性黑蒙,病因各不相同。鉴别要点在于单眼还是双眼、持续时间以及伴随症状。
| 症状 | 持续时间 | 眼别 | 特征 | 紧急程度 |
|---|---|---|---|---|
| 闪光暗点(偏头痛先兆) | 20~30分钟自行消退 | 双眼性(视野同侧) | 锯齿状光环、彩色光扩大 | 低(咨询偏头痛门诊) |
| 一过性黑蒙(TIA眼部症状) | 数秒至数分钟 | 单眼性 | 单眼完全看不见,感觉有幕布从上往下拉7) | 紧急(当天就诊神经内科/眼科) |
| 视网膜脱离前兆(闪光感) | 反复性 | 单眼性 | 在暗处出现闪光或闪电状光。伴有飞蚊症增加。 | 高(数日内就诊眼科) |
| 玻璃体出血 | 突然、持续 | 单眼性 | 飞蚊症急剧增加、模糊、视力下降 | 高(紧急眼科就诊) |
双侧偏盲的紧急性
Section titled “双侧偏盲的紧急性”如果双眼同时出现同侧半视野缺损(例如,双眼右侧视野均缺损),是脑梗死、脑肿瘤或枕叶病变的紧急征兆6)。需要立即就医。
5. 自我检查法(阿姆斯勒方格表)及就诊标准
Section titled “5. 自我检查法(阿姆斯勒方格表)及就诊标准”阿姆斯勒方格表的使用方法
Section titled “阿姆斯勒方格表的使用方法”使用阿姆斯勒方格表进行自我检查有助于监测AMD和黄斑疾病,据报道,在中心5度范围内检测AMD的灵敏度约为70%8)。但由于灵敏度有限,即使方格表无异常,也应继续定期进行眼科检查。
就诊紧急程度
Section titled “就诊紧急程度”| 紧急程度 | 症状 | 推荐行动 |
|---|---|---|
| 当日就诊(包括急诊) | 突然的幕状视野缺损 / 单眼突然无痛性视力丧失 / 单眼一过性视力消失 / 双眼同侧视野缺损 | 当天前往眼科或急诊。可能为视网膜脱离、RAO、TIA。 |
| 早期就诊(数日内) | 阿姆斯勒方格表检测到扭曲或暗点 / 单眼视力发生变化 / 飞蚊症突然增多伴闪光感 | 1~3天内到眼科进行OCT检查。 |
| 定期就诊 | 有AMD家族史、单眼病史、青光眼危险因素(高眼压、家族史、高度近视)1) | 每年1~2次眼科定期检查。 |
早期至中期的青光眼中心视力保持正常,因此很难自觉视野缺损。这是因为另一只眼和大脑会无意识地补偿缺损的视野。养成闭上一只眼检查视力的习惯,以及定期在眼科进行视野检查,对早期发现非常重要。根据多治见研究,约90%的青光眼患者未被诊断1),因此即使无症状,也建议40岁以上人群定期检查。
6. 扭曲与缺损的病理生理
Section titled “6. 扭曲与缺损的病理生理”黄斑疾病引起视物变形的机制
Section titled “黄斑疾病引起视物变形的机制”黄斑前膜中,视网膜胶质细胞在内界膜上增殖形成纤维组织,导致视网膜表面产生皱褶。这些皱褶扰乱感光细胞的排列,引起视物变形和视物变大。
**年龄相关性黄斑变性(AMD)**中,首先黄斑部的视网膜色素上皮(RPE)受损,出现玻璃膜疣形成和RPE异常。萎缩型AMD进展为地图状萎缩(GA),感光细胞丧失;渗出型AMD则形成脉络膜新生血管(CNV),出血和渗出液损害黄斑部。此过程中感光细胞功能丧失,导致视物变形和中心暗点。
**中心性浆液性脉络膜视网膜病变(CSC)**由于脉络膜通透性增高,导致RPE下和神经视网膜下积液,黄斑部局部隆起。这种隆起改变了焦距,引起视物变形和小视症2)。
青光眼导致视野缺损的机制
Section titled “青光眼导致视野缺损的机制”青光眼中,视神经乳头处的轴突损伤、眼压的机械压迫和缺血等机制导致视神经纤维变性和脱落1)。脱落的纤维对应的视网膜区域出现视野缺损,典型表现为弓形暗点和旁中心暗点。中心视力直到晚期才受影响,这是自觉延迟的主要原因。
视网膜脱离的病理
Section titled “视网膜脱离的病理”在孔源性视网膜脱离中,后玻璃体脱离伴随的视网膜牵引导致视网膜裂孔形成。液化玻璃体通过裂孔进入视网膜下腔,感觉神经视网膜从RPE脱离9)。脱离的视网膜的光感受器处于缺血状态,导致相应的视野缺损。中心部(黄斑)脱离时视力显著下降,长期病程后视力恢复困难。
7. 最新治疗与研究
Section titled “7. 最新治疗与研究”新一代抗VEGF药物(faricimab)
Section titled “新一代抗VEGF药物(faricimab)”Heier等人(2022年)的TENAYA/LUCERNE随机对照试验中,双重抑制VEGF-A和血管生成素-2(Ang-2)的faricimab在渗出性AMD中显示出长达16周给药间隔的非劣效性10)。延长给药间隔有望减轻患者负担。
萎缩性AMD(地图状萎缩)的补体抑制剂
Section titled “萎缩性AMD(地图状萎缩)的补体抑制剂”补体C3抑制剂pegcetacoplan在旨在抑制萎缩性AMD地图状萎缩(GA)进展的2期试验中,与安慰剂相比显示出抑制GA面积扩大的效果11)。萎缩性AMD此前缺乏有效治疗,因此作为新的治疗选择备受关注。
黄斑前膜手术中内界膜剥离的有效性
Section titled “黄斑前膜手术中内界膜剥离的有效性”Azuma等人(2017年)的系统评价和荟萃分析显示,在黄斑前膜手术中增加内界膜(ILM)剥离可改善术后视力和解剖学结果12)。复发风险降低也有报道。
使用家庭监测设备早期检测AMD
Section titled “使用家庭监测设备早期检测AMD”Chew等人(2014年)的HOME研究(随机对照试验)表明,与常规护理相比,家庭监测设备(ForeseeHome)能更早地检测到向渗出型AMD的转变,有助于改善视力预后13)。利用数字技术由患者自身进行的日常监测预计将在未来进一步普及。
8. 参考文献
Section titled “8. 参考文献”- Iwase A, Suzuki Y, Araie M, et al. The prevalence of primary open-angle glaucoma in Japanese: the Tajimi Study. Ophthalmology. 2004;111(9):1641-1648.
- Daruich A, Matet A, Dirani A, et al. Central serous chorioretinopathy: recent findings and new physiopathology hypothesis. Prog Retin Eye Res. 2015;48:82-118.
- 日本糖尿病眼学会. 糖尿病網膜症診療ガイドライン(第1版). 日眼会誌. 2020;124(12):955-981.
- Ehlers JP, Fekrat S. Retinal vein occlusion: beyond the acute event. Surv Ophthalmol. 2011;56(4):281-299.
- Hayreh SS. Acute retinal arterial occlusive disorders. Prog Retin Eye Res. 2011;30(5):359-394.
- Zhang X, Kedar S, Lynn MJ, et al. Homonymous hemianopia in stroke. J Neuroophthalmol. 2006;26(3):180-183.
- Biousse V, Trobe JD. Transient monocular visual loss. Am J Ophthalmol. 2005;140(4):717-721.
- Faes L, Bodmer NS, Bachmann LM, et al. Diagnostic accuracy of the Amsler grid and the preferential hyperacuity perimetry in the screening of patients with age-related macular degeneration: systematic review and meta-analysis. Eye (Lond). 2014;28(7):788-796.
- Feltgen N, Walter P. Rhegmatogenous retinal detachment—an ophthalmologic emergency. Dtsch Arztebl Int. 2014;111(1-2):12-22.
- Heier JS, Khanani AM, Quezada Ruiz C, et al. Efficacy, durability, and safety of intravitreal faricimab up to every 16 weeks for neovascular age-related macular degeneration (TENAYA and LUCERNE): two randomised, double-masked, phase 3, non-inferiority trials. Lancet. 2022;399(10326):729-740.
- Liao DS, Grossi FV, El Mehdi D, et al. Complement C3 inhibitor pegcetacoplan for geographic atrophy secondary to age-related macular degeneration: a randomized phase 2 trial. Ophthalmology. 2020;127(2):186-195.
- Azuma K, Ueta T, Eguchi S, et al. Effects of internal limiting membrane peeling combined with removal of idiopathic epiretinal membrane: a systematic review of literature and meta-analysis. Retina. 2017;37(10):1813-1819.
- Chew EY, Clemons TE, Bressler SB, et al. Randomized trial of the ForeseeHome monitoring device for early detection of neovascular age-related macular degeneration. The HOME Study. Ophthalmology. 2014;121(2):535-544.
