黄斑前膜剥离

黄斑前膜
一目了然的要点
Section titled “一目了然的要点”1. 什么是黄斑前膜?
Section titled “1. 什么是黄斑前膜?”黄斑前膜(Epiretinal Membrane; ERM)是在视网膜内界膜(ILM)上形成的纤维细胞增殖组织。也称为黄斑皱襞、玻璃纸样黄斑病变、视网膜前黄斑纤维化或玻璃体黄斑界面综合征11)。黄斑前膜可继发引起视网膜皱襞、黄斑水肿和牵拉性视网膜脱离。
黄斑前膜分为特发性和继发性两类。继发性黄斑前膜也称为黄斑皱襞(macular pucker)11)。
特发性黄斑前膜与后玻璃体脱离(PVD)相关,多见于50岁以上人群。继发性黄斑前膜继发于多种眼部疾病,如视网膜裂孔、孔源性视网膜脱离、眼内手术、外伤、视网膜血管阻塞、葡萄膜炎、糖尿病视网膜病变和视网膜色素变性等。
患病率因检查方法和目标人群而异,报告范围广泛。各研究的患病率总结如下。
| 研究 | 目标人群 | 患病率 | 检查方法 |
|---|---|---|---|
| 北京眼病研究 | 中国城市地区 | 2.2% | 眼底照相 |
| 邯郸眼病研究 | 中国农村地区 | 3.4% | 眼底照相 |
| 蓝山眼病研究 | 澳大利亚 | 7.0% | 眼底照相 |
| 墨尔本队列 | 澳大利亚 | 8.9% | 眼底照相 |
| Los Angeles Latino Eye Study | 西班牙裔 | 18.8% | 眼底照相 |
| MESA | 美国多种族 | 28.9% | 眼底照相 |
| Beaver Dam Eye Study(20年) | 美国白人(平均年龄74.1岁) | 34.1% | SD-OCT15) |
玻璃纸样黄斑病变(无症状性ERM)的患病率为1.8%~25.1%,症状性ERM(视网膜前黄斑纤维化)为0.7%~3.9%12)。据估计,美国约有3000万人受累12)。双侧受累占20%~35%11)。种族差异也有报道,MESA研究中,华裔39.0%、西班牙裔29.3%、白人27.5%、黑人26.2%16)。
5年内,29%的ERM进展、26%消退、39%保持稳定(Blue Mountains Eye Study)14)。玻璃纸样黄斑病变5年内仅20%进展。伴有PVD的ERM自然分离率为1.5%(1091眼中16眼),无PVD的ERM自然分离率为13.6%(157眼中21眼,平均随访33个月)12)。将手术推迟至症状出现与立即手术相比,预后不会恶化12)。在无后部玻璃体脱离的年轻患者中,偶尔会发生自然分离,因此应谨慎随访。
在2型神经纤维瘤病(NF2)中,黄斑前膜患病率高达80% 9)。玻璃体黄斑牵拉(VMT)的患病率为0.4%~2.0%(63岁以上),ERM和VMT常合并发生 12)。
严重程度分级(Gass分级)
Section titled “严重程度分级(Gass分级)”Gass分级广泛用于临床严重程度分类。
| 分级 | 表现 | 视力参考 |
|---|---|---|
| 0级 | 透明薄膜(玻璃纸样黄斑病变)。无视网膜内层变形 | 良好 |
| 1级 | 膜收缩导致视网膜皱襞。视网膜毛细血管变得模糊 | 通常≥0.5 |
| 2级 | 灰色不透明厚膜。黄斑皱褶明显 | 下降 |
并非所有黄斑前膜都需要手术。无症状、症状轻微或视力良好时,可选择观察。据报道,自然病程中5年内29%进展、26%消退、39%稳定14),将手术推迟至症状出现也不会恶化预后12)。通常,当矫正视力低于0.7且视物变形严重,或视力下降相对急性且认为由黄斑前膜引起时,考虑手术。最终根据患者的主观症状综合判断。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”黄斑前膜常无症状,在体检或其他疾病随访中偶然发现的情况并不少见。有症状时表现为以下症状。
- 视物变形:直线看起来弯曲。这是最具特征性且患者容易主诉的症状。
- 视力下降:随着膜的收缩和增厚而发生。
- 小视症:物体看起来变小。由膜的牵拉导致黄斑变形引起。
- 大视症:物体可能看起来比实际大。
- 单眼复视:一只眼睛看到重影。
- 阅读困难、驾驶困难、双眼视困难:这些是影响日常生活的常见主诉12)。
Amsler网格作为视物变形的自我监测工具很有用,患者可用其检查症状进展12)。
裂隙灯显微镜下可见黄斑表面光泽、视网膜皱襞和血管迂曲。通过加宽裂隙光观察黄斑,可结合OCT图像评估膜的厚度和分布区域。早期表现为水样光泽反射,具有特征性。病变进展时可出现黄斑水肿和假性黄斑裂孔。
厚而白色不透明的膜更容易引起症状并导致黄斑偏位12)。也可能出现正常中心凹凹陷消失、黄斑囊样改变、板层黄斑裂孔以及进展为全层黄斑裂孔。
玻璃体视乳头牵拉(Vitreopapillary traction):视乳头周围的玻璃体粘连可能合并ERM。需注意可能被误诊为视乳头水肿(淤血乳头)12)。
光学相干断层扫描血管成像(OCTA)可观察到中心凹无血管区(FAZ)的形态变化。黄斑前膜眼的FAZ面积为0.11 mm²,与健康眼的0.24 mm²相比显著缩小2)。
3. 病因与风险因素
Section titled “3. 病因与风险因素”黄斑前膜最重要的相关因素是玻璃体后脱离(PVD)。传统假说认为,PVD后残留的皮质玻璃体导致内界膜(ILM)裂开,胶质细胞和RPE细胞迁移至玻璃体腔,分化和增殖为成纤维细胞样细胞,从而形成黄斑前膜11)。
近年来获得支持的新假说认为,ILM裂开并非必需。该假说提出,ILM上残留的玻璃体皮质中的细胞被激活为肌成纤维细胞,导致膜形成和收缩12)。
基于玻璃体袋理论的病理机制
Section titled “基于玻璃体袋理论的病理机制”即使在玻璃体后脱离发生之前,后部玻璃体凝胶内也存在液化腔(后部玻璃体皮质前袋)。袋的后壁是薄而富有弹性的玻璃体皮质,位于黄斑前的这个后部玻璃体皮质上发生细胞增殖等修饰,被认为导致黄斑前膜的形成。
存在两种情况:一种是后部玻璃体未脱离,袋的后壁与黄斑粘连并牵拉视网膜;另一种是完全PVD发生时,残留于视网膜侧的袋的后壁导致黄斑扭曲。玻璃体袋的后壁上细胞增殖可形成黄斑前膜,这种情况多见于继发性病例或年轻人。当玻璃体后脱离发生时,可能出现自然分离。
需要注意的是,手术时后部玻璃体仍附着的病例占20.1%,Weiss环的存在并不一定意味着后部玻璃体完全分离12)。
在NF2相关的黄斑前膜中,免疫组化显示GFAP弱阳性、巢蛋白中度阳性,提示主要成分为Müller细胞来源9)。
主要风险因素如下所示。
- 年龄增长:50岁以上急剧增加,75岁以上患病率进一步上升。
- 玻璃体后脱离(PVD):特发性黄斑前膜的最大诱因。
- 女性:系统综述(超过49,000例)确认其为显著风险因素13)。
- 视网膜裂孔/视网膜脱离:继发性黄斑前膜的主要原因。
- 眼内手术史:白内障手术是继发性ERM的确定危险因素12)。
- 糖尿病和高脂血症:玻璃纸样黄斑病变的危险因素(MESA数据)12)。
- 视网膜血管阻塞和葡萄膜炎:作为炎症后的增殖反应发生。
- 视网膜色素变性:继发性ERM的病因之一。
- 放射治疗:已有质子束照射后继发性视网膜前膜的报道3)。
4. 诊断和检查方法
Section titled “4. 诊断和检查方法”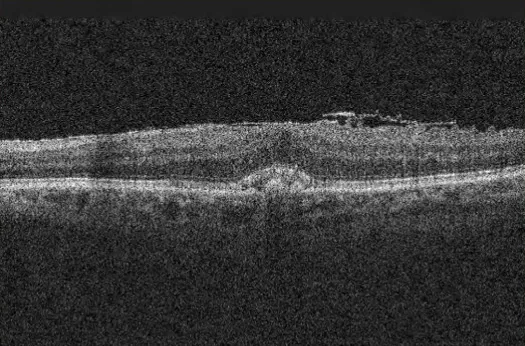
检查方法概述
Section titled “检查方法概述”总结各项检查的作用。
| 检查 | 主要目的 | 特点 |
|---|---|---|
| OCT | 膜显示、厚度评估、视网膜牵引确认 | 最重要、无创 |
| OCTA | 血管血流评估 | FAZ面积、新生血管检测 |
| FA | 血管通透性、无灌注评估 | 合并疾病的鉴别 |
| 眼底检查 | 表面光泽、皱襞确认 | 筛查 |
光学相干断层扫描(OCT)是诊断的核心。ERM在OCT上表现为内表面的高反射层,常通过内视网膜表面的脚(pegs)附着,并呈现波浪状断面。可见中心凹凹陷消失、视网膜外层隆起、囊样改变等。通过OCT还可以评估玻璃体或膜组织对视网膜的牵引、视网膜肿胀、囊样改变、有无视网膜脱离以及椭圆体带(EZ)的状态。术前预测ILM缺损时,en face OCT很有用,22.7%的病例术前已确认ILM缺损1)。
ERM合并VMT在ERM眼中占57%,据报道VMT眼中65%合并ERM12)。
**OCTA(光学相干断层扫描血管成像)**显示浅层毛细血管丛(SCP)的血管面积密度(VAD)升高2)。它也有助于检测黄斑前膜引起的视网膜内新生血管6)。
荧光素眼底血管造影(FA):早期ERM表现为相对正常的图像。随着膜收缩进展,在牵拉中心附近可见血管迂曲,周围血管变直。还可观察到牵拉下毛细血管的渗漏模式。当染料在囊腔中积聚时,需与假性晶状体眼CME鉴别(CME呈更花瓣状图案,伴有视盘强荧光)12)。FA/OCTA也有助于检测合并的视网膜血管闭塞、糖尿病视网膜病变、黄斑毛细血管扩张症和脉络膜新生血管12)。
EZ/IZ完整性与预后预测
Section titled “EZ/IZ完整性与预后预测”当术前OCT显示椭圆体带(EZ)和嵌合体带(IZ,视锥细胞外节尖端线)完整时,术后视力往往较好12)。外视网膜、EZ和光感受器外节长度在术后可以改善和正常化(各参数与视力改善相关)。一项使用时域OCT对101只眼的研究报告,光感受器层损伤是术后视力不良的预测因素12)。
与黄斑假孔的鉴别
Section titled “与黄斑假孔的鉴别”视网膜前膜的一种特殊类型是黄斑假孔。视网膜前膜的收缩导致中心凹凹陷呈圆柱状,呈现类似黄斑孔的表现。
临床鉴别点:黄斑假孔通常视力保持相对良好。裂隙灯检查中,Watzke-Allen征有助于鉴别:黄斑孔患者感觉裂隙光有中断(阳性),而黄斑假孔患者感觉裂隙光宽度均匀(阴性)。使用OCT可以轻松区分两者。
手术适应症判断标准
Section titled “手术适应症判断标准”视力障碍和视网膜增厚是手术适应症的前提。即使视力良好,如果视网膜增厚明显且视物变形严重,或合并全层黄斑孔,也需手术。
视力下降相对急性,且与白内障程度相比,视力障碍被认为主要由视网膜前膜引起,也是手术适应症。应具体询问症状进展速度、对患者职业和生活的影响(阅读困难、驾驶困难),最终根据患者的主观症状综合判断。手术是选择性的,非紧急12)。
OCT(光学相干断层扫描)是最重要的检查。它可以无创地显示视网膜表面的高反射膜状结构和视网膜增厚,用于诊断、手术适应症判断和术后随访。还可评估中心凹凹陷消失、椭圆体带状态和视网膜内囊样改变。术前EZ/IZ完整性对预测术后预后也有用12)。
5. 标准治疗方法
Section titled “5. 标准治疗方法”黄斑前膜治疗的标准术式是经睫状体扁平部玻璃体切除术(PPV)+ 黄斑前膜剥离 + ILM剥离。23G、25G、27G微切口玻璃体切除术(MIVS)是标准术式,可实现微创和早期恢复。
ILM剥离
染色剂的使用:亮蓝G(BBG,TISSUEBLUE®)已获FDA批准(2019年)用于ILM/ERM染色,并被广泛使用。ICG、台盼蓝和曲安奈德也被超说明书使用。低浓度被认为是安全的,但最小化光暴露时间很重要,争论仍在继续12)。周边玻璃体剃除(重点在套管附近)可降低医源性视网膜裂孔的风险。
- 视力改善率:约80%的病例获得Snellen 2行或以上的视力改善12)(既往报告为73%11))。10–20%视力不变或恶化。
- 视力改善程度:logMAR从0.4改善至0.1(术前术后比较)2)。
- 视物变形的改善:术前56%的患者有视物变形,术后降至13%11)。
- VFQ-25评分:术后6个月和24个月显著改善12)。
- 长期结果(Elhusseiny 2020,49眼,平均随访111个月):BCVA从术前0.56(20/72)改善至1年0.33(20/42)、3年0.25(20/35)、10年0.28(20/38),改善持续至3年,稳定维持至10年17)。
- 视力恢复过程:术后3–6个月视力逐渐改善,缓慢改善可能持续至术后12个月。术后1年仍可能存在视网膜增厚及相关的视功能损害。术后视力与术前视力密切相关,因此在视力明显下降前进行手术很重要。
ILM剥离的证据
Section titled “ILM剥离的证据”ILM剥离可有效预防ERM复发,现已纳入标准手术12)。
- 预防复发效果:未行ILM剥离时ERM复发率为8.6%~21%,行ILM剥离后为0%~2.6%12)。
- Ducloyer 2024 RCT(213眼):比较自然剥离101眼、主动ILM剥离51眼、未剥离49眼。复发率主动剥离组0% vs 未剥离组19.6%,差异显著。但主动ILM剥离组BCVA和微视野恢复略有延迟18)。
- 2017年荟萃分析:视力改善无明确差异,但ILM剥离组在抑制ERM复发方面更优19)。
- 结论:ILM剥离可有效预防复发,但对视力的优势不明确。可能出现内层视网膜缺损(DONFL),但功能影响未知。
VMT(玻璃体黄斑牵拉)的管理
Section titled “VMT(玻璃体黄斑牵拉)的管理”VMT(玻璃体黄斑牵拉)与ERM密切相关,常合并存在。
气体性玻璃体松解术(注气解除VMT):玻璃体内注入0.3ml C3F8,一项研究显示VMT解除率达85.7%,但DRCR Retina Network RCT报告视网膜裂孔和视网膜脱离发生率高于预期,因安全性问题提前终止12)。目前缺乏明确证据,需个体化评估风险与获益。
奥克纤溶酶(Ocriplasmin):重组蛋白酶。2012年FDA批准用于症状性VMA/VMT。III期试验显示VMA解除率27% vs 安慰剂10%(P<0.001)12)。对合并ERM的VMT效果有限(VMA解除率8.7% vs 安慰剂1.5%),对单纯ERM无效12)。副作用包括玻璃体漂浮物、闪光感、眼痛、视物模糊(约10%,第一周)。罕见严重副作用包括急性重度视力下降、ERG异常、色觉障碍,但大多可逆12)。
- 术后第1天复诊,术后1~2周再次检查(评估眼压、眼前节、中心视网膜、周边视网膜)12)。
- 若复视或双眼视困难持续存在:考虑转诊至斜视专科医生或视能训练师12)。
非手术治疗的报告
Section titled “非手术治疗的报告”标准治疗是手术,但以下非手术性自发或诱发脱离已有报告(均为病例报告级别)。
- 地塞米松玻璃体内植入剂(DEX植入剂):有报告称玻璃体内给药后观察到视网膜前膜自发脱离的病例7)。
- 抗VEGF+光动力疗法(PDT)后的自发脱离:有报告称光动力疗法后发生视网膜前膜自发脱离的病例4)。
这些仅为病例报告,目前并非标准治疗。
视力恢复在术后3~6个月内缓慢进行,有时可持续改善至术后12个月。术后1年仍可能残留视网膜增厚及伴随的视功能损害,因此长期随访很重要。长期结果显示,改善可持续至术后3年,稳定维持至术后10年 17)。术前视网膜变形程度和EZ完整性影响恢复预后。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”黄斑前膜的形成被理解为经过以下阶段的创伤愈合样反应 11)。
- PVD与残留玻璃体皮质:PVD时,部分玻璃体皮质残留在ILM上。
- ILM微小裂开(传统假说):残留玻璃体皮质的牵拉导致ILM产生微小裂口。
- 细胞迁移:视网膜胶质细胞(Müller细胞、星形胶质细胞)、RPE细胞和巨噬细胞通过ILM裂口迁移至玻璃体腔。
- 增殖与成纤维细胞分化:迁移的细胞增殖并分化为成纤维细胞样收缩细胞,形成黄斑前膜。
玻璃体细胞(hyalocyte)的作用
Section titled “玻璃体细胞(hyalocyte)的作用”作为特发性ERM的主要细胞成分,层状细胞(来源于后玻璃体膜的玻璃体细胞) 受到关注 12)。玻璃体细胞起源于骨髓来源细胞,并持续更新。胶质细胞和玻璃体细胞分化为成纤维细胞/肌成纤维细胞,导致细胞外基质形成和纤维化,从而形成ERM。ERM的组成多样,起源和原因也有多种。
在不需要ILM裂开的新假说中,ILM上残留玻璃体皮质中的玻璃体细胞被激活为肌成纤维细胞,直接形成并收缩ERM 12)。
病理组织学机制
Section titled “病理组织学机制”特发性病例中,玻璃体皮质内成纤维细胞、肌成纤维细胞、胶质细胞、巨噬细胞、炎症细胞、玻璃体细胞和视网膜色素上皮细胞等的增殖,加上细胞外基质的变化,形成膜组织。
继发性病例中,血-视网膜屏障破坏释放细胞因子,导致视网膜色素上皮细胞和胶质细胞在玻璃体皮质或内界膜上增殖形成膜。
对血管的影响:黄斑前膜的牵引导致中心凹无血管区(FAZ)面积缩小,表层毛细血管丛(SCP)的血管面积密度(VAD)显著升高2)。FAZ面积与最佳矫正视力(BCVA)之间存在显著负相关(r = −0.683)2),FAZ形态是视功能的重要指标。
在NF2相关的黄斑前膜中,肿瘤抑制基因功能丧失导致Müller细胞样胶质成分异常增殖,形成黄斑前膜。免疫染色显示GFAP弱阳性、巢蛋白中度阳性的模式9)。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”ILM剥离RCT(Ducloyer 2024)
Section titled “ILM剥离RCT(Ducloyer 2024)”Ducloyer等人(2024)对213只眼进行的RCT(自然剥离101眼、主动ILM剥离51眼、非剥离49眼)显示,复发率在主动剥离组为0%,非剥离组为19.6%,差异显著18)。但主动ILM剥离组术后BCVA和微视野恢复略有延迟。关于预防复发与视功能恢复之间的权衡,需要进一步评估长期结果。
长期手术结果(Elhusseiny 2020)
Section titled “长期手术结果(Elhusseiny 2020)”Elhusseiny等人(2020)对49只眼平均随访111个月(约9.3年)的报告显示,BCVA从术前0.56改善至1年0.33、3年0.25、10年0.28,术后3年内持续改善并稳定至10年17)。从长期维持视功能的角度支持早期手术干预。
OCTA评估术前术后血管血流
Section titled “OCTA评估术前术后血管血流”Frisina等人(2023)通过OCTA证实,特发性黄斑前膜眼的FAZ面积缩小至健康眼的一半左右(0.11 mm² vs 0.24 mm²),SCP的VAD显著升高2)。他们还报告了FAZ面积与BCVA之间的显著负相关(r = −0.683),表明OCTA是一种有前景的术前预后预测工具。logMAR视力术后从0.4显著改善至0.1。
利用en face OCT术前预测ILM缺损
Section titled “利用en face OCT术前预测ILM缺损”Sasajima 和 Zako(2023)报告,术前 en face OCT 在 22.7% 的病例中发现 ILM 缺损,从 ILM 缺损边缘进行剥离的技术(defect-edge technique)安全有效 1)。术前确定缺损部位有望提高手术计划的准确性。
AI 诊断的前景
Section titled “AI 诊断的前景”基于眼底照片或检眼镜检查的 AI 诊断 ERM 正处于评估阶段 12)。有人指出其在价格和可及性方面具有优势,有望用于筛查。但诊断准确性的验证仍在进行中,OCT 仍然是 ERM 诊断的事实标准。
黄斑前膜诱发的视网膜内新生血管
Section titled “黄斑前膜诱发的视网膜内新生血管”Giachos 等人(2021)报告了一例无糖尿病患者因黄斑前膜牵引诱发视网膜内新生血管的病例 6)。OCTA 可以详细评估血管,并确认黄斑前膜手术后新生血管消退。
BBG 染色剂的安全性方案
Section titled “BBG 染色剂的安全性方案”Venkatesh 等人(2022)报告了一例因 BBG 与内照明光组合导致黄斑损伤的病例 10),强调了使用 BBG 时限制曝光时间和适当光量管理的重要性。建立安全的染色方案是未来的课题。
PAMM 样并发症的认识与预防
Section titled “PAMM 样并发症的认识与预防”Koiwa 等人(2024)报告了一例黄斑前膜玻璃体手术后出现 PAMM 样旁中心凹视网膜缺血的病例 5),指出术前血流评估和术中眼压管理对预防并发症很重要。
8. 参考文献
Section titled “8. 参考文献”- Sasajima H, Zako M. Internal limiting membrane peeling technique from internal limiting membrane defect edge. Clin Case Rep. 2023;11(5):e7279. doi:10.1002/ccr3.7279. PMID: 37155426.
- Frisina R, De Salvo G, Tozzi L, et al. Effects of physiological fluctuations on the estimation of vascular flow in eyes with idiopathic macular pucker. Eye (Lond). 2023;37(7):1470-1478. doi:10.1038/s41433-022-02158-4. PMID: 35794376.
- Mashayekhi A, Shields CL, Shields JA, et al. Malignant epiretinal membrane after proton beam radiation. J Ophthalmic Vis Res. 2023;18(4):445-451. doi:10.18502/jovr.v18i4.14558.
- Munoz-Solano J, Preziosa C, Staurenghi G, Pellegrini M. Resolution of epiretinal membrane after anti-VEGF and photodynamic therapy of retinal hemangioblastoma. Am J Ophthalmol Case Rep. 2024;33:101994. doi:10.1016/j.ajoc.2024.101994. PMID: 38303898. PMCID: PMC10831802.
- Koiwa C, Chi P, Yamamoto S, Nakao S. Extramacular paracentral acute middle maculopathy-like retinal ischemia after vitrectomy for epiretinal membrane. Am J Ophthalmol Case Rep. 2024;36:102221. doi:10.1016/j.ajoc.2024.102221. PMID: 39634097. PMCID: PMC11615521.
- Giachos I, et al. ERM-induced intraretinal neovascularization. Am J Ophthalmol Case Rep. 2021;23:101180.
- Alshahrani ST, Al Zoba A, Uwaydah Z. Epiretinal membrane separation following dexamethasone intravitreal implant in diabetic macular edema: a case report. Ophthalmol Ther. 2022;11(2):737-742. doi:10.1007/s40123-022-00472-4. PMID: 35362248.
- Rivera-Valdivia N, et al. RPE atrophy after ERM/ILM peeling. Rom J Ophthalmol. 2022;66(1):79-83.
- Kunikata H, Nishiguchi KM, Watanabe M, Nakazawa T. Surgical outcome and pathological findings in macular epiretinal membrane caused by neurofibromatosis type 2. Digit J Ophthalmol. 2022;28(1):12-16. doi:10.5693/djo.02.2021.06.001. PMID: 35573141.
- Venkatesh R, Yadav NK, Pereira A, et al. Phototoxic maculopathy following brilliant blue G-assisted internal limiting membrane peeling. J Curr Ophthalmol. 2022;34(2):267-270. doi:10.4103/joco.joco_46_22.
- Flaxel CJ, Adelman RA, Bailey ST, et al. Idiopathic Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. Ophthalmology. 2020;127(2):P145-P183.
- Bailey ST, Vemulakonda GA, et al. Idiopathic Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. Ophthalmology. 2025;132(2):P203-P237.
- Xiao W, Chen X, Yan W, et al. Prevalence and risk factors of epiretinal membranes: a systematic review and meta-analysis of population-based studies. BMJ Open. 2017;7:e014644. doi:10.1136/bmjopen-2016-014644. PMID: 28951399.
- Fraser-Bell S, Guzowski M, Rochtchina E, et al. Five-year cumulative incidence and progression of epiretinal membranes: the Blue Mountains Eye Study. Ophthalmology. 2003;110(1):34-40. PMID: 12511343.
- Meuer SM, Myers CE, Klein BE, et al. The epidemiology of vitreoretinal interface abnormalities as detected by spectral-domain optical coherence tomography: the Beaver Dam Eye Study. Ophthalmology. 2015;122(4):787-795.
- Ng CH, Cheung N, Wang JJ, et al. Prevalence and risk factors for epiretinal membranes in a multi-ethnic United States population. Ophthalmology. 2011;118(4):694-699. doi:10.1016/j.ophtha.2010.08.009.
- Elhusseiny AM, Smiddy WE, Flynn HW Jr, et al. Long-term visual and anatomical outcomes after epiretinal membrane peeling. Retina. 2020;40(10):1952-1959. doi:10.1097/IAE.0000000000002705. PMID: 31764264.
- Ducloyer JB, et al. Pros and cons of internal limiting membrane peeling during epiretinal membrane surgery: a randomised clinical trial with microperimetry (PEELING). Br J Ophthalmol. 2024. doi:10.1136/bjo-2023-324990. PMID: 38901960.
- Chang WC, Lin C, Lee CH, et al. Vitrectomy with or without internal limiting membrane peeling for idiopathic epiretinal membrane: a meta-analysis. PLoS One. 2017;12(6):e0179105. doi:10.1371/journal.pone.0179105. PMID: 28622372. PMCID: PMC5476241.
