帐篷状脱离
形成机制:当牵拉发生在新生血管根部(epicenter)或沿视网膜血管时形成。
特征:脱离区域呈反拱形(帐篷状)。无活动性,脱离高度通常局限。典型于PDR早期至中期。

牵拉性视网膜脱离(TRD)是在后玻璃体脱离不完全的状态下,玻璃体对视网膜产生强烈牵拉力而发生的视网膜脱离。它是由视网膜上的增殖性组织或玻璃体牵拉引起的非孔源性视网膜脱离,脱离范围常为局限性,呈扁平或帐篷状,特征为几乎无活动性。
TRD根据原因大致分为以下两类。
纤维血管膜(包括新生血管)牵引:代表性疾病为增殖性糖尿病视网膜病变(PDR)、视网膜静脉阻塞(RVO)和早产儿视网膜病变(ROP)。以眼内缺血引起的新生血管形成为基础,纤维血管膜的收缩产生牵引力。
无新生血管的玻璃体视网膜牵引:代表性疾病为黄斑玻璃体牵引综合征和穿孔性眼外伤。以炎症或外伤后的增殖为基础。
视网膜脱离一般分为孔源性、牵拉性和渗出性三种类型。牵拉性脱离表现为无活动性的局限性脱离,临床上与呈泡状、有活动性的孔源性脱离和渗出性脱离相区别。部分病例合并视网膜裂孔,称为合并牵拉性-孔源性视网膜脱离(combined tractional-rhegmatogenous RD)。合并RD是更紧急的病变,其处理与单纯牵拉性不同。
增殖性玻璃体视网膜病变(PVR)是孔源性视网膜脱离术后继发的增殖过程,也可成为TRD的原因之一。
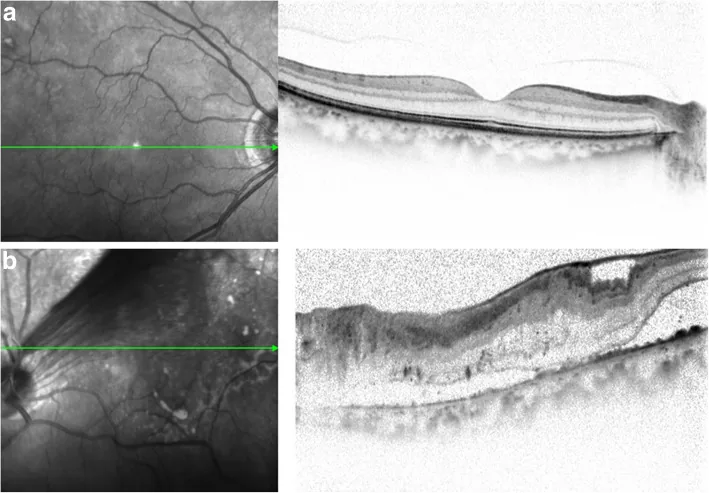
TRD的自觉症状因脱离的部位和范围而异。
糖尿病视网膜病变(DR)相关的牵拉性视网膜脱离(TRD)常合并玻璃体出血,可能导致视力突然下降1)。
TRD的特征性形态表现如下。
帐篷状脱离
形成机制:当牵拉发生在新生血管根部(epicenter)或沿视网膜血管时形成。
特征:脱离区域呈反拱形(帐篷状)。无活动性,脱离高度通常局限。典型于PDR早期至中期。
桌面状脱离
形成机制:当纤维血管膜与视网膜广泛粘连时形成。也称为富士山型。
特征:形成宽广平坦的脱离面。无活动性,若覆盖整个黄斑区,视力预后不良。
活动性评估:牵拉性RD无活动性是重要表现。若脱离呈圆顶状或有活动性,需考虑合并孔源性RD(combined RD)。
纤维血管膜的存在:PDR来源的TRD可见眼底新生血管与纤维组织融合形成的膜结构。膜的活动性(血管成分丰富程度、出血倾向)影响手术难度。
合并玻璃体出血:增殖性糖尿病视网膜病变中,纤维血管膜出血可能遮挡视野。此时眼底观察困难,需行B型超声检查。
牵拉性视网膜劈裂:增殖性糖尿病视网膜病变等导致视网膜表面强烈牵拉时,视网膜内层与外层可分离,表现为视网膜劈裂。表面形态呈帐篷状,OCT有助于诊断。
TRD由以下原因疾病引起。
1. 增殖性糖尿病视网膜病变(PDR):TRD中最常见的原因疾病。作为视网膜缺血的代偿,形成新生血管,纤维血管膜在视网膜上增殖和收缩,导致TRD。糖尿病视网膜病变诊疗指南(第1版)明确指出牵拉性视网膜脱离是PDR的严重并发症之一1)。
2. 早产儿视网膜病变(ROP):在第4期(部分TRD)和第5期(全TRD)发生TRD4)。在视网膜血管未发育的无血管区的未成熟视网膜上,出生后的高氧环境引起相对缺血,形成新生血管。
3. 穿孔性眼外伤:眼球穿孔创的炎症细胞浸润和血-视网膜屏障(BRB)破坏导致眼内增殖,形成增殖膜并产生牵拉。
4. 增殖性玻璃体视网膜病变(PVR):孔源性视网膜脱离术后继发的增殖增加了牵拉成分,可能导致类似TRD的病理状态。
5. 视网膜静脉阻塞(RVO):伴有新生血管形成的重症病例中,可能通过类似PDR的机制发生TRD。
6. 其他:Eales病(特发性周边静脉周围炎)、镰状细胞病、Coats病的一部分也可能发生TRD。
下表总结了各原因疾病和风险因素。
| 风险因素 | 相关疾病 |
|---|---|
| 糖尿病病程、血糖控制不良 | PDR |
| 低出生体重、早产(胎龄<32周) | ROP |
| 穿孔性眼外伤 | 外伤后TRD |
| 孔源性视网膜脱离手术史 | PVR |
| 全视网膜光凝未进行或不完全 | PDR |
| 视网膜静脉阻塞 | 缺血型RVO引起的TRD |
关于早产儿视网膜病变的抗VEGF治疗,可参考日本早产儿视网膜病变研究会的指南7)。
使用间接检眼镜或裂隙灯显微镜(前置镜)进行眼底观察是诊断TRD的基础。
OCT对诊断牵拉性视网膜劈裂特别有效。它可以在断层图像上显示由牵拉形成的帐篷状表面形态。可以定量评估黄斑部牵拉程度、视网膜内层与外层的分离以及脱离向黄斑进展的情况。
当玻璃体出血或严重白内障导致无法观察眼底时,这是必需的检查。可以评估视网膜脱离的有无、范围、形态和牵拉程度。增殖膜有时表现为高回声。
FA有助于评估新生血管活动性和检测无灌注区(NPA)1)。在PDR相关的TRD中,术前了解无灌注区的范围有助于规划术中光凝治疗。
以下总结了与TRD相似的疾病的鉴别诊断。
| 鉴别诊断 | 特征 | 可动性 | 形态 |
|---|---|---|---|
| 孔源性RD | 有裂孔 | 有 | 泡状 |
| 牵拉性RD | 有增殖膜 | 无 | 帐篷状或桌面状 |
| 渗出性RD | 无裂孔或增殖膜 | 无至轻度 | 光滑的圆顶状 |
| 混合性TRD-RRD | 裂孔+增殖膜 | 有 | 帐篷状与大泡状混合 |
TRD的手术适应证如下所示。
| 病态 | 方针 |
|---|---|
| 威胁黄斑部的牵拉性视网膜脱离 | 手术适应证1, 2) |
| 合并裂孔的牵拉性视网膜脱离(合并RD) | 手术适应证(更紧急)1, 2) |
| 可能导致黄斑移位的增殖膜 | 考虑手术1) |
| 黄斑部外的局限性TRD(无进展) | 可观察 |
对于黄斑部外的局限性TRD,如果脱离范围无扩大且无黄斑移位,可通过定期眼底检查和OCT检查进行监测观察。但若发现进展征象,应尽早考虑手术1)。
TRD的根本治疗是通过玻璃体手术解除牵拉。近年来,25G和27G微切口玻璃体手术(MIVS)已成为主流,在广角观察系统下进行手术是标准做法1)。
手术的基本步骤如下。
术前玻璃体内注射抗VEGF可能有助于减少术中出血、医源性裂孔和手术时间3)。在PDR伴TRD且纤维血管膜活动性高时考虑使用。
早产儿视网膜病变相关牵拉性视网膜脱离的手术方案因分期而异4)。
抗VEGF治疗可作为重症ROP的一线治疗7),但对于4-5期TRD,玻璃体手术是原则。
如果没有向黄斑进展的风险,可以观察。但如果出现脱离范围扩大或可能导致黄斑移位的增殖膜,应考虑早期手术。定期眼底检查和OCT监测进展很重要。
增殖性糖尿病视网膜病变引起的TRD通过以下阶段发生。
PDR源性TRD的病理
缺血→VEGF→新生血管的连锁反应是基础。
纤维血管膜的收缩对视网膜产生牵引力,导致TRD。血-视网膜屏障(BRB)破坏导致的细胞因子渗漏促进增殖。
ROP源性TRD的病理
视网膜血管未成熟→无血管区→缺血→新生血管是基础。
出生后的高氧环境导致相对缺血,嵴上的纤维血管增殖向玻璃体内进展,导致4-5期TRD。
TRD的基础是血-视网膜屏障(BRB)的破坏。当BRB被破坏时,眼内炎症和新生血管环境增强,纤维血管增殖进展。RPE、胶质细胞、巨噬细胞、成纤维细胞等参与增殖膜的形成9)。
增殖膜不仅涉及RPE,还复杂地涉及胶质细胞、巨噬细胞、成纤维细胞等。胶原蛋白的收缩导致对视网膜的牵引,从而引发TRD。
在穿孔性眼外伤后的TRD中,由于穿孔创口的炎症细胞浸润和BRB破坏,眼内增殖进展。成纤维细胞和RPE的增殖形成增殖膜,该膜收缩产生牵引,导致TRD。
评估早期玻璃体手术治疗糖尿病性重度玻璃体出血有效性的DRVS(Diabetic Retinopathy Vitrectomy Study)为TRD管理提供了基础证据。在1型糖尿病的重度玻璃体出血中,早期玻璃体手术组2年后矫正视力达到20/40或以上的比例为25%(观察组15%),在1型糖尿病中为36% vs 12%,显示出显著差异5)。2型糖尿病中未观察到显著差异5)。
在比较阿柏西普玻璃体内注射与玻璃体手术联合全视网膜光凝(PRP)治疗糖尿病性玻璃体出血的试验中,24周时视力改善无显著差异。但玻璃体出血的消退在手术组更快(4周 vs 36周)2)。
评估术前抗VEGF给药有效性的荟萃分析报告了术中出血量和医源性裂孔的减少3)。但有人指出抗VEGF注射后牵引可能暂时加重,建议注射后1-2周内早期手术2)。
随着25G和27G系统以及广角观察系统的普及,PDR源性TRD的微创玻璃体手术适应症已扩大1)。小切口技术有助于减少术后炎症和早期恢复,其在门诊手术中的应用正在增加8, 9)。
在DRCR Protocol S中,抗VEGF(雷珠单抗)在2年时显示出对PRP的非劣效性2)。然而,进展为TRD的比率没有显著差异,且已存在TRD时无法单独使用抗VEGF处理。抗VEGF在预防TRD方面可考虑,但TRD发生后,玻璃体手术是根本治疗。
通常不能期望仅靠抗VEGF注射改善TRD。抗VEGF对新生血管消退有效,但无法控制现有纤维增殖膜的收缩,甚至有报告称注射后牵拉加重2)。TRD的治疗原则是玻璃体手术。术前辅助使用抗VEGF可能有用,有研究表明可减少术中出血和医源性裂孔3)。