激光光凝

早产儿视网膜病变
1. 什么是早产儿视网膜病变?
Section titled “1. 什么是早产儿视网膜病变?”早产儿视网膜病变(ROP)是发育中的视网膜血管发生的增殖性疾病。
视网膜血管从胎龄约14周开始从视盘发生,向眼底前方生长。浅层血管在胎龄30周、深层血管在胎龄38~40周到达最周边部,完成生长。存在个体差异,颞侧比鼻侧距视盘更远,因此到达最周边部较晚,容易发生ROP。
早产儿出生时周边视网膜存在无血管区。发育中的血管在从稳定的母体环境突然变化时,在最不成熟的细胞所在的生长前端停止生长,并向异常方向增殖。无血管区释放VEGF(血管内皮生长因子)是其机制。
增殖进展的时期称为活动期,血管成分消退、留下纤维结缔组织和视网膜牵引或变性等后遗症的稳定状态称为瘢痕期。
ROP的发生频率和严重程度与视网膜血管生长的不成熟程度成正比。胎龄和出生体重越小,发病率越高,越容易加重。高浓度氧是加重ROP的最大诱因,此外呼吸窘迫综合征、换血、败血症、脑室内出血、手术史、营养和水分给予不平衡等也复杂相关。
1942年Terry首次报告,1967年永田进行了世界上首次光凝治疗,并发展为标准治疗。早产儿视网膜病变历史上曾发生三次流行1):第一次流行(1940-50年代)由保育箱内高浓度氧气引起,第二次流行(1970-80年代)伴随超低出生体重儿存活率的提高,第三次流行目前正在进行,发生在医疗资源有限的中低收入国家1)。ROP在儿童失明原因中所占比例1990年约为10%,现已上升至30%。全球每年约有184,700例早产儿发生ROP,约20,000名儿童失明或严重视力障碍1)。出生体重低于1,000克的超低出生体重儿中,86.1%发生ROP,需要治疗的病例达41%。美国ROP发病率从2004年的4.4%增加到2019年的8.1%1)。
发病率的大致情况如下。
| 对象组 | 发病率 |
|---|---|
| 超低出生体重儿(<1,000 g),日本 | 86.1% |
| 胎龄≤27周,美国 | 89.0% |
| 胎龄27-31周,美国 | 51.7% |
| 胎龄≥32周,美国 | 14.2% |
| 所有出生(总体),美国 | 0.12% |
主要风险因素如下所示1)。
| 风险因素 | 内容 |
|---|---|
| 胎龄小于32周 | 最重要的风险因素之一 |
| 出生体重小于1.5公斤 | 最重要的风险因素之一 |
| 高浓度、长期氧疗 | 发病的主要诱因 |
| 多胎妊娠 | 导致低出生体重 |
| 新生儿呼吸窘迫综合征(NRDS) | 需要呼吸管理的重症病例 |
| 败血症、脑室内出血 | 全身炎症、循环障碍 |
| 出生后体重增长延迟 | 与IGF-1水平低相关 |
| 输血/促红细胞生成素给药 | 氧输送能力变化 |
胎龄越短、出生体重越低,发病风险越高。尤其是胎龄小于32周、出生体重低于1500克的早产儿是主要风险人群。出生后高浓度氧疗等环境因素也与发病有关。多种危险因素叠加时容易重症化。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”早产儿视网膜病变的急性期发生在新生儿期和婴儿期,因此患儿本人无法诉说症状。家长或医护人员可能会注意到以下表现。
- 白色瞳孔(白瞳症):在进展期(4~5期),发生视网膜脱离时瞳孔呈白色。
- 斜视:反映视力不良或双眼视功能失衡。
- 眼球震颤:伴有严重视力障碍时出现。
临床所见和分期
Section titled “临床所见和分期”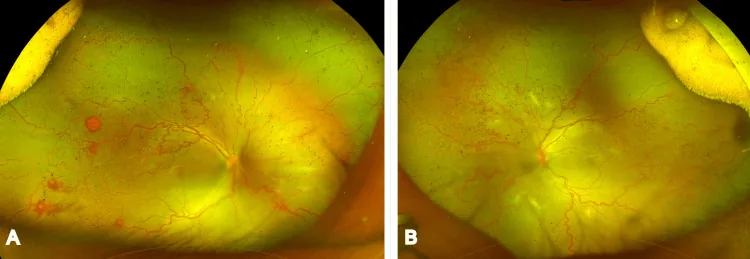
在日本,1975年制定了厚生省分类,并于1983年修订。将ROP分为逐步进展的I型(经典ROP)和快速导致视网膜脱离的暴发型II型。国际分类(ICROP)在2005年修订时全面采纳了厚生省分类的概念,内容基本相同。最新的ICROP第3版(ICROP3)于2021年发布2)。
厚生省分类与ICROP3的对应
| 厚生省分类 | 国际分类(ICROP3) |
|---|---|
| I型1期:视网膜内新生血管 | 第1期:分界线(demarcation line) |
| I型2期:分界线形成 | 第2期:嵴(ridge) |
| I型3期:玻璃体内渗出和增殖(早期/中期/晚期) | 第3期:视网膜外纤维血管增殖(轻度/中度/重度) |
| 4期:部分视网膜脱离 4A/4B | 第4期:部分视网膜脱离(4A黄斑外,4B累及黄斑) |
| 5期:全视网膜脱离 | 第5期:全视网膜脱离 |
| II型:暴发型 | A-ROP(旧称AP-ROP) |
| Plus disease(重症体征) | Plus disease |
病变发生部位用I~III区表示。I区是以视乳头为中心,以视乳头与黄斑中心凹距离的两倍为半径的圆内侧范围,相当于将+25 D或+28 D观察镜的边缘置于视乳头对侧缘时可见的范围。II区是I区外侧,以视乳头到鼻侧锯齿缘为半径的圆内侧范围。III区是II区外侧的颞侧新月形范围。病变越靠后(I区),严重程度越高。ICROP3增加了后II区(从I区边界起2个视乳头直径的带状区域)的概念2)。
第1期(分界线):在血管生长前端视网膜内形成白色分界线。
第2期(嵴):前卫区域的毯型间叶细胞增殖增厚,分界线向玻璃体腔突出形成嵴。
第3期(视网膜外纤维血管增殖):血管簇融合成弧形,玻璃体内新生血管形成血管腔,周围产生胶原等结缔组织。根据表现程度分为轻度、中度和重度。ICROP3将不伴嵴的平坦视网膜外新生血管概念纳入第3期2)。
第4期(部分视网膜脱离):纤维血管增殖内的结缔组织收缩牵拉视网膜,导致部分视网膜脱离。分为4A(未累及黄斑)和4B(累及黄斑)。
第5期(全视网膜脱离):纤维血管增殖广泛且强烈收缩,导致视网膜全脱离。ICROP3将第5期分为以下三个亚型2)。
| 亚型 | 特征 |
|---|---|
| 5A | 检眼镜下可见视乳头(开放漏斗状脱离) |
| 5B | 晶状体后纤维血管组织或闭合漏斗,视乳头不可见 |
| 5C | 5B + 前节异常(前房变浅、虹膜-角膜-晶状体粘连、角膜混浊) |
Plus disease 和 pre-plus disease
Section titled “Plus disease 和 pre-plus disease”在1~3期,当后方2个象限以上出现视网膜静脉扩张和动脉迂曲时,定义为plus disease。在ICROP3中,plus disease被修订为从正常经pre-plus到plus的连续谱系2)。plus disease的评估在I区内血管进行。
A-ROP(侵袭性ROP)
Section titled “A-ROP(侵袭性ROP)”在ICROP3中,以往的AP-ROP(侵袭性后部ROP)更名为A-ROP。这是因为定义扩展至包括非后部发病、较大早产儿以及资源有限地区的发病2)。
A-ROP的特征如下:发生于后部(多为I区,也包括后部II区),plus disease显著,形成全周性分流。有血管与无血管边界不清,玻璃体内新生血管呈扁平半透明状,难以识别。不表现为通常的1期至3期逐步进展,未经治疗则迅速进展至5期。包括后极在内的广泛毛细血管网缺失,广泛的VEGF释放是快速进展的基础。
如果早期病变的视网膜血管尖端出现分流或视网膜内出血,应立即进行光凝治疗。
瘢痕期分类(厚生省)
Section titled “瘢痕期分类(厚生省)”活动期消退后,瘢痕期分类如下。
- 1度:仅周边改变。眼底后极无明显异常,视力通常正常。
- 2度(轻度):轻度视乳头牵引。黄斑部无改变。
- 2度(中度):明显视乳头牵引。黄斑部外偏。
- 2度(重度):视乳头牵引。黄斑部器质性改变。
- 3度:后极部束状视网膜脱离(视网膜皱襞)。
- 4度:瞳孔区部分可见后部晶状体纤维增殖。
- 5度:完全后部晶状体纤维增殖。
3. 原因与风险因素
Section titled “3. 原因与风险因素”早产儿视网膜病变的发生涉及未成熟的视网膜血管系统与出生后氧环境及全身状态的相互作用。高浓度氧气是加重ROP的最大诱因,此外,呼吸窘迫综合征、换血、败血症、脑室内出血、手术史、营养和水分失衡等也复杂地参与其中。
| 风险因素 | 内容 |
|---|---|
| 胎龄 | <32周为高风险 |
| 出生体重 | <1,500 g为高风险 |
| 氧疗 | 高浓度、长期使用 |
| IGF-1低水平 | 出生后营养不良和疾病1) |
| 败血症、贫血、输血 | 全身状况恶化 |
| 呼吸窘迫综合征 | 需要呼吸管理的重症患儿 |
| 多胎出生 | 较小的双胞胎中晚期ROP更常见1) |
| 出生后体重增长不良 | WINROP/G-ROP算法的依据1) |
IGF-1(胰岛素样生长因子-1)是视网膜血管发育必需的信号因子,早产后低IGF-1状态促进血管生长停滞1)。
4. 病理生理学
Section titled “4. 病理生理学”视网膜血管发育与两阶段疾病模型
Section titled “视网膜血管发育与两阶段疾病模型”视网膜血管发育始于胎龄约14周,出生前到达最周边区域并完成。浅层血管在30周时到达,深层血管在38-40周时到达。早产儿出生时周边视网膜残留无血管区域。
ROP的病理生理学分为两个阶段来解释1)。
第一阶段(血管发育停滞期):早产儿的未成熟视网膜暴露于高氧环境(子宫外)时,通过氧传感器抑制VEGF和IGF-1。这导致正常视网膜血管发育停止,形成无血管区。
第二阶段(血管增殖期):随着无血管视网膜代谢成熟,为补偿缺血状态,VEGF过度产生。这种VEGF过量诱导血管内皮异常增殖,导致纤维血管增殖组织进入玻璃体腔(3期及以上)。
新生血管沿着玻璃体腔内有形玻璃体的纤维生长,并在周围产生胶原等结缔组织。当这些结缔组织收缩并牵拉与之粘连的视网膜时,就会发生视网膜脱离,导致严重的视力障碍或失明。
在A-ROP中,存在包括后极部在内的广泛毛细血管网缺失,VEGF从包括后极部在内的广泛区域释放,因此病情进展迅速。
IGF-1(胰岛素样生长因子-1)对视网膜血管和神经的协调发育至关重要,低IGF-1状态会延迟正常血管发育,增加ROP易感性1)。出生后体重增长延迟也与低IGF-1相关,是危险因素1)。
挤压综合征(crunch syndrome):抗VEGF治疗后,VEGF被抑制,TGF-β(促纤维化因子)相对升高,导致VEGF-TGF-β平衡失调,引起纤维血管膜快速收缩。这有加重牵拉性视网膜脱离的风险1)。
5. 筛查与诊断
Section titled “5. 筛查与诊断”筛查标准与首次检查时机
Section titled “筛查标准与首次检查时机”NICU中的筛查对象为胎龄小于34周或出生体重≤1800克的婴儿。此外,接受氧疗、机械通气、输血、患有败血症、脑室内出血、严重呼吸或循环障碍、全身麻醉手术或胎儿水肿的婴儿被视为高危人群,即使不符合上述标准也需进行眼底检查。
首次检查时机如下:
| 出生时胎龄 | 首次检查时机 |
|---|---|
| 小于26周 | 从矫正胎龄29周开始 |
| 26周及以上 | 从出生后3周开始 |
治疗适应证(1型ROP)
Section titled “治疗适应证(1型ROP)”治疗适应症基于ETROP研究中1型ROP的标准1)。符合以下任一情况时,建议在诊断后72小时内进行治疗。
- ① 伴有plus病变的I区所有ROP
- ② 不伴有plus病变的I区3期ROP
- ③ 伴有plus病变的II区3期ROP
- ④ A-ROP(尽快进行)
以上情况之外均视为2型ROP进行随访。伴有plus病变的II区2期ROP根据所用药物处理方式不同(RAINBOW试验中排除,但FIREFLEYE试验中纳入)3)。
根据检查结果推荐的检查间隔如下所示1)。
| 所见 | 下次检查间隔 |
|---|---|
| I区未成熟血管或1-2期、后极部II区未成熟血管、疑似A-ROP | 每周1次 |
| 后极部II区未成熟视网膜、II区2期、I区消退期 | 1-2周 |
| I区1期、II区未成熟血管(无ROP)、II区消退期 | 2周 |
| III区1-2期、III区退行期 | 2-3周 |
筛查终止标准为完全血管化至III区,或矫正胎龄45周时无1型ROP。抗VEGF治疗后需至少观察到矫正胎龄65周1)。
使用美多丽®P或新福林®·美多丽®P·赛普乐®按2:1:1比例混合的滴眼液(改良Capto滴眼法),在检查开始前1小时起每10分钟滴眼1次,共3次进行散瞳。
诊断与评估辅助技术
Section titled “诊断与评估辅助技术”- 广角眼底相机(RetCam等):可在散瞳下进行广范围眼底摄影。也用于远程读片。
- AI图像诊断:自动检测Plus病已达到与眼科专家同等或更高的准确率1)。基于深度学习模型的血管严重程度评分(VSS)已被开发为Plus病诊断的客观指标1)。
- 预测模型(G-ROP、WINROP):基于胎龄、出生体重和出生后体重增长,预测1型ROP的灵敏度达到100%1)。
- FIRST-ROP算法:对于中等风险婴儿(胎龄≥27周且出生体重≥800克),有建议可将筛查开始时间推迟至矫正胎龄34周1)。
- 荧光眼底血管造影:有助于评估复发的有无和范围。有望用于PAR评估3)。
胎龄不足26周的婴儿从矫正胎龄29周开始首次检查;胎龄26周及以上的婴儿从出生后3周开始首次检查。之后根据发现每1-3周重复一次。抗VEGF治疗后建议至少观察到矫正胎龄65周3)。当视网膜血管化完成且无需要治疗的发现时,检查结束。
取决于出生时的胎龄。出生胎龄不足26周的,从矫正胎龄29周开始首次眼底检查;出生胎龄26周及以上的,从出生后3周开始首次眼底检查。筛查对象为出生胎龄不足34周或出生体重≤1800g的婴儿,但即使不符合上述标准,如果存在氧疗、输血、败血症等危险因素,也需要进行检查。
6. 标准治疗方法
Section titled “6. 标准治疗方法”抗VEGF玻璃体内注射
适应症:优先选择用于I区和A-ROP
国内批准药物:雷珠单抗0.2 mg,阿柏西普0.4 mg
优点:即使后极部重症病例也易于实施,治疗时间短,患儿负担小
注意事项:复发风险高,必须长期随访
玻璃体手术
适应证:4期及以上的视网膜脱离
术式:经典ROP首选晶状体保留玻璃体手术(LSV)
结果:4A期复位率74%~91%,4B期62%~92%,5期22%~48%1)
巩膜扣带术
自1967年永田实施世界首例光凝治疗以来,光凝已成为ROP的标准治疗。基本方法是在间接检眼镜下对整个无血管区进行光凝。在明显的晶状体血管膜或瞳孔强直时可能难以实施。该操作耗时且需要术者熟练,广泛光凝可能导致视野缩小和近视。
CRYO-ROP试验显示,1年时不良结构结局在冷冻组为25.7%,观察组为47.4%,15年后差异仍显著(30% vs 52%)8)。ETROP试验显示早期治疗使不良结构结局从15.6%降至9.1%9)。
抗VEGF治疗
Section titled “抗VEGF治疗”由于VEGF参与视网膜新生血管形成,抗VEGF药物的玻璃体内注射已被尝试用于ROP。截至2022年12月,日本国内批准用于ROP治疗的抗VEGF药物有以下两种3)。
- 雷珠单抗(Lucentis®):0.2 mg/次(0.02 mL)。2019年11月在日本获批。
- 阿柏西普(Eylea®):0.4 mg/次(0.01 mL)。2022年9月在日本获批。
两者均仅以瓶装制剂获批用于ROP,根据说明书,再给药间隔至少为1个月3)。贝伐珠单抗在日本国内外均未获批用于ROP3)。
主要临床试验结果
| 试验名称 | 对象/药物 | 主要结果 |
|---|---|---|
| BEAT-ROP | I区3期+,贝伐珠单抗0.625 mg | I区复发率6%对比激光42%5, 1) |
| RAINBOW | 出生体重<1,500 g,雷珠单抗0.2 mg | 治疗成功率80.0%对比激光66.2%。2岁时高度近视5%对比20%6, 1) |
| FIREFLEYE | 胎龄≤32周或体重<1,500 g,阿柏西普0.4 mg | 成功率82.7%对比激光84.2%。全身麻醉率44.0%对比65.8%7, 1) |
复发率比较3):
- 阿柏西普:复发率13.9%
28%,平均复发时间1114.2周 - 雷珠单抗:复发率20.8%~83.0%,复发时间5.9~9.3周(复发更早)
雷珠单抗注射后14天血中VEGF下降已检测不到,认为全身影响较小。阿柏西普注射后约8周血浆中游离型阿柏西普降至定量下限以下3)。
儿童特有的注射技术3):
- 在角膜缘后方1.0~1.5 mm处进针(注意与成人的3~4 mm不同)
- 由于晶状体相对较大,应向下(后方)进针。朝向眼球中央方向有损伤晶状体的风险
- 使用30G或更细的注射针
- 在NICU保温箱或手术室中进行
- 根据设施选择滴眼麻醉、静脉麻醉或全身麻醉
抗VEGF治疗的目的大致分为三类。第一,辅助治疗(玻璃体手术前争取时间);第二,挽救治疗(光凝无效时预防视网膜脱离进展);第三,单药治疗(作为光凝的替代单独给药)。单药治疗后ROP趋于稳定,无血管区有血管生长,但长期可能复发增殖(闷烧性视网膜病变)。
抗VEGF治疗后的随访
Section titled “抗VEGF治疗后的随访”抗VEGF治疗后的观察时间表应遵循以下指南 3)。
- 注射后第一年:尽可能每2周进行一次眼底检查
- 追加激光或血管发育至III区后:每2至3个月一次
- 对于A-ROP:注射后2-3周内每周2次,直至约4个月每周1次,之后每1-2周一次
- 再燃的判断以plus disease的再次出现为重点,根据ETROP标准进行追加治疗
- 荧光眼底血管造影有助于了解再增殖的有无及范围
4期及以后的视网膜脱离需要手术治疗。在I型/经典ROP中,进行晶状体保留玻璃体手术(LSV),可获得良好的视网膜复位率和视力预后。4A期的早期手术影响视力预后。在II型/A-ROP中,由于血管纤维增殖活动性高,LSV效果不佳,常需摘除晶状体。
LSV的解剖成功率报告为:4A期74-91%,4B期62-92%,5期22-48% 1)。预期视力:4A期复位后20/80以上,4B期修复后行走视力,5期修复后手动 1)。LSV后白内障形成在10年内罕见,但发生时多在术后1年内 1)。
根据病变部位和严重程度选择。根据抗VEGF治疗指南(第2版),对于I区和A-ROP,抗VEGF治疗更有利,而对于II区病变,激光仍然是重要选择 3)。抗VEGF治疗对I区重症病例具有操作容易、治疗时间短、患儿负担小的优点,但也有再燃率高、需要长期定期检查的风险。在向家属说明各自的优缺点后选择。
因药物而异。阿柏西普再燃率为13.9-28%,雷珠单抗为20.8-83.0%,RAINBOW试验中31%需要追加治疗 3, 1)。A-ROP中75.0-87.5%需要追加治疗,尤其需要从注射后早期开始严密观察。
7. 长期预后与并发症
Section titled “7. 长期预后与并发症”退行与再激活
Section titled “退行与再激活”在ICROP3中,正式定义了消退(regression)和再激活(reactivation)的概念2)。消退分为完全消退和不完全消退。抗VEGF治疗后1-3天开始出现血管变化消退,而激光治疗后需要7-14天。消退的早期征象包括plus disease改善和周边无血管区血管延伸。
不完全消退后可能残留持续性无血管视网膜(PAR)。与激光治疗后或自然消退后相比,抗VEGF治疗后PAR更常见且范围更广2)。再激活(reactivation)在抗VEGF治疗后更常见,高峰在矫正胎龄37-60周。根据药物和剂量可能延迟2)。
未治疗ROP的晚期表现
Section titled “未治疗ROP的晚期表现”一项多中心回顾性研究(363只眼,186例患者,平均年龄34.5岁,平均胎龄26.6周,平均出生体重875克)报告了未治疗ROP的长期眼底表现如下4)。
- 格子样变性:196只眼(54.0%)
- 萎缩性裂孔:126只眼(34.7%)
- 视网膜裂孔:111只眼(30.6%)
- 视网膜脱离:140只眼(38.6%)
- 牵拉性视网膜劈裂:44只眼(12.1%)
- 黄斑牵拉:44只眼(12.1%)
视网膜脱离的危险因素包括胎龄≤29周(P < 0.05)和血管化至后极部2区(P = 0.009)4)。86.4%的视网膜脱离为孔源性或混合性,57.9%在30岁前发生4)。20%(28/140只眼)的脱离眼在初诊时被认为无法修复4)。71.6%存在不完全血管化(未达到3区)4)。
这些结果建议对未治疗ROP进行定期检查和超广角荧光素眼底血管造影评估4)。
激光光凝后高度近视在2岁时发生率为20%,5年后为24%。雷珠单抗0.2 mg组在2岁时为5%,5年后为8%,显著较低1)。早产儿独立于ROP具有高度近视和黄斑异常(中心凹无血管区缩小、中心凹凹陷变浅或消失)的风险。
眼压升高与青光眼
Section titled “眼压升高与青光眼”在未治疗的自然消退病例中,眼压升高见于23.2%,单纯光凝治疗为23.3%,急性期手术后为58.5% 1)。在5期ROP中为66.7%,无晶状体眼中为69.8% 1)。进展期ROP(4-5期)中10.0%在3年内发生青光眼,5期风险是4A期的6.76倍,晶状体摘除术后风险增加2.76倍 1)。
可能引起。一项未治疗ROP的多中心研究显示,即使在成年后,格子状变性(54%)、视网膜裂孔(30.6%)和视网膜脱离(38.6%)等晚期并发症的发生率也很高 4)。57.9%的视网膜脱离在30岁前发生,因此终身定期眼底检查至关重要。
这是需要担心的并发症。激光组5年后高度近视发生率为24%,而雷珠单抗0.2 mg组仅为8%,显著较低 1)。此外,早产本身也是高度近视和黄斑异常的独立危险因素。包括配镜和定期屈光检查在内的随访非常重要。
8. 最新研究与未来展望
Section titled “8. 最新研究与未来展望”PAR管理的未来
Section titled “PAR管理的未来”抗VEGF治疗后PAR的激光光凝最佳时机尚未确定 1)。一项回顾性研究表明,贝伐珠单抗后在修正胎龄60周进行预防性激光与减少不良结构结局相关 1)。荧光素眼底血管造影用于再激活风险评估(修正胎龄60周时)被认为有用 1)。
替代药物治疗
Section titled “替代药物治疗”- 口服普萘洛尔:2 mg/kg/日已被报道可预防2期ROP进展,但存在心肺并发症风险 1)。局部使用0.2%普萘洛尔滴眼液从1期开始使用安全有效 1)。
- AA/DHA补充:Mega Donna Mega试验(206例,胎龄<28周)报告AA+DHA组严重ROP发生率为15.8%,对照组为33.3%(减少50%)1)。
- 咖啡因:用于早产儿呼吸暂停的咖啡因可能通过下调VEGF和MMP抑制ROP进展 1)。
- 康柏西普(KH902):在中国已获批。报告疗效与雷珠单抗相当,复发率16.7%对23.3%(雷珠单抗)1)。
人工智能与远程医疗
Section titled “人工智能与远程医疗”基于深度学习模型的plus disease自动检测已达到与专家相当的准确率1)。血管严重程度评分(VSS)已被开发为plus disease严重程度的客观定量指标1)。SUNDROP等远程医疗项目已在包括中低收入国家在内的偏远地区扩大了筛查范围,便携式OCT的床旁评估也备受期待1)。
9. 参考文献
Section titled “9. 参考文献”- Marra KV, Chen JS, Nudleman E, Robbins SL. Review of retinopathy of prematurity management in the anti-VEGF era: evolving global paradigms, persistent challenges and our AI-assisted future. Clin Exp Ophthalmol. 2025;(in press/online).
- Chiang MF, Quinn GE, Fielder AR, et al. International classification of retinopathy of prematurity, third edition. Ophthalmology. 2021;128(10):e51-e68.
- 日本眼科学会・日本小児眼科学会. 未熟児網膜症診療ガイドライン(第2版). 2024.
- Hamad AE, Moinuddin O, Blair MP, et al. Late-onset retinal findings and complications in untreated retinopathy of prematurity. Ophthalmology. 2020;127(2):240-248.
- Mintz-Hittner HA, Kennedy KA, Chuang AZ; BEAT-ROP Cooperative Group. Efficacy of intravitreal bevacizumab for stage 3+ retinopathy of prematurity. N Engl J Med. 2011;364(7):603-615.
- Stahl A, Lepore D, Fielder A, et al. Ranibizumab versus laser therapy for the treatment of very low birthweight infants with retinopathy of prematurity (RAINBOW): an open-label randomised controlled trial. Lancet. 2019;394(10208):1551-1559.
- Stahl A, Sukgen EA, Wu WC, et al. Effect of intravitreal aflibercept vs laser photocoagulation on treatment success of retinopathy of prematurity: the FIREFLEYE randomized clinical trial. JAMA. 2022;328(4):348-359.
- Cryotherapy for Retinopathy of Prematurity Cooperative Group. Multicenter trial of cryotherapy for retinopathy of prematurity: preliminary results. Arch Ophthalmol. 1988;106(4):471-479.
- Good WV, Hardy RJ, Dobson V, et al; Early Treatment for Retinopathy of Prematurity Cooperative Group. The incidence and course of retinopathy of prematurity: findings from the Early Treatment for Retinopathy of Prematurity Study. Pediatrics. 2005;116(1):15-23.
