雷射光凝

早產兒視網膜病變
1. 什麼是早產兒視網膜病變?
Section titled “1. 什麼是早產兒視網膜病變?”早產兒視網膜病變(ROP)是發育中的視網膜血管發生的增殖性疾病。
視網膜血管從胎齡約14週開始從視盤發生,向眼底前方生長。淺層血管在胎齡30週、深層血管在胎齡38~40週到達最周邊部,完成生長。存在個體差異,顳側比鼻側距視盤更遠,因此到達最周邊部較晚,容易發生ROP。
早產兒出生時周邊視網膜存在無血管區。發育中的血管在從穩定的母體環境突然變化時,在最不成熟的細胞所在的生長前端停止生長,並向異常方向增殖。無血管區釋放VEGF(血管內皮生長因子)是其機制。
增殖進展的時期稱為活動期,血管成分消退、留下纖維結締組織和視網膜牽引或變性等後遺症的穩定狀態稱為瘢痕期。
ROP的發生頻率和嚴重程度與視網膜血管生長的不成熟程度成正比。胎齡和出生體重越小,發生率越高,越容易加重。高濃度氧是加重ROP的最大誘因,此外呼吸窘迫症候群、換血、敗血症、腦室內出血、手術史、營養和水分給予不平衡等也複雜相關。
1942年Terry首次報告,1967年永田進行了世界上首次光凝治療,並發展為標準治療。早產兒視網膜病變歷史上曾發生三次流行1):第一次流行(1940-50年代)由保溫箱內高濃度氧氣引起,第二次流行(1970-80年代)伴隨超低出生體重兒存活率的提高,第三次流行目前正在進行,發生在醫療資源有限的中低收入國家1)。ROP在兒童失明原因中所佔比例1990年約為10%,現已上升至30%。全球每年約有184,700例早產兒發生ROP,約20,000名兒童失明或嚴重視力障礙1)。出生體重低於1,000克的超低出生體重兒中,86.1%發生ROP,需要治療的病例達41%。美國ROP發生率從2004年的4.4%增加到2019年的8.1%1)。
發生率的大致情況如下。
| 對象組 | 發生率 |
|---|---|
| 超低出生體重兒(<1,000 g),日本 | 86.1% |
| 胎齡≤27週,美國 | 89.0% |
| 胎齡27-31週,美國 | 51.7% |
| 胎齡≥32週,美國 | 14.2% |
| 所有出生(總體),美國 | 0.12% |
主要風險因素如下所示1)。
| 風險因子 | 內容 |
|---|---|
| 胎齡小於32週 | 最重要的風險因子之一 |
| 出生體重小於1.5公斤 | 最重要的風險因子之一 |
| 高濃度、長期氧氣治療 | 發病的主要誘因 |
| 多胎妊娠 | 導致低出生體重 |
| 新生兒呼吸窘迫症候群(NRDS) | 需要呼吸管理的重症病例 |
| 敗血症、腦室內出血 | 全身發炎、循環障礙 |
| 出生後體重增長延遲 | 與IGF-1低值相關 |
| 輸血/紅血球生成素投予 | 氧氣運送能力變動 |
懷孕週數越短、出生體重越低,發生風險越高。尤其是懷孕週數小於32週、出生體重低於1500公克的早產兒是主要風險族群。出生後高濃度氧氣治療等環境因素也與發病有關。多種危險因子重疊時容易重症化。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”早產兒視網膜病變的急性期發生於新生兒期及嬰兒期,因此患兒本身無法表達症狀。家長或醫療人員可能會注意到以下表現。
- 白色瞳孔(白瞳症):在進展期(第4~5期),發生視網膜剝離時瞳孔呈現白色。
- 斜視:反映視力不良或雙眼視功能失衡。
- 眼球震顫:伴隨嚴重視力障礙時出現。
臨床所見與分期
Section titled “臨床所見與分期”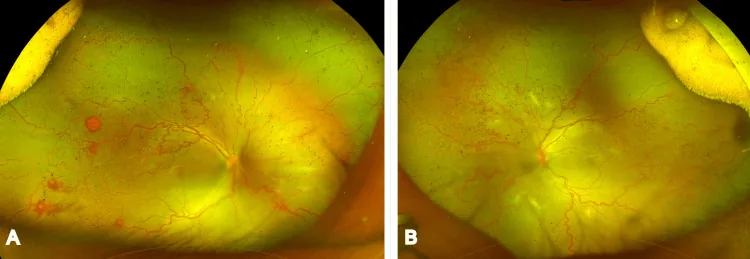
在日本,1975年制定了厚生省分類,並於1983年修訂。將ROP分為逐步進展的I型(典型ROP)及快速導致視網膜剝離的暴發型II型。國際分類(ICROP)在2005年修訂時全面採納了厚生省分類的概念,內容大致相同。最新的ICROP第3版(ICROP3)於2021年發布2)。
厚生省分類與ICROP3的對應
| 厚生省分類 | 國際分類(ICROP3) |
|---|---|
| I型1期:視網膜內新生血管 | 第1期:分界線(demarcation line) |
| I型2期:分界線形成 | 第2期:嵴(ridge) |
| I型3期:玻璃體內滲出和增殖(早期/中期/晚期) | 第3期:視網膜外纖維血管增殖(輕度/中度/重度) |
| 4期:部分視網膜剝離 4A/4B | 第4期:部分視網膜剝離(4A黃斑外,4B累及黃斑) |
| 5期:全視網膜剝離 | 第5期:全視網膜剝離 |
| II型:暴發型 | A-ROP(舊稱AP-ROP) |
| Plus disease(重症徵候) | Plus disease |
病變發生部位以I~III區表示。I區是以視乳頭為中心,以視乳頭與黃斑中心凹距離的兩倍為半徑的圓內側範圍,相當於將+25 D或+28 D觀察鏡的邊緣置於視乳頭對側緣時可見的範圍。II區是I區外側,以視乳頭到鼻側鋸齒緣為半徑的圓內側範圍。III區是II區外側的顳側新月形範圍。病變越靠後(I區),嚴重程度越高。ICROP3增加了後II區(從I區邊界起2個視乳頭直徑的帶狀區域)的概念2)。
第1期(分界線):在血管生長前端視網膜內形成白色分界線。
第2期(嵴):前衛區域的毯型間葉細胞增殖增厚,分界線向玻璃體腔突出形成嵴。
第3期(視網膜外纖維血管增殖):血管簇融合成弧形,玻璃體內新生血管形成血管腔,周圍產生膠原等結締組織。根據表現程度分為輕度、中度和重度。ICROP3將不伴嵴的平坦視網膜外新生血管概念納入第3期2)。
第4期(部分視網膜剝離):纖維血管增殖內的結締組織收縮牽拉視網膜,導致部分視網膜剝離。分為4A(未累及黃斑)和4B(累及黃斑)。
第5期(視網膜全剝離):纖維血管增殖廣泛且強烈收縮,導致視網膜全剝離。ICROP3將第5期分為以下三個亞型2)。
| 亞型 | 特徵 |
|---|---|
| 5A | 檢眼鏡下可見視乳頭(開放漏斗狀剝離) |
| 5B | 水晶體後方纖維血管組織或閉合漏斗,視乳頭不可見 |
| 5C | 5B + 前眼部異常(前房變淺、虹膜-角膜-水晶體黏連、角膜混濁) |
Plus disease 與 pre-plus disease
Section titled “Plus disease 與 pre-plus disease”在第1至3期,當後方2個象限以上出現視網膜靜脈擴張和動脈迂曲時,定義為plus disease。在ICROP3中,plus disease被修訂為從正常經pre-plus到plus的連續頻譜2)。plus disease的評估在I區內血管進行。
A-ROP(侵襲性ROP)
Section titled “A-ROP(侵襲性ROP)”在ICROP3中,以往的AP-ROP(侵襲性後部ROP)更名為A-ROP。這是因為定義擴展至包括非後部發病、較大早產兒以及資源有限地區的發病2)。
A-ROP的特徵如下:發生於後部(多為I區,也包括後部II區),plus disease顯著,形成全周性分流。有血管與無血管邊界不清,玻璃體內新生血管呈扁平半透明狀,難以識別。不表現為通常的第1期至第3期逐步進展,未經治療則迅速進展至第5期。包括後極在內的廣泛微血管網缺失,廣泛的VEGF釋放是快速進展的基礎。
如果早期病變的視網膜血管尖端出現分流或視網膜內出血,應立即進行光凝治療。
瘢痕期分類(厚生省)
Section titled “瘢痕期分類(厚生省)”活動期消退後,瘢痕期分類如下。
- 1度:僅周邊改變。眼底後極無明顯異常,視力通常正常。
- 2度(輕度):輕度視乳頭牽引。黃斑部無改變。
- 2度(中度):明顯視乳頭牽引。黃斑部外偏。
- 2度(重度):視乳頭牽引。黃斑部器質性改變。
- 3度:後極部束狀視網膜剝離(視網膜皺襞)。
- 4度:瞳孔區部分可見後部水晶體纖維增生。
- 5度:完全後部水晶體纖維增生。
3. 原因與風險因素
Section titled “3. 原因與風險因素”早產兒視網膜病變的發生涉及未成熟的視網膜血管系統與出生後氧氣環境及全身狀態的相互作用。高濃度氧氣是加重ROP的最大誘因,此外,呼吸窘迫症候群、換血、敗血症、腦室內出血、手術史、營養和水分失衡等也複雜地參與其中。
| 風險因素 | 內容 |
|---|---|
| 胎齡 | <32週為高風險 |
| 出生體重 | <1,500 g為高風險 |
| 氧氣治療 | 高濃度、長期使用 |
| IGF-1低值 | 出生後營養不良和疾病1) |
| 敗血症、貧血、輸血 | 全身狀況惡化 |
| 呼吸窘迫症候群 | 需要呼吸管理的重症兒童 |
| 多胞胎出生 | 較小的雙胞胎中晚期ROP較常見1) |
| 出生後體重增加不良 | WINROP/G-ROP演算法的依據1) |
IGF-1(胰島素樣生長因子-1)是視網膜血管發育必需的訊號因子,早產後低IGF-1狀態促進血管生長停滯1)。
4. 病理生理學
Section titled “4. 病理生理學”視網膜血管發育與兩階段疾病模型
Section titled “視網膜血管發育與兩階段疾病模型”視網膜血管發育始於胎齡約14週,出生前到達最周邊區域並完成。淺層血管在30週時到達,深層血管在38-40週時到達。早產兒出生時周邊視網膜殘留無血管區域。
ROP的病理生理學分為兩個階段來解釋1)。
第一階段(血管發育停滯期):早產兒的未成熟視網膜暴露於高氧環境(子宮外)時,透過氧感測器抑制VEGF和IGF-1。這導致正常視網膜血管發育停止,形成無血管區。
第二階段(血管增殖期):隨著無血管視網膜代謝成熟,為補償缺血狀態,VEGF過度產生。這種VEGF過量誘導血管內皮異常增殖,導致纖維血管增殖組織進入玻璃體腔(第3期及以上)。
新生血管沿著玻璃體腔內有形玻璃體的纖維生長,並在周圍產生膠原等結締組織。當這些結締組織收縮並牽拉與其粘連的視網膜時,就會發生視網膜剝離,導致嚴重的視力障礙或失明。
在A-ROP中,存在包括後極部在內的廣泛微血管網缺失,VEGF從包括後極部在內的廣泛區域釋放,因此病情進展迅速。
IGF-1(胰島素樣生長因子-1)對視網膜血管和神經的協調發育至關重要,低IGF-1狀態會延遲正常血管發育,增加ROP易感性1)。出生後體重增長延遲也與低IGF-1相關,是危險因素1)。
擠壓症候群(crunch syndrome):抗VEGF治療後,VEGF被抑制,TGF-β(促纖維化因子)相對升高,導致VEGF-TGF-β平衡失調,引起纖維血管膜快速收縮。這有加重牽引性視網膜剝離的風險1)。
5. 篩查與診斷
Section titled “5. 篩查與診斷”篩查標準與首次檢查時機
Section titled “篩查標準與首次檢查時機”NICU中的篩查對象為胎齡小於34週或出生體重≤1800克的嬰兒。此外,接受氧療、機械通氣、輸血、患有敗血症、腦室內出血、嚴重呼吸或循環障礙、全身麻醉手術或胎兒水腫的嬰兒被視為高風險族群,即使不符合上述標準也需進行眼底檢查。
首次檢查時機如下:
| 出生時胎齡 | 首次檢查時機 |
|---|---|
| 小於26週 | 從矯正胎齡29週開始 |
| 26週及以上 | 從出生後3週開始 |
治療適應症(1型ROP)
Section titled “治療適應症(1型ROP)”治療適應症基於ETROP研究中第1型ROP的標準1)。符合以下任一情況時,建議在診斷後72小時內進行治療。
- ① 伴有plus病變的zone I所有ROP
- ② 不伴有plus病變的zone I第3期ROP
- ③ 伴有plus病變的zone II第3期ROP
- ④ A-ROP(儘快進行)
以上情況之外均視為第2型ROP進行追蹤。伴有plus病變的zone II第2期ROP根據所用藥物處理方式不同(RAINBOW試驗中排除,但FIREFLEYE試驗中納入)3)。
根據檢查結果建議的檢查間隔如下所示1)。
| 所見 | 下次檢查間隔 |
|---|---|
| zone I未成熟血管或第1-2期、後極部zone II未成熟血管、疑似A-ROP | 每週1次 |
| 後極部zone II未成熟視網膜、zone II第2期、zone I消退期 | 1-2週 |
| zone I第1期、zone II未成熟血管(無ROP)、zone II消退期 | 2週 |
| III區第1-2期、III區退行期 | 2-3週 |
篩檢終止標準為完全血管化至III區,或矯正胎齡45週時無第1型ROP。抗VEGF治療後需至少觀察至矯正胎齡65週1)。
使用美多麗®P或新福林®·美多麗®P·賽普樂®按2:1:1比例混合的點眼液(改良Capto點眼法),在檢查開始前1小時起每10分鐘點眼1次,共3次進行散瞳。
診斷與評估輔助技術
Section titled “診斷與評估輔助技術”- 廣角眼底相機(RetCam等):可在散瞳下進行廣範圍眼底攝影。也用於遠距判讀。
- AI影像診斷:自動檢測Plus病已達到與眼科專家同等或更高的準確率1)。基於深度學習模型的血管嚴重程度評分(VSS)已被開發為Plus病診斷的客觀指標1)。
- 預測模型(G-ROP、WINROP):基於胎齡、出生體重和出生後體重增長,預測第1型ROP的敏感度達到100%1)。
- FIRST-ROP演算法:對於中等風險嬰兒(胎齡≥27週且出生體重≥800克),有建議可將篩檢開始時間延遲至矯正胎齡34週1)。
- 螢光眼底血管攝影:有助於評估復發的有無和範圍。有望用於PAR評估3)。
胎齡不足26週的嬰兒從矯正胎齡29週開始首次檢查;胎齡26週及以上的嬰兒從出生後3週開始首次檢查。之後根據發現每1-3週重複一次。抗VEGF治療後建議至少觀察至矯正胎齡65週3)。當視網膜血管化完成且無需要治療的發現時,檢查結束。
取決於出生時的胎齡。出生胎齡不足26週者,從矯正胎齡29週開始首次眼底檢查;出生胎齡26週及以上者,從出生後3週開始首次眼底檢查。篩檢對象為出生胎齡不足34週或出生體重≤1800克的嬰兒,但即使不符合上述標準,若存在氧氣治療、輸血、敗血症等危險因子,也需要進行檢查。
6. 標準治療方法
Section titled “6. 標準治療方法”抗VEGF玻璃體內注射
適應症:優先選擇用於第一區和A-ROP
國內核准藥物:雷珠單抗0.2毫克,阿柏西普0.4毫克
優點:即使後極部重症病例也易於實施,治療時間短,嬰兒負擔小
注意事項:復發風險高,必須長期追蹤
玻璃體手術
適應症:第4期及以後的視網膜剝離
術式:典型ROP首選水晶體保留玻璃體手術(LSV)
結果:第4A期復位率74%~91%,第4B期62%~92%,第5期22%~48%1)
鞏膜扣帶術
自1967年永田實施世界首例光凝治療以來,光凝已成為ROP的標準治療。基本方法是在間接檢眼鏡下對整個無血管區進行光凝。在明顯的水晶體血管膜或瞳孔僵直時可能難以實施。該操作耗時且需要術者熟練,廣泛光凝可能導致視野狹窄和近視。
CRYO-ROP試驗顯示,1年時不良結構結果在冷凍組為25.7%,觀察組為47.4%,15年後差異仍顯著(30% vs 52%)8)。ETROP試驗顯示早期治療使不良結構結果從15.6%降至9.1%9)。
抗VEGF治療
Section titled “抗VEGF治療”由於VEGF參與視網膜新生血管形成,抗VEGF藥物的玻璃體內注射已被嘗試用於ROP。截至2022年12月,日本國內核准用於ROP治療的抗VEGF藥物有以下兩種3)。
- 雷珠單抗(Lucentis®):0.2 mg/次(0.02 mL)。2019年11月在日本核准。
- 阿柏西普(Eylea®):0.4 mg/次(0.01 mL)。2022年9月在日本核准。
兩者均僅以瓶裝製劑核准用於ROP,根據仿單,再給藥間隔至少為1個月3)。貝伐珠單抗在日本國內外均未核准用於ROP3)。
主要臨床試驗結果
| 試驗名稱 | 對象/藥物 | 主要結果 |
|---|---|---|
| BEAT-ROP | zone I Stage 3+,貝伐珠單抗0.625 mg | zone I復發率6%對比雷射42%5, 1) |
| RAINBOW | 出生體重<1,500 g,雷珠單抗0.2 mg | 治療成功率80.0%對比雷射66.2%。2歲時高度近視5%對比20%6, 1) |
| FIREFLEYE | 胎齡≤32週或體重<1,500 g,阿柏西普0.4 mg | 成功率82.7%對比雷射84.2%。全身麻醉率44.0%對比65.8%7, 1) |
復發率比較3):
- 阿柏西普:復發率13.9%
28%,平均復發時間1114.2週 - 雷珠單抗:復發率20.8%~83.0%,復發時間5.9~9.3週(復發較早)
雷珠單抗注射後14天血中VEGF下降已檢測不到,認為全身影響較小。阿柏西普注射後約8週血漿中游離型阿柏西普降至定量下限以下3)。
兒童特有的注射技術3):
- 在角膜緣後方1.0~1.5 mm處進針(注意與成人的3~4 mm不同)
- 由於水晶體相對較大,應向下(後方)進針。朝向眼球中央方向有損傷水晶體的風險
- 使用30G或更細的注射針
- 在NICU保溫箱或手術室中進行
- 根據設施選擇點眼麻醉、靜脈麻醉或全身麻醉
抗VEGF治療的目的大致分為三類。第一,輔助治療(玻璃體手術前爭取時間);第二,挽救治療(光凝無效時預防視網膜剝離進展);第三,單藥治療(作為光凝的替代單獨給藥)。單藥治療後ROP趨於穩定,無血管區有血管生長,但長期可能復發增殖(悶燒性視網膜病變)。
抗VEGF治療後的追蹤
Section titled “抗VEGF治療後的追蹤”抗VEGF治療後的觀察時程應遵循以下指引 3)。
- 注射後第一年:盡可能每2週進行一次眼底檢查
- 追加雷射或血管發育至第III區後:每2至3個月一次
- 對於A-ROP:注射後2-3週內每週2次,直至約4個月每週1次,之後每1-2週一次
- 再燃的判斷以plus disease的再次出現為重點,根據ETROP標準進行追加治療
- 螢光眼底血管攝影有助於了解再增殖的有無及範圍
第4期及以後的視網膜剝離需要手術治療。在I型/典型ROP中,進行晶體保留玻璃體手術(LSV),可獲得良好的視網膜復位率和視力預後。第4A期的早期手術影響視力預後。在II型/A-ROP中,由於血管纖維增殖活動性高,LSV效果不佳,常需摘除晶體。
LSV的解剖成功率報告為:第4A期74-91%,第4B期62-92%,第5期22-48% 1)。預期視力:第4A期復位後20/80以上,第4B期修復後行走視力,第5期修復後手動 1)。LSV後白內障形成在10年內罕見,但發生時多在術後1年內 1)。
根據病變部位和嚴重程度選擇。根據抗VEGF治療指引(第2版),對於第I區和A-ROP,抗VEGF治療更有利,而對於第II區病變,雷射仍然是重要選擇 3)。抗VEGF治療對第I區重症病例具有操作容易、治療時間短、患兒負擔小的優點,但也有再燃率高、需要長期定期檢查的風險。在向家屬說明各自的優缺點後選擇。
因藥物而異。阿柏西普再燃率為13.9-28%,雷珠單抗為20.8-83.0%,RAINBOW試驗中31%需要追加治療 3, 1)。A-ROP中75.0-87.5%需要追加治療,尤其需要從注射後早期開始嚴密觀察。
7. 長期預後與併發症
Section titled “7. 長期預後與併發症”消退與再活化
Section titled “消退與再活化”在ICROP3中,正式定義了消退(regression)與再活化(reactivation)的概念2)。消退分為完全消退與不完全消退。抗VEGF後1-3天開始出現血管變化消退,而雷射後需要7-14天。消退的早期徵象包括plus disease改善和周邊無血管區血管延伸。
不完全消退後可能殘留持續性無血管視網膜(PAR)。與雷射後或自然消退後相比,抗VEGF後PAR更常見且範圍更廣2)。再活化(reactivation)在抗VEGF治療後更常見,高峰在矯正週數37-60週。根據藥物與劑量可能延遲2)。
未治療ROP的晚期發現
Section titled “未治療ROP的晚期發現”一項多中心回顧性研究(363眼、186例,平均年齡34.5歲,平均在胎26.6週,平均出生體重875克)報告了未治療ROP的長期眼底發現如下4)。
- 格子狀變性:196眼(54.0%)
- 萎縮性裂孔:126眼(34.7%)
- 視網膜裂孔:111眼(30.6%)
- 視網膜剝離:140眼(38.6%)
- 牽引性視網膜分離症:44眼(12.1%)
- 黃斑牽引:44眼(12.1%)
視網膜剝離的風險因子包括在胎29週以下(P < 0.05)與血管化至後極區2(P = 0.009)4)。86.4%的視網膜剝離為裂孔源性或混合型,57.9%在30歲前發生4)。20%(28/140眼)的剝離眼在初診時被認為無法修復4)。71.6%存在不完全血管化(未達區3)4)。
這些結果建議對未治療ROP進行定期檢查與超廣角螢光眼底攝影評估4)。
雷射光凝後高度近視在2歲時發生率為20%,5年後為24%。ranibizumab 0.2 mg組在2歲時為5%,5年後為8%,顯著較低1)。早產兒獨立於ROP具有高度近視與黃斑異常(中心凹無血管區縮小、中心凹凹陷變淺或消失)的風險。
眼壓升高與青光眼
Section titled “眼壓升高與青光眼”在未治療的自然消退病例中,眼壓升高見於23.2%,單純光凝治療為23.3%,急性期手術後為58.5% 1)。在第5期ROP中為66.7%,無水晶體眼中為69.8% 1)。進展期ROP(第4-5期)中10.0%在3年內發生青光眼,第5期風險是第4A期的6.76倍,水晶體摘除術後風險增加2.76倍 1)。
可能引起。一項未治療ROP的多中心研究顯示,即使在成年後,格子狀變性(54%)、視網膜裂孔(30.6%)和視網膜剝離(38.6%)等晚期併發症的發生率也很高 4)。57.9%的視網膜剝離在30歲前發生,因此終身定期眼底檢查至關重要。
這是需要擔心的併發症。雷射組5年後高度近視發生率為24%,而雷珠單抗0.2 mg組僅為8%,顯著較低 1)。此外,早產本身也是高度近視和黃斑異常的獨立危險因子。包括配鏡和定期屈光檢查在內的追蹤非常重要。
8. 最新研究與未來展望
Section titled “8. 最新研究與未來展望”PAR管理的未來
Section titled “PAR管理的未來”抗VEGF治療後PAR的雷射光凝最佳時機尚未確定 1)。一項回顧性研究表明,貝伐珠單抗後在修正胎齡60週進行預防性雷射與減少不良結構結果相關 1)。螢光眼底血管攝影用於再活化風險評估(修正胎齡60週時)被認為有用 1)。
替代藥物治療
Section titled “替代藥物治療”- 口服普萘洛爾:2 mg/kg/日已被報導可預防第2期ROP進展,但存在心肺併發症風險 1)。局部使用0.2%普萘洛爾眼藥水從第1期開始使用安全有效 1)。
- AA/DHA補充:Mega Donna Mega試驗(206例,胎齡<28週)報告AA+DHA組嚴重ROP發生率為15.8%,對照組為33.3%(減少50%)1)。
- 咖啡因:用於早產兒呼吸暫停的咖啡因可能通過下調VEGF和MMP抑制ROP進展 1)。
- 康柏西普(KH902):在中國已獲批。報告療效與雷珠單抗相當,復發率16.7%對23.3%(雷珠單抗)1)。
AI與遠距醫療
Section titled “AI與遠距醫療”深度學習模型自動檢測plus disease已達到與專家相當的準確率1)。血管嚴重度評分(VSS)已被開發為plus disease嚴重度的客觀定量指標1)。SUNDROP等遠距醫療計畫已在包括中低收入國家在內的偏遠地區擴大篩檢範圍,可攜式OCT的床邊評估也備受期待1)。
9. 參考文獻
Section titled “9. 參考文獻”- Marra KV, Chen JS, Nudleman E, Robbins SL. Review of retinopathy of prematurity management in the anti-VEGF era: evolving global paradigms, persistent challenges and our AI-assisted future. Clin Exp Ophthalmol. 2025;(in press/online).
- Chiang MF, Quinn GE, Fielder AR, et al. International classification of retinopathy of prematurity, third edition. Ophthalmology. 2021;128(10):e51-e68.
- 日本眼科学会・日本小児眼科学会. 未熟児網膜症診療ガイドライン(第2版). 2024.
- Hamad AE, Moinuddin O, Blair MP, et al. Late-onset retinal findings and complications in untreated retinopathy of prematurity. Ophthalmology. 2020;127(2):240-248.
- Mintz-Hittner HA, Kennedy KA, Chuang AZ; BEAT-ROP Cooperative Group. Efficacy of intravitreal bevacizumab for stage 3+ retinopathy of prematurity. N Engl J Med. 2011;364(7):603-615.
- Stahl A, Lepore D, Fielder A, et al. Ranibizumab versus laser therapy for the treatment of very low birthweight infants with retinopathy of prematurity (RAINBOW): an open-label randomised controlled trial. Lancet. 2019;394(10208):1551-1559.
- Stahl A, Sukgen EA, Wu WC, et al. Effect of intravitreal aflibercept vs laser photocoagulation on treatment success of retinopathy of prematurity: the FIREFLEYE randomized clinical trial. JAMA. 2022;328(4):348-359.
- Cryotherapy for Retinopathy of Prematurity Cooperative Group. Multicenter trial of cryotherapy for retinopathy of prematurity: preliminary results. Arch Ophthalmol. 1988;106(4):471-479.
- Good WV, Hardy RJ, Dobson V, et al; Early Treatment for Retinopathy of Prematurity Cooperative Group. The incidence and course of retinopathy of prematurity: findings from the Early Treatment for Retinopathy of Prematurity Study. Pediatrics. 2005;116(1):15-23.
