レーザー光凝固

未熟児網膜症(Retinopathy of Prematurity)
1. 未熟児網膜症とは
Section titled “1. 未熟児網膜症とは”未熟児網膜症(Retinopathy of Prematurity; ROP)は、発達途上の網膜血管に起こる増殖疾患である。
網膜血管は胎生第14週頃より視神経乳頭部から発生を始め、眼底の前方へ成長する。浅層血管は胎生第30週、深層血管は胎生第38〜40週に最周辺部に達して成長が完了する。個人差があり、耳側は鼻側より視神経乳頭からの距離が長いため、最周辺部への到達が遅くROPが起こりやすい。
早産児では周辺網膜に無血管領域が残存した状態で出生する。発達途上の血管は、安定した母体から急激に環境が変化すると、最も未熟な細胞が存在する成長の先端部で成長を停止し、異常な方向に増殖する。無血管領域からVEGF(血管内皮細胞増殖因子)が放出されることがその機序である。
増殖が進行する期間を活動期といい、鎮静化して血管成分が退縮し、線維結合組織や網膜の牽引・変性などの後遺症を残した状態を瘢痕期という。
ROPの発現頻度と重症度は、網膜血管の成長が未熟であるほど高い。在胎週数・出生体重が少ないほど発症率が高く、重症になりやすい。高濃度酸素はROPを悪化させる最も大きな誘因であり、その他に呼吸窮迫症候群、交換輸血、敗血症、脳室内出血、手術の既往、栄養や水分投与のアンバランスなどが複雑に関与する。
1942年にTerryが最初に報告し、1967年に永田が世界で初めての光凝固治療を行い、標準的治療として発展してきた。未熟児網膜症の流行は歴史的に3回起きており1)、第1の流行(1940〜50年代)は保育器内での高濃度酸素投与が原因、第2の流行(1970〜80年代)は超低出生体重児の救命率向上に伴うもの、第3の流行は現在進行中で医療資源の限られた中低所得国で生じている1)。小児の失明原因としてROPが占める割合は1990年では約10%であったが、現在は30%にまで上昇している。全世界で年間約184,700例の早産児がROPを発症し、約20,000人の小児が失明または重度視覚障害を来たすと推計される1)。出生体重1,000 g未満の超低出生体重児では86.1%に発症し、治療が必要な症例は41%にのぼる。米国でのROP発症率は2004年の4.4%から2019年の8.1%に増加している1)。
発症率の目安は以下のとおりである。
| 対象群 | 発症率 |
|---|---|
| 超低出生体重児(<1,000 g)、日本 | 86.1% |
| 在胎27週以下、米国 | 89.0% |
| 在胎27〜31週、米国 | 51.7% |
| 在胎32週以上、米国 | 14.2% |
| 全出生(全体)、米国 | 0.12% |
主なリスク因子を以下に示す1)。
| リスク因子 | 内容 |
|---|---|
| 在胎32週未満 | 最重要リスク因子の一つ |
| 出生体重1.5 kg未満 | 最重要リスク因子の一つ |
| 高濃度・長期の酸素投与 | 発症の主要誘因 |
| 多胎妊娠 | 低出生体重をもたらす |
| 呼吸窮迫症候群(NRDS) | 呼吸管理が必要な重篤例 |
| 敗血症・脳室内出血 | 全身炎症・循環障害 |
| 出生後体重増加の遅延 | IGF-1低値との関連 |
| 輸血・エリスロポエチン投与 | 酸素運搬能変動 |
在胎週数が短いほど、出生体重が少ないほど発症リスクが高い。特に在胎32週未満・出生体重1,500 g未満の早産児が主なリスク群である。高濃度酸素投与など出生後の環境因子も発症に関与する。複数のリスク因子が重なると重症化しやすい。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”未熟児網膜症の急性期は新生児期・乳児期に発症するため、患児自身が症状を訴えることはない。保護者や医療従事者が以下のような所見に気づくことがある。
臨床所見・病期分類
Section titled “臨床所見・病期分類”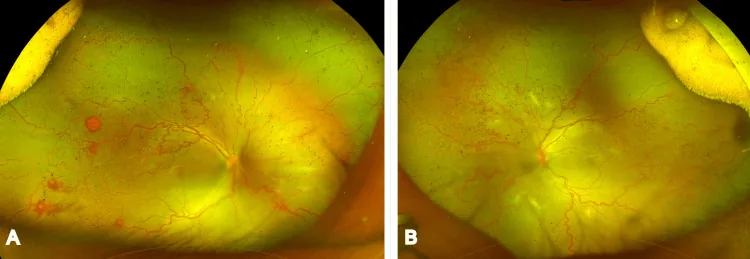
活動期の分類
Section titled “活動期の分類”わが国では1975年に厚生省分類が作成され、1983年に改定された。ROPを段階的に進行するI型(Classic ROP)と急速に網膜剥離に至る劇症のII型に分けた。国際分類(ICROP)は2005年の改定の際に厚生省分類の概念を全面的に取り入れており、内容はほぼ同じである。最新のICROP第3版(ICROP3)は2021年に発表された2)。
厚生省分類とICROP3の対応
| 厚生省分類 | 国際分類(ICROP3) |
|---|---|
| I型1期 網膜内血管新生 | Stage 1 境界線(demarcation line) |
| I型2期 境界線形成 | Stage 2 隆起(ridge) |
| I型3期 硝子体内滲出・増殖期(初期/中期/後期) | Stage 3 網膜外線維血管増殖(mild/moderate/severe) |
| 4期 部分的網膜剥離 4A/4B | Stage 4 部分的網膜剥離(4A 黄斑外・4B 黄斑含む) |
| 5期 網膜全剥離 | Stage 5 網膜全剥離 |
| II型 劇症型 | A-ROP(旧AP-ROP) |
| Plus disease(重症徴候) | Plus disease |
Zone分類
Section titled “Zone分類”病変の発生部位はzone I〜IIIで表す。zone Iは乳頭を中心に、乳頭と黄斑中心窩間の2倍を半径とする円の内側の範囲で、+25 Dあるいは+28 Dの観察レンズの端を乳頭の対側縁に置いて見える範囲に相当する。zone IIはzone Iより外側で、乳頭から鼻側鋸状縁までを半径とする円の内側の範囲。zone IIIはzone IIより外の耳側の三日月の範囲である。zone Iほど病変が後方であり、重症度が高い。ICROP3ではposterior zone II(zone I境界から2乳頭径の帯状領域)の概念が追加された2)。
各Stageの所見
Section titled “各Stageの所見”Stage 1(境界線):血管成長先端部の網膜内に白い境界線(demarcation line)が形成される。
Stage 2(隆起):前衛領域の絨毯型間葉細胞の増殖が厚くなり、境界線が硝子体腔に突出して隆起(ridge)が形成される。
Stage 3(網膜外線維血管増殖):vascular tuftが融合して弧状になり、硝子体内の新生血管が血管腔を形成し、周囲にコラーゲン等の結合組織が産生する。所見の程度によりmild・moderate・severeの3段階に分ける。ICROP3では、ridgeを伴わない平坦な網膜外血管新生(flat neovascularization)の概念がStage 3に追加された2)。
Stage 4(部分的網膜剥離):線維血管増殖内の結合組織が収縮して網膜を牽引し、部分的な網膜剥離が起こる。4A(黄斑非含)と4B(黄斑含む)に分類する。
Stage 5(網膜全剥離):線維血管増殖が広範囲で強く牽引し、網膜が全剥離する。ICROP3ではStage 5を以下の3亜型に分類した2)。
| 亜型 | 特徴 |
|---|---|
| 5A | 検眼鏡で視神経乳頭が見える(開放漏斗状剥離) |
| 5B | 水晶体後方線維血管組織または閉鎖漏斗で乳頭不可視 |
| 5C | 5B+前眼部異常(前房浅化・虹彩-角膜-水晶体癒着・角膜混濁) |
Plus disease・pre-plus disease
Section titled “Plus disease・pre-plus disease”stage 1〜3において、後方2象限以上の網膜静脈の拡張と動脈の蛇行がある場合をplus diseaseと規定する。ICROP3ではplus diseaseを正常からpre-plusを経てplusへ至る連続スペクトラムとして捉えるよう改訂された2)。plus diseaseの評価はzone I内の血管で行う。
A-ROP(Aggressive ROP)
Section titled “A-ROP(Aggressive ROP)”ICROP3では、従来のAP-ROP(Aggressive Posterior ROP)がA-ROPに改称された。後方以外の部位での発症や、より大きな早産児・資源の限られた地域での発症も包括するよう定義が拡張されたためである2)。
A-ROPの特徴は以下のとおりである。後方(多くはzone I、zone II後方も含む)に発症し、plus diseaseが顕著で全周性・シャントを形成する。有血管・無血管境界が不明瞭で、硝子体内新生血管が平坦な形で半透明であり識別しにくい。通常のstage 1からstage 3への段階的進行を示さず、未治療では急速にstage 5へ至る。後極を含む広範な毛細血管網の欠如があり、広範なVEGF放出が急速進行の基盤となる。
初期病変の網膜血管先端部のシャントや網膜内出血がみられれば、直ちに光凝固を行うべきである。
瘢痕期分類(厚生省)
Section titled “瘢痕期分類(厚生省)”活動期の鎮静化後は瘢痕期として以下のように分類される。
- 1度:周辺性変化のみ。眼底後極部に著変がなく、視力は一般に正常。
- 2度(弱度):わずかな牽引乳頭。黄斑部に変化はない。
- 2度(中等度):明らかな牽引乳頭。黄斑部外方偏位。
- 2度(強度):牽引乳頭。黄斑部に器質的変化。
- 3度:後極部に束状網膜剥離(網膜ひだ)。
- 4度:瞳孔領の一部にみえる後部水晶体線維増殖。
- 5度:完全後部水晶体線維増殖。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”未熟児網膜症の発症には、未熟な網膜血管系と出生後の酸素環境・全身状態の相互作用が関与する。高濃度酸素はROPを悪化させる最も大きな誘因であり、その他に呼吸窮迫症候群、交換輸血、敗血症、脳室内出血、手術の既往、栄養や水分投与のアンバランスなどが複雑に関与する。
| リスク因子 | 内容 |
|---|---|
| 在胎週数 | <32週が高リスク |
| 出生体重 | <1,500 gが高リスク |
| 酸素投与 | 高濃度・長期投与 |
| IGF-1低値 | 出生後の低栄養・疾患1) |
| 敗血症・貧血・輸血 | 全身状態の悪化 |
| 呼吸窮迫症候群 | 呼吸管理を要する重篤児 |
| 多胎出生 | 小さい方の双子でadvanced ROPが多い1) |
| 出生後体重増加不良 | WINROP/G-ROPアルゴリズムの根拠1) |
IGF-1(インスリン様成長因子-1)は網膜血管発達に必須のシグナル因子であり、早産後の低IGF-1状態が血管成長停止を促進する1)。
4. 病態生理
Section titled “4. 病態生理”網膜血管発達と2段階病態モデル
Section titled “網膜血管発達と2段階病態モデル”網膜血管の発達は胎生14週頃から始まり、出生前までに最周辺部に到達して完了する。浅層血管は胎生30週、深層血管は胎生38〜40週に到達する。早産児では周辺網膜に無血管領域が残存したまま出生する。
ROPの病態は2段階で説明される1)。
第1相(血管発達停止期):早産児の未熟網膜が高酸素環境(子宮外)に曝されると、酸素センサーを介してVEGFとIGF-1が抑制される。これにより正常な網膜血管発育が停止し、無血管帯が形成される。
第2相(血管増殖期):無血管網膜が代謝的に成熟するにつれ、虚血状態を補うべくVEGFが過剰産生される。このVEGF過剰が血管内皮の異常増殖を誘発し、硝子体腔への線維血管増殖組織形成(Stage 3以降)につながる。
新生血管は硝子体腔の有形硝子体の線維に沿って成長し、周囲にコラーゲン等の結合組織を産生する。この結合組織が収縮して接着している網膜を牽引すると網膜剥離が起こり、重篤な視力障害ないし失明に至る。
A-ROPでは後極を含む広範な毛細血管網欠如が存在し、後極を含む広範な領域からVEGFが放出されるため急速に進行する。
IGF-1(インスリン様成長因子-1)は網膜の血管・神経発達の協調に重要であり、低IGF-1状態は正常血管発育を遅延させてROP感受性を増大させる1)。出生後体重増加の遅延もIGF-1低値と関連してリスクとなる1)。
クランチ症候群(crunch syndrome):抗VEGF療法後にVEGFが抑制されると、TGF-β(線維化促進因子)の相対的上昇によりVEGF-TGF-βバランスが破綻し、線維血管膜の急速な収縮が起こる。これにより牽引性網膜剥離が悪化するリスクがある1)。
5. スクリーニングと診断
Section titled “5. スクリーニングと診断”スクリーニング基準と初回検査時期
Section titled “スクリーニング基準と初回検査時期”NICUでのスクリーニング対象は、在胎34週未満または出生体重1,800 g以下の児である。さらに、酸素投与・人工換気・輸血・敗血症・脳室内出血・高度の呼吸・循環障害を伴う児・全身麻酔手術・胎児水腫はハイリスク群として、この基準を外れても眼底検査を行う必要がある。
初回検査時期は以下のとおりである。
| 出生時在胎週数 | 初回検査時期 |
|---|---|
| 26週未満 | 修正在胎29週から |
| 26週以上 | 生後3週から |
治療適応(type 1 ROP)
Section titled “治療適応(type 1 ROP)”治療適応はETROP研究に基づくtype 1 ROPの基準による1)。以下のいずれかに該当する場合、診断後72時間以内の治療が推奨される。
- ① plus diseaseを伴うzone IすべてのROP
- ② plus diseaseを伴わないzone I stage 3 ROP
- ③ plus diseaseを伴うzone II stage 3 ROP
- ④ A-ROP(可及的速やかに施行)
上記以外はtype 2 ROPとして経過観察とする。plus diseaseを伴うzone II stage 2 ROPは、使用薬剤により対応が異なる(RAINBOW試験では対象外だがFIREFLEYE試験では対象に含まれた)3)。
フォローアップ間隔
Section titled “フォローアップ間隔”所見に応じた検査間隔の目安を以下に示す1)。
| 所見 | 次回検査まで |
|---|---|
| zone I 未熟血管またはstage 1-2、posterior zone IIの未熟血管、A-ROP疑い | 週1回 |
| posterior zone IIの未熟網膜、zone II stage 2、zone I退縮期 | 1〜2週 |
| zone I stage 1、zone II未熟血管(ROPなし)、zone II退縮期 | 2週 |
| zone III stage 1-2、zone III退縮期 | 2〜3週 |
スクリーニング終了基準はzone IIIまでの完全血管化、または修正在胎45週でtype 1 ROPなし、である。抗VEGF療法後は最低修正65週まで観察継続が必要である1)。
ミドリン®Pあるいはネオシネジン®・ミドリン®P・サイプレジン®を2:1:1で混合した点眼液(カプト点眼変法)を、診察開始前1時間から10分おきに3回点眼して散瞳する。
診断・評価の補助技術
Section titled “診断・評価の補助技術”- 広角眼底カメラ(RetCam等):散瞳下での広範囲眼底撮影が可能。遠隔読影にも利用される。
- AIによる画像診断:Plus diseaseの自動検出で眼科専門医と同等以上の精度が報告されている1)。DLモデルによるVSS(vascular severity score)がplus disease診断の客観的指標として開発されている1)。
- 予測モデル(G-ROP・WINROP):在胎週数・出生体重・出生後体重増加をもとにType 1 ROPの予測感度100%を達成1)。
- FIRST-ROPアルゴリズム:中等度リスク児(在胎27週以上かつ出生体重800 g以上)ではスクリーニング開始を修正34週まで遅延できるとする提案がある1)。
- 蛍光眼底造影:再増殖の有無と範囲の評価に有用。PAR評価への活用が期待される3)。
在胎26週未満なら修正29週から、在胎26週以上なら生後3週から初回検査を開始する。その後は所見に応じて1〜3週ごとに繰り返す。抗VEGF治療を行った場合は修正65週以降まで観察継続が推奨される3)。治療が必要な所見がなく網膜血管化が完成すれば終了となる。
家族への説明
Section titled “家族への説明”出生時の在胎週数によって異なる。在胎26週未満では修正在胎29週から、在胎26週以上では生後3週から初回眼底検査を開始する。スクリーニング対象は在胎34週未満または出生体重1,800 g以下だが、酸素投与・輸血・敗血症などのリスク因子があれば基準外でも検査が必要である。
6. 標準的な治療法
Section titled “6. 標準的な治療法”抗VEGF硝子体内注射
適応:zone I・A-ROPに優先的に選択
国内承認薬:ラニビズマブ0.2 mg、アフリベルセプト0.4 mg
利点:後極部重症例にも施行容易、治療時間が短く患児負担が少ない
注意:再燃リスク高く長期フォローアップ必須
硝子体手術
適応:Stage 4以降の網膜剥離
術式:Classic ROPでは水晶体温存硝子体手術(LSV)が第一選択
成績:Stage 4A復位率74〜91%、Stage 4B 62〜92%、Stage 5 22〜48%1)
強膜バックリング
レーザー光凝固
Section titled “レーザー光凝固”1967年に永田が世界初の光凝固治療を実施して以来、ROPの標準治療として確立されてきた。無血管領域全体への光凝固が基本であり、倒像検眼鏡下に行う。著明な水晶体血管膜や瞳孔強直がある場合には施行困難なことがある。凝固に時間を要し術者の習熟が必要で、広範囲の凝固では視野狭窄や近視を来す可能性がある。
CRYO-ROP試験では、1年後の不良構造転帰が冷凍凝固群25.7%対観察群47.4%であり、15年後も有意差が持続した(30%対52%)8)。ETROP試験では早期治療により不良構造転帰が9.1%対15.6%に減少した9)。
抗VEGF療法
Section titled “抗VEGF療法”VEGFが網膜血管新生に関与することから、抗VEGF薬の硝子体内注射がROPに対して試みられている。2022年12月時点で国内承認されているROP治療用抗VEGF薬は以下の2剤である3)。
- ラニビズマブ(ルセンティス®):0.2 mg/回(0.02 mL)。2019年11月に国内承認。
- アフリベルセプト(アイリーア®):0.4 mg/回(0.01 mL)。2022年9月に国内承認。
いずれもバイアル製剤のみがROPに対して承認されており、再投与間隔は添付文書上1か月以上である3)。ベバシズマブは国内外でROPに対して未承認である3)。
主要臨床試験の成績
| 試験名 | 対象・薬剤 | 主な結果 |
|---|---|---|
| BEAT-ROP | zone I Stage 3+、ベバシズマブ0.625 mg | zone Iでの再発6%対レーザー42%5, 1) |
| RAINBOW | 出生体重1,500 g未満、ラニビズマブ0.2 mg | 治療成功率80.0%対レーザー66.2%。2歳時高度近視5%対20%6, 1) |
| FIREFLEYE | 在胎32週以下または1,500 g未満、アフリベルセプト0.4 mg | 成功率82.7%対レーザー84.2%。全身麻酔率44.0%対65.8%7, 1) |
再燃率の比較3):
- アフリベルセプト:再燃率13.9〜28%、再燃時期の平均11〜14.2週
- ラニビズマブ:再燃率20.8〜83.0%、再燃時期5.9〜9.3週(再燃がより早い)
ラニビズマブは注射後14日目には血中VEGF低下が検出されず、全身影響が少ないと考えられる。アフリベルセプトでは血漿中遊離型アフリベルセプトが注射後約8週で定量下限値まで低下する3)。
小児特有の注射手技3):
- 輪部から1.0〜1.5 mm後方で刺入(成人の3〜4 mmとは異なる点に注意)
- 水晶体が相対的に大きいため下方(後方)に向けて刺入。眼球中央方向は水晶体損傷リスクがある
- 30ゲージ以下の注射針を使用
- NICUの保育器内または手術室で施行
- 麻酔は点眼麻酔・経静脈麻酔・全身麻酔から施設に応じて選択
抗VEGF療法の目的は3つに大別される。第1にadjunctive therapy(硝子体手術前の時間稼ぎ)、第2にsalvage therapy(光凝固が奏功しない場合の網膜剥離進行予防)、第3にmonotherapy(光凝固の代替としての単独投与)である。monotherapy後はROPが鎮静化して無血管領域へ血管が成長することが報告されているが、長期にわたって増殖が再発する可能性がある(くすぶり網膜症)。
抗VEGF療法後の経過観察
Section titled “抗VEGF療法後の経過観察”抗VEGF療法後の観察スケジュールは以下を目安とする3)。
- 投与後1年間:可能な限り2週間に1回の眼底検査
- レーザー追加後またはzone IIIまで血管発達後:2〜3か月に1回
- A-ROPに対しては投与後2〜3週まで週2回、4か月頃まで週1回、以降1〜2週に1回
- 再燃判断はplus diseaseの再出現に注目し、ETROP基準に準じて追加治療を行う
- 蛍光眼底造影が再増殖の有無・範囲の把握に有用である
Stage 4以降の網膜剥離には外科的治療が必要となる。I型/classic ROPでは水晶体温存硝子体手術(lens-sparing vitrectomy; LSV)が行われ、良好な網膜復位率と視力予後が得られる。Stage 4Aでの早期手術が視力予後を左右する。II型/A-ROPでは血管線維増殖の活動性が高いためLSVが奏功しにくく、水晶体除去を要することが多い。
LSVの解剖学的成功率はStage 4Aで74〜91%、Stage 4Bで62〜92%、Stage 5で22〜48%と報告されている1)。期待される視力はStage 4A復位後20/80以上、Stage 4B修復後歩行視力、Stage 5修復後手動弁とされる1)。LSV後の白内障形成は10年以内では稀だが、発生時は術後1年以内が多い1)。
病変の部位と重症度によって選択する。抗VEGF療法の手引き(第2版)ではzone IやA-ROPには抗VEGF療法が有利とされ、zone II病変ではレーザーが依然として重要な選択肢である3)。抗VEGF療法はzone Iの重症例に施行容易・治療時間短・患児負担少という利点があるが、再燃率が高く長期の定期検査が必要というリスクもある。それぞれの利点・欠点を家族に説明したうえで選択する。
薬剤によって異なる。アフリベルセプトでは13.9〜28%、ラニビズマブでは20.8〜83.0%に再燃が報告されており、RAINBOW試験では31%が追加治療を要した3, 1)。A-ROPでは75.0〜87.5%に追加治療が必要であり、特に投与後早期からの厳密な観察が不可欠である。
7. 長期予後と合併症
Section titled “7. 長期予後と合併症”退縮と再活性化
Section titled “退縮と再活性化”ICROP3では退縮(regression)と再活性化(reactivation)の概念が正式に定義された2)。退縮は完全退縮と不完全退縮に分類される。抗VEGF後は1〜3日で血管変化の退縮が開始するが、レーザー後は7〜14日かかる。退縮の初期徴候はplus diseaseの改善と周辺無血管領域への血管伸展である。
不完全退縮後にpersistent avascular retina(PAR)が残存することがある。PARはレーザー後・自然退縮後と比べ、抗VEGF後のほうが頻度が高く範囲が広い2)。再活性化(reactivation)は抗VEGF療法後に多く、修正37〜60週に最多である。薬剤・用量により遅延しうる2)。
未治療ROPの晩期所見
Section titled “未治療ROPの晩期所見”多施設後方視研究(363眼・186例、平均年齢34.5歳、平均在胎26.6週、平均出生体重875 g)によると、未治療ROPの長期眼底所見として以下が報告されている4)。
- 格子状変性:196眼(54.0%)
- 萎縮性裂孔:126眼(34.7%)
- 網膜裂孔:111眼(30.6%)
- 網膜剥離:140眼(38.6%)
- 牽引性網膜分離症:44眼(12.1%)
- 黄斑牽引:44眼(12.1%)
網膜剥離のリスク因子として在胎29週以下(P < 0.05)とposterior zone 2までの血管化(P = 0.009)が有意であった4)。網膜剥離の86.4%が裂孔原性または混合型であり、57.9%が30歳までに発症した4)。剥離眼の20%(28/140眼)が初診時に修復不能と判断された4)。不完全血管化(zone 3非到達)が71.6%に認められた4)。
この結果から、未治療ROPの定期検査と超広角蛍光眼底造影による評価が推奨される4)。
レーザー光凝固後の高度近視は2歳時で20%、5年後で24%に生じる。ラニビズマブ0.2 mg群では2歳時で5%、5年後で8%と有意に少ない1)。早産児はROPとは独立して高度近視・黄斑異常(中心窩無血管帯の縮小・中心窩陥凹の鈍化・消失)のリスクを持つ。
眼圧上昇・緑内障
Section titled “眼圧上昇・緑内障”未治療自然退縮例で眼圧上昇が23.2%、焼灼治療単独では23.3%、急性期手術後では58.5%に認められる1)。Stage 5では66.7%、無水晶体眼では69.8%に眼圧上昇が認められる1)。進行したROP(stage 4-5)の10.0%が3年以内に緑内障を発症し、stage 5はstage 4Aの6.76倍、水晶体摘出術後は2.76倍のリスクとなる1)。
8. 最新の研究と今後の展望
Section titled “8. 最新の研究と今後の展望”PAR管理の今後
Section titled “PAR管理の今後”抗VEGF療法後のPARに対するレーザー光凝固の至適タイミングは未確立である1)。ベバシズマブ後の修正60週での予防的レーザーが不良構造転帰の低減に関連するとの後方視研究がある1)。蛍光眼底造影による再活性化リスク評価(修正60週時点)が有用と報告されている1)。
代替薬物療法
Section titled “代替薬物療法”- 経口プロプラノロール:2 mg/kg/日でstage 2 ROPの重症化予防効果が報告されているが、心呼吸器合併症リスクがある1)。局所プロプラノロール0.2%点眼はstage 1から開始した場合に安全かつ有効との報告がある1)。
- AA/DHA補充:Mega Donna Mega Trial(206例、在胎28週未満)でAA+DHA群の重症ROP発生率15.8%対対照群33.3%(50%減少)が報告された1)。
- カフェイン:未熟児無呼吸に対して投与されるカフェインが、VEGFとMMPの下方制御を介してROPの進行を抑制する可能性が示唆されている1)。
- コンベルセプト(KH902):中国で承認済み。ラニビズマブと同等の有効性で、再発率16.7%対23.3%(ラニビズマブ)と報告されている1)。
AI・テレメディシン
Section titled “AI・テレメディシン”深層学習モデルによるplus disease自動検出が専門医と同等の精度を達成している1)。血管重症度スコア(VSS)がplus disease重症度の客観的定量指標として開発されている1)。SUNDROPなどのテレメディシンプログラムが低中所得国を含む遠隔地でのスクリーニング拡大を実現しており、携帯型OCTによるベッドサイド評価も期待される1)。
9. 参考文献
Section titled “9. 参考文献”- Marra KV, Chen JS, Nudleman E, Robbins SL. Review of retinopathy of prematurity management in the anti-VEGF era: evolving global paradigms, persistent challenges and our AI-assisted future. Clin Exp Ophthalmol. 2025;(in press/online).
- Chiang MF, Quinn GE, Fielder AR, et al. International classification of retinopathy of prematurity, third edition. Ophthalmology. 2021;128(10):e51-e68.
- 日本眼科学会・日本小児眼科学会. 未熟児網膜症診療ガイドライン(第2版). 2024.
- Hamad AE, Moinuddin O, Blair MP, et al. Late-onset retinal findings and complications in untreated retinopathy of prematurity. Ophthalmology. 2020;127(2):240-248.
- Mintz-Hittner HA, Kennedy KA, Chuang AZ; BEAT-ROP Cooperative Group. Efficacy of intravitreal bevacizumab for stage 3+ retinopathy of prematurity. N Engl J Med. 2011;364(7):603-615.
- Stahl A, Lepore D, Fielder A, et al. Ranibizumab versus laser therapy for the treatment of very low birthweight infants with retinopathy of prematurity (RAINBOW): an open-label randomised controlled trial. Lancet. 2019;394(10208):1551-1559.
- Stahl A, Sukgen EA, Wu WC, et al. Effect of intravitreal aflibercept vs laser photocoagulation on treatment success of retinopathy of prematurity: the FIREFLEYE randomized clinical trial. JAMA. 2022;328(4):348-359.
- Cryotherapy for Retinopathy of Prematurity Cooperative Group. Multicenter trial of cryotherapy for retinopathy of prematurity: preliminary results. Arch Ophthalmol. 1988;106(4):471-479.
- Good WV, Hardy RJ, Dobson V, et al; Early Treatment for Retinopathy of Prematurity Cooperative Group. The incidence and course of retinopathy of prematurity: findings from the Early Treatment for Retinopathy of Prematurity Study. Pediatrics. 2005;116(1):15-23.
