前部型
主な所見:水晶体後面の線維増殖膜(Mittendorf斑)、後囊下白内障、後部水晶体円錐
治療適応:水晶体後部に限局し眼底正常であれば手術適応あり
予後:3型中で最も良好。中央値視力 20/100(視力20/200以上54%)1)

第一次硝子体過形成遺残(persistent fetal vasculature: PFV)は、胎生期の硝子体血管系の退縮不全によって生じる先天性眼疾患である。旧称は第一次硝子体過形成遺残(persistent hyperplastic primary vitreous: PHPV)と呼ばれていた。1997年にGoldbergが、水晶体周囲の血管線維組織の遺残も含めてPFVの名称を提唱し12)、現在広く受け入れられている。
硝子体血管系は視神経乳頭から発する硝子体動脈(hyaloid artery)と前方の水晶体血管膜(tunica vasculosa lentis)からなる。胎生第5〜6週に間葉細胞が胎生裂から硝子体腔に進入して形成され、胎生第10週が最盛期となる。その後、胎生13〜15週より末梢から退縮が始まり、胎生後期には消退する。PFVではこの退縮不全が生じ、血管周囲組織の発生異常が引き起こされる。
片眼性で非遺伝性とされており、病因となる特定の遺伝子は明らかにされていない。典型例は小眼球を伴う白色瞳孔で発見されるが、斜視や弱視を契機として診断される場合もある。
PFVは乳幼児・小児白内障の約20%に合併するとされる2)3)。Pediatric Eye Disease Investigator Group(PEDIG)の白内障レジストリ994例中64例(6.4%)がPFV合併白内障であり1)、75%が無水晶体として手術(手術時月齢中央値2か月)、25%が偽水晶体として手術(手術時年齢中央値29か月)されている1)。28%に後眼部異常(硝子体・網膜・視神経の異常)を認め1)、家族歴を有するのは4〜6%にすぎない1)。
本質的には同一疾患の新旧の名称の違いである。PHPVは旧来の呼称で、硝子体血管(第一次硝子体)の過形成と遺残に着目した名称であった。1997年にGoldbergが、水晶体周囲の血管線維組織の遺残も包括してPFV(persistent fetal vasculature)という名称を提唱した。PFVはより広い病変スペクトラムを表現できるため、現在の標準名称となっている。
PFVはほとんどの場合片眼性(unilateral)であり、非遺伝性とされる。PEDIG研究においても両側PFVは3例のみで除外されている1)。両眼性の場合は家族性滲出性硝子体網膜症(FEVR)やNorrie病との鑑別が必要であり、遺伝子検査を含む精査が推奨される。
PFVは病変部の優位性から前部型・後部型・混合型の3型に分類される。
前部型
主な所見:水晶体後面の線維増殖膜(Mittendorf斑)、後囊下白内障、後部水晶体円錐
治療適応:水晶体後部に限局し眼底正常であれば手術適応あり
予後:3型中で最も良好。中央値視力 20/100(視力20/200以上54%)1)
後部型
混合型
主な所見:前部型と後部型の所見が混在。小眼球を伴うことが多い
治療適応:個々の病変範囲に応じて慎重に判断
予後:重度混合型では測定可能視力は19%のみ、61%が光覚なし8)
| 病型 | 主な所見 | 合併しうる異常 |
|---|---|---|
| 1. 硝子体血管(動脈)遺残 | 乳頭→硝子体後部中央の白色〜灰色索状物+Mittendorf斑 | 後囊下白内障、後部水晶体円錐 |
| 2. 硝子体血管本幹主体型 | 乳頭から太い索状物が立ち上がる | 乳頭周囲網膜牽引 |
| 3. 乳頭上限局型 | 乳頭上に白色組織 | 周囲網膜牽引 |
| 4. 乳頭からの網膜ひだ | 眼底周辺部の増殖組織の牽引 | 周辺部網膜異常 |
| 5. 硝子体腔全体占拠型 | 広範囲増殖、網膜全剥離、網膜異形成 | 小眼球が多い |
| 6. 水晶体後部線維増殖主体型 | 水晶体後部に限局、眼底ほぼ正常 | 治療適応あり |
| 7. 水晶体前部型 | 水晶体血管膜の増殖による前方線維増殖 | 瞳孔変形、閉鎖 |
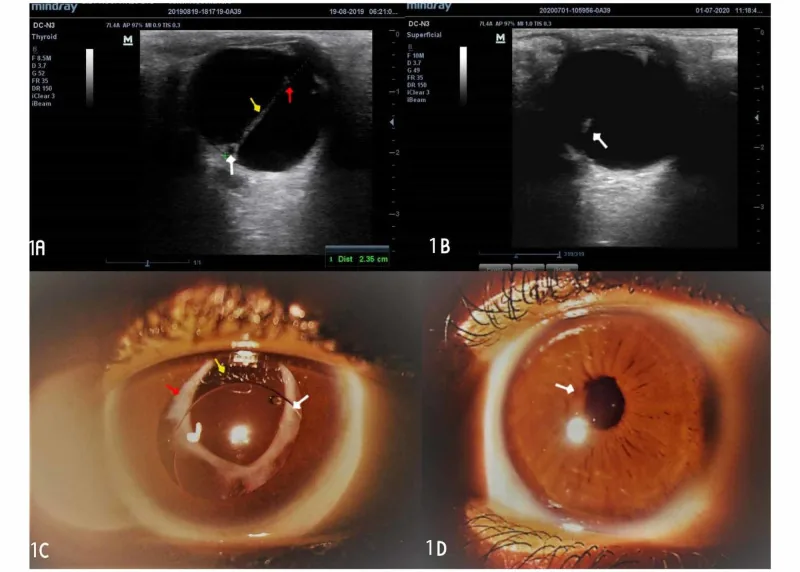
主な所見として片眼の小眼球、水晶体後面の混濁(Mittendorf斑)、網膜血管の走行異常、網膜異形成、延長した毛様体突起、水晶体後面から視神経乳頭に向かって伸びる索状物が認められる。索状物は牽引の原因となり、毛様体突起の延長を介して低眼圧をきたす。乳頭付近の索状組織に網膜が巻き込まれていることもある。硝子体血管退縮の程度により重症度が異なる。
PEDIG研究では、PFV白内障の28%(18/64眼)に後眼部異常を認め1)、偽水晶体眼の46%に後眼部病変があった(無水晶体眼28%との比較で年齢調整OR 4.47)1)。無水晶体PFV眼の96%で白内障手術時に前部硝子体切除が施行されている1)。
硝子体血管系の正常発達では、胎生第5〜6週に間葉細胞が胎生裂から硝子体腔に進入して硝子体血管系が形成される。胎生第10週が最盛期であり、その後末梢から退縮が始まる。具体的には胎生13〜15週より退縮が開始し、胎生後期には消退する。
PFVでは硝子体血管の退縮不全が生じ、血管周囲組織の発生異常が引き起こされる。この結果として水晶体混濁、網膜形成異常、小眼球が生じると考えられている。さらに遺残組織の牽引により毛様体突起の延長や網膜ひだが生じる。
PFVは片眼性・非遺伝性とされており、病因となる特定の遺伝子は同定されていない。家族歴を有するのは4〜6%にすぎず1)、ほとんどが散発性である。両眼性の場合はFEVR(NDP, LRP5, FZD4遺伝子変異)やNorrie病(NDP遺伝子変異)との遺伝的鑑別が重要となる。
低出生体重や早産との明確な関連は示されていないが、重度の硝子体血管遺残は稀に未熟児網膜症と類似した所見を呈することがある。
白色瞳孔を来す疾患との鑑別が最重要課題である。特に網膜芽細胞腫との鑑別は生命予後に直結する。
網膜芽細胞腫との鑑別
FEVRおよびNorrie病との鑑別
両眼性の場合に重要
両眼の網膜全剥離や水晶体後面線維増殖がある場合はFEVRやNorrie病との鑑別を要する。家族歴・遺伝子異常の検索が参考になる。次世代シークエンシング(NGS)パネル検査の活用が有用である。
| 疾患 | 側性 | 小眼球 | 遺伝性 | CT石灰化 | 特徴的所見 |
|---|---|---|---|---|---|
| PFV | ほぼ片眼性 | あり | 非遺伝性 | なし | 水晶体後面索状物、乳頭への線維膜 |
| 網膜芽細胞腫 | 70%片眼性 | なし | RB1変異(35–45%) | あり(特徴的) | 白色隆起腫瘤、硝子体播種 |
| FEVR | 両眼性 | なし | あり(FZD4等) | なし | 末梢網膜無血管野、牽引性網膜剥離 |
| Norrie病 | 両眼性 | ありうる | X連鎖劣性(NDP) | なし | 硝子体出血、網膜剥離、知的障害 |
| 未熟児網膜症 | 両眼性 | なし | なし | なし | 末梢網膜無血管野、血管増殖 |
透光体の混濁は白内障と同様に対応する。水晶体後部に限局し眼底に異常がなければ、先天白内障に準じて水晶体切除+線維増殖膜切除を行う。水晶体後面の索状物が視軸にかからず偏心していれば、必ずしも手術を要さない。眼底に病変が及んでいる場合は、一般的に手術の対象にならない。網膜剥離や牽引に対しては、ERG/VEPの反応が良好であれば外科的介入の根拠となる。水晶体前部の増殖で瞳孔変形・閉鎖がある場合は瞳孔形成術を行う。
水晶体除去ののちに屈折矯正と弱視治療を行う。術式は先天白内障に準じる。PEDIG研究では無水晶体PFV眼の96%で白内障手術時に前部硝子体切除が施行されており1)、初回手術時に前部硝子体切除を施行した場合の視軸混濁発症率は18%であるのに対し、施行しない場合は60%に上る1)。
術後は屈折矯正(コンタクトレンズまたは眼鏡)と健眼遮閉(アイパッチ)を組み合わせた弱視治療を行う。片眼性PFVでは弱視治療のコンプライアンスが視力予後を左右する。治療は視覚発達の臨界期(生後から10歳頃まで)に積極的に行う必要がある。
| 指標 | 無水晶体PFV眼 | 偽水晶体PFV眼 |
|---|---|---|
| 手術時年齢(中央値) | 月齢2か月 | 月齢29か月 |
| 5年時中央値視力 | 20/100(IQR 20/50–20/320) | 20/400(IQR 20/200–<20/800) |
| 視力20/200以上 | 59%(95%CI 39–76%) | 23%(95%CI 5–54%) |
| 年齢正常視力達成 | 10%(95%CI 2–27%) | 8%(95%CI 0–36%) |
| 緑内障関連有害事象(5年累積) | 24%(95%CI 9–37%) | 7%(95%CI 0–20%) |
| 視軸混濁 | 15%(95%CI 5–25%) | 45%(95%CI 13–66%) |
| 網膜剥離 | 4%(95%CI 0–10%) | 7%(95%CI 0–19%) |
全体の視力転帰として、42眼中4眼(10%、95%CI 3–23%)が年齢正常視力を達成し、48%(95%CI 32–64%)が視力20/200以上を達成した1)。偽水晶体PFV眼の視力20/200以上達成率(23%)は非PFV偽水晶体眼(68%)と比較して有意に不良であった(年齢調整OR=0.14、P=0.005)1)。無水晶体PFV眼は非PFV無水晶体眼と比較して同等の成績であった(年齢調整OR=1.90、P=0.14)1)。
病型別では、前部型の中央値視力は20/100(視力20/200以上54%)に対し、後部型の中央値視力は20/800(視力20/200以上36%)と不良であり、差は4 logMAR lines(P=0.09)であった1)。
他の報告では、Bataらの20年単施設研究(無水晶体PFV 58眼)で33%が視力20/200以上(平均追跡6.7年)4)、Antebyらの報告(無水晶体PFV 30眼)で16.7%が20/200以上(平均追跡8.5年)5)、de Saint Sauveurらの重度混合型PFV 36例では測定可能視力は19%のみ、61%が光覚なしと報告されている8)。
緑内障以外の主要合併症として視軸混濁(偽水晶体PFV眼の45%、無水晶体眼の15%)があり、視軸清明化手術の累積発症率は偽水晶体PFV眼で40%に達する1)。また、無水晶体PFV眼の13%(95%CI 2–22%)が5年以内に二次IOL挿入手術を要する1)。
網膜異形成には有効な治療方法はない。後眼部型では視力発達が見込めない場合が多い。顕著な小眼球に対しては整容面に配慮して早期から義眼装用を行う。義眼装用は眼窩発育の促進にも寄与する。
前部型(水晶体後部限局)では、術後5年で中央値視力20/100、視力20/200以上の達成率は54%とされる1)。ただし年齢正常視力を達成できるのは全体の10%にとどまる。後部型では中央値視力20/800と不良である1)。視力予後は病型・後眼部病変の有無・手術年齢・弱視治療のコンプライアンスが大きく影響する。
緑内障関連有害事象が最多であり、無水晶体PFV眼では5年累積発症率24%に達する1)。視軸混濁も重要な合併症であり、偽水晶体眼では45%に発症する1)。初回手術時の前部硝子体切除施行が視軸混濁の予防に重要(施行あり18%vs施行なし60%)1)。手術後も長期にわたる定期的な眼圧管理・視軸評価・屈折矯正が必要である。
胎生第5〜6週、間葉細胞が胎生裂(optic fissure)から硝子体腔に進入し、硝子体動脈(hyaloid artery)と水晶体血管膜(tunica vasculosa lentis)からなる硝子体血管系が形成される。この血管系は発達中の水晶体と眼球前節に酸素・栄養を供給する重要な役割を果たす。
胎生第10週が発達の最盛期であり、以後末梢から退縮が開始される。胎生13〜15週から退縮が本格化し、胎生後期にほぼ消退する。正常分娩時には硝子体血管系はほとんど認められないが、Mittendorf斑(水晶体後面に残存する小さな白点)として痕跡が残ることはある。
PFVでは硝子体血管の退縮不全が生じ、血管周囲の線維増殖組織の発生異常が引き起こされる。遺残した血管周囲の間葉系組織は増殖・線維化し、さまざまな臨床所見を呈する。
具体的な結果として以下が生じる。
片眼性・非遺伝性である理由として、胎生期の硝子体血管退縮は局所の血管新生・退縮シグナルによって制御されており、この制御機構の片眼のみの障害が想定されている。ただし具体的な分子機序は未解明である。
PFVの特定の原因遺伝子は未同定であるが、動物モデルでFZD4・LRP5・NDP等のWntシグナリング経路関連遺伝子の変異がPFV様表現型(硝子体血管遺残)を示すことが報告されている。これらはFEVRやNorrie病の原因遺伝子でもあり、PFVと関連疾患の遺伝的連続性を示唆する。次世代シークエンシング(NGS)パネル検査のPFV鑑別診断への臨床応用も進展している。
25ゲージ・27ゲージの極小切開硝子体手術(microincision vitreous surgery: MIVS)による後部型PFVへのアプローチが試みられている。新生児・乳児を対象とした小切開手術は侵襲を最小化し、術後炎症を抑制する利点があるとされる11)。
乳児期のIOL一期挿入 vs 無水晶体管理後の二次IOL挿入の長期成績比較がPFV研究の重要課題である。PEDIG研究の延長フォローデータにより、PFV特有のIOL挿入適応基準の確立が期待されている6)7)。
広角眼底カメラ・前眼部OCTによるPFVの非侵襲的評価が進歩している。特に前眼部OCTは後部水晶体円錐や後囊下白内障の形態評価、術前計画に有用である。