初期の症状
白色瞳孔(leukocoria):最多の初発症状。眼内で腫瘍が大きくなり、瞳孔が白く光って見える状態。
斜視:黄斑部に生じた腫瘍による視力不良が原因。視力不良眼が外側に偏位する。
視力低下の自覚:年長児で認められる。
眼をこするしぐさ:幼少児で視力不良眼に認められる。

網膜芽細胞腫は乳幼児の網膜に生じる悪性腫瘍である。幼若な網膜細胞ががん化・増殖し腫瘤を形成した状態であり、13番染色体長腕(13q14.2)に座位するRB1遺伝子の変異が原因の単一遺伝子疾患と考えられている。性差はなく、5歳までに95%が診断される。
発生頻度は15,000〜23,000出生に1人であり、日本では年間70〜80名が発症している。片側性と両側性の比率は3:2であり、診断時期は片側性が平均21か月、両側性が平均8か月と早期に診断される傾向がある。先進国における5年生存率は眼球内限局期で95%以上と良好である。
網膜芽細胞腫は遺伝子変異の種類によって2つに大別される。
| 分類 | 変異の種類 | 病態の特徴 | 遺伝リスク |
|---|---|---|---|
| 遺伝性(germline変異) | 生殖細胞系列のRB1変異 | 両側性・多発腫瘍が多い | 子の50%に遺伝 |
| 非遺伝性(somatic変異) | 1網膜細胞での体細胞変異 | 片眼性・単発腫瘍 | 次世代への遺伝なし |
遺伝性(germline mutation): 体のすべての細胞に第1ヒットの変異が存在する状態。第2ヒットが生じると発癌する。両側性・多発腫瘍を生じやすく、子どもの2人に1人(50%)に遺伝する。骨肉腫などの二次がん(20年で15.7%)のリスクがある。
非遺伝性(somatic mutation): 網膜の1細胞においてRB1遺伝子の両方の遺伝子座に変異が生じた場合。片眼性・単発腫瘍の形態をとり、次世代への遺伝リスクはない。
ただし、片眼性症例でも一部に生殖細胞系列RB1変異が含まれる。片眼性だからといって遺伝性を否定せず、遺伝カウンセリングと遺伝学的評価を前提に家族歴・発症年齢・腫瘍数を解釈する必要がある。1)
病期分類は眼球温存治療の方針に直結する。
| 病期 | 病変の状態 | 眼球温存率の目安 |
|---|---|---|
| T1(眼内初期病変) | 眼内限局、進行なし | 90%以上 |
| T2(眼内進行期病変) | 眼内進行 | 約50% |
| T3 | 眼外浸潤を伴う進行病変 | 約10% |
約40%が遺伝性(生殖細胞系列RB1変異)であり、50%の確率で子に遺伝する。残り約60%は非遺伝性(体細胞変異のみ)で次世代への遺伝リスクはない。遺伝性では両側性・多発の傾向がある。診断時に遺伝子検査を行い、遺伝カウンセリングを受けることが推奨される。
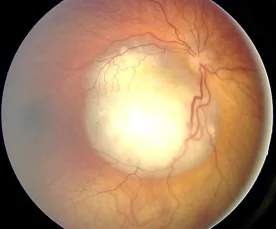
多くの場合は眼内で大きな腫瘍になり、白色瞳孔(leukocoria)を呈して発見される。黄斑部に生じた場合には視力不良で斜視になり発見されることがある。年長児であれば視力低下の自覚、幼少児では低視力の眼をこするしぐさが初発症状となることもある。
初期の症状
白色瞳孔(leukocoria):最多の初発症状。眼内で腫瘍が大きくなり、瞳孔が白く光って見える状態。
斜視:黄斑部に生じた腫瘍による視力不良が原因。視力不良眼が外側に偏位する。
視力低下の自覚:年長児で認められる。
眼をこするしぐさ:幼少児で視力不良眼に認められる。
進行期の症状
血管に富む白色隆起病変が認められ、石灰化を伴う場合には確定診断が容易である。硝子体播種(腫瘍細胞が崩れて硝子体へ散布した状態)を伴うことが多い。
Red reflex法は乳幼児の眼疾患スクリーニングの基本である。判定は両眼の瞳孔の大きさが等しく、明るく対称的な黄橙色であれば正常である。反射が暗かったり明るすぎたりした場合、または左右で差がある場合は異常として精査が必要である。
白色瞳孔の原因は網膜芽細胞腫以外にも、胎児血管遺残(第一次硝子体過形成遺残)、未熟児網膜症、Coats病など多数ある。しかし白色瞳孔を認めた場合は速やかに眼科受診し、網膜芽細胞腫を除外することが最優先である。診断の遅れは予後に直結するため、疑いがあれば即日紹介が望ましい。
13番染色体長腕(13q14.2)にあるRB1遺伝子の変異が原因である。RB1遺伝子は細胞分裂の制御に重要な役割を担うRB1蛋白(網膜芽細胞腫蛋白)を産生する。
1細胞内には2つの遺伝子座があり、一方の変異だけでは細胞機能は維持されるが、両方の変異を生じると細胞分裂を制御できなくなり悪性化する(2段階発癌説、Knudson仮説)。
家族歴が最大のリスク因子である。AAOOP(米国眼科腫瘍・病理学会)の推奨でのリスク定義を以下に示す1)。
| リスク分類 | 定義 | リスク値 |
|---|---|---|
| High | 親が両側性Rb、または1〜2親等に生殖細胞系列RB1変異キャリア | >7.5% |
| Intermediate | 親が片側性Rb | 約7.5% |
| Low | その他の遠縁家族歴 | <1% |
遺伝性症例では二次がんのリスクに注意が必要である。骨肉腫などが代表的であり、遺伝性症例において20年で15.7%に発生する。二次がんは10歳代以降に発症することが多い。
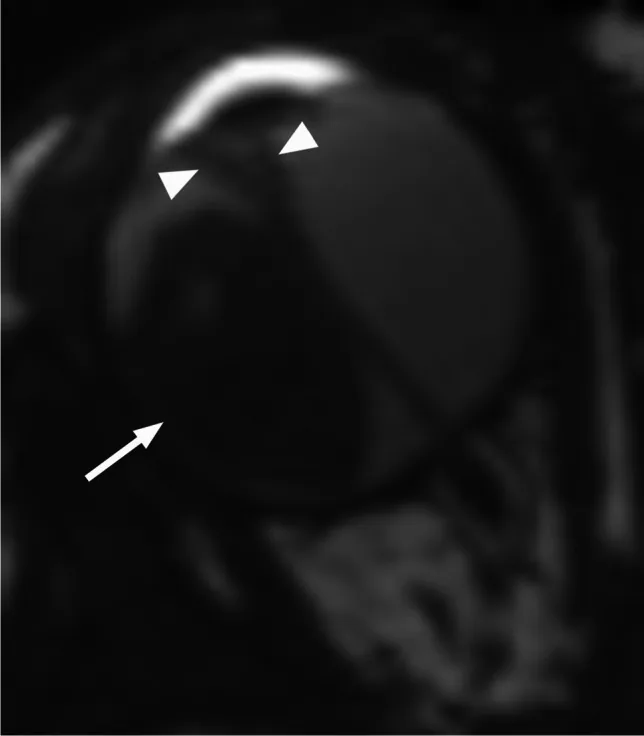
眼内腫瘍の生検は行わない。眼内病変は透明組織を通して直接観察可能であり、臨床診断の確度が高い。また眼内腫瘍の生検を行うと腫瘍細胞の眼球外撒布を生じ、転移のリスクが避けられないためである。眼球温存治療を行う場合は臨床診断に基づいて治療を開始する。
白色瞳孔をきたす疾患の鑑別が最重要である。
家族性Rbを有する小児のスクリーニングについて、AAOOP推奨2018が国際的に広く参照されている1)。
| リスク | スクリーニングスケジュール | 終了時期 |
|---|---|---|
| High(>7.5%) | 出生〜8週: 2〜4週毎 → 8〜12週: 月1回 → 1〜2歳: 2か月毎 → 2〜3歳: 3か月毎 → 3〜4歳: 4か月毎 → 4〜7歳: 6か月毎 | 7歳(RB1変異保持者は生涯) |
| Intermediate(1〜7.5%) | 出生〜3か月: 月1回 → 漸減 | 7歳 |
| Low(<1%) | 出生〜3か月: 月1回 → 漸減 | 7歳 |
オランダ全国データの後ろ向きコホート研究(1991〜2019年、332名中38名が家族性Rb)では、完全スクリーニングを受けた28名は全員1歳未満で診断(中央値18日)されたのに対し、不完全スクリーニングの10名では中央値420日(59日〜4.8歳)と大幅に遅れた2)。また低リスク群(<3%)のスクリーニング終了年齢を2歳に短縮するプロトコル改訂も提案されている2)。
家族性症例では、出生直後からの眼底スクリーニング継続そのものが予後に直結する。古典的登録研究でも、家系内発症の診断時期はスクリーニング頻度と密接に関連し、現在はRB1変異の有無を組み合わせて終了時期を個別化する方向へ進んでいる。1, 2)
AAOOP推奨では7歳まで定期的な眼底検査を推奨している。完全スクリーニングを行った場合、ほとんどは1歳未満で診断される。遺伝子検査でRB1変異リスクが否定されれば検診の早期終了も可能である。RB1変異保持者は7歳以降も1〜2年毎の不定期経過観察が推奨される。
眼内初期病変で視機能も期待できる場合には眼球温存治療を積極的に行う。眼内進行期では視機能が期待できないことも多いが、家族の希望があれば温存治療を検討する。治療は高度な専門性を要し、早期に専門施設への紹介が重要である。
① レーザー治療(光凝固)
腫瘍径3mm程度までの腫瘍が対象。赤外線レーザーの直接照射により90%程度の局所制御が可能である。黄斑部に腫瘍のある場合は、不可逆の視機能障害を回避するために全身化学療法を先行することが推奨される。
② 冷凍凝固
赤道部より周辺の3mm程度の腫瘍が治療対象。凍結・融解を3回繰り返すtriple freeze-thaw法が一般的であり、レーザーと同様に90%程度の局所制御が得られる。
③ 小線源治療
腫瘍厚5mm以下・横径15mm以下で、視神経乳頭から離れた限局腫瘍が対象。日本および欧州では¹⁰⁶Ru(ルテニウム-106、β線源)、北米では¹²⁵I線源が用いられる。腫瘍に対応する強膜面に一時的に線源を縫着する治療であり、特殊治療室が必要で施設が限定される。80〜90%の局所制御が可能である。
④ 全身化学療法(VEC療法)
眼球内進行期腫瘍に対して第一選択として行われる。3剤併用化学療法が広く行われており、単独治療で治癒するのは10%以下。腫瘍縮小後に局所治療(レーザー・冷凍凝固・小線源治療)で地固めを行う。
| 薬剤 | 用量(体表面積基準) | 用量(36か月以下の体重基準) | 投与スケジュール |
|---|---|---|---|
| ビンクリスチン(オンコビン®) | 1.5 mg/m² | 0.05 mg/kg | day1 |
| カルボプラチン(パラプラチン®) | 560 mg/m² | 18.6 mg/kg | day1 |
| エトポシド(ベプシド®) | 150 mg/m² | 5 mg/kg | day1, 2 |
3〜4週ごとに2〜6回繰り返す(いずれも点滴静注)。
⑤ 選択的眼動脈注入(IAC)
カテーテルを用いて眼動脈へ直接薬剤(メルファラン;アルケラン®注射液)を投与する。眼球局所へ多くの薬剤を投与し、全身への薬剤量を減らすことで骨髄抑制などの副作用を軽減できる。保険適用外であるが、世界20か国以上で実施されている研究的治療である。
⑥ 硝子体注入
硝子体播種に対して、全身化学療法・動脈注入の治療効果は限定的であるため、メルファラン(アルケラン®注射液)の硝子体注入を併用する。保険適用外の研究的治療である。
⑦ 放射線外照射
40〜46Gyのx線を分割照射する。1990年代までは眼球温存治療の主軸であったが、眼窩骨の変形・二次がんの増加が明らかとなり、現在では他治療で制御できない場合に限定して行われている。
以下の場合には眼球摘出を行うことが推奨される。視神経を長く切除するように心掛ける。
視神経断端陽性・強膜外浸潤は後療法の絶対適応であり、全身化学療法と放射線治療を行う。著明な脈絡膜浸潤・篩状板を越える視神経浸潤などは転移の相対的リスク因子として評価する。
眼球温存が可能な条件
眼球摘出が必要な条件
眼内初期病変(T1)では90%以上の眼球温存が可能である。全身化学療法(VEC療法)で腫瘍を縮小し、レーザー・冷凍凝固・小線源治療で地固めを行う。進行例(T3)では眼球温存率が約10%となり、眼球摘出が必要となる場合がある。治療法の選択は病期と視機能の見込みに基づき専門医が判断する。
13番染色体長腕(13q14.2)にあるRB1遺伝子は、細胞分裂の制御に重要な役割を担うRB1蛋白(pRb)をコードする。pRbはE2F転写因子に結合して細胞周期のG1/S移行を抑制することで、細胞増殖を制御する腫瘍抑制蛋白である。
Knudsonが提唱した2段階発癌説では、1細胞内のRB1遺伝子の2つの遺伝子座がともに不活化されることで悪性化が生じるとされる。
遺伝性症例では、全身の細胞にRB1の第1ヒットが存在する。網膜以外の細胞(骨・軟部組織など)で第2ヒットが生じると二次原発悪性腫瘍が発症する。骨肉腫が最多であり、10歳代以降に発症することが多い。放射線外照射を受けた遺伝性症例では二次がん発生リスクがさらに高まるため、放射線外照射は現在では限定的使用とされている。
IAC(intra-arterial chemotherapy)はメルファランを眼動脈に直接注入することで、全身毒性を最小化しながら眼球内への高濃度薬剤送達を実現する。硝子体播種を有する進行例でも眼球温存の機会を広げることができる。現在も大規模コホートでの長期成績評価が進行中である。
硝子体播種への対応として硝子体内メルファラン注入が実施されているが、国際的な用量・投与間隔のプロトコル標準化が課題である。複数の症例シリーズで高い播種制御率が報告されており、今後の前向き試験による位置づけの確立が期待される。
オランダコホート研究では、完全スクリーニングの受診と早期診断(中央値18日)の相関が明確に示され、スクリーニング中断の弊害が定量化された2)。また低リスク群のスクリーニング終了年齢の短縮(2歳)に関する提案など、リスク層別化に基づいたプロトコルの最適化が進んでいる2)。AAOOP推奨の世界的普及と地域別プロトコルの標準化が今後の課題である1)。
まれではあるが、先天性脳奇形や染色体異常を背景に網膜芽細胞腫が併存する症例報告がある。Dandy-Walker症候群を伴う両側性網膜芽細胞腫の報告では、眼症状だけでなく神経発達背景を含めた全身評価の重要性が示されている。4)
次世代シーケンシング(NGS)の普及により、生殖細胞系列RB1変異の検出感度が向上している。液体生検(血中循環腫瘍DNA)を用いたモニタリングの可能性も研究されており、侵襲的な生検を回避した予後層別化への応用が期待される。
遺伝性網膜芽細胞腫の長期サバイバーを対象とした二次がんサーベイランスプロトコルの標準化が求められている。特に全身MRIを用いた多臓器スクリーニングの実施頻度・終了時期については、継続的なコホート研究による根拠の蓄積が進められている。
選択的眼動脈注入(IAC)と硝子体内化学療法(IVitC)は、進行例や硝子体播種例の眼球温存率を押し上げた治療として国際的に定着しつつある。保存的治療の総説では、転移リスクを悪化させずに眼球温存を拡張する戦略として位置づけられており、各国の導入状況と専門施設集約化が成績に影響する。5)
先進国の5年生存率95%以上に対して、アフリカ・アジアの低・中所得国では25〜70%にとどまるとの報告がある。系統的レビューと国の所得レベル別解析では、生存率と眼球温存率の格差が一貫して示されており、遅発診断・医療アクセス不足・専門施設不足が主な要因とされる。Red reflex法を含む地域密着型スクリーニングプログラムの普及が国際的課題である。6, 7)