周辺部型
頻度:多くを占める典型的な病型。
眼底所見:眼底周辺部に橙赤色円形の腫瘤を形成。著明に拡張・蛇行した流入動脈と流出静脈を伴う。
進行:毛細血管瘤→腫瘍の明確化→滲出性変化→滲出性網膜剥離→線維増殖と段階的に進行する。

網膜毛細血管腫(retinal capillary hemangioma)は、若年者の網膜もしくは視神経乳頭に生じる橙色の良性腫瘍である。脳血管芽腫と病理学的相同性があるため、近年では網膜血管芽腫(retinal hemangioblastoma)とも呼ばれる。単発性/多発性、片眼性/両眼性、孤発性/症候性に生じる。
孤発性に網膜血管芽腫のみが生じた場合をVon Hippel病と呼称する。全身性腫瘍症候群を伴う場合はVHL病(von Hippel-Lindau病)と診断される。日本眼科学会の用語集ではVHL診療の手引き(2024年版)に準拠し「網膜血管腫」と記載されているが、本記事では一般的な呼称として「網膜毛細血管腫」を用いる。
VHL病は、癌抑制遺伝子であるVHL遺伝子(3p25-26)の変異を原因とする常染色体顕性遺伝の遺伝性腫瘍症候群である。頻度は3万6千人に1人とされる。VHL病では網膜血管腫のほか、小脳・延髄・橋・脊髄の血管芽腫、腎細胞癌、褐色細胞腫、腹部臓器(膵・腎・副腎)の嚢胞など多臓器に病変を合併する。生命予後は全身病変の管理にも依存するため、多診療科連携が必須である。
VHL診療の手引き(2024年版)による診断基準では、家族歴がある場合は血管芽腫・網膜血管腫など1病変以上で診断される1)。家族歴がない場合は、2病変以上(血管芽腫または網膜血管腫を含む)、もしくはVHL遺伝子変異の確認+1病変で診断される。若年者の孤発性網膜血管腫、特に10歳未満では後にVHL病と診断されることが多いため、全身検索と遺伝子検査を積極的に検討する。
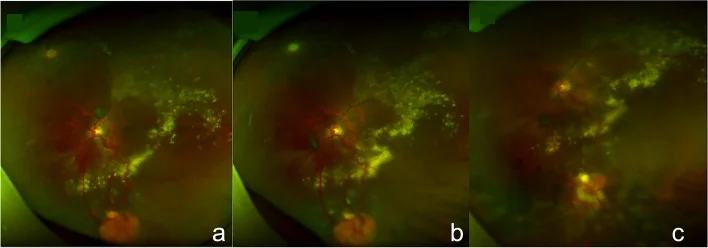
網膜血管芽腫は発生様式と部位によって以下のように分類される。
周辺部型
頻度:多くを占める典型的な病型。
眼底所見:眼底周辺部に橙赤色円形の腫瘤を形成。著明に拡張・蛇行した流入動脈と流出静脈を伴う。
進行:毛細血管瘤→腫瘍の明確化→滲出性変化→滲出性網膜剥離→線維増殖と段階的に進行する。
視神経乳頭型
頻度:全体の約15%。
眼底所見:視神経乳頭近傍に発生。流入・流出血管の同定が困難なことが多い。
予後:50%以上の症例で視力0.1以下となる予後不良の病型。治療法は未確立である。
初期は無症状のことが多い。病変が進行すると以下の症状が出現する。
出血は稀であるが、進行例では硝子体出血が生じることもある。
眼底所見として、孤立性または多発性の円形網膜腫瘤が特徴的である。周辺部のものは拡張・蛇行した流入・流出血管を伴い、病変は通常30歳までに出現する。約半数が両眼性であり、多発性に眼底のさまざまな部位に生じることもある。
腫瘤自体は毛細血管と泡沫状間質細胞から構成される血管芽細胞腫であり、多量のVEGF(血管内皮増殖因子)を産生する。VEGFにより滲出性網膜剥離が生じ、視力低下をきたす。
蛍光眼底造影では特徴的な3段階の変化が認められる。
進行すると以下の重篤な病態に移行する。
広角眼底撮影やOCT血管造影(OCTA)は、病変の評価と経過観察に有用である1)。OCTでは腫瘤の形態、網膜下液の有無、黄斑浮腫の評価が可能である。
VHL病の頻度は3万6千人に1人である。日本のVHL患者数は600〜1,000例と推定されている。VHL患者における網膜血管腫の発症頻度は40〜70%であり、平均発症年齢は25歳とされる1)。
VHL遺伝子は常染色体顕性遺伝(旧称:常染色体優性遺伝)の形式をとる。VHL遺伝子変異が一方のアレルに生殖細胞系列変異(1st hit)として存在し、体細胞での2nd hitにより腫瘍抑制機能が失われる(2-hit仮説)。
遺伝学的リスク因子として、VHL遺伝子の病原性変異を保有する家系では全員にサーベイランスが必要であり、40歳未満の網膜血管腫症例にはVHL遺伝子検査の適応を考慮する1)。
VHL診療の手引き(2024年版)に基づく診断基準は以下の通りである1)。
| 状況 | 診断基準 |
|---|---|
| 家族歴あり | 血管芽腫・網膜血管腫など1病変以上 |
| 家族歴なし | 2病変以上(血管芽腫/網膜血管腫含む)またはVHL遺伝子変異+1病変 |
眼底検査において、周辺部の橙赤色腫瘤と拡張・蛇行した流入・流出血管の組み合わせが特徴的である。以下の検査を組み合わせて評価する。
VHL家系では出生直後(0歳)から眼底検査を開始し、最低年1回の定期検査を継続する1)。無散瞳眼底カメラと広角眼底撮影を組み合わせることで、周辺部病変の見落としを防ぐ。
VHL病では網膜以外の臓器に複数の病変が生じうるため、多職種による定期的な全身検索が必須である1)。
VHL遺伝子検査は、40歳未満の孤発性網膜血管腫症例や、VHL病が疑われる患者・その家族に適応される1)。遺伝カウンセリングと並行して実施することが望ましい。
以下の疾患との鑑別が必要である。
周辺部型は眼底周辺部に多く生じるため、散瞳下での詳細な眼底検査が必要である。初期の小さな腫瘍は毛細血管瘤様の外観を呈することもあり、広角眼底撮影を活用することで見落としを防ぐことができる。視神経乳頭型は乳頭周囲の腫瘤として出現し、流入・流出血管の同定が困難なことが多い。
血管腫の位置・大きさ・滲出性変化の程度に応じて治療法を選択する。血管腫が増大すると難治となるため、早期発見・早期治療が重要である。病変が小さいうちに治療を開始することで視機能予後の改善が期待できる。
レーザー光凝固
適応:周辺部型の第一選択。1乳頭径大以下では根治が期待できる。
方法:血管腫の直接凝固を十分な効果が得られるまで繰り返し施行する。1乳頭径未満の小病変にも早期光凝固を推奨する1)。
限界:1乳頭径を超える大型病変では複数回の治療が必要となる。
冷凍凝固
適応:大型病変や、レーザー光凝固の到達が困難な症例。
方法:血管腫の大きさや突出の程度に応じて冷凍凝固を選択する。
滲出性変化合併時:網膜下液排液・ジアテルミーなどを併施するが難治である。
牽引性網膜剥離:線維増殖が進行し牽引性網膜剥離をきたした場合には硝子体手術を施行する。
PDT・抗VEGF療法:近年、光線力学的療法(PDT)と抗VEGF薬(ベバシズマブ・ラニビズマブ等)の単独および併用療法の症例報告が蓄積している3)。滲出性変化の補助的な抑制に用いられるが、保険適用外であり症例ごとの判断が必要である。
視神経乳頭型は治療法が未確立である1)。レーザー光凝固は視神経・黄斑障害のリスクが高く、適応の判断が特に慎重に求められる。以下の治療法が症例報告レベルで報告されているが、いずれも標準治療としては確立されていない。
介入タイミングの慎重な判断が必要であり、専門施設での多職種カンファレンスが推奨される。
治療後も再発・新病変が出現しやすいため、生涯にわたる経過観察が必要である。各治療後は効果確認のため3〜6ヶ月以内に眼底検査を実施し、新病変の有無を確認する。VHL病では複数の病変が時間差で出現するため、全周の眼底検索を怠らない。
VHL病の生命予後には腎細胞癌・中枢神経系血管芽腫の管理が重要である。脳神経外科・泌尿器科・内分泌科等との多診療科連携のもと、各臓器病変に対して適切なサーベイランスと介入を行う。
VHL遺伝子は染色体3p25-26に位置する癌抑制遺伝子であり、E3ユビキチンリガーゼ複合体の構成成分であるpVHL蛋白をコードする。pVHL蛋白の主な機能は低酸素誘導因子(HIF)α鎖のユビキチン化・プロテアソーム分解である。
正常条件下では、HIFαはpVHLにより認識されてユビキチン化され、速やかに分解される。VHL遺伝子が不活性化されるとpVHL機能が失われ、HIFαが蓄積する。
VHL病では生殖細胞系列変異(1st hit)に加え、体細胞での2nd hit(LOH: heterozygosity の喪失など)によってVHL遺伝子機能が完全に喪失し、腫瘍が形成される。
HIFαが核内に蓄積すると、VEGF・PDGF・EPOなど多数の血管新生・細胞増殖関連遺伝子の転写が恒常的に活性化される。VHL病ではHIF-2α(EPAS1)が主要なdriverとして機能する1)。
網膜血管芽腫は2種類の細胞で構成される。
この間質細胞が腫瘍の本体であり、VEGFの恒常的産生が腫瘍の血管増生と滲出性網膜剥離の直接的原因となる。
VHL遺伝子の変異型と臨床表現型の関連(Type 1: 非褐色細胞腫型、Type 2: 褐色細胞腫合併型など)は一部知られているが、詳細な型分類と眼病変の頻度差については今後のさらなる解析が待たれる。
belzutifanはHIF-2αを選択的に阻害する低分子化合物であり、2021年にFDA(米国食品医薬品局)が転移性腎細胞癌・中枢神経系血管芽腫・網膜血管芽腫を有するVHL病患者に対して承認した7)。
第2相試験(LITESPARK-004)での網膜血管腫に対する成績は以下の通りである1)。
主な有害事象として貧血(約90%)・倦怠感(約66%)が報告されている。日本での治験も予定されており、今後の標準治療候補として注目される1)。
Jonaschら(2021)が報告した第2相試験では、belzutifan 120 mgを1日1回経口投与したVHL病患者において、網膜血管芽腫に対して100%の縮小効果が確認された7)。
光線力学的療法(PDT)は周辺部・視神経乳頭型いずれの病型にも適応が報告されている。
di Nicolaら(2022)は、網膜血管芽腫に対するPDT療法の有効性を報告し、特に傍視神経乳頭型への適用可能性を示した4)。 Schmidt-ErfurthらはPDTの視神経乳頭型への適用可能性と合併症リスクを評価した6)。
Hussainらは傍視神経乳頭型の網膜毛細血管腫に対する陽子線治療の効果を報告した5)。治療困難な視神経乳頭型への選択肢として症例集積が進んでいる。
腫瘍の直接縮小効果は限定的であるが、滲出性変化の補助的コントロールとして使用される症例の報告が増えている1)。プロトコールは確立されておらず、症例ごとの判断が必要である。
2026年4月時点では、belzutifanは日本での一般的な使用は認められていない。FDAは2021年に承認しているが、日本では治験の準備段階にある1)。VHL病と診断された患者で標準治療が困難な場合は、治験参加の可能性について主治医・専門施設に相談することを検討する。