表層型(イチゴ状血管腫)
濃赤色の境界鮮明な腫瘤:皮膚表面に半球状に隆起し、鮮やかな赤色を呈する典型的な外観。
皮膚表面・結膜の網状血管走行:皮膚表面および結膜面に網目状の血管走行がみられる。霰粒腫との鑑別点となる重要な所見。
非典型例:色調変化が小さく隆起も軽度なタイプも存在する。

眼瞼の血管腫は、血管内皮細胞の増殖による良性腫瘍であり、乳児期に発生するものを乳児血管腫(infantile hemangioma)という。従来は「苺状血管腫」や「毛細血管腫」と呼ばれていたが、現在はISSVA分類(国際血管奇形研究学会、2018改訂)2)に基づいて乳児血管腫と分類される。一方、従来の「海綿状血管腫」は乳児血管腫とは異なる病態であり、「静脈奇形」として血管奇形に分類される。
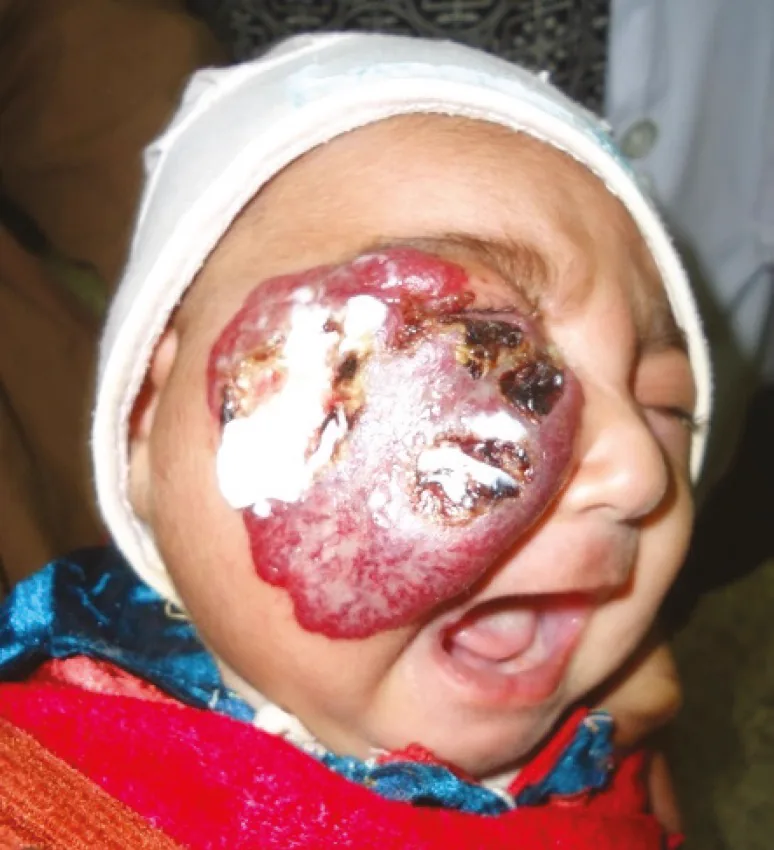
乳児血管腫は先天性であり、生後2週頃から増殖が始まる。1〜2か月で増殖のピークを迎え、1歳半頃まで増大が続く。その後、数年かけて縮小していく。70%は就学前後までに自然消退する。まれに急激に増大し眼瞼全体に浸潤して開瞼困難となる例もある。
ISSVA分類(2018)2)は血管性病変を「血管性腫瘍」と「血管奇形」に大別する。乳児血管腫は血管内皮細胞の真の増殖による腫瘍であり「血管性腫瘍」に分類される。一方、静脈奇形は血管の形成異常であり「血管奇形」に分類される。両者は発生機序・自然経過・治療方針が異なるため、正確な分類が治療選択に重要である。
乳児血管腫の70%は就学前後までに自然消退する。生後2週頃から増大が始まり1歳半頃まで増大した後、数年かけて縮小する経過をたどる。ただし、開瞼困難をきたすほど大型の病変は形態覚遮断弱視の原因となるため、自然消退を待たずに早期治療が必要な場合がある。静脈奇形(旧称:海綿状血管腫)は自然消退しないため、管理方針が異なる。
乳児血管腫は乳児に発生するため、自覚症状は保護者の観察による。
乳児血管腫は発生部位によって表層型・深在型・混合型に分けられる。
表層型(イチゴ状血管腫)
濃赤色の境界鮮明な腫瘤:皮膚表面に半球状に隆起し、鮮やかな赤色を呈する典型的な外観。
皮膚表面・結膜の網状血管走行:皮膚表面および結膜面に網目状の血管走行がみられる。霰粒腫との鑑別点となる重要な所見。
非典型例:色調変化が小さく隆起も軽度なタイプも存在する。
深在型(皮下型)
皮下深層発生:皮膚表面の発赤は目立たず、皮下に腫瘤を触知する。
青紫色の皮膚変色:静脈血の透見により皮膚が青紫色を呈する。境界は不鮮明。
混合型:表層型と深在型が合併する例(混合型)もある。
生後より赤色で境界明瞭な隆起性病変として現れるのが典型的な乳児血管腫の臨床像である。眼瞼を翻転して結膜側も観察し、網状血管走行の有無を確認することが診断上重要である。
乳児血管腫は血管内皮細胞の増殖によって生じる。VEGF(血管内皮増殖因子)が増殖に関与することが示されており、これはプロプラノロールの作用機序の根拠にもなっている。
GLUT-1(グルコーストランスポーター1)は乳児血管腫に特徴的な免疫組織化学マーカーである3)。胎盤微小血管と共通の免疫表現型を示し、静脈奇形ではGLUT-1が陰性である。この特性は病理組織診断における鑑別に利用される。
多くの症例では臨床所見のみで診断が可能である。
以上の3点が揃えば、臨床的に乳児血管腫と診断できる。
深在型や眼窩進展が疑われる場合に施行する。
臨床診断が困難な場合や悪性を除外する目的で施行する。
| 鑑別疾患 | 鑑別のポイント |
|---|---|
| 眼瞼リンパ管腫 | 自然寛解なし、眼表層・眼窩深部に発生、GLUT-1陰性 |
| 霰粒腫 | 皮膚表面の血管走行なし、血流シグナルなし |
| カポジ型血管内皮腫 | 消費性凝固障害(Kasabach-Merritt症候群)を合併 |
| 横紋筋肉腫 | 急速増大、生後より遅い発症(乳幼児〜学童期) |
| 母斑症 | 初期より一定の病変範囲、増大傾向なし |
自然退縮の傾向が高いため、多くの症例は経過観察が第一選択である。以下のいずれかに該当する場合は積極的治療を検討する。
弱視リスクがある場合は早期(生後5週〜5か月が至適)にプロプラノロールを開始する7)。
| 治療法 | 適応 | 備考 |
|---|---|---|
| 経過観察 | 弱視リスクなし・小型病変 | 70%は就学前消退 |
| プロプラノロール内服 | 第一選択(中〜大型) | 2〜3 mg/kg/日、小児科管理下 |
| チモロール0.5%局所塗布 | 表層型・小型病変 | 1日2回(保険適用外) |
| パルスダイレーザー(585〜595 nm) | 表層型 | 早期照射で早期退縮 |
| ステロイド局所注射 | β遮断薬不耐容例 | トリアムシノロン 3〜5 mg/kg |
| 手術 | 退縮後の残存腫瘤 | 整容目的 |
β受容体遮断薬であるプロプラノロールは現在の標準的な第一選択薬である7)。β2受容体遮断によるVEGF・bFGF産生抑制、血管収縮、血管内皮細胞のアポトーシス誘導が作用機序として推測されている。
プロプラノロール経口投与に関する無作為化比較試験(NEJM, 2015)では、プロプラノロール群(3 mg/kg/日、6か月間)が対照群に対して有意に優れた治療成績を示した7)。
チモロール点眼液(0.5%)を1日2回、血管腫表面に塗布する(保険適用外)。表層型・小型病変に対して有効性が報告されている11)。プロプラノロールの全身投与が困難な症例への選択肢となる。効果が確認された時点で投与を中止する。
パルスダイレーザー(585〜595 nm)は表層型乳児血管腫に有効である8)。早期照射により早期退縮・隆起性変化の抑制が期待できる。表面の赤色病変に対して効果的であり、深在成分には効果が及ばない。
プロプラノロール不耐容例や特定の局所病変に対して、トリアムシノロン(3〜5 mg/kg)の局所注射が用いられる9)。従来の第一選択であったが、現在はプロプラノロール導入後に適応が限定された。
開瞼困難による形態覚遮断弱視、および血管腫による眼球圧迫・角膜変形に起因する乱視性弱視の両方に注意が必要である。腫瘍のサイズと形態覚遮断弱視のリスクを継続的に評価し、屈折矯正・健眼遮閉を行う。
主な副作用は低血糖・徐脈・低血圧・気管支攣縮である。低血糖は哺乳不良時や食事摂取不足時に起こりやすく、授乳・食事と同タイミングでの内服が推奨される。気管支攣縮のリスクから喘息・反応性気道疾患は禁忌とされる。これらのリスク管理のため、小児科専門医の指導下での入院導入が推奨される。
乳児血管腫は血管内皮細胞の真の増殖による腫瘍であり、静脈奇形(血管奇形)とは病態が根本的に異なる。VEGF(血管内皮増殖因子)が腫瘍の増殖に中心的な役割を果たす。プロプラノロールのβ2受容体遮断はVEGF・bFGFの産生抑制、血管収縮、アポトーシス誘導を介して腫瘍縮小をもたらすと考えられている7)。
GLUT-1(グルコーストランスポーター1)陽性は乳児血管腫の特異的な免疫表現型であり、胎盤微小血管との共通性を示す3)。この特性は腫瘍の発生起源に関する仮説(胎盤由来の血管内皮前駆細胞)を支持している。GLUT-1は静脈奇形・リンパ管腫・化膿性肉芽腫などの他の血管性病変では陰性であり、鑑別診断において実用的なマーカーとなる。
静脈奇形(旧称:海綿状血管腫)は血管の形成異常(奇形)であり、厳密には腫瘍ではない。拡張した静脈血管腔が塊を形成し、内腔は平坦な内皮細胞で覆われる。GLUT-1陰性であり、増殖因子による増殖性はほとんどない。自然消退しないため、治療適応は乳児血管腫と異なる。
ISSVA分類(2018改訂版)2)は血管性病変を「血管性腫瘍」(血管内皮細胞の増殖による)と「血管奇形」(血管の形成異常による)に二分する枠組みを提供している。乳児血管腫は「血管性腫瘍」に、静脈奇形・リンパ管奇形は「血管奇形」に分類される。この分類は治療方針の決定に直接的な意義を持つ。プロプラノロールなどの血管内皮増殖を抑制する薬剤は血管性腫瘍に有効であるが、血管奇形には効果が限定的である。
眼瞼の大型血管腫が眼球を圧迫すると角膜の非対称変形をきたし、不規則乱視・不同視が生じる。この乱視が適切に矯正されない場合、視力発達が阻害されて乱視性弱視・不同視弱視が生じる。形態覚遮断弱視は開瞼困難により光刺激そのものが遮断されることによる。視覚の感受性期(生後〜7〜8歳)に介入が遅れると、弱視が不可逆的になる危険がある。
プロプラノロール(非選択的β遮断薬)の代替として、選択的β1遮断薬であるアテノロールが検討されている。後ろ向き非劣性研究10)では、アテノロール(1 mg/kg/日)はプロプラノロール(2 mg/kg/日)に対して治療成績で非劣性を示した。喘息・反応性気道疾患を持つ乳児へのプロプラノロール禁忌例でも安全に使用できる可能性があり、今後の前向き試験の結果が注目される。
チモロールマレイン酸塩ゲル(0.5%)の局所塗布に関する無作為化比較試験11)では、生後5〜24週の表層型乳児血管腫に対する有効性と安全性が検証された。局所への吸収による全身性の副作用リスクは低いことが示されたが、長期安全性データの蓄積が求められている。
シロリムス(rapamycin)はmTOR経路を阻害し、血管内皮細胞増殖を抑制する。難治性複合血管奇形(静脈奇形・リンパ管奇形・動静脈奇形の複合例)に対するシロリムスの有効性と安全性を検討した前向き研究12)では、複合血管奇形の84%で症状改善が報告された。乳児血管腫への適応は限定的であるが、難治性血管奇形の新たな治療選択肢として期待されている。
Léauté-Labrèze C, Harper JI, Hoeger PH. Infantile haemangioma. Lancet. 2017;390(10089):85-94.
Wassef M, Blei F, Adams D, et al. Vascular anomalies classification: recommendations from the International Society for the Study of Vascular Anomalies. Pediatrics. 2015;136(1):e203-e214.
North PE, Waner M, Mizeracki A, et al. GLUT1: a newly discovered immunohistochemical marker for juvenile hemangiomas. Hum Pathol. 2000;31(1):11-22.
Metry D, Heyer G, Hess C, et al. Consensus statement on diagnostic criteria for PHACE syndrome. Pediatrics. 2009;124(5):1447-1456.
Kasabach HH, Merritt KK. Capillary hemangioma with extensive purpura. Am J Dis Child. 1940;59:1063-1070.
Dubois J, Patriquin HB, Garel L, et al. Soft-tissue hemangiomas in infants and children: diagnosis using Doppler sonography. AJR Am J Roentgenol. 1998;171(1):247-252. doi:10.2214/ajr.171.1.9648798. PMID:9648798.
Léauté-Labrèze C, Hoeger P, Mazereeuw-Hautier J, et al. A randomized, controlled trial of oral propranolol in infantile hemangioma. N Engl J Med. 2015;372(8):735-746.
Batta K, Goodyear HM, Moss C, et al. Randomised controlled study of early pulsed dye laser treatment of uncomplicated childhood haemangiomas. Lancet. 2002;360(9332):521-527.
Weiss AH, Kelly JP. Reappraisal of astigmatism induced by periocular capillary hemangioma and treatment with intralesional corticosteroid injection. Ophthalmology. 2008;115(2):390-397.
Bayart CB, Tamburro JE, Gee AW, et al. Atenolol versus propranolol for treatment of infantile hemangiomas during the proliferative phase: a retrospective noninferiority study. Pediatr Dermatol. 2017;34(4):413-421.
Chan H, McKay C, Adams S, et al. RCT of timolol maleate gel for superficial infantile hemangiomas in 5- to 24-week-olds. Pediatrics. 2013;131(6):e1739-e1747.
Adams DM, Trenor CC, Hammill AM, et al. Efficacy and safety of sirolimus in the treatment of complicated vascular anomalies. Pediatrics. 2016;137(2):e20153257.