正乱視の所見
直乱視(WTR):強主経線が垂直方向。若年者に多く最も頻度が高い。
倒乱視(ATR):強主経線が水平方向。加齢とともに増加し、高齢白内障患者で多い。
斜乱視:強主経線が斜め方向。0度・90度から30度以上ずれた位置にある。
後部角膜乱視(PCA):平均0.3D。急峻経線は多くの場合垂直方向に位置し、直乱視眼ではPCAが前部乱視を一部打ち消す。倒乱視眼ではPCAが前部乱視に加算される傾向がある5)。

乱視(astigmatism)は、眼球の屈折面が球面でなく、経線方向により屈折力が異なることで、外界の一点から出た光が眼内で一点に結像しない屈折状態である。ある経線で最も強い屈折力(強主経線)を示し、これと直角方向で最も弱い屈折力(弱主経線)を示す。
眼球光学系の全乱視は角膜乱視と水晶体乱視の合計である。大部分は角膜乱視が占める。水晶体亜脱臼がある場合は水晶体乱視が強くなる。
乱視軸による分類(主経線の方向で分類する):
| 分類 | 強主経線の方向 | 特徴 |
|---|---|---|
| 直乱視(WTR: with-the-rule) | 垂直方向(60〜120度) | 乱視中で最も多い。若年者に多い |
| 倒乱視(ATR: against-the-rule) | 水平方向(0〜30度・150〜180度) | 加齢とともに増加 |
| 斜乱視(oblique) | 斜め方向(31〜59度・121〜149度) | 水平・垂直以外の方向 |
屈折状態による分類:
| 分類 | 定義 |
|---|---|
| 単純近視性乱視 | 一方の焦線が網膜上、もう一方が網膜前方 |
| 単純遠視性乱視 | 一方の焦線が網膜上、もう一方が網膜後方 |
| 複合近視性乱視 | 両焦線とも網膜前方 |
| 複合遠視性乱視 | 両焦線とも網膜後方 |
| 混合乱視 | 一方の焦線が網膜前方、もう一方が網膜後方 |
病因による分類:
| 分類 | 定義 |
|---|---|
| 正乱視(regular astigmatism) | 2つの主経線が直交(90度)し、各経線上で屈折が均一。円柱レンズで矯正可能 |
| 不正乱視(irregular astigmatism) | 2つの主経線が直交しないか、同一経線上でも屈折が一定しない。円柱レンズでは矯正不可。ハードコンタクトレンズで矯正 |
白内障手術を受ける患者の系統的レビューでは、47%の眼に1.0D以上の既存角膜乱視が存在する。術前角膜乱視が1.0D以上の症例は約1/3程度とされ、これらはトーリック眼内レンズによる乱視矯正の好適応となる。加齢に伴い直乱視から倒乱視へのシフトが生じるため、白内障手術を受ける高齢患者では倒乱視の比率が高くなる傾向がある。
乱視は不同視弱視の原因としても重要であり、1.5D以上の乱視差(乱視性不同視)や2.0D以上の両眼乱視が弱視リスクを著しく高める7)。小児では2D超の乱視に対して完全矯正眼鏡の早期装用が経線弱視(meridional amblyopia)予防に有効である7)。
屈折矯正手術を受ける患者における乱視の有病率も高い。SMILE手術対象患者では平均乱視度数が1〜2D程度であり、手術計画において乱視矯正軸の正確な設定が重要である2)。
乱視の自覚症状は度数によって異なる。
| 程度 | 主な症状 |
|---|---|
| 軽度(1D未満) | 無症状または軽微な眼精疲労 |
| 中等度(1〜3D) | 視力低下・眼精疲労・頭痛。乱視表で特定方向の線が濃く見える |
| 高度(3D以上) | 著明な視力低下。小児では経線弱視(meridional amblyopia)のリスク |
近見作業での眼精疲労・頭痛・眼痛が主な訴えとなる。特に遠視性乱視では調節負荷が加わるため眼精疲労が顕著になる。不正乱視では円柱レンズで完全矯正できないため、ハードコンタクトレンズ(HCL)での矯正が必要となる。
正乱視の所見
直乱視(WTR):強主経線が垂直方向。若年者に多く最も頻度が高い。
倒乱視(ATR):強主経線が水平方向。加齢とともに増加し、高齢白内障患者で多い。
斜乱視:強主経線が斜め方向。0度・90度から30度以上ずれた位置にある。
後部角膜乱視(PCA):平均0.3D。急峻経線は多くの場合垂直方向に位置し、直乱視眼ではPCAが前部乱視を一部打ち消す。倒乱視眼ではPCAが前部乱視に加算される傾向がある5)。
不正乱視の所見
角膜乱視の多くは先天的な角膜形状の非対称性による。眼球光学系の全乱視の大部分を角膜乱視が占める。
加齢と乱視の変化
若年〜中年では直乱視(WTR)が多いが、加齢に伴い倒乱視(ATR)へのシフトが生じる5)。これは加齢による水晶体周辺部の硬化や眼瞼圧迫の影響で角膜経線方向が変化するためと考えられている。白内障手術を受ける高齢患者では倒乱視が相対的に多くなる。
不正乱視の原因
不正乱視は、円錐角膜・角膜瘢痕(感染症・外傷後)・翼状片・角膜手術後・眼表面疾患(ドライアイ・アレルギー)などにより生じる。角膜形状解析装置がないと判断が難しく、不正乱視の有無の評価には角膜形状解析が必須である。
術後乱視の原因
白内障手術・角膜移植後には術後乱視が生じる。角膜輪部切開(LRI)・フェムトセカンドレーザー弧状切開(FLACS-AK)・縫合誘発乱視などが関与する。縫合を用いた嚢外摘出術後の乱視は、抜糸によって軽減できる場合があるが、予測性が低い点に注意が必要である。
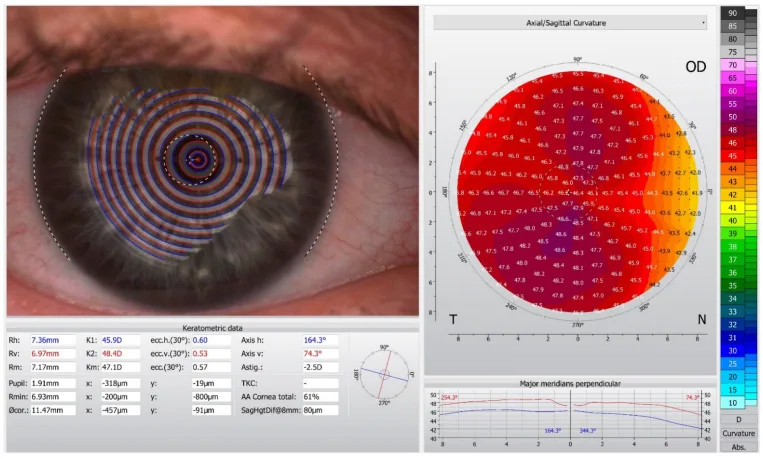
正確な角膜乱視の計測が適切な矯正法選択と良好な術後成績の基盤となる。
| 測定機器 | 計測対象 | 用途・備考 |
|---|---|---|
| オートレフラクトケラトメータ | 前部角膜乱視・屈折値 | スクリーニング。角膜乱視の量と軸を測定 |
| 光学式バイオメータ(IOLマスター700・Lenstar等) | 前部角膜乱視・眼軸長 | IOL度数計算の標準機器 |
| 角膜形状解析装置(トポグラフィ) | 前部角膜形状(2D) | 正乱視・不正乱視の鑑別に必須。不正乱視の有無を確認 |
| 角膜トモグラフィ(Scheimpflug撮影) | 前後部角膜乱視(TCA・3D) | 高PCA症例に推奨。PCA実測値が得られる |
検影法: 他覚的屈折測定。散瞳下での精密検査に有用。
クロスシリンダ法: 乱視軸・度数の精密測定に用いる自覚的検査法。
角膜形状解析装置: 不正乱視の評価に必須。不正乱視の有無は角膜形状解析装置がないと判断が難しい。角膜乱視と屈折乱視が大きく異なる場合、挿入された眼内レンズの固定位置に問題がないか確認する。
乱視の定量には球面度数・円柱度数・軸の3要素に加え、Thibosのpower vector解析も活用される。球面等価(M)・Jackson交叉円柱成分(J0:垂直-水平乱視)・Jackson交叉円柱成分(J45:斜め乱視)の3成分で乱視を記述し、治療前後の乱視変化を3次元的に評価する手法である9)。特にトーリックIOLの術後評価において、乱視の残余量と残余軸のベクター分析が軸ずれ量の推定や再手術計画に有用である。
Alpins法はトーリックIOL・LASIK・LRIなどの乱視矯正手術前後の評価に用いられる統計的解析法である。目標矯正量(target induced astigmatism: TIA)・実際に達成された矯正量(surgically induced astigmatism: SIA)・残余乱視(difference vector: DV)の3ベクターから成り、矯正指数・誤差指数・成功指数などを算出できる9)。術後評価において、単純な乱視度数の比較ではなく軸の変化も含めた包括的評価が可能な点が特徴である。
白内障手術後の乱視は水晶体が摘出されているため、そのほとんどが角膜乱視である。オートケラトメータの数値のみで判断するのではなく、角膜形状解析を用いて不正乱視の有無を確認することが重要である6)。成人白内障PPPでは術後残余乱視の目標を0.5D以下としている6)。
術後乱視評価の流れ(成人白内障PPPに基づく)
| 時期 | 評価内容 |
|---|---|
| 術直後〜1週 | IOL軸位の確認(トーリックIOL)、縫合誘発乱視の評価 |
| 術後1ヶ月 | 屈折の暫定評価(未安定のため処方見送り可) |
| 術後3ヶ月 | 安定化後の残余乱視評価。眼鏡処方・追加治療の検討 |
| 残余乱視≥0.75D | 患者症状を評価し、眼鏡処方またはレーザー追加矯正を検討 |
角膜縫合を伴う術式(白内障嚢外摘出術等)では、抜糸による乱視軽減が可能な場合がある。現代の超音波乳化吸引術(phacoemulsification)後の縫合関連乱視は少ないが、適切な切開サイズ・位置・閉創が術後乱視最小化の基本である6)。
軸マーキング(トーリックIOL使用時):
術前に角膜輪部に基準マーキングを行い、術中にトーリックIOLの軸合わせを正確に実施する。デジタル眼球回旋トラッキングシステムや術中収差計(intraoperative aberrometry)は軸マーキング精度の向上に貢献している8)。
術後乱視評価の手順
白内障手術後3ヶ月以降に以下を確認する6)。
トーリックIOL挿入後のIOL軸ずれ確認にはスリット照明・前眼部OCTが有用である。IOL軸の確認は術後早期(1週間以内)が回転矯正の成功率が高く、3ヶ月以降では水晶体嚢線維化により再位置合わせが困難になる場合がある4)。
乱視の矯正法は乱視の種類(正乱視・不正乱視)、度数、原因疾患、年齢、患者の生活環境によって選択する。
| 矯正方法 | 適応 | 特徴 |
|---|---|---|
| 眼鏡(円柱レンズ) | 正乱視 | 最も一般的。不正乱視には不適。経線不等像視に注意 |
| ソフトコンタクトレンズ(トーリックSCL) | 正乱視(軽〜中等度) | 利便性が高い。回転安定性の維持が課題 |
| ハードコンタクトレンズ(RGP) | 不正乱視・高度正乱視 | 角膜前面に均一な屈折面を形成。円錐角膜の不正乱視矯正の主軸 |
| 強膜レンズ(スクレラルCL) | 高度不正乱視(円錐角膜末期等) | 強膜で支持するため角膜への接触が少ない。不正乱視矯正に優れる |
小児では2D以上の乱視で弱視(経線弱視)のリスクがあり、早期の完全矯正眼鏡の常時装用が重要である7)。経線不等像視が問題になる場合は、円柱度数の低減または軸シフト(15度以内)を検討する。
屈折矯正手術による乱視矯正は長期にわたって矯正効果が弱くなることがある。特に倒乱視例では加齢による倒乱視化が加わり、再手術を検討することがある。LASIKの場合は残余角膜厚に注意する。
エビデンスに基づく角膜屈折矯正手術ガイドライン(SMILE)では、等価球面度数10D以下(近視10D以下、乱視3D以下)が適応とされている2)。LASIK・PRKは近視性乱視・遠視性乱視の双方に適応があるが、遠視矯正の退行リスクは近視矯正より大きい1)。フェムトセカンドレーザー弧状切開(FLACS-AK)の5年成績では、術前平均1.63 Dの乱視が術後0.53 Dへ有意に低下し、5年後も0.55 Dで安定することが示されている3)。
SMILEによる乱視矯正
SMILE(small incision lenticule extraction)は近視性乱視に対して積極的に用いられている。KLEx(keratorefractive lenticule extraction)ガイドラインでは、乱視矯正量は最大3Dまでが推奨され、残余角膜厚は250μm以上・フラップ厚+残余間質床の合計を重視する設計が基本とされる2)。LASIKと比較してフラップ合併症が回避でき、角膜神経保護・生体力学的安定性の観点でも優れるとされているが、乱視軸の精度設定には術者の習熟が必要である。
遠視矯正LASIKは近視矯正と比較して退行率が高く、+4D以上の遠視では長期成績が不安定である。遠視性乱視(複合遠視性乱視・混合乱視)に対する手術は正乱視であることの確認と術前の徹底的な角膜形状評価が前提条件となる1)。
白内障手術は眼内レンズ(IOL)を挿入する機会でもあり、追加の侵襲なく乱視矯正が可能である。術後残余乱視の目標は0.5D以下とされる。
| 矯正法 | 適応乱視量 | 特徴 |
|---|---|---|
| トーリックIOL | ≥1.0D(正乱視) | 最も予測性が高い。不正乱視は禁忌 |
| LRI(輪部減張切開) | 最大3.0D(予測性は1.5Dまで) | 高価装置不要。トーリックIOL禁忌例にも使用可 |
| FLACS-AK(フェムトセカンドレーザー弧状切開) | 1.0〜3.0D | 切開精度高く予測性に優れる |
| エキシマレーザー(LASIK・PRK) | 残余乱視の二次矯正 | 球面度数同時矯正可能。残余角膜厚に注意 |
| ピギーバック(アドオンレンズ) | 残余屈折が大きい症例 | 後房型レンズを追加挿入 |
| 抜糸 | 縫合誘発乱視(嚢外摘出術後) | 現代では適応が限られる |
IOL面での円柱度数は1.5〜6.0Dに対応し、角膜面では0.75〜4.75Dの乱視矯正が可能である。1.0D以上の正乱視に対して考慮すべきであり、2.0D超では強いエビデンスが支持する4)。
メタ解析(13試験)では、トーリックIOLは非トーリックIOLと比較して術後裸眼遠見視力(UDVA)を有意に改善し(平均差 -0.07 logMAR、95% CI -0.10〜-0.04)、20/25以上未達のリスクを低減することが示されている4)。
軸ずれの影響: 1度の軸ずれで矯正効果は約3.3%低下する。30度の軸ずれで矯正効果はほぼ消失し、それ以上では非トーリックIOLより術後視機能が低下する可能性がある。
トーリックIOLの禁忌: 不正乱視(円錐角膜・角膜瘢痕・角膜拡張症)、チン小帯脆弱・断裂、後嚢破損、散瞳不良、重度ドライアイ、バックリングを伴う硝子体網膜手術・緑内障インプラント既往。
FLACS-AK(フェムトセカンドレーザー弧状切開)
前眼部OCTの測定結果に基づきレーザー照射デザインを設計するため、手動切開より切開精度と深度の均一性が高い。
Phamら(2025)は34眼を対象にした5年間追跡コホート研究で、FLACS-AKと白内障手術の同時施行により術前平均角膜乱視1.63±0.886Dが術後3ヶ月に0.53±0.628Dへ有意に低下し(p=0.001)、5年間安定(5年後0.55±0.624D)することを示した3)。UDVA 20/25以上の達成率は67.6%で5年間変化なく、MRSEが±0.50D以内の割合は5年後91.2%に達した3)。
乱視眼に入射した光は、強主経線方向で前方に結像(前焦線)し、弱主経線方向でさらに後方に結像(後焦線)する。この2つの焦線の間に最小錯乱円(circle of least confusion)が形成される(Sturmのコノイド)。等価球面(spherical equivalent)は強主経線と弱主経線の平均屈折値であり、最小錯乱円位置での屈折状態に相当する。
眼球光学系の全乱視は角膜乱視と水晶体乱視の合計である。大部分は角膜乱視が占めるが、水晶体亜脱臼があると水晶体乱視が強くなる。白内障(水晶体混濁)を摘出すると水晶体乱視は消失するため、術後の乱視は基本的に角膜乱視のみとなる。
後部角膜は負の屈折力を持ち、その急峻経線は多くの眼で垂直方向に位置する。このためPCAは前部角膜乱視と反対方向に作用することが多い。直乱視眼ではPCAが前部乱視を一部打ち消し、倒乱視眼ではPCAが前部乱視に加算される。
Jinら(2023)は高PCA(≥0.5D)の62眼を対象とした後方視的研究で、TCAを用いたトーリックIOL計算を行った場合、ATR群(矯正指数1.14±0.29)・WTR群(矯正指数1.25±0.18)の双方で術後過矯正が生じることを報告した5)。ATR群の誤差量は0.22±0.52D(p=0.03)、WTR群は0.65±0.60D(p=0.00)で、いずれも過矯正方向に有意にずれていた5)。WTR眼での過矯正は軸が反転し術後倒乱視状態を招くため、TCAに基づくトーリックIOL計算はATR眼に推奨されるが、WTR眼では特に注意が必要である5)。
若年者では直乱視(WTR)が多いが、加齢に伴い倒乱視(ATR)へシフトする。加齢による水晶体周辺部の硬化や眼瞼圧迫の影響で角膜経線方向が変化するためと考えられている。このシフトはトーリックIOLの度数計算やLRI計画においても考慮すべき因子である。
乱視のATRシフトの速度は加齢とともに加速し、60歳代以降に特に顕著になる。このシフトはIOL計算時に将来的な乱視変化を加味した計画(目標残余乱視を直乱視側にやや残す等)の根拠となっている4)。長眼軸長眼(強度近視)ではATRへの移行が速い傾向があるとされ、これらの症例でのトーリックIOL計算はより慎重な評価が必要である4)。
3D以上の乱視では、強主経線方向の視力発達が抑制される経線弱視(meridional amblyopia)の存在が考えられる。2Dを超える乱視では完全矯正を常用させることが視力発達に重要である。早期発見・早期矯正によって良好な視力矯正が期待できる。
弱視PPP(2022年改訂)では、乱視性不同視(片眼のみの強い乱視)1.5D以上が弱視リスク因子として認識されており、屈折スクリーニング(フォトスクリーニング)での早期発見が推奨される7)。特に斜乱視(軸が45度・135度近傍)では正面視での視力に比べて周辺視・移動視での視機能低下が生じやすいとされる。
乱視に対する調節麻痺下屈折検査では、円柱度数・軸の正確な評価が不可欠である。アトロピン点眼前後での円柱度数・軸の変化が大きい場合には、水晶体乱視の関与を疑う。無水晶体眼・人工水晶体眼では角膜乱視がほぼ全乱視を占める6)。
円錐角膜は進行性の角膜拡張症であり、著明な不正乱視を呈する。Scheimpflug撮影(Pentacam等)を用いたトモグラフィーでは後面突出・薄化・Amslerグリッド陽性などの特徴的パターンが認められる。KLEx(SMILE)のガイドラインでは円錐角膜の疑い例(後面最大高度≥16μm等)を禁忌として厳格な術前スクリーニングを義務付けている2)。
円錐角膜の不正乱視に対しては:
紫外線照射により術後にIOLの屈折力を微調整できるレンズである。術後に残余屈折を確認してから光照射で度数を最終調整することで、乱視矯正の精度向上が期待される4)。
手術中に無水晶体眼または有水晶体眼の屈折状態をリアルタイム測定し、最適なIOL度数・軸をガイドするシステムである。IAとBarrett Toricカルキュレーターはいずれも75%の眼で0.5D未満の残余乱視を達成し、術前計算群の53%を上回るとされる。リアルタイムでの修正により再手術リスク低減が期待されるが、専用機器と追加時間が必要である4)。
術前の詳細な角膜イメージングと患者固有の屈折プロファイルに基づく個別化IOLの開発が進められている。屈折異常の遺伝的背景を解明し、個人の眼の特性に応じた治療計画を立てる精密医療(personalized medicine)へのアプローチが模索されている4)。
KLExガイドラインでは、SMILEによる乱視矯正成績についてLASIKと比較した系統的レビューが組み込まれている2)。乱視矯正精度(残余乱視0.5D以内の達成率)はSMILEで75〜90%程度と報告されており、LASIK(70〜85%)と同等または軽度優位である。ただし乱視軸の予測性はSMILEよりLASIKがやや安定しているとする報告もある。
SMILEの乱視矯正では軸の精度管理に課題があり、術前のデジタル眼球回旋トラッキングと術中のノモグラム調整が精度向上の鍵である。フェムトセカンドレーザーの照射位置のわずかなズレが乱視残余に直結するため、手術経験と技術習熟が不可欠である2)。
乱視矯正手術(LASIK・SMILE・トーリックIOL)後の長期経過では、以下の問題が生じうる。
これらの合併症を最小化するためには、術前スクリーニング(PCを含む角膜形状解析・残余実質床の計算)と長期的な術後フォローアップが必須である1)。
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-139.
Wang Y, Xie L, Yao K, et al. Evidence-based guidelines for keratorefractive lenticule extraction surgery. Ophthalmology. 2025. doi:10.1016/j.ophtha.2025.
Pham TMK, Nguyen XH, Pham TTT, Hoang TT. Five years follow-up outcomes of femtosecond laser-assisted cataract surgery on patients with preexisting corneal astigmatism. Int Med Case Rep J. 2025;18:373-379.
Mallareddy V, Daigavane S. Innovations and outcomes in astigmatism correction during cataract surgery: a comprehensive review. Cureus. 2024;16(8):e67828. doi:10.7759/cureus.67828
Jin T, Yu L, Li J, Zhou Y. Refractive outcomes of toric intra-ocular lens implantation in cases of high posterior corneal astigmatism. Indian J Ophthalmol. 2023;71(8):2967-71. doi:10.4103/IJO.IJO_3385_22
American Academy of Ophthalmology. Cataract in the Adult Eye Preferred Practice Pattern. Ophthalmology. 2022;129(1):P1-P126.
American Academy of Ophthalmology. Amblyopia Preferred Practice Pattern 2022 Update. Ophthalmology. 2023;130(3):P136-P178.
Kamari M, et al. Diagnosis of Dry Eye Disease Using Ocular Imaging Techniques. Diagnostics (Basel). 2021;11(8):1466.
Kanclerz P, Przewłócka K, Arnold RW. Agreement in non-cycloplegic and cycloplegic refraction between a photoscreener and a calibrated autorefractor. BMC Ophthalmol. 2024;24:130. doi:10.1186/s12886-024-03394-0