IOL 偏位・脱臼
Zinn 小帯断裂による IOL 落下の診断と手術適応。強膜内固定術(フランジ法・鑷子法)の選択。

眼内レンズ(intraocular lens; IOL)は、白内障手術で混濁した水晶体を除去した後に眼内に永久留置する人工レンズである。IOL が挿入された眼は偽水晶体眼(pseudophakia)と呼ばれる。眼鏡やコンタクトレンズによる矯正と異なり、IOL は眼球光学系に直接組み込まれるため、像の拡大・縮小が生じず、最も自然で生理的な視機能が得られる。
現在最も普及している IOL は折りたたみ可能な foldable IOL であり、光学部(optic)と支持部(haptic)から構成される。光学径は標準的に 6.0 mm で、超音波水晶体乳化吸引術(PEA)の 2.4〜2.8 mm 小切開創からインジェクターを用いて挿入できる。一部の難症例では 7.0 mm の大光学径 IOL が使用され、眼底検査時の観察性向上や囊外固定時の中心固定性改善に寄与する。
素材による分類を以下に示す。
| 素材 | 特徴 | 主な適応 |
|---|---|---|
| 疎水性アクリル | 後発白内障が少ない。グリスニング(glistenings)に注意 | 現在の標準選択 |
| 親水性アクリル | 生体適合性が高い。長期使用でカルシウム沈着(IOL 混濁)リスクあり | 特殊設計 IOL |
| シリコーン | 折りたたみ性が良好。シリコーンオイル眼内タンポナーデ施行眼では不適 | 一部の PIOL |
| PMMA | 硬質素材。切開創を 5〜7 mm に広げる必要がある | 特殊固定 IOL・二次挿入 |
構造面では、光学部と支持部が同一素材の 1ピースレンズ と異素材の 3ピースレンズ がある。1ピースは通常の囊内固定(bag-in-the-lens)に用い、3ピースは囊外固定・強膜固定・縫着術に適している。1ピースを囊外(毛様溝)に誤って固定すると、支持部が虹彩を擦過して虹彩色素散布や炎症遷延を引き起こすため注意を要する。
球面 IOL では光軸近くを通る近軸光線と周辺光線の焦点位置がずれる球面収差が生じる。これに対し 非球面 IOL は各屈折面の傾斜を変化させ周辺光線と近軸光線を同一焦点に収束させることで球面収差を低減する。現在ほぼすべての IOL が非球面設計を採用しており、コントラスト感度が向上する。ただし非球面設計は偏心・傾斜によってコマ様収差が増加するため、Zinn 小帯が脆弱で IOL 固定が不安定な症例では球面 IOL を選択する判断もある。
着色(黄色フィルター)IOL は短波長光(青色光)の透過率を低下させ、ヒト成人水晶体の分光透過率に近似させた設計で、網膜光障害リスクの軽減が期待される。
1981年に Sanders らが SRK 式(Sanders-Retzlaff-Kraff 式)を提唱し、IOL 度数計算が系統化された1)。1984年には Mazzocco が折りたたみシリコーン IOL を開発し、小切開手術への道を開いた。日本は折りたたみ IOL の世界初認可国であり、その後のインジェクター開発でも国際的に先駆的な役割を担っている。1953年に Strampelli が行った前房型 IOL 挿入は数年後に 70〜80% の症例に水疱性角膜症を引き起こし頓挫したが、これが後の IOL 設計改良への原動力となった。
最も普及している IOL で、1 点のみに焦点を合わせる設計である。保険適用(選定療養)で行われる標準的な選択肢であり、術後正視を目標にすれば遠方は裸眼で良好に見えるが、近方視には読書用眼鏡が必要になる。コントラスト感度が最も高く、夜間のグレア・ハローが最小である点が強みである。
術後の老視対策として以下の選択肢がある。
→ 詳細は 単焦点眼内レンズ を参照。
複数の焦点距離で良好な視力を提供し、眼鏡依存の軽減(スペクタクル・インディペンデンス)を目的とした付加価値 IOL である。光の利用効率が分散するためコントラスト感度低下やグレア・ハローが生じやすい点を術前に十分説明する必要がある。選定療養として患者の自己負担が発生する。
遠方と近方の 2 点に焦点を合わせる。中間距離(50〜80 cm のパソコン作業等)にはやや不向きであった。回折型(AcrySof IQ ReSTOR、TECNIS Multifocal)と屈折型がある。
回折型では 0 次回折光が遠方、1 次回折光が近方の焦点となる設計であり、2 次以降の回折光(約 18%)が高周波コントラスト感度の低下要因となる。アポダイズ型は瞳孔周辺部の段差を低くすることで薄暮時の遠方視機能を改善している。
8 つの RCT を含むメタ解析では、単焦点 IOL と比較して多焦点 IOL は裸眼近方視力(UCNVA、6/6 以下の割合: RR 0.20、95% CI 0.07〜0.58、782 眼)および眼鏡非依存率(RR 0.63、95% CI 0.55〜0.73、1,000 眼)で優れていた。一方、ハロー(RR 3.58、95% CI 1.99〜6.46、662 眼)の頻度は多焦点 IOL で有意に高かった。3)
遠方・中間距離・近方の 3 点に焦点を合わせ、現在の多焦点 IOL の主流となっている。2010年に最初の三焦点 IOL が臨床導入され4)、現在の代表製品は AcrySof IQ PanOptix(Alcon)、AT LISA tri(Carl Zeiss)、FineVision(PhysIOL)、TECNIS Synergy(J&J Vision)などである。
22 試験 2,200 眼のメタ解析では、三焦点 IOL は EDOF IOL と比較して近方視力(UCNVA: MD = 0.12 logMAR、p < 0.00001)および眼鏡非依存率(OR = 0.26、p = 0.02)で優れていた。一方、遠方視力(UDVA)および中間視力(UIVA)に両群間の有意差はなく、Quality of Vision スコアも三焦点 IOL が有意に高かった(MD = 1.24、p = 0.03)。5)
三焦点 IOL の系統的レビューでは、三焦点は二焦点と比較して中間視力が有意に良好であった(DCIVA: MD −0.16 logMAR、95% CI −0.22〜−0.10)が、CDVA・遠方視力・近方視力・コントラスト感度・患者満足度に有意差はなかった。4)
Extended Depth of Focus(EDOF)IOL は光を単一焦点ではなく連続した焦点域に分散させることで、遠方から中間距離にわたる広い焦点域(depth of focus)を提供する。2014年に最初の CE マーク取得製品が登場した4)。代表製品は TECNIS Symfony(J&J Vision)、TECNIS Eyhance、AcrySof IQ Vivity(Alcon)などである。
上述のメタ解析(22 試験)では EDOF IOL は三焦点 IOL と比較して遠方矯正視力(CDVA: MD = −0.01 logMAR、p = 0.01)でわずかに優れ、グレア・ハローの頻度に両群間の有意差はなかった。5) ESCRS ガイドラインは、EDOF IOL を「中間視力を重視しつつ光学的副作用を最小化したい患者への選択肢」として推奨している。4) EDOF IOL(AcrySof IQ Vivity)を評価した米国登録試験では、最低矯正遠方視力(BCVA)は単焦点対照群と同等(モノキュラー CDVA 0.00 logMAR)であり、メソピックコントラスト感度の低下は中等度にとどまった。17)
→ 詳細は 多焦点眼内レンズ を参照。
角膜の正乱視を補正するために設計された IOL で、光学部の弱主経線にマーキングが施されており、このマークを角膜強主経線に一致させて囊内固定する。軸が 1° ずれるごとに矯正効果は約 3.3% 減少し、30° 軸がずれると矯正効果が消失するのみならず、非トーリック IOL と比較してかえって視機能が低下する可能性がある。
トーリック IOL の適応基準の目安(施設ごとに設定):
ESCRS ガイドライン(2024)は、角膜乱視 1.0 D 以上の眼でトーリック IOL を考慮することを推奨し、2.0 D 以上では強いエビデンス(GRADE ++)がある。4) 13 試験のメタ解析では、トーリック IOL は非トーリック IOL(弛緩切開あり/なし)と比較して術後 UDVA(MD −0.07 logMAR、95% CI −0.10〜−0.04)および 20/25 未達率(RR 0.59、95% CI 0.50〜0.70)で優れていた。14)
Zinn 小帯脆弱・後囊破損症例や散瞳不十分例は正確な軸合わせが困難なため適応外となる場合が多い。計算には各メーカー提供のオンラインカリキュレーター、または装置内蔵の Barrett Toric 式・Haigis-T 式を用いる。
→ 詳細は トーリック眼内レンズ を参照。
水晶体を保持したまま虹彩後面・毛様溝に固定する IOL で、屈折矯正手術の一形態である。代表的なものは ICL(Implantable Collamer Lens; EVO+ ICL)で、コラマー素材でできた後房型 PIOL であり、高い生体適合性を持つ。角膜を削らず可逆性があり、中等度から強度近視まで幅広く対応できる。
日本眼科学会の屈折矯正手術ガイドライン(第 8 版)では、有水晶体眼内レンズ手術の適応年齢を原則として 21〜45 歳とし、適応屈折量は 6 D 以上の近視としている。3〜6 D 未満の中等度近視および 15 D を超える強度近視には慎重対応が求められる。エキシマレーザー手術と同様の禁忌事項(活動性外眼部炎症・白内障・ぶどう膜炎等)に加え、浅前房・角膜内皮障害・進行性円錐角膜が追加禁忌となる。6)
術前評価として必須なのは角膜内皮細胞密度検査・前眼部画像解析(前房深度を含む)・角膜径測定(水平径)である。6)
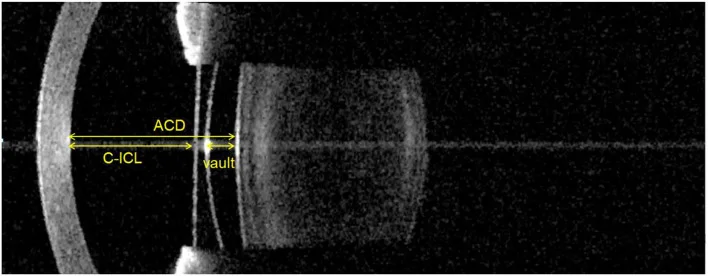
→ 詳細は 有水晶体後房レンズ(ICL) を参照。
既存の単焦点 IOL の上に、毛様体溝固定で追加装着する補助 IOL である。過去に単焦点 IOL を挿入した眼でも、老視矯正・乱視矯正・近視矯正を後付けで行える。囊内固定 IOL との距離が比較的一定であり、長期安定性が良好とされる。
→ 詳細は アドオン眼内レンズ を参照。
| 種類 | 焦点域 | コントラスト感度 | グレア・ハロー | 乱視矯正 | 保険適用 | 追加費用目安(両眼) |
|---|---|---|---|---|---|---|
| 単焦点 | 1点(遠方または近方) | ◎ | なし | △(トーリックは別途) | ○(選定療養) | 0〜数万円 |
| 二焦点(回折型) | 遠+近 | ○ | ++(中等度) | △〜○ | × | 30〜50万円 |
| 三焦点 | 遠+中+近 | ○ | ++(中等度) | △〜○ | × | 40〜60万円 |
| EDOF | 遠〜中(連続) | ◎〜○ | +(軽度) | △〜○ | × | 35〜55万円 |
| トーリック(単焦点) | 1点(遠方優先) | ◎ | なし | ◎ | ×(選定療養) | 10〜15万円 |
| 有水晶体(PIOL・ICL) | 遠方(角膜矯正不要) | ◎ | なし | EVO+ で△〜○ | × | 50〜70万円 |
| アドオン | 既存IOL+老視補正 | ○ | + | ○ | × | 30〜45万円 |
費用は両眼自由診療の概算目安。施設・選択レンズにより大きく異なる。
IOL 選択は術後の見え方に直結するため、術前の丁寧な意思確認が不可欠である。ESCRS 白内障ガイドラインは「患者の期待値の評価と詳細なインフォームド・コンセントが適切な IOL 選択の最重要前提である」と明示している。4) 把握すべき情報:
多焦点 IOL(三焦点・EDOF)に適した条件:
多焦点 IOL 挿入後に眼鏡依存が解消されない場合や光学的副作用が改善しない場合、1 年以内の IOL 交換率が上昇することがメタ解析で示されている。3)
トーリック IOL は角膜の正乱視矯正に有効だが、いくつかの前提条件がある。
後部角膜乱視の影響を考慮するため、Barrett Toric 計算式または光学式眼軸長測定装置内蔵の Haigis-T 式を使用することが推奨される。7) また、座位と仰臥位の眼球回旋(ocular cyclotorsion)は平均 4〜5° 生じるため、写真を用いたマーキングや画像ガイドシステム(CALLISTO eye, VERION)による自動軸合わせが精度向上に有用である。画像ガイドシステムと手動マーキングを比較した前向き試験では、画像ガイド群で術後残余乱視が有意に少なかった(0.33 D vs. 0.51 D、p = 0.003)。19)
夜間の車の運転が多い方や精密な視覚作業が中心の方には単焦点 IOL の方が向いていることがあります。逆に、スマートフォン・パソコン・読書など幅広い距離を眼鏡なしでこなしたい方には多焦点 IOL が候補になります。ただし、眼の状態(黄斑疾患・緑内障・ドライアイなど)によっては多焦点 IOL が適さない場合があります。担当医との術前相談が最も重要です。
精密な IOL 度数計算には、光学式眼軸長測定装置による複数パラメータの同時計測が標準となっている。光学式は超音波 Aモード法と比較して測定誤差が小さく、国内では 2010年に「光学的眼軸長測定」として保険収載された後、急速に普及した。FD(フーリエドメイン)方式の採用により測定成功率が従来の約 90% から 98% 程度に向上し、測定値の標準偏差も 0.02 mm に収まるようになっている。7)
| 装置 | 測定方式 | 主な搭載機能 |
|---|---|---|
| IOLMaster 700(Carl Zeiss) | SS-OCT(スウェプトソース) | 眼軸長・角膜屈折力・前房深度・水晶体厚・角膜径、ゴールドスタンダード |
| ARGOS(Santen/Santek) | FD-OCT(セグメント方式) | 各組織の屈折率を個別計測。IOLMaster 700 より眼軸長が短く測定される傾向 |
| OA-2000(Tomey) | FD-OCT | B-scan 像と A-scan 波形を並列表示 |
| 超音波 Aモード法 | 超音波(1,550 m/s) | 全例対応可能だが誤差が大きい(術後屈折誤差の過半数の原因とされる)7) |
光学式は超音波法より 0.2〜0.3 mm 長く眼軸長を表示するため、IOL 定数(A 定数など)は測定装置専用のものを使用することが必須である。ARGOS はセグメント方式を採用するため、IOLMaster 700 との IOL 定数の互換使用は避けなければならない。7)
| 計算式 | 世代 | 特徴 | 主な用途 |
|---|---|---|---|
| SRK/T 式 | 第 3 世代 | 国内で 90% 以上が使用。臨床実績豊富、A 定数 | 標準眼軸(22〜25 mm)のファーストライン |
| Haigis 式 | 第 3 世代 | 前房深度を独立変数として使用。a0・a1・a2 の 3 定数(200 眼以上での最適化が必要) | 前房が浅い/深い眼 |
| Barrett Universal II 式 | 第 4 世代 | 厚肉レンズ理論に基づく。ローパワー IOL での精度が良好。APACRS ウェブサイトで無料計算可能 | 長眼軸・短眼軸・ローパワー IOL |
| Hill-RBF | AI(機械学習) | ビッグデータからパターン認識。数式によらない | 長眼軸、強度近視 |
| Kane 式 | AI(機械学習+理論式) | 性別も変数として使用 | 極度の強度近視(眼軸長 ≥ 30 mm) |
国内では第 3 世代の SRK/T 式が汎用されているが、眼軸長や前眼部解剖(眼球均整)に応じて複数の計算結果を比較することが望ましい。白内障手術希望者の約 15% に眼軸長と角膜屈折力による眼球均整が整っていない眼球が認められるため、使用する計算式に注意を要する。7)
13,301 眼を用いた多施設研究では、Barrett Universal II・Olsen・Haigis 式が SRK/T・Holladay 1・Hoffer Q と比較して有意に精度が高く(Holladay 2 もほぼ同等の精度)、長眼軸・短眼軸ともに第 4 世代以降の式が優れていた。15) 短眼軸(AL < 22 mm)を対象とした別のメタ解析でも、Barrett Universal II は Haigis・SRK/T に比べて有意に MAE が小さかった(p < 0.05)。18)
強度近視(眼軸長 ≥ 30 mm)の 80 眼を対象とした研究では、AI 式(Kane・Hill-RBF)は SRK/T と比較して平均絶対誤差(MAE)が有意に小さく(Kane: 0.51 D vs. Hill-RBF: 0.52 D vs. Barrett Universal II: 0.66 D vs. SRK/T: 有意差あり、p < 0.05)、1.0 D 超の屈折誤差率も Kane・Hill-RBF は 7.5% に抑えられたのに対し SRK/T では 42.5% に達した。8) 眼軸長 ≥ 32 mm の眼では Kane 式が最も低い MAE(0.44 D)と MedAE(0.40 D)を達成した。8) 眼軸長 ≥ 28 mm を対象としたRong 2019の別報でも、Barrett Universal IIのMedAEは0.37 Dであり、Haigisの0.46 Dより有意に小さかった(p = 0.038)。眼軸長 ≥ 30 mmの眼では、Barrett Universal IIがHaigisより良好な精度を示した。16)
| 症例 | 推奨計算式 | 注意点 |
|---|---|---|
| 標準眼(AL 22〜25 mm) | SRK/T、Haigis、Barrett Universal II | 複数式で比較 |
| 長眼軸(AL > 26 mm) | Barrett Universal II、Hill-RBF、Kane | ローパワー IOL 時の精度差に注意15,16) |
| 短眼軸(AL < 22 mm) | Barrett Universal II、Haigis、Holladay 2 | 高度屈折誤差のリスクあり。ELP 予測誤差が大きい18) |
| 角膜屈折手術後(LASIK 後) | Haigis-L、Shammas No-history、Barrett True-K、OKULIX | ASCRS オンラインカリキュレーターを複数式で比較9,20) |
| 毛様溝(囊外)固定 | SRK/T 等で計算後 −1.0 D 補正 | 長眼軸でローパワーは補正を少なく、短眼軸はハイパワーで −2.0 D |
| 強膜内固定(鑷子法) | 囊外固定と同様の補正 | 術式によって差あり |
| 円錐角膜・角膜移植後 | 専用計算式(Seitz-Langenbucher 等)または熟練者の判断 | 標準式では誤差が大きい |
LASIK 後眼は局所的に平坦な角膜形状を呈するため、オートケラトメータによる中心部屈折力の過大評価が生じやすく、術後遠視化(hyperopic shift)の原因となる。LASIK 術前データがない場合でも使用可能な計算式(Haigis-L, Shammas No-history, Barrett True-K など)が各光学式眼軸長測定装置に搭載されており、さらに ASCRS(米国白内障屈折矯正手術学会)の無料オンラインカリキュレーターを複数式で比較することが対策となる。7,9) LASIK 後眼 110 眼を対象とした研究では、Barrett True-K をバイオメーター単独で使用した場合の精度は複数式の平均値アプローチと同等であり(MAE 0.41 D vs. 0.42 D、p = 0.81)、単独使用でも信頼性があることが示されている。20)
術前に患者の生活環境・仕事・趣味を踏まえて目標屈折値を設定する(等価球面値による予測値)。
| 生活スタイル | 推奨目標屈折値 |
|---|---|
| 遠方視優先(車の運転、スポーツ) | 正視(0.00 D)〜−0.25 D |
| バランス型 | −0.25〜−0.50 D(軽度の近視寄り) |
| 近方視優先(読書・細かい作業) | −1.50〜−2.00 D(モノビジョン候補) |
| モノビジョン(非優位眼) | −1.50〜−2.00 D |
| 多焦点 IOL(ほとんどの製品) | 正視(±0.25 D 以内が必須) |
乱視矯正 IOL の計算には、光学式眼軸長測定装置内蔵の計算式(Haigis-T 式や Barrett Toric 式など)を使用すると計測値入力の手間がなくなり誤入力の心配もない。光学式の眼軸長・角膜屈折力・IOL 定数を一貫して使用することが基本原則である。7)
軽度の屈折誤差(±0.5 D 以内)であれば眼鏡で補正できます。誤差が大きい場合(±1.5 D 以上)はアドオン IOL の追加や IOL 交換(IOL exchange)を検討します。多焦点 IOL では 0.5 D 未満の誤差でも患者満足度が大きく低下することがあるため、術前の精密な計測と計算式の選択が特に重要です。
IOL 挿入後は本来の水晶体調節(毛様体筋収縮による厚みの変化)は消失する。しかし臨床上は「偽調節(pseudoaccommodation)」と呼ばれる現象が生じ、わずかな近方視が可能になることがある。偽調節は角膜の多焦点性・乱視・瞳孔のピンホール効果・IOL の球面収差などによって生じ、単焦点 IOL でも 0.5〜1.0 D 程度の偽調節が認められる場合がある。
単焦点 IOL では若年者の正常水晶体と同等かそれ以上のコントラスト感度が得られる。一方、多焦点 IOL は光分散によって高周波領域のコントラスト感度が低下する。軽度の白内障や IOL 挿入眼では、視力に変化がなくてもコントラスト感度が低下していることがある。三焦点 IOL と EDOF IOL のメタ解析(22 試験)では、コントラスト感度に両群間の有意差は認められなかった。5) 多焦点 IOL 全般(8 RCT 含む Cochrane メタ解析)においても、単焦点と比較してコントラスト感度はわずかに低下するが、その臨床的意義は不明確とされている。3)
術後 5 年以内に後発白内障(posterior capsule opacification; PCO)が発生すると、コントラスト感度が著しく低下することがある。疎水性アクリル IOL は親水性アクリルと比較して PCO 発生率が低いことが示されており、Square edge 光学部設計もその予防に有効である。10)
ハロー(halo)は光源周囲に見える光輪、グレア(glare)は光源による眩しさ・視界の白濁である。多焦点 IOL では単焦点と比較してハロー(RR 3.58、95% CI 1.99〜6.46)およびグレアが有意に増加する。3) EDOF IOL は従来の二焦点・三焦点 IOL よりも光学的副作用が少ないが、完全には消失しない。5)
対応策:
非着色 IOL 挿入直後は、ヒト水晶体よりも短波長光透過率が高いため、青みがかった色覚(青視症 cyanopsia)を訴えることがある。着色(黄色フィルター)IOL では同様の現象が軽減される。数日〜数週間で神経適応し、ほとんどの患者で自覚しなくなる。
疎水性アクリル IOL の光学部にみられる点状の反射をグリスニング(glistenings)という。深層に発生するものが glistenings、表層のものが subsurface nano glistenings(SSNG)と呼ばれる。いずれも光学部材質内の小間隙に房水が取り込まれたものであり、素材の劣化ではない。通常は視機能に影響しないが、網膜機能が低下した症例での視機能低下も報告されている。現在販売されている IOL では製法が改良されており、これらの現象は以前より軽減されている。親水性アクリル IOL では長期使用でリン酸カルシウムが表面に沈着し、強い混濁(カルシウム沈着)を生じることがある。10)
| 合併症 | 発生率(目安) | 概要 | 対応 |
|---|---|---|---|
| 後発白内障(後囊混濁) | 術後 5 年で 20〜40% | IOL 後面の後囊に水晶体上皮細胞が増殖し、視機能が低下する | Nd:YAG レーザー後囊切開術 |
| IOL 偏位・脱臼 | Zinn 小帯弱体化眼では数 %/年 | 加齢・外傷・偽落屑症候群による Zinn 小帯断裂で IOL が硝子体内に落下 | 強膜内固定術・縫着術・IOL 交換11) |
| 瞳孔捕捉(虹彩捕捉) | 強膜内固定後等で数 % | IOL 光学部が瞳孔前方に逸脱する状態。 | 散瞳・体位変換・光学部径大きな IOL への交換12) |
| IOL 混濁 | 疎水性グリスニング 数%・親水性カルシウム沈着 数年後 | 素材による変質で視機能低下 | IOL 交換10) |
| PIOL 後の緑内障 | ICL 術後の眼圧上昇 1〜5% | 隅角閉塞・瞳孔ブロックによる眼圧上昇 | 術前の前房深度評価・術後定期管理13) |
IOL 偏位・脱臼
Zinn 小帯断裂による IOL 落下の診断と手術適応。強膜内固定術(フランジ法・鑷子法)の選択。
IOL 混濁
グリスニング・SSNG・カルシウム沈着・後発白内障の機序と管理。IOL 素材の選択に影響する情報。
バイオメトリー(IOL 度数計算)
光学式眼軸長測定装置による精密な眼軸長・角膜屈折力・前房深度の同時計測。 IOL度数計算のためのバイオメトリー
強膜内固定術
Sanders DR, Retzlaff J, Kraff MC. Comparison of the SRK II formula and other second generation formulas. J Cataract Refract Surg. 1988;14(2):136-141.1)
European Society of Cataract and Refractive Surgeons. ESCRS recommendations for cataract surgery. Draft version September 2024. Chapter 4.6: patient selection for correcting presbyopia. https://www.escrs.org/escrs-guideline-for-cataract-surgery/2)
de Silva SR, Evans JR, Kirthi V, Ziaei M, Leyland M. Multifocal versus monofocal intraocular lenses after cataract extraction. Cochrane Database Syst Rev. 2016;12(12):CD003169. doi:10.1002/14651858.CD003169.pub4. PMID:27943250; PMCID:PMC6463930.3)
European Society of Cataract and Refractive Surgeons. ESCRS recommendations for cataract surgery. Draft version September 2024. Chapters 4.6-4.7 and 6.1-6.3. https://www.escrs.org/escrs-guideline-for-cataract-surgery/4)
Karam M, Alkhowaiter N, et al. Extended Depth of Focus Versus Trifocal for Intraocular Lens Implantation: An Updated Systematic Review and Meta-Analysis. J Refract Surg. 2022. 22 studies, 2200 eyes.5)
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第 8 版). 日眼会誌. 2024;128(2):135-142.6)
Werner L. Intraocular lenses: overview of designs, materials, and pathophysiologic features. Ophthalmology. 2021;128(11):e74-e93.7)
Suzuki Y, Kamoi K, Uramoto K, Ohno-Matsui K. Artificial intelligence driven intraocular lens power calculation in extreme axial myopia. Sci Rep. 2025. 80 eyes, axial length ≥30.0 mm, Institute of Science Tokyo.8)
American Academy of Ophthalmology. Cataract in the Adult Eye Preferred Practice Pattern®. AAO; 2021.9)
Grzybowski A, Markeviciute A, Zemaitiene R. A narrative review of intraocular lens opacifications: update 2020. Ann Transl Med. 2020;8(22):1547. doi:10.21037/atm-20-4207. PMID:33313292; PMCID:PMC7729367.10)
Tripathi M, Rao S, Sinha R. Scleral-fixated IOLs - A comprehensive review of current practices and emerging trends. Indian J Ophthalmol. 2025;73(7):933-945. doi:10.4103/IJO.IJO_2812_24. PMID:40586185; PMCID:PMC12356440.11)
Choi SR, Jeon JH, Kang JW, Heo JW. Risk factors for and management of pupillary intraocular lens capture after intraocular lens transscleral fixation. J Cataract Refract Surg. 2017;43(12):1557-1562. PMID: 29335100. doi:10.1016/j.jcrs.2017.08.021.12)
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第 8 版). 有水晶体眼内レンズ手術の禁忌・慎重事項. 日眼会誌. 2024;128(2):135-142.13)
Kessel L, Andresen J, Tendal B, Erngaard D, Flesner P, Hjortdal J. Toric intraocular lenses in the correction of astigmatism during cataract surgery: a systematic review and meta-analysis. Ophthalmology. 2016;123(2):275-286. doi:10.1016/j.ophtha.2015.10.002. PMID:26601819.14)
Melles RB, Holladay JT, Chang WJ. Accuracy of intraocular lens calculation formulas. Ophthalmology. 2018;125(2):169-178. doi:10.1016/j.ophtha.2017.08.027. PMID:28951074.15)
Rong X, He W, Zhu Q, et al. Intraocular lens power calculation in eyes with extreme myopia: comparison of Barrett Universal II, Haigis, and Olsen formulas. J Cataract Refract Surg. 2019;45(6):732-737.16)
McCabe C, Berdahl J, Reiser H, et al. Clinical outcomes in a U.S. registration study of a new EDOF intraocular lens with a nondiffractive design. J Cataract Refract Surg. 2022;48(11):1297-1304. PMID: 35616507. PMCID: PMC9622364. doi:10.1097/j.jcrs.0000000000000978.17)
Wang Q, Jiang W, Lin T, Wu X, Lin H, Chen W. Meta-analysis of accuracy of intraocular lens power calculation formulas in short eyes. Clin Exp Ophthalmol. 2018;46(4):356-363. doi:10.1111/ceo.13058. PMID:28887901.18)
Webers VSC, Bauer NJC, Visser N, et al. Image-guided system versus manual marking for toric intraocular lens alignment in cataract surgery. J Cataract Refract Surg. 2017;43(6):781-788. doi:10.1016/j.jcrs.2017.03.041. PMID:28732612.19)
Ferguson TJ, Downes RA, Randleman JB. IOL power calculations after LASIK or PRK: Barrett True-K biometer-only calculation strategy yields equivalent outcomes as a multiple formula approach. J Cataract Refract Surg. 2022;48(7):784-789. doi:10.1097/j.jcrs.0000000000000883. PMID:35067661.20)