前房隅角支持型
代表例:AcrySof(Alcon)
前房隅角に支持部を置く設計。角膜内皮細胞の慢性減少・瞳孔楕円化・核白内障が問題となり、現在は市場から撤退している。若年の屈折矯正には推奨されない。

有水晶体眼内レンズ(Implantable Collamer Lens; ICL)は、後房型有水晶体眼内レンズ(posterior chamber phakic intraocular lens; pIOL)の一種である。自己水晶体を温存したまま、虹彩と水晶体の間(毛様溝)にレンズを挿入して屈折異常を矯正する。白内障手術と同様に手術顕微鏡下で行う内眼手術であるが、水晶体は摘出しない。
中等度〜高度近視(特に6D以上)が主な適応であり、角膜を切除しないため角膜拡張症のリスクがない。調節力が保存され、可逆性に優れる点が特徴である。LASIKやSMILEの適応外(角膜薄・高度近視)の症例に特に有用である。
ICL手術の適応決定は複数の要素を統合的に判断する必要がある。
これらを総合評価した上で、外来での詳細説明とインフォームドコンセントを経て手術を行う2)。
1953年にStrampelliが最初の前房型pIOLを開発した。初期レンズは角膜内皮不全や緑内障などの合併症が多発したが、1977年にWorstが虹彩固定型を、1986年にFyodorovが後房型を開発し安全性が向上した。STAAR Surgical社は1993年に最初の後房型pIOLを発売し、2005年に米国FDA承認を取得した。2022年3月にはEVO/EVO+ ICLが米国でFDA承認を受け、世界で200万枚以上が使用されている1)。
STAAR Surgical社が開発した「コラマー(collamer)」は以下の組成からなる特許素材である。
コラーゲン含有により生体組織との親和性が高く、ガスと代謝産物の透過性に優れ、炎症反応がきわめて少ない1)。フィブロネクチン等のタンパク吸着が少なく、スペキュラーマイクロスコピーとレーザーフレアセルメーターによる長期評価でも慢性炎症を認めない。
最新のEVO ICLは光学部中央に直径0.36mmのポート(KS-AquaPORT)を備える。これにより以下の利点が生まれた。
EVO+モデルは有効光学部が大きく(最大7.5mm)、瞳孔径の大きな若年世代のグレア・ハロー・高次収差を低減する効果が期待される。FDA臨床試験(中等度近視200眼)では99.7%の眼で適切なvaultが維持され、閉塞隅角・色素散布・前嚢下白内障の発生は0件であった1)。
屈折矯正手術のガイドライン(第8版)では有水晶体眼内レンズ手術の適応を以下のとおり規定している2)。
| 項目 | 基準 |
|---|---|
| 年齢 | 原則21〜45歳(老視年齢は慎重) |
| 矯正量 | 6D以上の近視を主対象 |
| 中等度近視(3D以上6D未満) | 慎重適応 |
| 強度近視(15D超) | 慎重適応 |
| 前房深度 | ≥2.8mm(角膜内皮から3.0mm以上) |
| Toric ICL適応乱視 | 1.0D〜4.0D |
米国FDA承認(EVO ICL)に基づく適応は21〜45歳・眼鏡面で−3.0D〜−20.0D・前房深度3.0mm以上である1)。
| 検査項目 | 目的 |
|---|---|
| 裸眼・矯正視力 | ベースライン評価 |
| 自覚的・他覚的屈折検査(散瞳下含む) | 度数決定 |
| 角膜形状解析(トポグラフィー) | 円錐角膜の除外 |
| 角膜内皮細胞検査 | ≥2300 cells/mm²(21歳以上)の確認 |
| 前眼部OCT/UBM | 前房深度・隅角間距離の計測 |
| 眼底検査(散瞳下) | 網膜裂孔・格子状変性の確認 |
| 眼圧測定 | 緑内障除外 |
| 瞳孔径測定 | 夜間視覚症状の予測 |
前眼部OCTまたは超音波生体顕微鏡(UBM)による前房深度・隅角間距離の測定が必須であり、レンズサイズ決定に重要である2)。
ガイドライン(第8版)では以下が絶対的禁忌とされる2)。
慎重事項としては、緑内障・正常眼圧緑内障・全身性結合組織疾患・ドライアイ・非進行性軽度円錐角膜疑い症例が含まれる2)。
前房隅角支持型
代表例:AcrySof(Alcon)
前房隅角に支持部を置く設計。角膜内皮細胞の慢性減少・瞳孔楕円化・核白内障が問題となり、現在は市場から撤退している。若年の屈折矯正には推奨されない。
前房虹彩固定型
代表例:Artisan/Verisyse(Ophtec/Abbott)、折りたたみ可能版Artiflex/Veriflex
虹彩中周辺部にクローで固定する。角膜内皮細胞の慢性減少が懸念されるが、隅角支持型より安全性が高い。大切開が必要であり術後乱視に注意を要する9)。
後房型(ICL)
ESCRSガイドラインでは、前房型pIOL挿入後に白内障手術が必要となった場合の術前評価として、虹彩損傷の有無・周辺虹彩切開の開通性・角膜内皮細胞密度と形態の確認を推奨している9)。
レンズサイズの正確な決定は術後成績に直結する。ICLのサイズは13.2mm・13.7mm・14.0mm・14.5mmの4種類があり、適切なサイズ選択がvault管理の鍵である。
サイズ決定方法の比較:
| 方法 | 測定値 | 特徴 |
|---|---|---|
| WTW+ACD法 | 水平角膜径+前房深度 | 簡便だが精度は中等度 |
| 前眼部OCT STS法 | 毛様溝間距離(sulcus-to-sulcus) | 直接計測でより精度が高い |
| UBM STS法 | 超音波生体顕微鏡で毛様溝径 | 前眼部OCT不適例に使用 |
前眼部OCTまたはUBMによる毛様溝径(STS)の直接計測はWTWよりもvault予測精度が高く、術前の標準的評価として推奨される4)。
理想的なボルト(vault)(ICLと水晶体前面の間隙)は250〜750μmである2)。
| ボルト状態 | リスク |
|---|---|
| 250μm未満(低ボルト) | 水晶体との接触→前嚢下白内障 |
| 250〜750μm(適正) | 最良の安全域 |
| 750μm超(高ボルト) | 虹彩を前方に押し出す→隅角狭小化・色素散布・瞳孔ブロック |
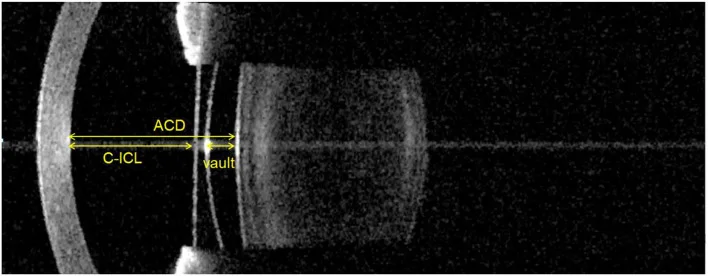
前房型ではVan der Hejdeノモグラムを使用し、屈折値・角膜屈折力・前房深度から度数を計算する9)。術後vaultは年単位で経時的に低下する傾向があり(水晶体の加齢性膨隆による)、定期的な前眼部OCT評価が重要である4)。
EVO/EVO+ ICLでは周辺虹彩切開は不要である。従来型Visian ICLを使用する場合は、手術2〜3週間前に上方2箇所にYAGレーザー虹彩切開術を施行していた1)。
術後に一過性の眼圧上昇が生じることがあるため、手術日には術後2時間以上の経過観察が望ましい2)。
両眼同時手術も可能だが、感染リスクが高い症例では片眼ずつの施術が望ましい2)。
米国FDA臨床試験の中等度近視群(200眼)における6か月時の成績を示す1)。
| 指標 | EVO ICL | SMILE | Topo-LASIK |
|---|---|---|---|
| UDVA 20/20以上 | 94.5% | 84.2% | 88.9% |
| ±0.50D以内 | 91.5% | 93.7% | 93.0% |
| CDVA維持率 | 98.0% | — | — |
| 安全性指数 | 1.21 | — | — |
EVO ICLは角膜屈折矯正術と同等以上の有効性と安全性を示している1)。
眼圧上昇
感染・炎症
その他
ガイドライン(第8版)に基づく術後モニタリング項目:視力・屈折・vault・角膜内皮細胞密度・眼圧・眼底を術後1日・1週間・1か月・3か月・6か月に確認し、以後6〜12か月ごとに生涯継続する2)。Vaultが250μm未満になった場合はICLサイズ変更・交換を、750μm超の場合も隅角鏡検査で評価を行う。
術後早期の眼圧上昇の原因は複数考えられる3)。
Moshirfarら(2024)が報告した症例では、術後IOP上昇に対し粘弾性物質残留と早期ステロイドレスポンスが原因と推定された3)。6週間の経過観察とステロイド減量により、レンズ摘出や虹彩切開を要さず正常化した。
6か月時の角膜内皮細胞減少率は平均2.2%であった1)。長期研究では術後早期のリモデリング後に安定化し、8年後の減少率は3.6±7.9%と報告されている1)。前房型pIOLは後房型より内皮細胞の慢性減少リスクが高く、長期経過でのモニタリングが重要である9)。
Liら(2023)はICL手術後1週間で発症した遅発性TASS 2例を報告した6)。角膜後沈着物(KP)と前房内フィブリン形成を認めたが、プレドニゾロン0.5 mg/kg内服+1%点眼1時間毎を4〜5週間行い、視力・前房所見ともに改善した。発生率は0.24%(827眼中2眼)であった。
Zhangら(前房出血症例報告)はICL術後に虹彩毛様体嚢胞の破裂により前後房出血をきたした23歳女性を報告した8)。0.3%トブラマイシン・0.1%デキサメタゾン点眼(1日4回)と1%硫酸アトロピン眼用ゲル(1日2回)による保存的治療を17日間継続し、ICL摘出なしで治癒した。
Zhengら(2023)はICL術後20日目に発症したStaphylococcus epidermidis眼内炎の1例を報告した7)。硝子体注射(バンコマイシン1 mg+セフタジジム2 mg)を2回施行し、ICL摘出や硝子体手術なしで裸眼視力22/20まで回復した。ICL術後の眼内炎発生率は約0.017〜0.036%と推定されている。
最も多い原因は粘弾性物質の残留で、数日以内に自然改善する。ステロイド点眼の減量やIOP降下薬の追加で対応する。瞳孔ブロックやレンズサイズ不適合が原因の場合は、虹彩切開やレンズ交換が必要となることがある3)。
コラマーはきわめて高い生体適合性を持つ。スペキュラーマイクロスコピーとレーザーフレアセルメーターによる検査で炎症反応がないことが確認されている1)。コラーゲン含有により生体組織との親和性が高く、ガスと代謝産物の透過性に優れている。表面エネルギーが低くフィブロネクチン等のタンパクを吸着しにくい特性が、長期の低炎症状態を維持する理由とされる。
ICLの光学部は水晶体の上方にアーチ状に架かる形で配置される。水晶体との間のボルトが適切に維持されることで、房水が水晶体表面を流れ、水晶体への栄養供給が維持され白内障形成を防ぐ。
EVO ICLの中央孔(KS-AquaPORT)は、後房から前房への生理的な房水の流れを可能にする。これにより以下の効果が得られる。
vault過剰(>750μm)ではICLが虹彩を前方に押し出し、虹彩毛様体との接触により色素が遊離し色素散布緑内障を引き起こす。続いて隅角が狭小化し閉塞隅角緑内障へ進展する可能性がある3)。vault不足(<250μm)では代謝産物が水晶体前嚢下に蓄積し、前嚢下白内障を形成する。FDA試験では99.7%の眼で満足なvaultが得られ、閉塞隅角・色素散布・前嚢下白内障の発生は0件であった1)。
前房型pIOLでは、レンズが角膜内皮に近接することで微小動揺が内皮細胞に機械的ストレスを与える。慢性的な細胞障害により内皮細胞密度が経年的に低下し、最終的に角膜内皮不全(水疱性角膜症)に至る可能性がある。後房型ICLは角膜内皮から離れているため、このリスクが大幅に低い9)。Kohnenらの長期データでは、前房型pIOLの年間内皮細胞減少率は後房型の2〜3倍高いと報告されている9)。
pIOLは眼内に追加的な屈折力を持つレンズを設置することで、網膜上の焦点位置を調整する。近視では凹(マイナス)レンズにより光線の収束を遅らせ、網膜前方の焦点を網膜上に移動させる。眼鏡と異なり眼球の主点に近い位置にあるため像の拡大・縮小がほとんどなく、生理的な視覚を提供する。コントラスト感度が良好に保たれる点もICLの特徴である。
Igarashiらによる8年間追跡では、等価球面度数は安定しており(−10.3Dから+0.09D変化のみ)、角膜内皮細胞密度の減少率は3.6±7.9%と後房型ICLは長期安定性に優れる5)。5年間追跡でも有効性・安全性の維持が確認されている10)。アルフォンソらの5年追跡(Toric ICL含む)でも屈折誤差の経年的増加は認めなかった10)。
LASIKは角膜実質を切除して屈折矯正を行うため、術後に角膜構造が不可逆的に変化する。ICLは角膜を温存するため、以下の点で優位性がある。
Wang Yらのエビデンスに基づくガイドラインでは、角膜バイオメカニクスを保存する点でICRLex(ICL)がLASIKより優れた特性を持つことが示されている12)。
SMILE(小切開レンチキュール摘出術)はLASIKより角膜フラップがないため、フラップ関連合併症がない。しかしICLと比較すると以下の差異がある。
| 比較項目 | ICL(EVO ICL) | SMILE |
|---|---|---|
| 可逆性 | あり | なし |
| 適応近視 | 3〜20D | 最大10D |
| ドライアイ | 低リスク | LASIKより低いが発生あり |
| 角膜バイオメカニクス | 完全保存 | LASIK比で保存 |
| UDVA 20/20達成 | 94.5%(FDA試験)1) | 約84〜90% |
2020年7月にCEマーク承認を取得した焦点深度拡張型(EDOF)ICLである。非球面光学系により近方・中間視力の矯正を提供し、有水晶体眼および偽水晶体眼(単焦点IOL挿入後)の両方に適応がある。対象年齢は21〜60歳で、米国ではFDA承認待ちの段階にある。
従来は6D以上の強度近視を主な対象としていたが、EVO ICLの安全性向上により中等度〜低度近視にも適応が拡大しつつある。FDA臨床試験では被験者の約3分の1が6D未満の中等度近視であり、全範囲の近視で安全性と有効性が一貫していることが示された1)。
波長掃引型前眼部OCTの登場により、隅角間距離や毛様溝径の精密な測定が可能となった。術後ボルトの予測精度が向上し、白内障や閉塞隅角のリスク低減に貢献している。Igarashiらの研究では、swept-source OCTベースの光学生体計測装置と前眼部OCTのvault計測値は良好な相関を示したが、系統的な差異があるため術後モニタリングではデバイスを統一することが推奨されている4)。
近視の世界的蔓延は深刻な公衆衛生問題となっており、2050年には世界人口の49億人が近視、9.4億人が強度近視となると予測されている11)。強度近視(−6D以上)では網膜裂孔・緑内障・黄斑変性などの眼科的合併症リスクが増大する。ICLは6D以上の高度近視の標準的な外科的矯正として、長期的な安全性と有効性エビデンスが蓄積されている。
Packerによるメタアナリシス(2016年)では、中央孔設計のICLが非中央孔設計と比較して前嚢下白内障・閉塞隅角・瞳孔ブロックのリスクを有意に低減することが確認された13)。
Sunら(2023年)は術後vault過剰(高vault)症例に対しICLを90°回転させることでvaultを低下させる手技を報告した14)。平均vaultが1,249μmから459μmに改善し、隅角角度・眼圧も正常化した。ICL交換を避けた非侵襲的な管理法として注目されている。ESCRSガイドラインでは前房型pIOL挿入後の白内障手術において、虹彩損傷・周辺虹彩切開の開通性・角膜内皮細胞の評価を推奨している15)。
従来は6D以上の強度近視を主な対象としていたが、EVO ICLの安全性向上により中等度〜低度近視にも適応が拡大しつつある。FDA臨床試験では被験者の約3分の1が6D未満の中等度近視であり、全範囲の近視で安全性と有効性が一貫していることが示された1)。屈折矯正手術のガイドライン(第8版)では3D以上6D未満は慎重適応としており2)、近視の程度・角膜形状・患者のニーズを総合的に考慮して適応を判断する。
低度近視(6D未満)ではLASIKやSMILEが一般的な選択肢となるが、角膜が薄い場合やコンタクトレンズ装用困難・ドライアイを有する場合にはICLが選択肢となる。ICLの可逆性という特徴は、将来的に術後の屈折変化(近視進行・老視の影響等)に対応できる点でも優れている。
EVO ICL FDA臨床試験では、97.6%の患者が手術に満足しており、視覚の質においてもコントラスト感度・高次収差・夜間視機能に良好な成績が示されている1)。眼鏡・コンタクトレンズからの解放、スポーツ・水中活動の自由など生活の質(QOL)改善が高い満足度につながっている。ただし、術後早期のグレア・ハロー(特に暗所での光輪)は一部の患者で問題となるため、術前の暗所瞳孔径測定と十分な説明が重要である。