術後早期(1〜7日)
視力回復:翌日から著明に改善。多くの症例で1日目から裸眼で日常生活が可能。
角膜所見:切開部(2〜3mm)の上皮は通常1〜2日で修復。角膜浮腫は数日で消退。
注意点:過度な目こすりは切開部の上皮損傷を招く。

SMILE(small incision lenticule extraction)は、フェムトセカンドレーザーを用いて角膜実質内に屈折矯正用のレンチクル(レンズ状角膜片)を形成し、2〜3mmの小切開から摘出することで近視および近視性乱視を矯正する屈折矯正手術である。エキシマレーザーを使用せず、フェムトセカンドレーザー1台で完結する点が従来のLASIK・PRKと根本的に異なる。
2008年に臨床導入されて以来、現在は世界で最も普及したレーザー屈折矯正手術のひとつとなっており、2023年末時点で世界累計800万件以上が実施されている2)。日本では2023年3月22日に薬事承認を取得した1)。初期はFLEx(femtosecond lenticule extraction)として大切開で施行されていたが、切開サイズを2〜3mmに縮小したSMILEが標準術式として普及した。Sekundo et al.13)による最初の有効性・安全性試験以来、数多くの研究が蓄積され、現在では有効性・安全性・予測精度の高い屈折矯正手術として確立している。
この手術の本質的な特徴は「フラップを作らない」点にある。LASIKはまず角膜フラップを作製して引き上げ、エキシマレーザーを照射するが、SMILEはフラップ作製なしに角膜実質内だけを切除する。これにより角膜の構造的連続性が保たれ、前角膜実質の保護が得られる。角膜神経の切断も最小限になるため、術後ドライアイのリスクがLASIKより低い2)。
近視矯正量は等価球面度数10D(近視10D以下、乱視3D以下)まで適応とされる1)。適応年齢は18歳以上であり、屈折度数が安定していることが前提条件となる1)。術前の角膜形状評価(TBI・CBI等によるバイオメカニクス評価を含む)が全例で必須とされており、潜伏型円錐角膜の検出・除外が手術の安全性を左右する最重要課題である2)。
SMILE手術はフェムトセカンドレーザーのみを使用し、角膜フラップを作製せずにレンチクルを摘出します。LASIKはフラップを作製してエキシマレーザーを照射するため、フラップ関連合併症(ずれ・折り畳み・上皮迷入等)のリスクがあります。PRKは上皮を除去してエキシマレーザーを照射するため術後疼痛が大きく、回復に時間を要します。SMILEは疼痛が少なく(LASIKと同程度)、フラップ関連合併症もなく、ドライアイはLASIKより軽度です。また術後エクタジア発症率もLASIKより低く(10万眼あたり11 vs 90)、バイオメカニクス的優位性があります2)。適応範囲は等価球面度数10D以内(近視10D以下・乱視3D以下)で、LASIKの適応(近視・遠視・乱視)より若干狭いことに留意が必要です1)。
SMILE手術の対象は屈折異常(近視・近視性乱視)であり、以下の訴えを持つ患者が適応候補となる。
術後1〜3日は以下が生じることがある。いずれも通常数日以内に改善する。
術後早期(1〜7日)
視力回復:翌日から著明に改善。多くの症例で1日目から裸眼で日常生活が可能。
角膜所見:切開部(2〜3mm)の上皮は通常1〜2日で修復。角膜浮腫は数日で消退。
注意点:過度な目こすりは切開部の上皮損傷を招く。
術後1〜3か月
安定期:屈折・視力ともに安定していく時期。屈折値は術後6か月までに安定する。
ドライアイ:一時的な乾燥感が続くことがある。角膜神経の回復に伴い改善。
フォローアップ:術後1か月・3か月・6か月の定期診察が推奨される1)。
術後合併症(要注意)
多くの場合、翌日から裸眼での日常生活が可能です。車の運転は術後翌日の視力確認後に可能になる場合が多いですが、医師の指示に従ってください。激しい運動やコンタクトスポーツは通常1〜2週間後に許可されます。水泳・サウナなど感染リスクのある活動は1か月以上避けることが推奨されます。
SMILE手術の適応・禁忌・リスク因子を理解することが、安全な手術の前提となる。
屈折矯正手術のガイドライン第8版1)では以下が絶対禁忌とされる:
KLExガイドライン2)によれば:
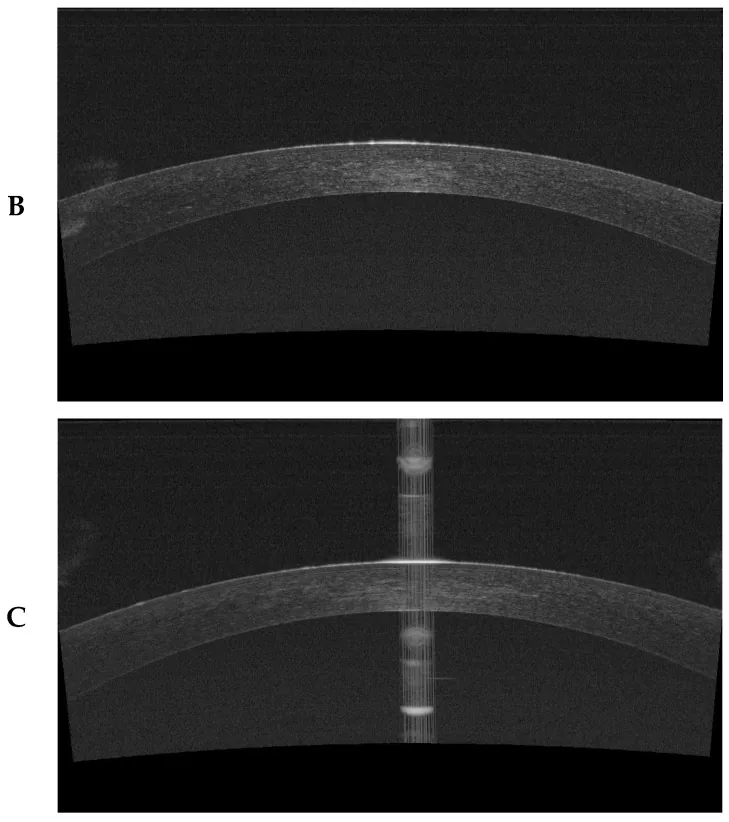
術前には以下の検査を実施し、適応を慎重に評価する1)。
| 検査項目 | 目的 | 注意点 |
|---|---|---|
| 視力検査(裸眼・矯正) | ベースライン評価 | 最高矯正視力も必須 |
| 屈折値検査(自覚・他覚・散瞳下) | 矯正量の決定 | 調節麻痺下屈折が推奨2) |
| 角膜曲率半径計測 | 矯正量・手術設計 | — |
| 細隙灯顕微鏡検査 | 眼表面・前眼部評価 | 円錐角膜早期の検出 |
| 角膜形状検査(トポグラフィ/トモグラフィ) | 円錐角膜スクリーニング | 最重要検査。Scheimpflug or OCT推奨 |
| 角膜厚測定(パキメトリ) | RST計算 | 手術設計の根幹 |
| 涙液検査 | ドライアイ評価 | 術後悪化リスクの評価 |
| 眼底検査 | 近視性変化の評価 | 強度近視では周辺部も確認 |
| 眼圧測定 | 緑内障除外 | 低眼圧は禁忌 |
| 瞳孔径測定(暗所) | 光学ゾーン設計 | 夜間ハロー予測 |
| 角膜径測定 | 手術設計 | — |
| 角膜内皮細胞検査 | 術前ベースライン | SMILEの必須追加検査1) |
| 角膜生体力学検査(Corvis・ORA等) | 拡張症リスク評価 | TBI・CBI・CRFが有用2) |
円錐角膜は絶対禁忌であり、見落とすと術後角膜拡張症が生じる危険がある。TBI(tomographic and biomechanical index)が最も高い診断精度を示し(SUCRA 96.2%)、CBI(同83.8%)と組み合わせた包括評価が推奨される2)。シェインプラグ断層撮影(Pentacam等)による角膜前後表面・角膜厚の3次元評価を必ず実施する。
安全な手術設計の目安は以下のとおり2):
ソフトコンタクトレンズは通常1〜2週間前から中止します。ハードコンタクトレンズ(酸素透過性・強膜レンズ)は角膜形状への影響が大きいため、3週間〜1か月以上の中止が必要です。術前検査は必ずコンタクトレンズ中止後に行います。正確な角膜形状を把握するために欠かせない手順です。
SMILE手術は点眼麻酔下で日帰り実施される。標準的な手順は以下のとおり2):
総手術時間は両眼で15〜30分程度。片眼の実際のレーザー照射時間は25〜40秒程度と極めて短く、患者の身体的・精神的・時間的負担が少ない。
KLExガイドライン2)に基づくDLK(びまん性層間角膜炎)の治療方針:
| Grade | 頻度 | 治療 |
|---|---|---|
| Grade I(末梢部のみ) | 1.42%2) | 局所ステロイド(フルオロメトロン6〜8回/日)+ 経過観察 |
| Grade II(中心部まで) | 0.29%2) | 局所ステロイド強化(プレドニゾロン酢酸塩1時間ごと) |
| Grade III(融合・巣状) | 0.08%2) | 高用量ステロイド + 層間洗浄を考慮 |
| Grade IV(重症) | 0.02%2) | ステロイド層間洗浄(必須)+ 全身ステロイド |
ステロイドによる適切治療で、多くの症例では1週間以内に病巣が改善し、約3週間で症状が消失する2)。
低矯正・屈折回帰に対しては術後6か月以降、屈折が安定した時点でenhancement手術を検討する1)。選択肢としては:
エンハンスメント施行時の残余角膜厚(キャップ・レンチクル摘出腔・残余実質床の合算)が安全基準(RST ≥ 280μm)を満たすことが確認必須である2)。低矯正の発生率はノモグラム最適化やAI駆動の予測モデルの活用により継続的に改善されており、近年のエンハンスメント率は5%以下とされる施設も増えている。
低矯正・過矯正・屈折回帰が生じた場合に強化手術(エンハンスメント)を検討します。通常は術後6か月以降、屈折が安定した時点で判断します。フェムトセカンドレーザーで元のキャップ面にフラップを作製してエキシマレーザーを追加照射する方法が一般的です。残余角膜厚の確認が必須となります。
フェムトセカンドレーザーは角膜実質内で集光し、プラズマ化と微細な光破砕によってレンチクル前面・後面のインターフェースを形成する。この2層の切開面の間に挟まれた角膜実質(レンチクル)が摘出されることで、角膜曲率が変化して近視が矯正される。
レンチクルの形状(前面・後面の曲率差)は屈折矯正量に応じて設計される。中央部が厚く周辺部が薄い凸レンズ状の実質片を除去することで、角膜の屈折力が低下し近視が矯正される。
レンチクルの最小厚は通常15〜20μm以上とされており、これ以下のレンチクル厚では安全な摘出が困難になる場合がある。乱視矯正においては、非対称なレンチクル形状(軸非対称)を正確に位置決めするために輪部マーキングやアイトラッキングシステムの精度が重要である6)。SMILEの光学ゾーン径は通常6.0〜7.0mmで設定されるが、KLExガイドラインでは大きな光学ゾーン(≥6.5mm)のほうが術後の高次収差(特にコマ収差)が少なく良好な夜間視機能が得られることが示されており2)、角膜厚が十分な場合は大きい光学ゾーンの設定が推奨される。一方で光学ゾーン拡大は切除量増加(→RST減少)を伴うため、バイオメカニクスと視機能のバランスを考慮した個別設計が重要である2)。
SMILEはLASIKと比較して角膜生体力学的特性を良好に保つ。KLExガイドラインのメタ解析では、術後12か月時点でのCRF(Corneal Resistance Factor)の低下量がFS-LASIKより有意に少なかった(MD, −1.13; 95%CI −1.36〜−0.90; P<0.001)2)。またCH(Corneal Hysteresis)の低下もFS-LASIKより少なかった(MD, −1.17; 95%CI −1.45〜−0.89; P<0.001)2)。
この優位性の理由は、角膜の前実質(機械的強度が最も高い部位)を温存するキャップ構造にある。キャップ(前実質)は層板構造の連続性を保ち、LASIKのフラップよりも高い生体力学的強度を提供する2)。
SMILEのキャップがLASIKのフラップと異なる点は、①ヒンジがなく全周に角膜との連続性を保つ、②キャップ下の小切開(2〜3mm)のみが外部と連絡する閉鎖型構造、③前方実質の強固なコラーゲン線維が温存される、の3点である。この設計により、術後の外傷によるフラップずれが発生しないという副次的利点もある2)。LT index(最大レンチクル厚/中心角膜厚比)≦28%の管理値は、この生体力学的優位性を維持するための重要な指標であり、28%を超える場合はキャップによる補強効果を超えてバイオメカニクスへの悪影響が生じるとされる2)。
SMILEは角膜輪部付近の小切開(2〜3mm)のみから器具を挿入するため、角膜前実質の知覚神経(角膜神経叢)の切断が最小限に抑えられる。LASIKでは360°の角膜フラップ作製時に全周の神経が切断される。このため術後のドライアイ症状の発生頻度・重症度がSMILEではLASIKより低い。FS-LASIKとSMILEの比較研究でもSMILEのほうが術後の角膜神経密度の回復が速く、涙液パラメータへの影響が小さいことが報告されている4)。
in vivo共焦点顕微鏡(IVCM)を用いた角膜神経密度の経時的評価では、SMILE後の神経叢密度は術後3か月で術前の70〜80%程度まで回復するのに対し、LASIK後では同時期に40〜60%程度の回復にとどまる例が多いとされる4)。この差異が術後ドライアイの重症度の差に対応していると考えられている。神経密度の完全回復には通常6〜12か月を要し、一部の患者では2年以上かかることもある。術前のドライアイ合併例では神経密度の回復が遅延することがあり、術前からの積極的なドライアイ治療が術後の経過を改善する可能性がある。
術後角膜拡張症は、RST不足やレンチクル厚過多による角膜生体力学的強度の低下と、術前からの亜臨床的円錐角膜が主要因とされる。KLExガイドライン2)の解析では、ectasia症例の65.5%に術前の異常・疑い角膜形状があり、52.3%でRST < 280μmであった。
SMILEでのエクタジア発症はLASIKより稀(10万眼あたり11 vs 90)だが5)、発症した場合の管理はLASIK後エクタジアと同様である。進行が確認されたら角膜クロスリンキング(CXL)が第一選択治療となり、2022年より日本でも保険適用されている。
不透明気泡層(OBL: opaque bubble layer)は水蒸気・二酸化炭素の層間蓄積によって生じる。室温18〜25℃・湿度30〜70%の管理と適切なレーザーエネルギー設定が予防策となる2)。OBLが広範に発生し瞳孔域を覆う場合は、完全消退を待ってからレンチクル剥離操作に移行することが推奨される。無理に操作を続けると剥離平面の誤認(wrong plane dissection)のリスクが高まる。
Li et al(2019)の5年間比較研究では、SMILE群・FS-LASIK群ともに安全性・有効性が維持されており、長期的な角膜生体力学への影響に有意差は認められなかった3)。SMILE群では5年経過後も屈折安定性が良好に保たれていた。両術式ともに5年時点での裸眼視力(UDVA)が優れており、BCVA(最高矯正視力)の維持も良好であることが示されている3)。
Moshirfar et al.5)の系統的レビューでは、PRK・LASIK・SMILEのエクタジア発生率をそれぞれ10万眼あたり20・90・11と算出している。SMILEのエクタジア発生率がLASIKの約1/8であることが示されたが、SMILEの追跡期間がまだ短く過小評価の可能性が指摘されている5)。同レビューでは、既知のリスク因子をいずれも持たない眼でもエクタジアが発症することが確認されており、術前スクリーニングのさらなる精密化が求められている。
Dishler et al.6)が報告した米国FDA承認のためのSMILE前向き多施設試験(myopia with astigmatism)では、術後12か月時点で平均残余等価球面度数が−0.07D(±0.38D SD)、UCVAが20/20以上を達成した割合が95.4%であり、安全性・有効性ともに基準を満たした。乱視矯正においては輪部マーキングによる回旋誤差補正が精度改善に有効であることも示されている6)。
Song et al.7)の系統的レビューおよびメタ解析では、SMILEとLASIKの乱視矯正成績を比較し、矯正精度・残余乱視・視力成績に有意差はなかったが、高乱視(>2.0D)症例ではSMILEの回旋誤差制御が成績に影響することが示された。輪部マーキングおよびアイトラッキングシステムの活用が推奨されている7)。
Reinstein et al.8)は、PRK・LASIK・SMILEの相対的角膜tensile strengthを数学モデルで比較した。SMILEはLASIKと比較して前方実質を温存するキャップ構造を有するため、同等の矯正量においてより多くの角膜強度を保持することが示された。この理論的根拠がSMILEの低いエクタジア発症率と整合していると論じられている8)。
Shetty et al.9)の1年間追跡研究では、SMILEはLASIKと比較して術後の角膜バイオメカニクス(CRF・CH)の低下が有意に小さかった。この差は術後3か月以降に明確になり、12か月時点でも維持された。前実質の保護がキャップの生体力学的寄与による可能性が示唆されている9)。
AAO角膜拡張症PPP10)では、SMILEはLASIKよりもエクタジアリスクが低いことが明記されており、PRKと類似したリスクプロフィールとされている。ただしSMILEにおいても術前の潜伏型円錐角膜スクリーニングが不可欠であり、CBI・TBIを含む包括的バイオメカニクス評価が推奨されている10)。
Gomes et al.11)の国際コンセンサスでは、拡張症の進行の定義(角膜前面急峻化・後面急峻化・角膜菲薄化のうち少なくとも2つの一貫した変化)が提唱されており、SMILEを含む屈折矯正手術後のエクタジア管理においてもこの基準が適用される。
Santhiago et al.12)は、LASIK後エクタジアにおけるPTA(percent tissue altered)≥40%が独立したリスク因子であることを示した。SMILE(KLEx)ではキャップがフラップと異なり角膜強度に寄与するため、LASIK基準のPTA閾値をそのまま適用することには議論があるが、LT index ≤28%・RST ≥280μmの管理値は共通して重要である12)。
KLExガイドラインのメタ解析では、低乱視群(<2.0D)と比べて高乱視群(>2.0D)で術後残余乱視が有意に多く、矯正精度が低下することが確認されている。輪部マーキングや3点固定(triple centration)による回旋誤差補正が精度を改善する2)。
Sekundo et al.13)はフェムトセカンドレーザーによるレンチクル抽出(FLEx)の最初の有効性・安全性試験(6か月成績)を報告した。FLExはSMILEの前身技術であり、本試験が後のSMILE開発の礎となった。切開サイズをFLExの7mmからSMILEの2〜3mmに縮小することで角膜神経保護と安全性向上が達成された。
Jones et al.14)のTFOS DEWS IIIでは、SMILEがLASIKと比較して術後ドライアイ症状・角膜神経密度に与える影響が有意に小さいことが複数の研究から支持されていることが報告されている。屈折矯正手術後の眼表面最適化において、術前MGD治療・ジクアホソル・IPLの周術期使用が推奨されている14)。
術前の角膜生体力学パラメータを組み合わせたAI駆動のノモグラム調整が、屈折予測精度を25%以上改善するとの報告がある2)。今後はマルチモーダルデータを活用したパーソナライズドノモグラムの開発が期待される。
Randleman et al.15)のエクタジアリスクスコアリングシステムは、LASIK後エクタジアの術前予測に有用であり、角膜形状異常・RST低値・若年・薄い角膜・高度近視の5因子から構成される。SMILEにおいても同様の因子が術後エクタジアのリスクを高めるため、術前スクリーニングにこのスコアリングの概念が活用できる15)。
SMILE以外にも、CLEAR(cornea lenticule extraction for advanced refractive correction)・SILK(smooth incision lenticule keratomileusis)など複数のフェムトセカンドレーザーによるレンチクル抽出技術が開発されており、さらなる技術標準化が進んでいる2)。CLEARはSMILEの変形版であり、切開デザインを改善して遠視・老視矯正への適用拡大を目指している。SILKは切断面の平滑化と気泡発生の抑制を目的に開発されており、レンチクル剥離のしやすさと視力回復の速さを改善するとされる。これらの新技術はSMILEで確立されたフラップレス・バイオメカニクス温存という原則を継承しながら、適応拡大・精度向上・合併症低減を目指している。
SMILEで抽出されたレンチクルを同種角膜インレイとして遠視・老視・円錐角膜患者に再移植する試みが研究されている。免疫反応が軽微な可能性があるが、現時点では実験段階であり一般臨床応用には至っていない。レンチクルを遠視矯正に再利用するケースでは、摘出されたレンチクルを凍結保存し適切な患者へ移植することで角膜の厚さと屈折力を変化させる原理であり、バンク角膜に代わるリソースとしての可能性が論じられている。ただし長期的な安全性・有効性については引き続きエビデンスの蓄積が必要である。
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-138.
Wang Y, Xie L, Yao K, et al. Evidence-Based Guidelines for Keratorefractive Lenticule Extraction Surgery. Ophthalmology. 2025;132:397-419.
Li M, Li M, Chen Y, et al. Five-year results of small incision lenticule extraction (SMILE) and femtosecond laser LASIK (FS-LASIK) for myopia. Acta Ophthalmol. 2019;97:e373-e380.
Recchioni A, Sisó-Fuertes I, Hartwig A, et al. Short-term impact of FS-LASIK and SMILE on dry eye metrics and corneal nerve morphology. Cornea. 2020;39(7):851-857.
Moshirfar M, Tukan AN, Bundogji N, et al. Ectasia after corneal refractive surgery: a systematic review. Ophthalmol Ther. 2021;10:753-776.
Dishler JG, Slade S, Seifert S, Schallhorn SC. Small-incision lenticule extraction (SMILE) for the correction of myopia with astigmatism: outcomes of the United States Food and Drug Administration premarket approval clinical trial. Ophthalmology. 2020;127:1020-1030.
Song J, Cao H, Chen X, et al. Small incision lenticule extraction (SMILE) versus laser assisted stromal in situ keratomileusis (LASIK) for astigmatism corrections: a systematic review and meta-analysis. Am J Ophthalmol. 2023;247:181-199.
Reinstein DZ, Archer TJ, Randleman JB. Mathematical model to compare the relative tensile strength of the cornea after PRK, LASIK, and SMILE. J Refract Surg. 2013;29:454-460.
Shetty R, Francis M, Shroff R, et al. Corneal biomechanical changes and tissue remodeling after SMILE and LASIK. Invest Ophthalmol Vis Sci. 2017;58:5703-5712.
American Academy of Ophthalmology Corneal/External Disease Preferred Practice Pattern Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: AAO; 2024.
Gomes JA, Tan D, Rapuano CJ, et al. Global consensus on keratoconus and ectatic diseases. Cornea. 2015;34:359-369.
Santhiago MR, Smadja D, Gomes BF, et al. Association between the percent tissue altered and post-LASIK ectasia in eyes with normal preoperative topography. Am J Ophthalmol. 2014;158:87-95.e1.
Sekundo W, Kunert K, Russmann C, et al. First efficacy and safety study of femtosecond lenticule extraction for the correction of myopia: six-month results. J Cataract Refract Surg. 2008;34:1513-1520.
Jones L, Downie LE, Korb D, et al. TFOS DEWS III: Management and Therapy. Am J Ophthalmol. 2025;279:289-386.
Randleman JB, Woodward M, Lynn MJ, Stulting RD. Risk assessment for ectasia after corneal refractive surgery. Ophthalmology. 2008;115:37-50.