LASIKフラップ合併症は術中(フラップ作製〜復位)と術後(早期・晩期)に大別される
フェムトセカンドレーザー 導入でフリーキャップ・ボタンホール等の術中合併症は著減したが、DLK ・フラップずれ・上皮迷入 はなお発生するDLK はGrade 1〜4で重症度評価し、Grade 1〜2はステロイド 点眼頻回投与、Grade 3〜4は緊急フラップリフト・洗浄が原則フラップずれは術後1週間が最高リスク期で、認識次第に緊急対応が必要
上皮迷入 は2mm以上または視力 低下を認める場合にフラップリフト・掻爬を行う LASIK は点眼麻酔下で角膜 に約100μmのフラップを作製し、その下の角膜実質 にエキシマレーザーを照射したのちフラップを元の位置に復位する屈折 矯正手術である。フラップ合併症はこのフラップの作製・復位・術後経過に伴う構造的・炎症性・感染性の障害の総称である。
屈折 矯正手術のガイドライン(第8版)では、LASIK 術後合併症として「フラップ異常」と「びまん性層間角膜炎 (DLK )」が明記されており、「種々のフラップトラブルが生じる可能性があり、適切に対処する必要がある」とされている1) 。
フラップ合併症は発生時期によって術中 (フラップ作製〜復位時)と術後 (術直後から晩期)に大別される。また病態によって、構造的・炎症性・上皮性に分類できる。
フラップ作製デバイスには従来のマイクロケラトームとフェムトセカンドレーザー がある。現在フラップ作製のほとんどはフェムトセカンドレーザー で行われており、フラップ精度の向上とフリーキャップ・不均一フラップなどの術中合併症の著しい減少に寄与している。一方で、フェムトセカンドレーザー 特有の合併症(OBL・縦方向ガスブレイクスルー等)も知られている。
SMILE はフラップを作製せず角膜 内にレンチクルを作製して摘出する術式であり、フラップ関連合併症が原理的に発生しない。KLEx(小切開角膜片抽出術 )のエビデンスに基づく国際ガイドラインでは、フラップがないことがSMILE の安全性上の優位性の一つとして位置づけられている2) 。
Q
フェムトセカンドレーザーならフラップトラブルは起きないのか?
A
フェムトセカンドレーザー の導入によりフラップの精度は大幅に向上し、フリーキャップや不均一フラップなどのマイクロケラトーム特有のトラブルは著しく減少しています。しかし、フェムトセカンドレーザー 特有の合併症(OBL:opaque bubble layer、縦方向ガスブレイクスルーなど)が発生する場合があります。また、DLK ・フラップずれ・上皮迷入 はフェムトセカンドレーザー 使用時でも発生しうる合併症です。完全に合併症がなくなるわけではなく、適切な術前評価と術中・術後管理が依然として重要です。
術中フラップ合併症は主にフラップ作製デバイスの特性に起因する。マイクロケラトーム使用時とフェムトセカンドレーザー 使用時で異なる合併症プロフィールを持つ。術中合併症の認識と対処のタイムリーさが、最終的な視力 転帰を大きく左右する。術前に合併症発生時の対応プロトコルを熟知し、術中に迷いなく判断できる準備が術者に求められる1) 。
マイクロケラトーム関連
不完全フラップ :ケラトームの途中停止による不完全切開。フラップ復位後、3〜6カ月後に再手術を検討する。
フリーキャップ(free cap) :ヒンジが形成されずフラップが完全に分離した状態。マイクロケラトームでの発生率は0.004〜1.31%と報告されている3) 。実質床が整っていればレーザー照射を続行し、BSSで湿潤保護しながら再装着・治療用コンタクトレンズで固定する。
ボタンホール(buttonhole) :フラップ中央部の穿孔。発生率は約0.2%と報告されている3) 。フラップを復位し、3〜6カ月後まで再手術を延期する。
薄い/厚い/不均一フラップ :予定フラップ厚からの偏差。薄すぎるフラップは角膜 強度低下のリスクとなる。
フェムトセカンドレーザー関連
OBL(opaque bubble layer) :レーザー切開時に生じる気泡が角膜実質 内に留まる現象。多くは自然消退するが、瞳孔 域への侵入で眼球追尾が妨げられる場合がある。
縦方向ガスブレイクスルー :切開面から前房 方向への気泡逸出。前房 内気泡が生じると一時的に眼圧 上昇を引き起こすことがある。
フラップエッジの不整 :レーザーパラメータ設定の問題で辺縁が不整になる場合。
スポット切断エラー :局所的なレーザー切断不全による不完全フラップの変形。
フリーキャップ発生時、術者はレーザー照射の続行か中止かを判断する。実質床が整っている場合 は照射を続行できる。フリーキャップはBSS(平衡塩液)を滴上した湿潤環境で取り扱い、乾燥による変形を防ぐ。照射完了後、フリーキャップを上皮側を上にして正しい軸で再装着する。術前の非対称マーキングが正しい向きの確認に不可欠である。実質床が不整な場合 はレーザー照射を行わずフラップを戻す。
再装着後は**治療用コンタクトレンズ(BCL)**を当てることが多い。角膜内皮 のポンプ機能によりキャップは強固に再接着する。術後約30分間は粘着テープで閉瞼しておくと脱落予防に有効である。扁平角膜 (40D未満)と不十分な吸引はフリーキャップの主なリスク因子であり、術前の角膜 曲率計測と適切な吸引リング選択が予防の基本となる。
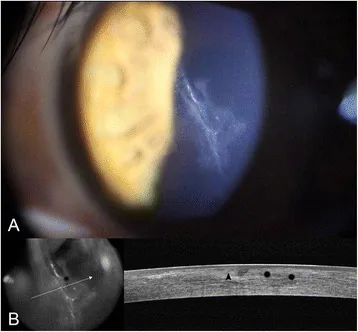
LASIKフラップ縦方向裂傷・ずれの細隙灯後方照明像とAS-OCT断面像 BMC Ophthalmol. 2016 Jul 18;16:111. Figure 1. PM
CI D: PMC4950235. DOI: 10.1186/s12886-016-0288-7. License: CC BY 4.0.
細隙灯後方照明像(A):
瞳孔 中央を含む長さ5.0 mmの垂直裂傷を伴うLAS
IK フラップが確認され、フラップずれ・皺に特徴的な斜行する輝線状パターンが
角膜実質 に認められる。
前眼部OCT 像(B):裂傷部での
ボーマン膜 分離(黒矢頭)とフラップ辺縁からの
上皮迷入 疑い(黒アスタリスク)が断層像で示される。本文「術後早期フラップ合併症」の項で扱うフラップずれ・フラップ皺に対応する。
術後早期(術後1カ月以内)に発生するフラップ合併症は、構造的・炎症性・上皮関連の3カテゴリに分類できる。
フラップ構造的合併症
フラップずれ(flap displacement) :外傷・眼を擦ることで術後早期に発生する。緊急フラップリフト・BSS洗浄・復位が必要。術後1週間は特に注意が必要である。発生率は術後1週間で0.1〜0.3%と報告されている4) 。
フラップ皺(striae/folds) :マクロストリエ(肉眼的な皺)は視機能に影響することがあり、時間経過とともに軽減しない場合は早期にフラップ整復を行う。マイクロストリエは通常視機能への影響は少ない。
炎症性合併症
DLK (diffuse lamellar keratitis)IK 全体での発生率は約0.1〜1%と報告される5) 。Grade 1〜2ではプレドニゾロン1%(またはフルオロメトロン0.1%)点眼の頻回投与で多くが軽快する。Grade 3〜4では緊急フラップリフト・洗浄が必要となる場合がある。
界面デブリ(interface debris) :フラップ下の異物(手術器具由来・タルク等)。通常は無害だが、視軸上に位置する場合は除去を検討する。
上皮関連合併症
上皮迷入 (epithelial ingrowth)6) 。軽症は経過観察。2mm以上の進行または視力 低下を認める場合はフラップリフト・掻爬・辺縁処理を行う。
フラップ辺縁上皮障害 :フラップ辺縁の上皮不整・段差。多くは保存的治療で軽快する。
Linebarger/Goodman分類に基づく4段階のGrade分類が治療方針の決定に用いられる5) 。
Grade 所見 視力 への影響治療方針 Grade 1 周辺部のみに白色顆粒状浸潤(中心部正常) ほぼ影響なし プレドニゾロン1%点眼を1〜2時間毎に頻回点眼 Grade 2 浸潤が中央部に向かって拡大 軽度低下 ステロイド 点眼を継続・増量して翌日再診Grade 3 中央部に達する高度浸潤・基質融解の初期兆候 中等度低下 ステロイド 点眼継続+フラップリフト・洗浄を強く検討Grade 4 中央部基質融解(keratolysis)・瘢痕形成 著明低下 緊急フラップリフト・洗浄。ステロイド 全身投与を考慮
Q
フラップがずれたらどうなるのか?
A
術後早期にフラップがずれると、視力 の急激な低下や不正乱視 が生じます。原因は外傷(目をこすること、スポーツ時の衝撃など)が多く、術後1週間が最もリスクの高い時期です。フラップずれを認めたら緊急で眼科を受診する必要があります。治療はフラップをリフトしてBSS(平衡生理食塩水)で界面を洗浄し、フラップを正確に復位させてエアバブルで固定します。適切に対処されれば視力 は回復することが多いですが、放置すると不正乱視 や感染のリスクが高まります。
術後1カ月以降に発生するフラップ関連の問題を術後晩期合併症として分類する。
晩期フラップずれ :LASIK フラップは術後何年経過しても完全に癒合しないため、外傷(自動車事故・スポーツ時の直接眼球外傷等)により術後数年以降でもフラップずれが発生することがある4) 。フラップずれを認識した時点でのリフト・洗浄・復位が治療の原則であり、時間が経過するほど上皮迷入 の合併リスクが高まる。術後5年以降の外傷事例も報告されており、屈折 矯正手術の既往を担当医に伝えることの重要性が患者教育の観点からも強調される1) 。
晩期上皮迷入 の進行 :術後早期に認識されていた軽症の上皮迷入 が数年にわたり増大し、フラップ融解・不正乱視 を引き起こす場合がある。エンハンスメント手術(再矯正手術)は上皮迷入 リスクをさらに高める因子として知られており、既往のある眼では術後の観察間隔を短縮することが推奨される6) 。フラップリフト・掻爬後の再発率は5〜20%と報告されており、辺縁アルコール処理・フラップ辺縁縫合(エチブレン)等の追加処置が有効とされる6) 。
ドライアイ の遷延IK 術後の角膜 神経切断による反射性涙液分泌低下は術後6〜12カ月で多くの症例で回復するが、一部では難治性ドライアイ として遷延する7) 。屈折 矯正手術のガイドライン(第8版)においてドライアイ はLASIK 術後合併症として明記されており、術前からの評価と積極的な術後治療が求められる1) 。SMILE とFS-LASIK の比較研究では、SMILE 後のほうが角膜 神経密度の回復が速く、涙液パラメータへの影響が小さいことが示されており7) 、術式選択における一つの考慮事項となる。
フラップ辺縁のネクローシス :稀な合併症として、フラップ辺縁の乏血性ネクローシスが生じることがある。角膜 地形図上では特徴的な辺縁起伏として認識される。
術後エクタジア (角膜拡張症 ) :フラップ作製後の残存実質床(RST)不足または術前の潜伏型円錐角膜 が顕在化することにより、術後に角膜拡張症 が発症することがある。LASIK 術後エクタジア の有病率は10万眼あたり約90と報告されており14) 、PRKの約20の約4.5倍である14) 。RST < 280μmはエクタジア リスクの急上昇する閾値であり、PTA(percent tissue altered)≥ 40%も独立したリスク因子とされている13) 。Randlemanスコアリングシステムでは角膜 形状異常・RST低値・若年・角膜 薄い・高度近視 の5因子を総合評価することで術前リスク層別が可能である11) 。
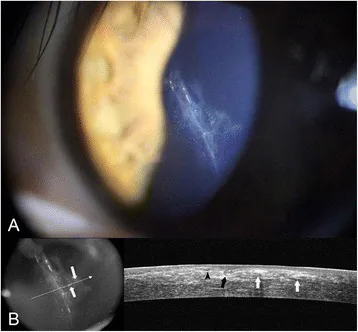
LASIKフラップ辺縁からの上皮迷入:細隙灯写真とOCT像 BMC Ophthalmol. 2016 Jul 18;16:111. Figure 2. PM
CI D: PMC4950235. DOI: 10.1186/s12886-016-0288-7. License: CC BY 4.0.
細隙灯写真(A):LAS
IK 術後2週でフラップ界面に
上皮迷入 (epithelial ingrowth)と上皮嚢胞(白矢印)が確認され、フラップ辺縁から中央方向への白濁増殖が認められる。
OCT 像(B):フラップと
ボーマン膜 の裂傷縁(黒矢頭)および反対側フラップ辺縁の屈曲(黒矢印)が断層像で示され、界面への上皮侵入深度が確認できる。本文「診断と管理」の項で扱う
上皮迷入 に対応する。
屈折 矯正手術のガイドライン(第8版)では、術翌日に必ず細隙灯顕微鏡による観察を行って異常をチェックし、術後6カ月まで経過観察を続けることが原則とされている1) 。
細隙灯顕微鏡検査 DLK では周辺部の細かな点状浸潤が特徴的であり、中心部への拡大をタイムリーに認識することが治療判断の根拠となる。上皮迷入 は、フラップ辺縁から内側方向への白濁として認識され、辺縁から中心までの距離(mm)を定量的に記録することが重要である。
前眼部OCT (AS-OCT )上皮迷入 の深さ・範囲の確認、DLK vs IFS (インターフェース液症候群 )の鑑別に不可欠である。IFS ではフラップ下に均一な低輝度の液体層が確認され、DLK では点状・線状の高輝度域が主体となる8) 。前眼部OCT はまた、フラップの位置ずれの程度(ずれた距離・深さ)を定量化し、治療の緊急度判断に役立つ。
眼圧測定 DLK とIFS の鑑別において必須。ゴールドマン圧平眼圧計 の中央部測定では液体クッション効果により偽低値が出ることがあるため、周辺部測定またはダイナミック・コントア眼圧 計での測定が推奨される8) 。
角膜形状解析 (トポグラフィ)乱視 ・拡張症の評価に用いる。術後経時的な観察により変化を捉えることができる。Grade 4 DLK による基質融解後は、Pentacam等の断層撮影で後面エレベーションの変化を確認し、エクタジア 発症の有無を評価することが重要である。
角膜 培養・スメア前房 炎症・充血 ・濃密な浸潤・フラップ辺縁からの膿性分泌物等)には、フラップリフトと同時に培養を採取して菌種・薬剤感受性を評価する。感染性角膜 炎はDLK と臨床的に類似することがあるため、疑わしい場合は早期の菌学的検索が不可欠である。
合併症 治療 時間的緊急度 Grade 1〜2 DLK プレドニゾロン1%点眼を1〜2時間毎の頻回点眼 準緊急(翌日再診) Grade 3 DLK ステロイド 点眼+フラップリフト・洗浄の検討緊急(当日〜翌日) Grade 4 DLK 緊急フラップリフト・洗浄(ステロイド 全身投与考慮) 緊急(当日) フラップずれ(早期) フラップリフト・BSS洗浄・復位・エアバブル固定 緊急(当日) フラップずれ(晩期) フラップリフト・洗浄・復位(上皮迷入 除去も同時に) 緊急(発見当日) フラップ皺(視機能影響) フラップリフト・整復・再固定 準緊急(数日以内) 上皮迷入 (2mm以上/視力 低下)フラップリフト・掻爬・辺縁アルコール処理 予定(経過観察後) フリーキャップ(術中) BSSで保護・照射後に正確な再装着・BCL固定 術中対応 不完全フラップ/ボタンホール フラップ復位・手術延期 3〜6カ月後に再手術検討
Q
DLKと診断されたらどうするのか?
A
DLK のGrade(重症度)によって治療方針が異なります。Grade 1〜2では、プレドニゾロン1%点眼液を1〜2時間毎の頻回点眼で治療します。ほとんどの症例はこのステロイド 点眼治療で軽快します。Grade 3では上記に加えてフラップリフト・洗浄を検討します。Grade 4(中央基質融解)では緊急のフラップリフト・洗浄が必要となり、ステロイド の全身投与も考慮されます。自己判断せず、術後にフラップ下の混濁や視力 低下を感じたら速やかに担当眼科医に連絡してください。
フラップ合併症の発生率は術式(マイクロケラトームvs.フェムトセカンドレーザー )・施設の経験・患者選択基準によって大きく異なる。以下に主要な文献から得られた発生率を示す3) 12) 。
合併症 発生率 デバイス フリーキャップ 0.004〜1.31% マイクロケラトーム(フェムトセカンドでは極めて稀) ボタンホール 約0.2% マイクロケラトーム OBL(opaque bubble layer) 10〜30% フェムトセカンドレーザー (多くは自然消退)フラップずれ(術後1週以内) 0.1〜0.3% 両デバイス共通 DLK (全Grade)0.1〜1% 両デバイス共通 上皮迷入 0.5〜2%(エンハンスメント後は最大20%) 両デバイス共通 術後エクタジア 10万眼あたり約90 LASIK 全般
フェムトセカンドレーザー の普及により、フリーキャップ・ボタンホール等の重篤な術中合併症は著しく減少した。しかし、DLK ・フラップずれ・上皮迷入 はフェムトセカンドレーザー 使用時でも同様に発生することに留意が必要である12) 。
DLK Grade 3〜4・フラップ融解を伴う高度上皮迷入 ・大面積のフラップ皺は、適切な治療が遅れると恒久的な視力 低下の原因となる。Stulting et al.12) の疫学調査では、DLK の約0.1%が基質融解(Grade 4)に至り、適切な治療を受けた場合でも一部は残存する不正乱視 が報告されている。術後1週間以内の毎日または隔日の診察がリスクの高い早期においてLASIK 後に推奨される1) 。
LASIK フラップはマイクロケラトームまたはフェムトセカンドレーザー により角膜 前面から約100μmの層板状切開を行うことで作製される。フェムトセカンドレーザー はフォトディスラプション(光破壊)によるプラズマ形成と微細気泡の線状配列で切開面を形成する。マイクロケラトームは機械的な切削により切開する。角膜 混濁がある症例や放射状角膜 切開術(RK)後の症例にはマイクロケラトームを用いるか、PRKを選択することがある。
DLK は非感染性の界面炎症反応である。角膜実質 の切削粉末・手術器具由来の残留物・上皮由来の刺激物質などがフラップ界面で多核白血球浸潤を誘発する。一過性の炎症で自然軽快することが多いが、Grade 4に進行すると基質融解(keratolysis)が生じ、不正乱視 の恒久的な原因となる。術後1〜3日以内の診察で早期発見・早期介入が予後を左右する。
フラップ辺縁の上皮細胞がフラップ下界面に侵入し増殖する。侵入した上皮細胞はフラップ下で細胞巣を形成し、増大するにつれてフラップの融解・不正乱視 ・視力 低下を引き起こす。フラップリフトを伴うenhancement手術後に発生リスクが高まる。フラップエッジの位置や再手術既往のある眼が危険因子となる6) 。
LASIK フラップは術後も角膜実質 との接着が完全には回復せず、フラップは角膜 の構造的強度にほとんど寄与しない。フラップ厚が厚いほど、残存実質床(residual stromal bed, RST)が薄くなり角膜バイオメカニクス への影響が大きくなる9) 。残存実質床の薄化は角膜拡張症 発症リスクの増大と関連し、RST < 280μmでリスクが急上昇するとされる2) 。LASIK 手術後はSMILE と比較して角膜バイオメカニクス 的脆弱性が大きいことが、術後12カ月時点でのCRF(Corneal Resistance Factor)低下量において有意差をもって報告されている(MD, −1.13; 95% CI −1.36〜−0.90; P<0.001)2) 。
有限要素解析によるシミュレーション研究では、フラップ厚さがバイオメカニクスに与える影響が定量的に示されている9) 。フラップ厚が増大するにつれて角膜 後面の前方変位量が増加し、薄いフラップのほうが後面安定性に有利であることが示された。ただし薄すぎるフラップは作製精度の問題(不均一さ・OBL等)が生じやすいというトレードオフがある。フェムトセカンドレーザー では±10μmの精度でフラップを作製できるため、100〜120μm前後の薄型フラップも安全に作製可能であり、バイオメカニクスとフラップの確実な作製のバランスを考慮した設計が推奨される。術後の残存実質床(RST)の絶対値はLASIK におけるエクタジア リスク評価の最重要指標であり、RST < 280μmでは手術適応を再検討することが推奨される2) 15) 。
フラップ下の閉鎖空間は通常の角膜 感染とは異なる管理を要する。抗菌薬点眼は起炎菌に応じた選択が必要であり、重症例ではフラップリフト・洗浄を行う。屈折 矯正手術のガイドライン(第8版)では「術者に求められる高度バリアプレコーションズの遵守、器具の滅菌および術野の消毒とドレーピングを厳格に行うことが不可欠」とされている1) 。
インターフェース液症候群 (IFS )はステロイド 誘発性眼圧 上昇に起因するフラップ下液体貯留であり、DLK との鑑別が治療方針を180度変える重要課題である。IFS では眼圧 上昇(ゴールドマン圧平眼圧計 では偽低値が出るため注意)を示し、前眼部OCT では均一な低輝度の液体貯留層を認める。ステロイド の継続投与はIFS を悪化させるため、前眼部OCT と眼圧測定 による鑑別が不可欠である8) 。遅発性のIFS は術後数カ月〜数年後に発症することもあり、フラップ下の液体貯留を認めたら眼圧 計測(特に周辺部・ダイナミック・コントア眼圧 計)を必ず行う必要がある8) 。
フラップ作製角(縦方向・水平方向ベベル角)の変更、フラップヒンジの幅と角度の調整により、フラップのセキュリティが向上し、術後フラップずれのリスクが低下している。特に鼻側ヒンジより上側ヒンジが術後安定性に優れるとの報告がある10) 。フラップ辺縁の側面角を鋭角にする設計(side-cut angle 90°以上)が辺縁部での上皮迷入 リスクを低下させるとの見解もある10) 。また、フラップ厚の均一性はフェムトセカンドレーザー のほうがマイクロケラトームより優れており、有限要素解析ではフラップ厚がバイオメカニクスに与える影響が定量化されている9) 。
SMILE はフラップを作製しないことから、本節で述べたフラップ関連合併症(フラップずれ・DLK ・上皮迷入 ・フリーキャップ・ボタンホール)が原理的に発生しない。KLExガイドラインではectasia発生率がLASIK の10万眼あたり90に対してSMILE では11であり、SMILE のほうが術後エクタジア リスクが低いことが示されている2) 。ただし、SMILE にも層間炎症(DLK 様)・レンチクル残存・タキシン切断等の固有の合併症がある。
術後エクタジア が進行した場合、角膜クロスリンキング (CXL )が第一選択治療である。0.1%リボフラビン点眼後にUVA(3mW/cm²、30分間)を照射するDresden protocolが標準法であり、多くの症例で進行が停止する15) 。加速CXL (9mW/cm²×10分)は治療時間を短縮できる15) 。LASIK 後エクタジア へのCXL の有効性は円錐角膜 への有効性よりやや低い傾向があるが、早期介入が予後を改善する15) 。日本では2022年よりCXL が保険適用となっている。Randlemanスコアリングシステムを用いた術前リスク評価11) 、AAO 角膜拡張症 PPP17) の推奨する術前スクリーニングにより、エクタジア 発症を最大限予防することが重要である。
施設単位でのDLK 発生率をモニタリングし、クラスター発生(短期間に複数症例が集中する)を認識することが重要である。クラスター発生は手術室内の汚染物質・器具の滅菌不備・洗浄液の問題を示唆することが多い16) 。発生率が0.5%を超えるような場合には、手術室・器具・洗浄液の包括的な点検が推奨される。
日本眼科学会屈折 矯正委員会. 屈折 矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-138.
Wang Y, Xie L, Yao K, et al. Evidence-Based Guidelines for Keratorefractive Lenticule Extraction Surgery. Ophthalmology. 2025;132:397-419.
Moshirfar M, Anderson E, Hsu M, et al. LASIK flap complications. StatPearls. 2024.
Ursea R, Feng MT, Zhou M, Cain W, Weikert MP. Temporal analysis of LASIK flap displacement presenting as late complication. Clin Ophthalmol. 2011;5:1535-1538.
Johnson JD, Harissi-Dagher M, Pineda R, et al. Diffuse lamellar keratitis: incidence, associations, outcomes, and a new classification system. J Cataract Refract Surg. 2001;27(10):1560-1566.
Jabbur NS, Chicani CF , Kuo IC, O’Brien TP. Risk factors in interface epithelial ingrowth after LASIK . J Refract Surg. 2004;20(4):343-348.
Recchioni A, Sisó-Fuertes I, Hartwig A, et al. Short-term impact of FS-LASIK and SMILE on dry eye metrics and corneal nerve morphology. Cornea. 2020;39(7):851-857.
Vera-Duarte GR, Guerrero-Becerril J, Müller-Morales CA, et al. Delayed-onset pressure-induced interlamellar stromal keratitis (PIS K) and interface epithelial ingrowth 10 years after laser-assisted in situ keratomileusis. Am J Ophthalmol Case Rep. 2023;32:101874.
Fang L, Wang Y, Yang R, et al. Effects of the LASIK flap thickness on corneal biomechanical behavior: a finite element analysis. BMC Ophthalmol. 2020;20:67.
Slade SG. The use of the femtosecond laser in the customization of corneal flaps in laser in situ keratomileusis. Curr Opin Ophthalmol. 2007;18(4):314-319.
Randleman JB, Woodward M, Lynn MJ, Stulting RD. Risk assessment for ectasia after corneal refractive surgery. Ophthalmology. 2008;115:37-50.
Stulting RD, Randleman JB, Cowan LA, Thompson KP, Bradley EV, Lynn MJ. The epidemiology of diffuse lamellar keratitis. Cornea. 2004;23(7):680-688.
Santhiago MR, Smadja D, Gomes BF, et al. Association between the percent tissue altered and post-LASIK ectasia in eyes with normal preoperative topography. Am J Ophthalmol. 2014;158:87-95.e1.
Moshirfar M, Tukan AN, Bundogji N, et al. Ectasia after corneal refractive surgery: a systematic review. Ophthalmol Ther. 2021;10:753-776.
Hersh PS, Stulting RD, Muller D, et al. U.S. multicenter clinical trial of corneal collagen crosslinking for treatment of corneal ectasia after refractive surgery. Ophthalmology. 2017;124:1475-1484.
Linebarger EJ, Hardten DR, Lindstrom RL. Diffuse lamellar keratitis: diagnosis and management. J Cataract Refract Surg. 2000;26(7):1072-1077.
American Academy of Ophthalmology Corneal/External Disease Preferred Practice Pattern Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: AAO ; 2024.