細隙灯顕微鏡所見
顆粒状浸潤:フラップ下に白色〜灰白色の細かい顆粒状浸潤が散在。「砂」様の外観。
分布の変化:Grade 1は周辺部優位。Grade 2以上では中心部に向かって進展する。
境界の特徴:病巣は境界不明瞭で、フラップ辺縁から中心に向かって広がる傾向がある。
前房炎症:前房炎症は通常軽微または欠如。前房炎症が強い場合は感染性角膜炎との鑑別を優先する。

びまん性層間角膜炎(diffuse lamellar keratitis:DLK)は、LASIK術後にフラップと角膜実質床のインターフェース(層間)に生じる非感染性のびまん性炎症反応である。「サハラの砂」(Sands of Sahara)と形容される細かい白色顆粒状浸潤がフラップ下に散在することが特徴的である。
屈折矯正手術のガイドライン(第8版)では、エキシマレーザー手術およびSMILEの両術式においてDLKが術後合併症として明記されており、適切な対処が求められている1)。LASIK全体における発生率は約0.1〜1%と報告される2)。近年フェムトセカンドレーザーによるフラップ作製が主流となってからもDLKは一定頻度で発生しており、SMILE術後にもDLK様の層間炎症が観察される。KLEx(小切開角膜片抽出術)ガイドラインにおいても、SMILE術後DLKの全体発生率は0.84%と報告されており、Grade I(末梢部限局)が1.42%、Grade II(中心部進展)が0.29%、Grade III(融合・巣状)が0.08%、Grade IV(重症)が0.02%の内訳となっている3)。
感染性角膜炎とは病態が全く異なり、菌の関与がない点が本疾患の本質である。一方、見た目が類似する炎症性疾患であるIFS(インターフェース液症候群/PISK)との鑑別は治療方針を180度変えるため、最も重要な臨床課題である。
DLKはLASIK術後に最も多く発生しますが、SMILE(小切開角膜抽出術)後にも発生することがあります。屈折矯正手術のガイドライン(第8版)でも、エキシマレーザー手術とSMILEの両者でDLKが術後合併症として挙げられています。PRKはフラップを作製しないためDLKは発生しません。フェムトセカンドレーザー普及後もDLKの発生はゼロにはなっておらず、術後1〜5日の緻密な観察と早期介入が良好な予後のカギです。特にGrade 1〜2の早期発見と迅速なステロイド治療開始が、Grade 3〜4への進行を予防する上で最も重要です。なお、PRKはフラップを作製しないためDLKは発生しない一方、術後のhaze(上皮下混濁)のリスクがあり、マイトマイシンCを用いた予防的処置が施される場合があります。術式の特徴を熟知した上での個別の患者への説明が求められます。
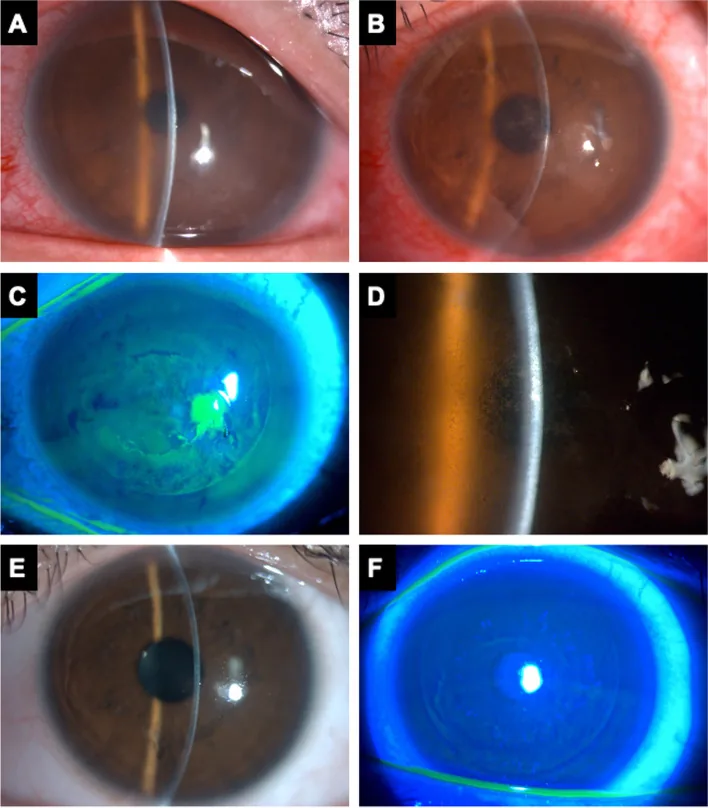
DLKの自覚症状は重症度(Grade)に依存する。
発症時期は術後1〜5日が典型的であり、フラップ作製直後から炎症メディエーターが蓄積して発現すると考えられている。ただし、術後数週間〜数カ月後の遅発型も報告されており、ステロイド点眼を中断した際に再燃する症例もある。
細隙灯顕微鏡での反帰光(retroillumination)観察がDLKの診断において最も重要な所見をもたらす。反帰光で観察すると後方から光が当たるため、フラップ下の細胞浸潤の状況が把握しやすくなる。初心者のうちは「砂嵐のような外観」という形容が直感的に分かりにくいこともあるが、経験を積むと非常に特徴的な所見として認識できるようになる。Grade 1〜2では顆粒状浸潤が主として周辺部に分布し、Grade 2以上では浸潤が中央部に向かって進展する。「サハラの砂(Sands of Sahara)」という呼称は、細かい白色顆粒状浸潤の広がり方を的確に表す臨床的な表現として用いられている。
細隙灯顕微鏡所見
顆粒状浸潤:フラップ下に白色〜灰白色の細かい顆粒状浸潤が散在。「砂」様の外観。
分布の変化:Grade 1は周辺部優位。Grade 2以上では中心部に向かって進展する。
境界の特徴:病巣は境界不明瞭で、フラップ辺縁から中心に向かって広がる傾向がある。
前房炎症:前房炎症は通常軽微または欠如。前房炎症が強い場合は感染性角膜炎との鑑別を優先する。
前眼部OCT所見
DLKの発症には複数の誘因が関与している。いずれも「フラップ下の閉鎖空間に炎症誘発物質が封入される」という共通の機序を経由する。
内因性誘因:
外因性誘因:
環境・施設要因: DLKのクラスター発生(施設内での短期集中的多発)は、手術室内の汚染物質(有機揮発物・エンドトキシン等)を示唆することが多い6)。施設全体でのDLK発生率モニタリングにより原因を特定し、環境改善措置を講じることが重要である。特定のロットの洗浄剤・滅菌液・点眼液との関連が報告されている。
感染性炎症(細菌・真菌・アカントアメーバ)はDLKの定義上除外されるが、感染が誘因となりDLK様反応を惹起することもある。
発生率に影響する因子:
DLKはGrade 1〜4の4段階で重症度を評価する。この分類は治療方針の決定に直結する2)。
| Grade | 細隙灯所見 | 視力への影響 | 治療方針 |
|---|---|---|---|
| Grade 1 | 周辺部のみに白色顆粒状浸潤(中心部は正常) | ほぼ影響なし | ステロイド点眼頻回投与・経過観察 |
| Grade 2 | 浸潤が瞳孔域を含む中央部に向かって拡大 | 軽度視力低下 | ステロイド点眼増量・翌日再診 |
| Grade 3 | 中央部に達する高度浸潤・基質融解の初期兆候 | 中等度視力低下 | ステロイド点眼+フラップリフト・洗浄を強く検討 |
| Grade 4 | 中央部基質融解(keratolysis)・瘢痕形成 | 著明な視力低下 | 緊急フラップリフト・洗浄(ステロイド全身投与考慮) |
DLKの診断で最も重要な鑑別は以下の2疾患である。
IFS(インターフェース液症候群/PISK)との鑑別:
IFSはステロイド誘発性眼圧上昇に起因するフラップ下液体貯留であり、炎症細胞を伴わず眼圧上昇が本態である。DLKをIFSと誤診してステロイド投与を継続すると眼圧がさらに上昇してIFSが悪化する4)。一方でIFSをDLKと誤診してステロイドを控えると、DLKは進行して角膜ストロマ融解に至る。
| 鑑別点 | DLK | IFS(PISK) |
|---|---|---|
| 発症時期 | 術後1〜5日 | 術後数日〜数カ月(遅発例あり) |
| 炎症細胞 | 多核白血球浸潤あり | 炎症細胞なし(浮腫のみ) |
| 眼圧 | 正常 | 上昇(ゴールドマン計測は偽低値) |
| 前眼部OCT | 点状高輝度域 | 均一な低輝度液体層(フラップ離解) |
| ステロイド反応 | 有効(Grade 1〜2) | 悪化する |
| 治療 | ステロイド点眼増量 | ステロイド中止+眼圧降下薬 |
感染性角膜炎との鑑別:
感染性角膜炎(細菌・真菌・アカントアメーバ)は前房炎症を伴うことが多い。強毒菌や真菌による実質炎では前房内フィブリン析出を認める場合がある。非感染性角膜炎(DLK含む)では前房炎症は通常軽微である。局所集中する浸潤・充血・分泌物が強い場合は感染を疑う。
| 検査 | 目的 | DLKでの所見 |
|---|---|---|
| 細隙灯顕微鏡(反帰光) | 顆粒状浸潤の評価 | フラップ下の点状白色浸潤 |
| 前眼部OCT | フラップ下液体 vs 炎症細胞の鑑別 | 点状高輝度域(IFSは均一液体層) |
| 眼圧測定 | IFSの除外 | 正常(IFSでは上昇) |
| 角膜培養・スメア | 感染性角膜炎の除外 | 陰性 |
| 角膜形状解析 | 基質融解による不正乱視の評価 | 進行例では不規則パターン |
屈折矯正手術のガイドライン(第8版)1)では術翌日の細隙灯顕微鏡検査が義務付けられているが、DLK管理においては以下の観察頻度が推奨される:
Grade 1〜2 DLKの多くは術後2週間以内に完全消退するが、Grade 3〜4は基質融解により永続的な不正乱視が残存する可能性があるため、治療完了後も3〜6か月にわたる角膜形状解析のフォローアップが推奨される9)。
DLKとIFS(インターフェース液症候群)の鑑別で最重要な点は「眼圧」です。IFSでは眼圧が上昇しますが、ゴールドマン圧平眼圧計の中央測定では液体クッション効果により偽低値が出ることがあるため、周辺部またはダイナミック・コントア眼圧計での測定が推奨されます。前眼部OCTでは、DLKでは点状の高輝度域、IFSではフラップを持ち上げる均一な低輝度液体層が特徴的です。DLKは術後早期(1〜5日)に疼痛と白色顆粒浸潤で発症するのに対し、IFSは霧視と眼圧上昇が主徴で炎症細胞を欠きます。治療がまったく逆(DLK→ステロイド増量、IFS→ステロイド中止+眼圧降下)なため、誤診は深刻な結果をもたらします。
治療はGrade分類に従って決定する。
ステロイド点眼の頻回投与が第一選択である。
ステロイド点眼を継続しながら、フラップリフト・生食洗浄を強く考慮する。
SMILEでのGrade IIIでは高用量ステロイドに加えて層間洗浄を考慮する3)。SMILE術後の層間洗浄はLASIKよりアクセスが難しいため、十分な経験を有する術者が行う必要がある。
緊急フラップリフト・洗浄が必須である。
| Grade | 初期対応 | 再診間隔 | 介入閾値 |
|---|---|---|---|
| 1 | プレドニゾロン1%点眼 1〜2時間毎 | 翌日〜2日後 | Grade 2以上への進行でフラップリフト検討 |
| 2 | 同上・増量。翌日再診確認 | 翌日 | 改善なければ翌日フラップリフト |
| 3 | ステロイド点眼+フラップリフト・洗浄 | 当日〜翌日 | 原則フラップリフト実施 |
| 4 | 緊急フラップリフト・洗浄(全身ステロイド考慮) | 当日緊急 | 即時介入 |
GradeによってDLKの治療は異なります。Grade 1〜2であれば、プレドニゾロン1%点眼液を1〜2時間おきの頻回点眼で治療します。多くの症例はこの治療で1〜2週間以内に改善します。Grade 3では点眼に加えてフラップリフト(フラップの再開放)と生食洗浄が必要になる場合があります。Grade 4(基質融解)では緊急のフラップリフト・洗浄が必要であり、全身ステロイドも考慮されます。自己判断で点眼を中断せず、術後に視力低下や強い羞明を感じたら速やかに担当医に連絡してください。
DLKは多核白血球(好中球)主体の非感染性炎症反応である。フラップ作製時に生じた切削粉末・手術器具由来の微粒子・生体由来の刺激物質が角膜インターフェースの閉鎖空間に封入されると、局所でサイトカイン(IL-1β・IL-6・TNF-α等)・ケモカイン(IL-8・MCP-1等)が産生され好中球が集積する。この炎症反応は感染性炎症と異なり細菌・真菌の増殖を伴わない。
フラップは術後も完全には再癒合しないため、インターフェースは半閉鎖空間として機能する。この空間が炎症細胞と炎症メディエーターを「封じ込める」構造的特性がDLKの局在をフラップ下に限定させる。
フラップ界面の内腔は通常の角膜実質と接触する部分が少ないため、好中球の動員経路は主に角膜緣部の血管網や角膜實質内の既存細胞(角膜実質細胞・ランゲルハンス細胞)を経由すると考えられている。炎症の発症から重症化(Grade 1→4)にかけての速度は個人差が大きく、一部の症例では術後1〜2日で急速にGrade 4まで進行することがある。術後数日間の緻密な観察がDLKの管理において絶対に欠かせない理由はここにある。
重症DLK(Grade 4)では、好中球由来の基質分解酵素(MMP-8・MMP-9等のマトリックスメタロプロテアーゼ)が大量に放出されてコラーゲン線維を分解し、角膜ストロマ融解が生じる。融解が中心部に達すると恒久的な視力低下・不正乱視の原因となる。早期介入(フラップリフト・洗浄)によってMMP産生好中球を物理的に除去することが、融解進行阻止の重要な根拠となる。
DLKでは炎症性多核白血球と単核球の層間集積が病理学的に認められるのに対し、IFSでは炎症細胞は欠如し実質浮腫のみが認められる4)。この病理学的相違が両疾患の治療方針を分ける根本的根拠である。
フェムトセカンドレーザーによるフラップ作製ではマイクロケラトームと比較してフラップ精度が向上したが、レーザー照射によるOBL(opaque bubble layer)形成が一過性の界面反応を惹起することがある。フォトディスラプション(光破壊)によるプラズマ形成と微細気泡は、局所の炎症反応の誘因になる可能性がある5)。フェムトセカンドレーザー特有のDLK増加は必ずしも示されていないが、OBL関連炎症とDLKの鑑別が重要とされている。
OBLはフェムトセカンドレーザー使用時に10〜30%の症例で認められ、多くは術後数時間〜数日で自然消退する。ただし広範なOBLはエキシマレーザーの眼球追尾を妨げ、照射精度低下の原因となるため、術中に確認された場合は消退を待つことが多い。OBL自体が炎症を引き起こすとは考えられていないが、OBLとDLKが同時に観察される場合は、DLKの進行評価に反帰光照明が特に有用である。
SMILEでのDLKはキャップ(フラップ相当)下の層間で生じるが、LASIK同様の病態・治療原則が適用される3)。ただし2〜3mmの小切開から器具を挿入するため、層間洗浄の難度がLASIKより高い。KLExガイドラインでは適切なステロイド治療により多くの症例で1週間以内に病巣が改善し、約3週間で症状が消失するとしている3)。
SMILE術後DLKの発生率(0.84%)はLASIK術後DLKの発生率(0.1〜1%)と概ね類似しており、術式そのものよりもフラップ/キャップ界面の存在が共通の誘因と考えられる。SMILEではフラップ関連合併症(フラップずれ・フリーキャップ等)は発生しないが、DLKの管理においては同様の注意が必要であり、術後1〜5日の観察が特に重要である。Grade 3〜4のSMILE後DLKに対する層間洗浄は、担当医が十分なSMILE術後管理の経験を有することが前提となる3)。
DLKは屈折矯正手術後の合併症の中でも、早期診断と適切な治療により視力転帰が大幅に改善しうる疾患である。術後早期の綿密な観察スケジュールを設け、患者に症状悪化時の早期受診を十分に指導することが、DLKによる視力障害を予防するための基本的かつ最も重要な管理戦略である。
DLKの発症率は手術環境の改善によって低減されることが知られている。具体的には、洗浄液の品質管理(蒸留水・BSS等の純度)、外科用手袋の変更(タルクフリー手袋の使用)、器具の超音波洗浄強化、手術室の陽圧維持によるエンドトキシン混入防止が重要とされる6)。施設単位でのDLK発生率の継続モニタリングが、原因特定と対策立案に不可欠である。
2022年のブラジル眼科アーカイブスの総説では、既存のGrade 1〜4分類を補完する拡張分類が提唱され、線維性応答(Grade 5)や前房浸潤を伴う重症型(Grade 6相当)の概念も示されている7)。ただし現時点では国際的なコンセンサスはGrade 1〜4分類が標準である。
術前・術中に局所ステロイド(プレドニゾロン等)を使用することでDLK発生率を低下させる可能性があるとの報告がある8)。一方でステロイド感受性の高い患者では眼圧上昇のリスクがあるため、個別のリスク評価が必要である。
DLKは屈折矯正手術後合併症のうちでも診断と治療の判断を要求する代表的な疾患である。Swanson et al.9)の総説では、屈折矯正手術後のDLK・上皮迷入・フラップ関連合併症のそれぞれについて発生率・危険因子・治療成績が整理されており、DLKが最も頻度の高い合併症(LASIK術後0.1〜1%)であることが確認されている。Phipps et al.10)のレビューでは、DLKの病態・Grade分類・鑑別診断・治療について最新のエビデンスが体系的に整理されており、Grade 1〜2は保存的治療で90%以上が回復し、Grade 3〜4では早期フラップリフト・洗浄が視力予後を左右することが強調されている。
Moshirfar et al.11)のフラップ合併症レビューでは、DLKがマイクロケラトームとフェムトセカンドレーザーの両デバイスで同様の頻度で発生することが示されており、フラップ界面の存在そのものがDLKの必要条件であることが論じられている。フェムトセカンドレーザー特有のOBL(opaque bubble layer)形成がDLK発症の誘因となる可能性についても検討されている11)。
Venkataraman et al.12)は、LASIK後10年以上経過して発症したIFSを含む遅発性IFSの症例シリーズを報告し、IFSがLASIK後のいかなる時点でも発症しうること、発症時の眼圧測定(周辺部測定・ダイナミック・コントア眼圧計の使用)と前眼部OCTが鑑別に不可欠であることを示した12)。
Slade13)はフェムトセカンドレーザーによるフラップカスタマイズ(フラップ厚・ヒンジ角度・側面カット角)がフラップのセキュリティと合併症プロフィールに与える影響を論じており、適切なフラップ設計(均一な厚さ・適切なヒンジ幅・鋭角側面カット)が術後のフラップずれ・DLK発生率の低減に寄与することを示している13)。
Randleman et al.14)のエクタジアリスクスコアリングシステムは、術後エクタジアの発症予測因子として「角膜形状異常・RST低値・若年・薄い角膜・高度近視」の5因子を同定した。エクタジアとDLKは独立した合併症であるが、Grade 3〜4 DLKで基質融解が生じた場合は角膜の構造的脆弱性が高まり、潜在的なエクタジアリスクが増大する可能性がある14)。
AAO角膜拡張症PPP15)では、術後エクタジアの管理においてCXL(角膜クロスリンキング)が第一選択治療として推奨されており、DLKによる基質融解が進行した症例でもCXL適応を検討する場合があることが示されている。ただしCXLの適応は進行が確認された場合に限られ、DLK単独ではCXL適応とはならない15)。
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-138.
Johnson JD, Harissi-Dagher M, Pineda R, et al. Diffuse lamellar keratitis: incidence, associations, outcomes, and a new classification system. J Cataract Refract Surg. 2001;27(10):1560-1566.
Wang Y, Xie L, Yao K, et al. Evidence-Based Guidelines for Keratorefractive Lenticule Extraction Surgery. Ophthalmology. 2025;132:397-419.
Vera-Duarte GR, Guerrero-Becerril J, Müller-Morales CA, et al. Delayed-onset pressure-induced interlamellar stromal keratitis (PISK) and interface epithelial ingrowth 10 years after laser-assisted in situ keratomileusis. Am J Ophthalmol Case Rep. 2023;32:101874.
Kymionis GD, Naoumidi TL, Aslanides IM, Pallikaris IG, Siganos CS. Diffuse lamellar keratitis after laser in situ keratomileusis with the IntraLase femtosecond laser. J Cataract Refract Surg. 2007;33(8):1471-1473.
Stulting RD, Randleman JB, Cowan LA, Thompson KP, Bradley EV, Lynn MJ. The epidemiology of diffuse lamellar keratitis. Cornea. 2004;23(7):680-688.
Rosa DS, de Macedo ELS, Leal LA, et al. Diffuse lamellar keratitis after LASIK: literature review and proposed new grading. Arq Bras Oftalmol. 2022;85(2):198-204.
Linebarger EJ, Hardten DR, Lindstrom RL. Diffuse lamellar keratitis: diagnosis and management. J Cataract Refract Surg. 2000;26(7):1072-1077.
Swanson ME, Naidoo KS. Corneal complications following refractive surgery: a review. Cont Lens Anterior Eye. 2016;39(4):268-278.
Phipps MD, Nassiri N. Diffuse lamellar keratitis. StatPearls. 2023.
Moshirfar M, Anderson E, Hsu M, et al. LASIK flap complications. StatPearls. 2024.
Venkataraman P, Shroff A, Prabu S, Senthilkumar N. Behind the blur: Understanding interface fluid syndrome in post-LASIK patients. Indian J Ophthalmol. 2025.
Slade SG. The use of the femtosecond laser in the customization of corneal flaps in laser in situ keratomileusis. Curr Opin Ophthalmol. 2007;18(4):314-317.
Randleman JB, Woodward M, Lynn MJ, Stulting RD. Risk assessment for ectasia after corneal refractive surgery. Ophthalmology. 2008;115:37-50.
American Academy of Ophthalmology Corneal/External Disease Preferred Practice Pattern Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: AAO; 2024.