活動性病変

多巣性脈絡膜炎(MCP)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 多巣性脈絡膜炎とは
Section titled “1. 多巣性脈絡膜炎とは”多巣性脈絡膜炎(multifocal choroiditis with panuveitis; MFCwP)は、「特発性多巣性脈絡膜炎(IMFC; idiopathic multifocal choroiditis)」とも呼ばれ、網膜色素上皮(RPE)と脈絡膜毛細血管レベルに複数の炎症性病変を呈する自然発症の炎症性疾患である。炎症エピソードを繰り返し、両眼性・同時性または非同時性に発症する。
1984年にDeutschとTesslerが「偽POHS(pseudo-POHS)」として28症例を報告した。1986年にMorganとShatzが「再発性多巣性脈絡膜炎(recurrent multifocal choroiditis)」として11症例を記述し、POHS患者には見られない硝子体炎症を特徴として指摘した。MCPとPIC(点状内層脈絡膜症)はともに白点症候群(white dot syndromes; WDS)の一亜型であり、外網膜・脈絡膜毛細血管・脈絡膜を主座とする炎症性疾患群に属する1)。両疾患は同一疾患スペクトラムの可能性も示唆されている1)。
多モード画像診断の進歩により、MCPとPICは同一スペクトラムの異なる表現型(硝子体炎の有無と病巣サイズで区別)と再定義されている6)。白斑症候群(white dot syndromes)の一群として、多発性消失性白点症候群(MEWDS)・PIC・MCP・びまん性網膜下線維化症候群(DSF)・急性後部多発性斑状色素上皮症(APMPPE)などとともに AZOOR complex の概念内に位置づけられる。
ぶどう膜炎診療ガイドライン(日眼会誌 2019;123(6):635-696)では「汎ぶどう膜炎を伴う多発性脈絡膜炎」としてPICの鑑別疾患に挙げられており5)、硝子体炎を伴う点でPICとの重要な鑑別点とされている。
最大の違いは硝子体炎の有無である。POHSには硝子体炎が伴わないがMCPでは通常片眼または両眼に硝子体炎が見られる。またMCPでは軽度の前房炎症も認められることがある。さらにMCPはヒストプラスマ抗体陰性であり、ヒストプラスマ流行地域(米国オハイオ川流域等)の居住歴がない患者でも発症しうる点も鑑別の手がかりとなる。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”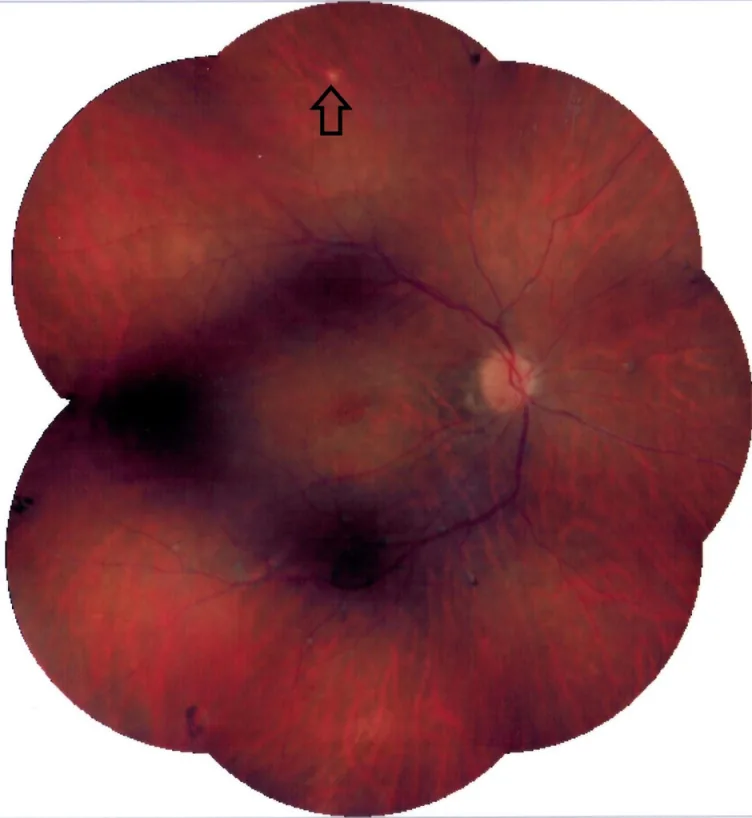
- 飛蚊症:硝子体炎による。最も一般的な初発症状のひとつ
- 視力低下・霧視:黄斑浮腫、脈絡膜新生血管、または病変の中心窩への進展による
- 光視症:活動性炎症病変の刺激による
- 変視症:黄斑部の病変や浮腫による歪視
- 暗点(スコトマ):炎症病変に対応した視野欠損
- 羞明・眼の不快感:前房炎症の程度により変動する
前房炎症(軽度)と硝子体炎症を伴う点がPICとの重要な鑑別点である5)。近視患者では硝子体炎の評価が困難なことがあり、OCT-A や ICG 所見が補助診断として有用である7)。
病変は4タイプに分類される:活動性炎症病変・非活動性炎症病変・二次性活動性脈絡膜新生血管・二次性非活動性脈絡膜新生血管。
非活動性病変
色調:灰色で境界明瞭。瘢痕線維化と色素沈着が見られる。
形態:萎縮性の打ち抜き状(punched-out)変色した網膜色素上皮病変として認められる。
予後:病変が瘢痕化すると視力回復が困難になることがある。
その他の合併症:
- 緑内障
- 視神経萎縮
- 黄斑萎縮
- 進行性網膜下瘢痕
- 嚢胞様黄斑浮腫(嚢胞状黄斑浮腫)
長期コホートでは、CNVが視力低下の主要因であり、嚢胞様黄斑浮腫や黄斑前膜も視力低下と関連した9)。視力低下リスクの評価では、CNV、中心窩にかかる萎縮瘢痕、黄斑部病変密集に注意する。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”MCPの病因は不明である。先行する感染症が免疫反応を刺激するという仮説があるが、特定の病原体は同定されていない。
疫学的特徴:
- 白人女性に多い
- 発症時平均年齢30歳(範囲:6〜69歳)
- ほとんどの患者が近視
- 既知の全身疾患や眼疾患のない健常者に影響
遺伝的素因: MCPはIL-10および腫瘍壊死因子(TNF)のハプロタイプと関連している。AZOOR complex の一疾患としての遺伝的素因 + 環境因子説が提唱されている。
病態仮説: 炎症病変は網膜色素上皮および脈絡膜毛細血管レベルから始まる。外来抗原によって網膜光受容体および網膜色素上皮で抗原感作が生じ、ブルッフ膜(Bruch’s membrane)の完全性が損なわれる可能性がある。これにより脈絡膜新生血管膜が発生する余地が生じ、最大60%の患者で脈絡膜新生血管が発生しうる。
4. 診断と検査方法
Section titled “4. 診断と検査方法”MCPは臨床診断であり、除外診断である。感染性・悪性・全身性疾患を除外することが必須である。ぶどう膜炎診療ガイドラインでも「定まった診断基準なし、特徴的所見と除外診断」とされている5)。
MCPの診断要件:
- 両眼性・後極部主体の多発小白斑
- 前眼部炎症または硝子体炎の存在(PICとの鑑別に必須)
- 感染性・全身性疾患の除外(梅毒・結核・サルコイドーシス等)
- 悪性疾患(リンパ腫・転移)の除外
多モード画像診断
Section titled “多モード画像診断”| 検査 | 活動性病変所見 | 非活動性病変所見 |
|---|---|---|
| 蛍光眼底造影(FA) | 早期過蛍光→後期染色 | ウィンドウ欠損による過蛍光 |
| インドシアニングリーン蛍光造影(ICG) | 早期〜中期の低蛍光1) | 全相での低蛍光斑 |
| 眼底自発蛍光 | 高自発蛍光病変(視神経周囲・後極部) | 低自発蛍光の萎縮性病変 |
光干渉断層計(OCT)所見:
- 活動性病変:網膜色素上皮下腔への物質沈着による RPE 隆起1)
- EDI-OCT:活動性病変下の脈絡膜肥厚
- 網膜下・網膜色素上皮下液体の存在は脈絡膜新生血管を示唆
- OCT血管造影(OCT-A):脈絡膜毛細血管レベルの血流低下領域(活動性炎症病変に対応)1)
急性炎症病変と脈絡膜新生血管の鑑別には、フルオレセイン蛍光眼底造影だけでなく、SD-OCTやOCT-Aを含む多画像評価を組み合わせる2, 7)。
MCPとPICの画像的鑑別: MCP・IMFC と PIC の鑑別において、近視性CNVや PIC に特徴的な所見の整理が重要である。MCPでは病巣サイズが45〜350μmと大きく、ICGで広範囲の低蛍光を示す傾向がある。PICではより小型(125〜250μm)で後極部に限局し、硝子体炎を伴わない7)。
感染性:POHS、梅毒、結核、トキソプラズマ症、ウエストナイルウイルス、ニューモシスチス脈絡膜炎
非感染性:サルコイドーシス、PIC(点状内層脈絡膜症)、バードショット網脈絡膜症、急性後部多発性斑状色素上皮症
悪性:リンパ腫、転移
基本的臨床検査:血算、総合代謝パネル、アンジオテンシン変換酵素、胸部X線、梅毒検査、クォンティフェロンTBゴールド
結核流行地域(インドなど)では、多巣性脈絡膜炎の最大40%が眼結核と関連する可能性があるとされており3)、光干渉断層計で網膜色素上皮下の炎症性病変として観察されることがある3)。
多モード画像診断が鑑別に有用である。結核性多巣性脈絡膜炎では、光干渉断層計で網膜色素上皮下炎症性病変に外境界膜の断裂や楕円体帯の限局的消失を認めることがある3)。クォンティフェロンTBゴールド検査や画像診断を組み合わせて評価する。結核流行地域や、結核の既往・露出歴がある場合は積極的に除外検査を行う。
5. 標準的な治療法
Section titled “5. 標準的な治療法”炎症の程度・活動性病変・合併症・視力低下に基づいて治療を選択する。嚢胞様黄斑浮腫、濃い硝子体炎、または脈絡膜新生血管膜発現が治療適応となる。
ステロイド療法
Section titled “ステロイド療法”経口ステロイド:治療の第一選択。活動性病変で硝子体炎・前房炎症を伴う場合はプレドニゾロン 0.5〜1 mg/kg/日を中心にステロイド全身投与を行い、炎症消退に応じて漸減する5)。
局所ステロイド:
- トリアムシノロンアセトニド(ケナコルト-A):テノン嚢下または眼内注射。作用持続期間2〜3か月
- デキサメタゾン硝子体内インプラント 0.7mg(オズデックス®):後眼部非感染性ぶどう膜炎に適応。作用持続期間3〜4か月。投与30分以内に眼圧測定、2〜7日後に細隙灯検査を要する
- フルオシノロンアセトニドマイクロインプラント(イリュービエン®):最長3年間の低用量ステロイド持続放出
免疫調節療法
Section titled “免疫調節療法”難治性・再発性・ステロイド依存性症例では免疫調節薬を検討する。シクロスポリン・アザチオプリン・ミコフェノール酸モフェチル(MMF)で維持療法を行い、難治例は抗TNFα製剤(アダリムマブ)を検討する5)。
国際研究グループの調査(n=221名のぶどう膜専門医)では、多巣性脈絡膜炎-PICスペクトラム疾患に対して、従来型免疫調節薬の第一選択はメトトレキサート(39.4%)、生物学的製剤の第一選択はアダリムマブ(95.5%)であった4)。
長期視力予後の観点から、炎症制御とCNV管理が重要である。Johns HopkinsのMFCPUコホートでは、CNV、嚢胞様黄斑浮腫、黄斑前膜などの後極部合併症が視力低下と関連した9)。Kedharらの比較研究でも、MFCPUではPICより白内障、嚢胞様黄斑浮腫、黄斑前膜などの炎症合併症が多いことが示されている8)。
抗VEGF療法
Section titled “抗VEGF療法”活動性の脈絡膜新生血管および黄斑浮腫に対して硝子体内抗VEGF療法を使用する。抗VEGF単独では炎症背景の CNV 制御が不十分なことが多く、ステロイド療法・免疫調節療法との併用が推奨される。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”炎症病変は網膜色素上皮と脈絡膜毛細血管レベルから始まり、外来抗原によって網膜色素上皮で抗原感作が生じると仮説されている。
MCPとPICはともに外層網膜・脈絡膜毛細血管・脈絡膜に関与し、同一疾患スペクトラムの可能性がある1)。MCPは慢性・両眼性・再発性の炎症性疾患で、前部ぶどう膜炎・硝子体炎を伴う後部病変が特徴である一方、PICは硝子体炎・前眼部炎症所見を伴わない点で異なる1)。Spaideらによる多モード画像診断を用いた再定義では、MCPとPICを「脈絡膜毛細血管板の原発性炎症性疾患」として統一的に捉え、硝子体炎の有無を主要鑑別点としている6)。
OCT血管造影(OCT-A)所見では、脈絡膜毛細血管レベルでの明確な血流低下領域が活動性炎症病変に対応しており1)、外層網膜変化が一次性脈絡膜関与の続発変化である可能性を支持する。OCT-Aは活動性炎症のモニタリング・CNV検出の両面で有用性が高まっている。
炎症によってブルッフ膜の完全性が損なわれ、これが脈絡膜新生血管膜発生の足がかりとなる。MCPでは最大60%の患者で脈絡膜新生血管が発生しうる。CNVは炎症性(inflammatory)CNVとして抗VEGF療法への反応が得られるが、下地の炎症制御が不可欠である。
遺伝的要因としてIL-10および腫瘍壊死因子のハプロタイプとの関連が示されているが、正確なメカニズムは依然不明のままである。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”OCT血管造影による脈絡膜毛細血管評価
Section titled “OCT血管造影による脈絡膜毛細血管評価”OCT血管造影は、MCP病変の脈絡膜毛細血管において明確な血流低下を示し、活動性炎症病変に対応する1)。治療後の脈絡膜血管変化のモニタリングにも応用されており、蛍光造影を行わずに疾患活動性を非侵襲的に評価できる可能性がある。
OCT血管造影は、脈絡膜毛細血管の血流低下エリアを光干渉断層計上の網膜色素上皮隆起やインドシアニングリーン蛍光造影の低蛍光スポットと対応させて描出できることが示されており、病態生理学的理解を深めている1)。
疾患スペクトラムの再定義と個別化治療
Section titled “疾患スペクトラムの再定義と個別化治療”Spaideらは多モード画像診断によりMFCwPとPICを再定義し、同一スペクトラムである可能性を示唆した6)。より精密な病型分類と個別化治療の開発が進んでいる。近視性CNVとMCP/PICのCNVを鑑別する多モード画像診断の基準も提唱されており7)、抗VEGF療法の適正適用が期待されている。
8. 参考文献
Section titled “8. 参考文献”- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- Vance SK, Khan S, Klancnik JM, Freund KB. Characteristic spectral-domain optical coherence tomography findings of multifocal choroiditis. Retina. 2011;31(4):717-723. PMID: 21386760. doi:10.1097/IAE.0b013e318203c1ef.
- Kaza H, Gala JM, Rani PK. Subfoveal retinal pigment epithelium inflammatory lesion presenting as a sign of reactivation of tubercular multifocal choroiditis. BMJ Case Rep. 2021;14:e240280.
- Branford JA, et al. Practice patterns of systemic immunomodulatory drug treatment for non-infectious uveitis: an international study. Br J Ophthalmol. 2025;109:482-489.
- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(PIC・地図状脈絡膜炎節参照). 日本眼科学会雑誌. 2019;123(6):635-696.
- Spaide RF, Goldberg N, Freund KB. Redefining multifocal choroiditis and panuveitis and punctate inner choroidopathy through multimodal imaging. Retina. 2013;33(7):1315-1324.
- Dolz-Marco R, Fine HF, Freund KB. How to differentiate myopic choroidal neovascularization, idiopathic multifocal choroiditis, and punctate inner choroidopathy using clinical and multimodal imaging findings. Ophthalmic Surg Lasers Imaging Retina. 2017;48(3):196-201.
- Kedhar SR, Thorne JE, Wittenberg S, Dunn JP, Jabs DA. Multifocal choroiditis with panuveitis and punctate inner choroidopathy: comparison of clinical characteristics at presentation. Retina. 2007;27(9):1174-1179. doi:10.1097/IAE.0b013e318068de72.
- Thorne JE, Wittenberg S, Jabs DA, Peters GB, Reed TL, Kedhar SR, Dunn JP. Multifocal choroiditis with panuveitis: incidence of ocular complications and of loss of visual acuity. Ophthalmology. 2006;113(12):2310-2316. doi:10.1016/j.ophtha.2006.05.067.
