คอรอยด์ อักเสบหลายจุด (MCP ; multifocal choroiditis with panuveitis; MFCwP) เป็นโรคเรื้อรังทั้งสองข้าง ซึ่งมีรอยโรคอักเสบหลายจุดในระดับเยื่อบุผิวรงควัตถุจอตาและเส้นเลือดฝอยคอรอยด์ หรือที่เรียกว่า idiopathic multifocal choroiditis (IMFC ) หรือร่วมกับ panuveitis (MFCwP) แตกต่างจาก punctate inner choroidopathy (PIC ) โดยมี vitritis และการอักเสบของช่องหน้าตา
พบบ่อยในหญิงผิวขาว อายุเฉลี่ยที่เริ่มป่วย 30 ปี ผู้ป่วยส่วนใหญ่มีสายตาสั้น
เส้นเลือดใหม่ในคอรอยด์ (CNV ) เกิดขึ้นในผู้ป่วยถึง 60% และเป็นภาวะแทรกซ้อนที่สำคัญที่สุดที่ส่งผลต่อพยากรณ์การมองเห็น เป็นการวินิจฉัยโดยการแยกโรค จำเป็นต้องแยกจากโรคติดเชื้อ โรคร้าย และโรคทางระบบ
การรักษาหลักคือการใช้สเตียรอยด์ ร่วมกับการปรับภูมิคุ้มกัน ต้องจัดการในระยะยาว
โรคคอรอยด์ อักเสบหลายจุดร่วมกับ panuveitis (MFCwP) หรือที่เรียกว่า idiopathic multifocal choroiditis (IMFC ) เป็นโรคอักเสบที่เกิดขึ้นเองโดยมีรอยโรคอักเสบหลายจุดที่ระดับ retinal pigment epithelium (RPE ) และ choroidal capillaries อาการอักเสบเกิดขึ้นซ้ำๆ เป็นสองตา พร้อมกันหรือไม่พร้อมกัน
ในปี 1984 Deutsch และ Tessler รายงาน 28 รายในชื่อ “pseudo-POHS ” ในปี 1986 Morgan และ Shatz บรรยาย 11 รายในชื่อ “recurrent multifocal choroiditis” และชี้ให้เห็น vitritis เป็นลักษณะที่ไม่พบในผู้ป่วย POHS ทั้ง MCP และ PIC (punctate inner choroidopathy) เป็นชนิดย่อยของ white dot syndromes (WDS ) และอยู่ในกลุ่มโรคอักเสบที่มีผลต่อจอประสาทตา ชั้นนอก choroidal capillaries และคอรอยด์ เป็นหลัก 1) มีข้อเสนอว่าทั้งสองโรคอาจเป็นสเปกตรัมของโรคเดียวกัน 1)
ด้วยความก้าวหน้าของการวินิจฉัยด้วยภาพหลายรูปแบบ MCP และ PIC ถูกนิยามใหม่เป็นฟีโนไทป์ที่แตกต่างกันของสเปกตรัมเดียวกัน (แยกโดยการมีหรือไม่มี vitritis และขนาดรอยโรค) 6) ในฐานะส่วนหนึ่งของ white dot syndromes พวกมันถูกจัดอยู่ในแนวคิด AZOOR complex ร่วมกับ multiple evanescent white dot syndrome (MEWDS ), PIC , MCP , diffuse subretinal fibrosis syndrome (DSF) และ acute posterior multifocal placoid pigment epitheliopathy (APMPPE )
ในแนวทางปฏิบัติทางคลินิกสำหรับ uveitis (Jpn J Ophthalmol 2019;123(6):635-696) ระบุ “multifocal choroiditis with panuveitis” เป็นโรคที่ต้องแยกจาก PIC และการมี vitritis เป็นจุดแยกสำคัญจาก PIC 5)
Q
POHS กับ MCP ต่างกันอย่างไร?
A
ความแตกต่างที่สำคัญที่สุดคือการมีหรือไม่มีภาวะวุ้นตา อักเสบ (vitritis) POHS จะไม่มีวุ้นตา อักเสบ แต่ใน MCP มักพบวุ้นตา อักเสบในตาข้างเดียวหรือทั้งสองข้าง นอกจากนี้ MCP อาจพบการอักเสบของช่องหน้าม่านตา เล็กน้อยได้ด้วย ยิ่งไปกว่านั้น MCP มีผลตรวจแอนติบอดีต่อฮิสโตพลาสมาเป็นลบ และสามารถเกิดในผู้ป่วยที่ไม่มีประวัติอาศัยในพื้นที่ที่มีฮิสโตพลาสมาชุกชุม (เช่น ลุ่มแม่น้ำโอไฮโอ สหรัฐอเมริกา) ซึ่งเป็นจุดช่วยในการวินิจฉัยแยกโรค
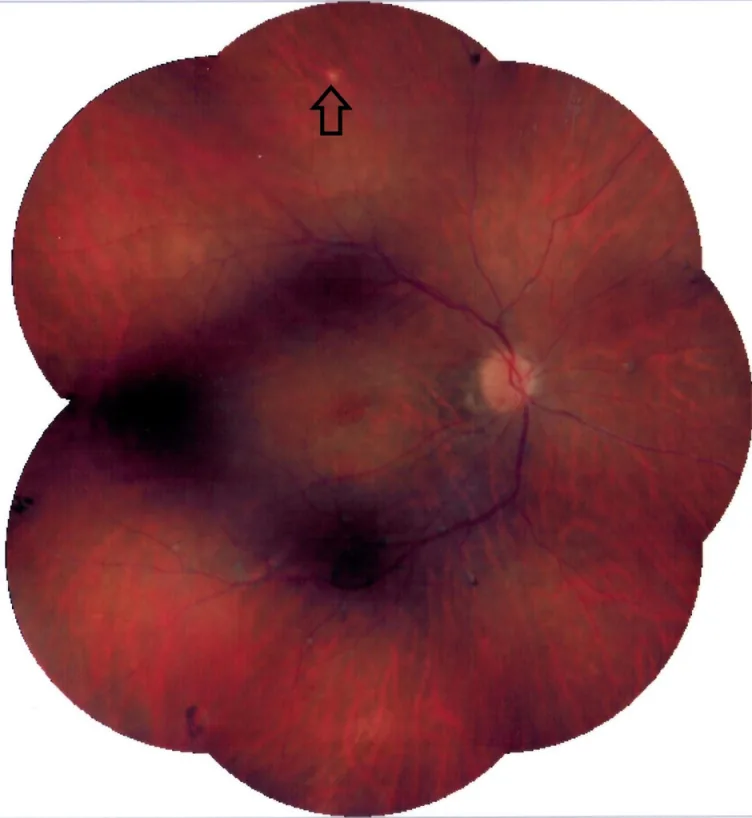
ภาพถ่ายจอประสาทตาของโรคคอรอยด์อักเสบหลายจุด (multifocal choroiditis) พบรอยแผลเป็นคอริโอเรตินอลหลายจุดรอบขั้วประสาทตาและด้านล่าง และรอยโรค active สีซีดด้านบน Soheilian M, et al. Presumed Tubercular Multifocal Choroiditis. J Ophthalmic Vis Res. 2024. Figure 1. PM
CI D: PMC11795012. License: CC BY.
ภาพถ่ายจอประสาทตา ประกอบแสดงรอยแผลเป็นคอริโอเรตินอลสีดำหลายจุดรอบขั้วประสาทตาและใกล้ส่วนโค้งหลอดเลือดด้านล่าง ที่บริเวณส่วนปลายกลางด้านบนยังพบรอยโรคสีเหลืองขาวซีด ซึ่งแสดงถึงการมีรอยโรค active และรอยโรคแผลเป็นร่วมกันในโรคคอรอยด์ อักเสบหลายจุด
จุดลอยในตา (floaters) : เนื่องจากวุ้นตา อักเสบ เป็นหนึ่งในอาการเริ่มแรกที่พบบ่อยที่สุดสายตาพร่า มัว / มองไม่ชัด : เนื่องจากจอประสาทตา บวมน้ำ (macular edema), หลอดเลือดคอรอยด์ งอกใหม่ (CNV ), หรือรอยโรคลุกลามถึงรอยบุ๋มจอตา (fovea)เห็นแสงวาบ (photopsia) : เนื่องจากการกระตุ้นของรอยโรคอักเสบ activeภาพบิดเบี้ยว (metamorphopsia)จอประสาทตา จุดบอด (scotoma) : การสูญเสียลานสายตาที่สอดคล้องกับรอยโรคอักเสบกลัวแสง / รู้สึกไม่สบายตา : เปลี่ยนแปลงตามระดับการอักเสบของช่องหน้าม่านตา
การมีภาวะอักเสบของช่องหน้าม่านตา (เล็กน้อย) และวุ้นตา อักเสบเป็นจุดสำคัญในการแยกโรคจาก PIC 5) ในผู้ป่วยสายตาสั้น การประเมินวุ้นตา อักเสบอาจทำได้ยาก และผล OCT -A และ ICG มีประโยชน์ในการวินิจฉัยเสริม7)
รอยโรคแบ่งเป็น 4 ชนิด: รอยโรคอักเสบ active, รอยโรคอักเสบ inactive, หลอดเลือดคอรอยด์ งอกใหม่ทุติยภูมิชนิด active, และหลอดเลือดคอรอยด์ งอกใหม่ทุติยภูมิชนิด inactive
รอยโรค active
สี : รอยโรคสีเหลืองถึงเทา ขอบเขตไม่ชัดเจน ร่วมกับจอประสาทตา บวมน้ำ
ขนาด : อยู่ในช่วง 45–350 ไมโครเมตร กระจายหรือรวมกลุ่มกันที่ขั้วหลังและส่วนรอบนอก
สิ่งที่พบร่วม : น้ำใต้จอประสาทตา , หัวประสาทตาบวมและคั่งเลือด, จุดรับภาพบวมน้ำแบบถุงน้ำ (14–41%), อาจเกิดเส้นเลือดใหม่ในคอรอยด์
รอยโรคที่ไม่ทำงาน
สี : เทา ขอบเขตชัดเจน พบพังผืดแผลเป็นและการสะสมของเม็ดสี
ลักษณะ : ปรากฏเป็นรอยโรคของเยื่อบุผิวเม็ดสีจอประสาทตา ฝ่อ เปลี่ยนสีแบบทะลุ (punched-out)
พยากรณ์โรค : การฟื้นฟูการมองเห็น อาจทำได้ยากเมื่อรอยโรคกลายเป็นแผลเป็น
ภาวะแทรกซ้อนอื่นๆ :
ต้อหิน ฝ่อของประสาทตา
ฝ่อของจุดรับภาพ
แผลเป็นใต้จอประสาทตา ที่ลุกลาม
จอประสาทตา บวมน้ำแบบถุงน้ำ (จอประสาทตา บวมน้ำแบบถุงน้ำ)
ในกลุ่มประชากรระยะยาว CNV เป็นสาเหตุหลักของการมองเห็น ลดลง และจอประสาทตา บวมน้ำแบบถุงน้ำรวมถึงเยื่อเหนือจอประสาทตา ก็สัมพันธ์กับการมองเห็น ลดลง 9) ในการประเมินความเสี่ยงของการมองเห็น ลดลง ควรให้ความสนใจกับ CNV , แผลเป็นฝ่อที่เกี่ยวข้องกับรอยบุ๋มจอประสาทตา , และการสะสมของรอยโรคที่จุดรับภาพ
ไม่ทราบสาเหตุของ MCP มีสมมติฐานว่าการติดเชื้อก่อนหน้านี้กระตุ้นการตอบสนองทางภูมิคุ้มกัน แต่ยังไม่มีการระบุเชื้อก่อโรคที่จำเพาะ
ลักษณะทางระบาดวิทยา:
พบบ่อยในหญิงผิวขาว
อายุเฉลี่ยเมื่อเริ่มป่วย 30 ปี (ช่วง: 6–69 ปี)
ผู้ป่วยส่วนใหญ่มีสายตาสั้น
เกิดในบุคคลที่มีสุขภาพดีโดยไม่มีโรคทางระบบหรือโรคตาที่ทราบ
ความโน้มเอียงทางพันธุกรรม:
MCP เกี่ยวข้องกับ haplotypes ของ IL-10 และ tumor necrosis factor (TNF ) มีการเสนอทฤษฎีความโน้มเอียงทางพันธุกรรมร่วมกับปัจจัยสิ่งแวดล้อมในฐานะโรคหนึ่งในกลุ่ม AZOOR complex
สมมติฐานการเกิดโรค:
รอยโรคอักเสบเริ่มต้นที่ระดับ retinal pigment epithelium และ choroidal capillaries แอนติเจนจากภายนอกอาจทำให้เกิดการกระตุ้นแอนติเจนที่ retinal photoreceptors และ retinal pigment epithelium ซึ่งอาจทำลายความสมบูรณ์ของ Bruch’s membrane ทำให้เกิดช่องว่างสำหรับการเกิด choroidal neovascular membrane ซึ่งอาจเกิดขึ้นได้ถึง 60% ของผู้ป่วย
ในปัจจุบันเนื่องจากยังไม่ทราบสาเหตุที่แน่ชัด จึงไม่มีวิธีการป้องกันที่แนะนำ หากมีอาการ (จุดลอยเพิ่มขึ้นอย่างรวดเร็ว การมองเห็น ลดลง มองเห็นภาพบิดเบี้ยว ) ควรรีบไปพบจักษุแพทย์ การตรวจตาเป็นประจำช่วยในการตรวจพบภาวะแทรกซ้อนได้ตั้งแต่เนิ่นๆ
MCP เป็นการวินิจฉัยทางคลินิกและการวินิจฉัยแยกโรค จำเป็นต้องแยกโรคติดเชื้อ โรคร้าย และโรคทางระบบออก แม้ในแนวทางการรักษา uveitis ก็ระบุว่า “ไม่มีเกณฑ์การวินิจฉัยที่แน่นอน อาศัยลักษณะเฉพาะและการวินิจฉัยแยกโรค”5)
ข้อกำหนดในการวินิจฉัย MCP :
จุดขาวเล็กหลายจุดทั้งสองข้าง ส่วนใหญ่อยู่ที่ขั้วหลัง
มีการอักเสบของส่วนหน้าหรือ vitreous inflammation (จำเป็นเพื่อแยกจาก PIC )
การแยกโรคติดเชื้อและโรคทางระบบ (ซิฟิลิส วัณโรค ซาร์คอยโดซิส ฯลฯ)
การแยกโรคร้าย (มะเร็งต่อมน้ำเหลือง การแพร่กระจาย)
การตรวจ ลักษณะรอยโรคที่ยังทำงาน ลักษณะรอยโรคที่ไม่ทำงาน การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) การเรืองแสงมากเกินไประยะแรก → การย้อมสีระยะปลาย การเรืองแสงมากเกินไปจากช่องว่างหน้าต่าง การถ่ายภาพหลอดเลือดด้วยอินโดไซยานีนกรีน (ICG) การเรืองแสงน้อยระยะแรกถึงระยะกลาง 1) จุดเรืองแสงน้อยในทุกเฟส การเรืองแสงอัตโนมัติของจอตา รอยโรคเรืองแสงอัตโนมัติสูง (รอบหัวประสาทตาและขั้วหลัง) รอยโรคฝ่อที่มีการเรืองแสงอัตโนมัติต่ำ
ผลการตรวจ Optical Coherence Tomography (OCT ):
รอยโรคที่ยังทำงานอยู่: การยกตัวของ RPE เนื่องจากการสะสมของสารใต้ช่องว่างใต้ RPE 1)
EDI-OCT : คอรอยด์หนา ตัวใต้รอยโรคที่ยังทำงานอยู่
การมีของเหลวใต้จอประสาทตา และใต้ RPE บ่งชี้ถึงการสร้างเส้นเลือดใหม่ในคอรอยด์
OCT Angiography (OCT -A): บริเวณที่มีการไหลเวียนเลือดลดลงในระดับเส้นเลือดฝอยคอรอยด์ (สอดคล้องกับรอยโรคอักเสบที่ยังทำงานอยู่)1)
เพื่อแยกรอยโรคอักเสบเฉียบพลันและการสร้างเส้นเลือดใหม่ในคอรอยด์ จำเป็นต้องใช้การถ่ายภาพหลายรูปแบบร่วมกัน รวมถึง SD-OCT และ OCT -A นอกเหนือจากการตรวจหลอดเลือดด้วยฟลูออเรสซีน 2, 7)
การแยกความแตกต่างทางภาพระหว่าง MCP และ PIC :
ในการแยก MCP /IMFC และ PIC สิ่งสำคัญคือการจัดระเบียบลักษณะเฉพาะของ CNV สายตาสั้น และ PIC ใน MCP ขนาดรอยโรคจะใหญ่กว่า (45-350 ไมครอน) และมักแสดงการเรืองแสงต่ำเป็นบริเวณกว้างในการตรวจ ICG ใน PIC รอยโรคจะเล็กกว่า (125-250 ไมครอน) และจำกัดอยู่ที่ขั้วหลัง โดยไม่มีภาวะวุ้นตา อักเสบ7)
ติดเชื้อ: POHS , ซิฟิลิส, วัณโรค, ทอกโซพลาสโมซิส, ไวรัสเวสต์ไนล์, จอประสาทตา อักเสบจาก Pneumocystis
ไม่ติดเชื้อ: ซาร์คอยโดซิส , PIC (โรคคอรอยด์ ชั้นในแบบจุด), โรคจอประสาทตา คอรอยด์ อักเสบแบบ birdshot, โรคเยื่อบุเม็ดสีจอประสาทตา อักเสบแบบแผ่นหลายจุดหลังเฉียบพลัน
ร้ายแรง: มะเร็งต่อมน้ำเหลือง, การแพร่กระจาย
การตรวจทางคลินิกพื้นฐาน: การนับเม็ดเลือดสมบูรณ์, ชุดการเผาผลาญที่ครอบคลุม, เอนไซม์แปลงแองจิโอเทนซิน, เอกซเรย์ทรวงอก, การตรวจซิฟิลิส, การตรวจ QuantiFERON TB Gold
ในพื้นที่ที่มีวัณโรคระบาด (เช่น อินเดีย) มากถึง 40% ของกรณีจอประสาทตา อักเสบหลายจุดอาจเกี่ยวข้องกับวัณโรคตา3) และสามารถสังเกตได้เป็นรอยโรคอักเสบใต้ RPE ในการตรวจ OCT 3)
Q
จะแยกจอประสาทตาอักเสบหลายจุดจากวัณโรคได้อย่างไร?
A
การถ่ายภาพหลายรูปแบบมีประโยชน์ในการวินิจฉัยแยกโรค ในจอประสาทตา อักเสบหลายจุดจากวัณโรค OCT อาจแสดงการฉีกขาดของเยื่อจำกัดชั้นนอกและการสูญเสียโซนรูปไข่เฉพาะที่ในรอยโรคอักเสบใต้ RPE 3) การประเมินทำโดยการรวมการตรวจ QuantiFERON TB Gold และการถ่ายภาพ ในพื้นที่ที่มีวัณโรคระบาดหรือมีประวัติ/การสัมผัสวัณโรค ควรทำการตรวจคัดกรองอย่างจริงจัง
เลือกการรักษาตามระดับการอักเสบ รอยโรคที่ยังทำงาน ภาวะแทรกซ้อน และการมองเห็น ลดลง จอประสาทตา บวมน้ำชนิดซีสตอยด์ ภาวะวุ้นตา อักเสบรุนแรง หรือการเกิดเยื่อใหม่ในคอรอยด์ เป็นข้อบ่งชี้ในการรักษา
สเตียรอยด์ ชนิดรับประทานวุ้นตา อักเสบหรือการอักเสบของช่องหน้าตา ให้สเตียรอยด์ ทั่วร่างกายด้วยเพรดนิโซโลน 0.5–1 มก./กก./วัน แล้วค่อยๆ ลดขนาดลงเมื่อการอักเสบทุเลา5) .
สเตียรอยด์ เฉพาะที่
ไตรแอมซิโนโลน อะซีโทไนด์ (Kenacort-A)การปลูกฝังเดกซาเมทาโซนในแก้วตา 0.7 มก. (Ozurdex ®) : ข้อบ่งใช้สำหรับม่านตาอักเสบ ชนิดไม่ติดเชื้อในส่วนหลัง ระยะเวลาออกฤทธิ์ 3–4 เดือน ต้องวัดความดันลูกตา ภายใน 30 นาทีหลังฉีด และตรวจด้วยกล้องจุลทรรศน์ร่องกราดหลังจาก 2–7 วันการปลูกฝังฟลูโอซิโนโลน อะซีโทไนด์ ชนิดไมโคร (Iluvien ®) : ปล่อยสเตียรอยด์ ขนาดต่ำอย่างต่อเนื่องนานถึง 3 ปี
สเตียรอยด์
ผู้ป่วยประมาณ 35% ที่ใช้สเตียรอยด์ ในลูกตามีความดันลูกตา สูงขึ้น จำเป็นต้องติดตามความดันลูกตา สูง ต้อกระจก และเยื่อบุตาอักเสบ เป็นประจำ ภาวะแทรกซ้อนอื่นๆ ได้แก่ หนังตาตก และต้อกระจก
ในกรณีที่ดื้อต่อการรักษา กลับเป็นซ้ำ หรือพึ่งพาสเตียรอยด์ ให้พิจารณายาปรับภูมิคุ้มกัน ใช้ไซโคลสปอรีน อะซาไธโอพรีน หรือไมโคฟีโนเลต โมเฟทิล (MMF) สำหรับการรักษาประคับประคอง และในกรณีดื้อต่อการรักษาให้พิจารณายาต้าน TNF α (อะดาลิมูแมบ )5) .
ในการสำรวจของกลุ่มวิจัยนานาชาติ (n=221 จักษุแพทย์ผู้เชี่ยวชาญม่านตาอักเสบ ) ทางเลือกแรกของยาปรับภูมิคุ้มกันแบบดั้งเดิมสำหรับโรคกลุ่มคอรอยด์ อักเสบหลายจุด-PIC คือ methotrexate (39.4%) และทางเลือกแรกของยาชีววัตถุ คือ adalimumab (95.5%)4) .
จากมุมมองการพยากรณ์การมองเห็น ระยะยาว การควบคุมการอักเสบและการจัดการ CNV มีความสำคัญ ในกลุ่มศึกษา MFCPU ของ Johns Hopkins ภาวะแทรกซ้อนของขั้วหลัง เช่น CNV จอประสาทตา บวมน้ำชนิดซีสตอยด์ และเยื่อเหนือจอประสาทตา สัมพันธ์กับการมองเห็น ลดลง9) การศึกษาเปรียบเทียบของ Kedhar และคณะยังแสดงให้เห็นว่า MFCPU มีภาวะแทรกซ้อนจากการอักเสบ เช่น ต้อกระจก จอประสาทตา บวมน้ำชนิดซีสตอยด์ และเยื่อเหนือจอประสาทตา มากกว่า PIC 8) .
ใช้การรักษาด้วย anti-VEGF ชนิดฉีดเข้าน้ำวุ้นตา สำหรับจอประสาทตา ใหม่ที่คอรอยด์ ที่ยังทำงานอยู่และจอประสาทตา บวมน้ำ การใช้ anti-VEGF เพียงอย่างเดียวมักไม่เพียงพอในการควบคุม CNV ที่มีพื้นหลังอักเสบ จึงแนะนำให้ใช้ร่วมกับการรักษาด้วยสเตียรอยด์ และการปรับภูมิคุ้มกัน
รอยโรคอักเสบสันนิษฐานว่าเริ่มต้นจากระดับเยื่อบุผิวรงควัตถุจอประสาทตา และเส้นเลือดฝอยคอรอยด์ ซึ่งเกิดการกระตุ้นแอนติเจนที่เยื่อบุผิวรงควัตถุจอประสาทตา จากแอนติเจนภายนอก
ทั้ง MCP และ PIC เกี่ยวข้องกับจอประสาทตา ชั้นนอก เส้นเลือดฝอยคอรอยด์ และคอรอยด์ และอาจเป็นสเปกตรัมของโรคเดียวกัน1) MCP เป็นโรคอักเสบเรื้อรัง เป็นสองข้าง กำเริบซ้ำ โดยมีรอยโรคส่วนหลังร่วมกับม่านตาอักเสบ ส่วนหน้าและวุ้นตา อักเสบ ในขณะที่ PIC แตกต่างตรงที่ไม่มีวุ้นตา อักเสบหรือการอักเสบของส่วนหน้า1) ในการนิยามใหม่โดยใช้ภาพถ่ายหลายรูปแบบโดย Spaide และคณะ มอง MCP และ PIC อย่างเป็นเอกภาพว่าเป็น “โรคอักเสบปฐมภูมิของแผ่นเส้นเลือดฝอยคอรอยด์ ” โดยมีหรือไม่มีวุ้นตา อักเสบเป็นจุดแยกหลัก6)
ในการตรวจ OCT angiography (OCT -A) พบว่าบริเวณที่มีการไหลเวียนเลือดลดลงอย่างชัดเจนในระดับเส้นเลือดฝอยคอรอยด์ สอดคล้องกับรอยโรคอักเสบที่ยังทำงานอยู่1) สนับสนุนว่าการเปลี่ยนแปลงของจอประสาทตา ชั้นนอกอาจเป็นการเปลี่ยนแปลงทุติยภูมิจากการเกี่ยวข้องของคอรอยด์ ปฐมภูมิ OCT -A มีประโยชน์มากขึ้นทั้งในการติดตามการอักเสบที่ยังทำงานอยู่และการตรวจหา CNV
การอักเสบทำให้ความสมบูรณ์ของเยื่อบรูชเสียหาย ซึ่งเป็นพื้นฐานสำหรับการเกิดเยื่อจอประสาทตา ใหม่ที่คอรอยด์ ใน MCP จอประสาทตา ใหม่ที่คอรอยด์ อาจเกิดขึ้นได้ถึง 60% ของผู้ป่วย CNV ชนิดอักเสบตอบสนองต่อการรักษาด้วย anti-VEGF แต่การควบคุมการอักเสบพื้นฐานเป็นสิ่งจำเป็น
ปัจจัยทางพันธุกรรมแสดงความสัมพันธ์กับ haplotypes ของ IL-10 และ tumor necrosis factor แต่กลไกที่แน่ชัดยังไม่ทราบ
OCT angiography แสดงการไหลเวียนเลือดที่ลดลงอย่างชัดเจนในเส้นเลือดฝอยคอรอยด์ ของรอยโรค MCP ซึ่งสอดคล้องกับรอยโรคอักเสบที่ยังทำงานอยู่1) นอกจากนี้ยังใช้ในการติดตามการเปลี่ยนแปลงของหลอดเลือดคอรอยด์ หลังการรักษา และสามารถประเมินกิจกรรมของโรคได้โดยไม่ต้องส่องกล้องหลอดเลือดด้วยฟลูออเรสซีน
OCT angiography แสดงให้เห็นความสามารถในการ描绘บริเวณที่การไหลเวียนเลือดในเส้นเลือดฝอยคอรอยด์ ลดลง และเชื่อมโยงกับการยกตัวของเยื่อบุผิวรงควัตถุจอประสาทตา ใน OCT และจุดเรืองแสงน้อยในการตรวจหลอดเลือดด้วยอินโดไซยานีนกรีน ซึ่งช่วยให้เข้าใจพยาธิสรีรวิทยาได้ลึกซึ้งยิ่งขึ้น1)
Spaide และคณะได้ให้นิยามใหม่ของ MFCwP และ PIC โดยใช้การวินิจฉัยภาพแบบหลายรูปแบบ ซึ่งชี้ให้เห็นว่าอาจอยู่ในสเปกตรัมเดียวกัน 6) การจำแนกชนิดย่อยของโรคที่แม่นยำยิ่งขึ้นและการพัฒนาการรักษาเฉพาะบุคคลกำลังดำเนินไป เกณฑ์การวินิจฉัยภาพแบบหลายรูปแบบเพื่อแยกความแตกต่างระหว่าง CNV จากสายตาสั้น และ CNV ใน MCP /PIC ก็ได้รับการเสนอเช่นกัน 7) ซึ่งคาดว่าจะนำไปสู่การใช้การรักษาด้วย anti-VEGF อย่างเหมาะสม
Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
Vance SK, Khan S, Klancnik JM, Freund KB. Characteristic spectral-domain optical coherence tomography findings of multifocal choroiditis. Retina. 2011;31(4):717-723. PMID: 21386760. doi:10.1097/IAE.0b013e318203c1ef.
Kaza H, Gala JM, Rani PK. Subfoveal retinal pigment epithelium inflammatory lesion presenting as a sign of reactivation of tubercular multifocal choroiditis. BMJ Case Rep. 2021;14:e240280.
Branford JA, et al. Practice patterns of systemic immunomodulatory drug treatment for non-infectious uveitis: an international study. Br J Ophthalmol. 2025;109:482-489.
日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(PIC ・地図状脈絡膜炎節参照). 日本眼科学会雑誌. 2019;123(6):635-696.
Spaide RF, Goldberg N, Freund KB. Redefining multifocal choroiditis and panuveitis and punctate inner choroidopathy through multimodal imaging. Retina. 2013;33(7):1315-1324.
Dolz-Marco R, Fine HF, Freund KB. How to differentiate myopic choroidal neovascularization, idiopathic multifocal choroiditis, and punctate inner choroidopathy using clinical and multimodal imaging findings. Ophthalmic Surg Lasers Imaging Retina. 2017;48(3):196-201.
Kedhar SR, Thorne JE, Wittenberg S, Dunn JP, Jabs DA. Multifocal choroiditis with panuveitis and punctate inner choroidopathy: comparison of clinical characteristics at presentation. Retina. 2007;27(9):1174-1179. doi:10.1097/IAE.0b013e318068de72.
Thorne JE, Wittenberg S, Jabs DA, Peters GB, Reed TL, Kedhar SR, Dunn JP. Multifocal choroiditis with panuveitis: incidence of ocular complications and of loss of visual acuity. Ophthalmology. 2006;113(12):2310-2316. doi:10.1016/j.ophtha.2006.05.067.