โรคจุดขาวในคอรอยด์ ชั้นใน (PIC ) เป็นโรคอักเสบของคอรอยด์ ที่ไม่ทราบสาเหตุ พบมากในหญิงสาวที่มีสายตาสั้น
รอยโรคสีขาวอมเหลืองขนาดเล็ก 100-300 ไมครอน เกิดขึ้นหลายจุดที่ขั้วหลังตา โดยไม่มีวุ้นตา อักเสบหรืออักเสบในช่องหน้าตา
ภาวะหลอดเลือดใหม่ในคอรอยด์ (CNV ) เกิดร่วมด้วยในอัตราสูง 40-76% ซึ่งเป็นสาเหตุหลักของการมองเห็น ลดลง
การตรวจ OCT angiography (OCTA ) มีประโยชน์ในการระบุ CNV ที่ตรวจพบได้ยากด้วยการตรวจหลอดเลือดแบบเดิมการพยากรณ์โรคทางสายตาดีในกรณีที่ไม่มี CNV ส่วนใหญ่ดีขึ้นเพียงแค่ติดตามอาการ
ในกรณีที่มี CNV การฉีดยา anti-VEGF เข้าในวุ้นตา ร่วมกับสเตียรอยด์ ได้ผลดี
โรคจุดขาวในคอรอยด์ ชั้นใน (punctate inner choroidopathy) เป็นโรคอักเสบของคอรอยด์ ที่ไม่ทราบสาเหตุ รายงานครั้งแรกโดย Watzke และคณะในปี 1984 จัดเป็นหนึ่งในกลุ่มอาการจุดขาว (white dot syndromes) ซึ่งเป็นกลุ่มโรคอักเสบที่ส่งผลต่อจอประสาทตา ชั้นนอก, ชั้นเส้นเลือดฝอยคอรอยด์ และคอรอยด์ 7) ในแนวทางการรักษาม่านตาอักเสบ (วารสารจักษุวิทยาญี่ปุ่น 2019;123(6):635-696) จัดเป็นม่านตาอักเสบ ส่วนหลังที่ไม่ติดเชื้อซึ่งมีรอยโรคที่จอตา มีลักษณะเริ่มต้นช้าและเป็นข้างเดียวหรือสองข้าง 8) .
เกิดในหญิงสาวที่มีสายตาสั้น เป็นหลัก (ประมาณ 90% เป็นเพศหญิง) 5) การศึกษาขนาดใหญ่รายงานอายุเริ่มต้นเฉลี่ย 36 ปี และระดับสายตาสั้น เฉลี่ย -4.5 ไดออปเตอร์ 5) พบมากในหญิงสาวที่มีสายตาสั้น ปานกลาง ในระยะเฉียบพลันจะมีรอยโรคสีขาวอมเหลืองขนาดเล็กหลายจุดที่ขั้วหลังตา ซึ่งเมื่อเวลาผ่านไปจะกลายเป็นรอยโรคฝ่อ
โรคจุดขาวในคอรอยด์ ชั้นในและคอรอยด์ อักเสบหลายจุด (MFC) ถูกเสนอว่าอาจเป็นสเปกตรัมของโรคเดียวกัน เนื่องจากทั้งสองส่งผลต่อคอรอยด์ , เยื่อบุผิวรับสี (RPE ) และจอประสาทตา ชั้นนอก 7) การแยกโรคทั้งสองขึ้นอยู่กับการมีหรือไม่มีวุ้นตา อักเสบและการกระจายของรอยโรค PIC ไม่มีวุ้นตา อักเสบและรอยโรคจำกัดอยู่ที่ขั้วหลังตา ในขณะที่ MFC มีวุ้นตา อักเสบและรอยโรคกระจายไปถึงบริเวณรอบนอก 6) .
Q
โรคจุดขาวในคอรอยด์ชั้นในและคอรอยด์อักเสบหลายจุด (MFC) แตกต่างกันอย่างไร?
A
PIC ไม่มีวุ้นตา อักเสบและรอยโรคจำกัดที่ขั้วหลังตา ในขณะที่ MFC มีวุ้นตา อักเสบหรืออักเสบในช่องหน้าตา และรอยโรคกระจายถึงบริเวณรอบนอกกลาง โรคทั้งสองอาจเป็นสเปกตรัมเดียวกัน
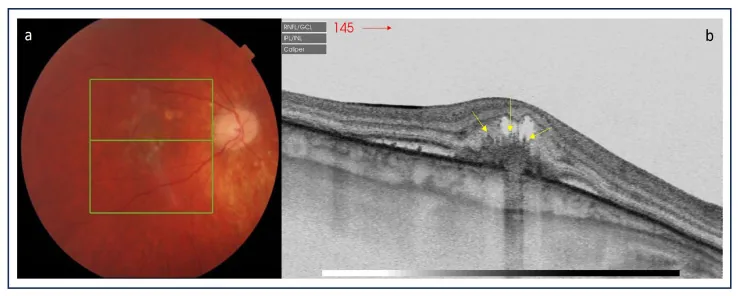
ภาพถ่ายจอตาและ OCT ของโรคจุดขาวในคอรอยด์ชั้นใน แสดงรอยโรคเล็กที่ขั้วหลังตา รอยโรคสะท้อนแสงสูงที่จุดภาพชัด และของเหลวใต้จอประสาทตา Karska-Basta I, et al. Diagnostic Challenges in Inflammatory Choroidal Neovascularization. Medicina (Kaunas). 2024. Figure 5. PM
CI D: PMC10972505. License: CC BY.
ในภาพถ่าย
จอประสาทตา ข้างซ้าย พบรอยโรคเล็กสีขาวเหลืองที่ขั้วหลัง ใน
OCT ข้างขวา พบรอยโรคสะท้อนแสงสูงที่จุดรับภาพร่วมกับ
ของเหลวใต้จอประสาทตา และใน
จอประสาทตา ซึ่งเป็นภาพของรอยโรคที่ยัง active ของ
PIC อาการเริ่มแรกที่พบบ่อยที่สุดของโรคจุดอักเสบในชั้นคอรอยด์ ชั้นในคือ จุดบอดในตาข้างเดียวและการมองเห็น ลดลง
การมองเห็น ลดลงการมองเห็น ครั้งแรกอยู่ระหว่าง 0.4 ถึง 0.05 ตามรายงาน ประมาณ 67% ยังคงการมองเห็นที่แก้ไขแล้ว ที่ 0.4 หรือดีกว่า ในระยะสงบ จะเหลือรอยแผลเป็นกลมขอบเขตชัดเจนพร้อมเม็ดสี 8) จุดบอด : รู้สึกมีจุดบอดตรงกลางหรือใกล้จุดกลางแสงวาบ แสงวาบ ภาพบิดเบี้ยว จุดลอย : พบในผู้ป่วยบางราย
ในการตรวจจอประสาทตา พบจุดเล็กสีขาวเหลืองขนาด 100–300 ไมครอน จำกัดอยู่ที่ขั้วหลัง กระจายแบบสุ่มจำนวน 12–25 จุด รอยโรคเกิดที่ระดับจอประสาทตา ชั้นนอก เซลล์เยื่อบุผิวจอประสาทตา และคอรอยด์ ชั้นใน 80% เป็นสองตาแต่มักไม่สมมาตร 1)
ลักษณะของรอยโรคในโรคจุดอักเสบในชั้นคอรอยด์ ชั้นในสรุปได้ดังนี้
รอยโรคที่ยัง active
รอยโรคคอรอยด์ และจอประสาทตา สีขาวเหลือง : จุดเล็กสีเทาเหลืองขอบเขตชัดเจนที่ขั้วหลัง บริเวณรอบหัวประสาทตาไม่ได้รับผลกระทบ
ไม่มีการอักเสบภายในลูกตา : ไม่มีอาการอักเสบในช่องหน้าหรือวุ้นตา ซึ่งเป็นลักษณะเฉพาะของโรคจุดอักเสบในชั้นคอรอยด์ ชั้นใน 3)
จอประสาทตา ชั้นรับความรู้สึกหลุดลอกจอประสาทตาลอก แบบมีน้ำใต้รอยโรคที่ active
รอยโรคระยะแผลเป็น
แผลเป็นคอริโอเรตินอลฝ่อ : ทิ้งรอยแผลเป็น “ทะลุ” ขอบเขตชัดเจนหลังการอักเสบสงบ อาจมีเม็ดสีหรือรัศมีสีจางร่วมด้วย
การขยายตัวของแผลเป็นตามเวลา : แม้การอักเสบจะสงบแล้ว แผลเป็นอาจค่อยๆ ขยายตัว ทำให้การมองเห็น ลดลงหากอยู่ใกล้รอยบุ๋มจอตา
เส้นเลือดใหม่คอรอยด์ (CNV ) : เกิดขึ้นใน 40-76% ของผู้ป่วย5) และเป็นสาเหตุหลักของการมองเห็น ลดลง
วิวัฒนาการ 5 ระยะของรอยโรคคอรอยโดพาทีพันคทาอินเทอร์นาได้รับการจำแนกใน SD-OCT 2)
การแทรกซึมของคอรอยด์
การเกิดก้อนใต้ชั้นอาร์พีอี
ก้อนคอริโอเรตินอล
การถดถอย
ไส้เลื่อนจอตา
สาเหตุของคอรอยโดพาทีพันคทาอินเทอร์นายังไม่ทราบแน่ชัด แต่เชื่อว่าเป็นโรคภูมิต้านตนเองที่มีพื้นฐานความไวต่อพันธุกรรมหลายยีน กระตุ้นโดยสิ่งเร้าจากสิ่งแวดล้อม เช่น การติดเชื้อ การฉีดวัคซีน หรือความเครียด
ความสัมพันธ์กับ HLA-DR2 : มีรายงานความสัมพันธ์ระหว่างคอรอยโดพาทีพันคทาอินเทอร์นากับ HLA-DR2แฮพลโลไทป์ IL-10 : คอรอยโดพาทีพันคทาอินเทอร์นาและ MFC แสดงความสัมพันธ์ทางพันธุกรรมที่คล้ายกันที่ตำแหน่ง IL10 และ TNF อัลลีล HLA-DRB1*15 : มีรายงานการพบอัลลีลนี้ในผู้ป่วยโรคคอรอยด์ อักเสบชนิดจุดด้านใน 6) กรณีในครอบครัว : มีรายงานกรณีในครอบครัว เช่น กลุ่มแม่-ลูกสาว
ปัจจัย รายละเอียด เพศ เพศหญิงประมาณ 90–93% อายุ 18–40 ปี (เฉลี่ย 36 ปี) สายตาสั้น −3.25 ถึง −10.0 D
มีการรายงานการเกิดและการกลับมาทำงานของโรคคอรอยด์ อักเสบชนิดจุดด้านในหลังการติดเชื้อ COVID-19 การติดเชื้อ SARS-CoV-2 อาจกระตุ้นให้เกิดความผิดปกติของการควบคุมภูมิคุ้มกันตนเองในบุคคลที่มีความบกพร่องทางพันธุกรรม นอกจากนี้ ยังมีรายงานการกลับเป็นซ้ำของโรคคอรอยด์ อักเสบชนิดจุดด้านในหลังการฉีดวัคซีน COVID-19 3)
Scott และคณะ (2024) รายงานกรณีหญิงอายุ 38 ปีที่มีการกลับเป็นซ้ำของโรคคอรอยด์ อักเสบชนิดจุดด้านใน 7 วันหลังฉีดวัคซีน Pfizer-BioNTech COVID-19 ร่วมกับเยื่อหุ้มเส้นเลือดใหม่คอรอยด์ ชนิดอักเสบ (iCNV M) การกลับเป็นซ้ำไม่เกิดขึ้นเมื่อฉีดวัคซีนภายใต้ภาวะกดภูมิคุ้มกัน แต่เกิดขึ้นหลังจากเข็มที่สี่โดยไม่มีภาวะกดภูมิคุ้มกัน 3)
Q
วัคซีนโควิด-19 อาจทำให้โรคคอรอยด์อักเสบชนิดจุดชั้นในแย่ลงได้หรือไม่?
A
มีรายงานการกลับเป็นซ้ำของโรคคอรอยด์ อักเสบชนิดจุดชั้นในหลังการฉีดวัคซีนโควิด-193) อย่างไรก็ตาม ประโยชน์ของวัคซีนมีมากกว่าความเสี่ยงของการกลับเป็นซ้ำของการอักเสบในตา ผู้ป่วยที่มีประวัติโรคนี้ควรปรึกษาจักษุแพทย์เกี่ยวกับการติดตามก่อนและหลังการฉีดวัคซีน
การวินิจฉัยโรคคอรอยด์ อักเสบชนิดจุดชั้นในขึ้นอยู่กับผลการตรวจทางคลินิก การวินิจฉัยที่แน่นอนทำได้โดยการตรวจภาพถ่ายเสริมร่วมกัน การทดสอบผิวหนังฮิสโตพลาสมา (histoplasma skin test) ให้ผลลบ
ในการตรวจ FA รอยโรคที่ยังทำงานอยู่จะแสดงการเรืองแสงมากเกิน (hyperfluorescence) ในระยะหลอดเลือดแดงต้น และมีการรั่วซึมและย้อมสีในระยะปลาย7) ตรวจพบรอยโรคได้มากกว่าการตรวจทางคลินิก เยื่อหุ้มเส้นเลือดใหม่คอรอยด์ (CNV M) จะปรากฏเป็นเครือข่ายเส้นเลือดใหม่ที่ไม่สม่ำเสมอคล้ายลูกไม้
ในการตรวจ ICG จะพบรอยโรคที่มีการเรืองแสงน้อย (hypofluorescence) ในระยะกลางที่ขั้วหลังและรอบขั้วประสาทตา7) ตรวจพบจุดเรืองแสงน้อยที่อยู่ใต้ระดับคลินิกใน 32% ของดวงตาที่ได้รับผลกระทบ ซึ่งช่วยเพิ่มความสามารถในการวินิจฉัย
SD-OCT มีประโยชน์ในการวินิจฉัยและติดตามโรคคอรอยด์ อักเสบชนิดจุดชั้นใน ในรอยโรคที่ยังทำงานอยู่ จะพบการยกตัวเฉพาะที่สะท้อนแสงสูงของชั้นเยื่อบุผิวเม็ดสีจอประสาทตา (RPE ) และการขาดตอนของโซน ellipsoid (EZ )7) รอยโรคที่ให้ผลบวกต่อเส้นเลือดใหม่คอรอยด์ จะมีขนาดความสูง ความกว้าง และปริมาตรที่ใหญ่กว่าเมื่อเทียบกับรอยโรคที่ให้ผลลบ ร่วมกับการขาดตอนของ EZ และเยื่อบรูค (Bruch’s membrane) และความไม่ชัดเจนของจอประสาทตา ชั้นนอก
ในการตรวจ OCT แบบภาพลึก (EDI-OCT ) ความหนาของคอรอยด์ ใต้รอยโรคที่ยังทำงานอยู่จะเพิ่มขึ้นและลดลงหลังการรักษา (สัญญาณฟองน้ำ) ซึ่งช่วยในการแยกความแตกต่างจากเส้นเลือดใหม่คอรอยด์ จากสายตาสั้น
OCTA เป็นวิธีการถ่ายภาพที่สำคัญในการวินิจฉัยโรคคอรอยด์ พาธีชนิดจุดภายใน (punctate inner choroidopathy) สามารถระบุหลอดเลือดใหม่ในคอรอยด์ ทุติยภูมิที่ตรวจพบได้ยากด้วย FA หรือ SD-OCT ทั่วไปได้ในอัตราสูง
ในการตรวจด้วย OCTA สามารถพิสูจน์การมีอยู่ของหลอดเลือดใหม่ในคอรอยด์ ในผู้ป่วยโรคคอรอยด์ พาธีชนิดจุดภายในจำนวนมาก รวมถึงกรณีที่ FA ไม่สามารถสรุปผลได้
Leclaire และคณะ (2021) รายงานกรณีที่หลอดเลือดใหม่ในคอรอยด์ ทุติยภูมิถูกระบุได้ด้วย OCT -A เท่านั้น ไม่พบในการตรวจ FAG หรือ SD-OCT ซึ่งบ่งชี้ว่าอาจมีหลอดเลือดใหม่ในคอรอยด์ ทุติยภูมิที่ไม่มีอาการทางคลินิกจำนวนมาก 5)
Stattin และคณะ (2021) รายงานการใช้ SS-OCTA เพื่อติดตามการเปลี่ยนแปลงความหนาแน่นของหลอดเลือดในหลอดเลือดใหม่ในคอรอยด์ ทุติยภูมิจากโรคคอรอยด์ พาธีชนิดจุดภายใน และใช้เป็นแนวทางในการตัดสินใจรักษาด้วยการยับยั้ง VEGF 4)
รอยโรคที่ยังทำงานอยู่ของโรคคอรอยด์ พาธีชนิดจุดภายในจะปรากฏเป็นบริเวณที่มีการเรืองแสงเองต่ำ (hypoautofluorescence) 1) รัศมีที่มีการเรืองแสงเองสูงรอบรอยโรคที่ยังทำงานอยู่อาจเป็นสัญญาณทางอ้อมของการอักเสบที่ไม่สามารถควบคุมได้ รอยโรคแผลเป็นฝ่อก็ปรากฏเป็นจุดที่มีการเรืองแสงเองต่ำเช่นกัน 1)
การเรืองแสงเองของจอตาเป็นการตรวจที่ไม่รุกรานและรวดเร็ว มีประโยชน์ในการประเมินการกระจายของรอยโรค ติดตามประสิทธิภาพการรักษา และตรวจหาการกลับเป็นซ้ำ 1)
ประมาณ 41% พบจุดบอดขยายใหญ่ขึ้น และยังพบจุดบอดกลาง และจุดบอดกึ่งกลางด้วย ผู้ป่วย 45% มีลานสายตาปกติ
โรคที่ต้องแยกออกมีดังนี้:
กลุ่มอาการจุดขาว จางหลายจุด (MEWDS )6) คอรอยด์ อักเสบหลายจุดและยูเวียอักเสบทั้งหมด (MCP )วุ้นตา เสบและรอยโรคลามไปถึงส่วนรอบนอกโรคเยื่อบุเม็ดสีส่วนหลังหลายจุดเฉียบพลัน (APMPPE ) : แสดงรอยโรคเป็นปื้นขนาดใหญ่โรคฮิสโตพลาสโมซิสทางตาที่สันนิษฐาน (POHS ) : พบการฝ่อรอบหัวประสาทตาและรอยโรคแบบเจาะทะลุที่ส่วนรอบนอกเยื่อบุโพรงจอประสาทตา ใหม่จากสายตาสั้น : สามารถแยกจากเยื่อบุโพรงจอประสาทตา ใหม่อักเสบได้ด้วย EDI-OCT คอรอยด์ อักเสบแบบเซอร์พิจิโนซากลุ่มอาการพังผืดใต้จอประสาทตา ร่วมกับยูเวียอักเสบ : มีพังผืดใต้จอประสาทตา ที่ดำเนินไปเรื่อยๆ 8) ท็อกโซพลาสโมซิสที่ตาและวัณโรคที่ตา : ต้องแยกออกว่าเป็นโรคติดเชื้อ 8) จุดฟุคส์ในสายตาสั้น มาก : แยกเป็นโรคเสื่อม 8)
Q
ความแตกต่างระหว่างคอรอยโดพาทีแบบจุดในและกลุ่มอาการจุดขาวหลายจุดที่หายไปคืออะไร?
A
กลุ่มอาการจุดขาว หลายจุดที่หายไปมักเป็นข้างเดียวและหายเองได้ภายในไม่กี่สัปดาห์ แทบไม่ทิ้งรอยแผลเป็นหรือเยื่อบุโพรงจอประสาทตา ใหม่ 6) คอรอยโดพาทีแบบจุดในมักเป็นสองข้าง ทิ้งรอยแผลเป็นฝ่อและมีอัตราการเกิดเยื่อบุโพรงจอประสาทตา ใหม่สูง การมีหรือไม่มีการไหลเวียนเลือดใน OCTA ก็ช่วยในการวินิจฉัยแยกโรค
หากไม่มีหลักฐานของเยื่อบุโพรงจอประสาทตา ใหม่ การพยากรณ์โรคทางสายตาดี และส่วนใหญ่ไม่จำเป็นต้องรักษา ข้อยกเว้นเพียงอย่างเดียวคือมีรอยโรคอักเสบที่ยังทำงานอยู่ใกล้จุดตรึงมาก ซึ่งจะพิจารณาการรักษาทางยา
สำหรับรอยโรคที่ทำงานใกล้รอยบุ๋มจอตา จะฉีดไตรแอมซิโนโลน อะซีโทไนด์ ใต้เยื่อหุ้มเทนอนส่วนหลัง หรือให้สเตียรอยด์ ทางปาก (เพรดนิโซโลน 40-60 มก./วัน แล้วค่อยๆ ลด) 8) หากเยื่อบุโพรงจอประสาทตา ใหม่นอกรอยบุ๋มจอตา ไม่ตอบสนองต่อสเตียรอยด์ อาจลองจี้ด้วยแสง
ในกรณีที่มีเยื่อบุโพรงจอประสาทตา ใหม่ จำเป็นต้องรักษาอย่างจริงจัง
เป็นการรักษาหลักสำหรับคอรอยโดพาทีแบบจุดในที่มีเยื่อบุโพรงจอประสาทตา ใหม่ ใช้ยาเบวาซิซูแมบ รานิบิซูแมบ และอะฟลิเบอร์เซปต์
Stattin และคณะ (2021) รายงานกรณีเส้นเลือดใหม่ในคอรอยด์ ทุติยภูมิจากจอประสาทตา อักเสบชนิดพั้นคเทตอินเทอร์นาที่รักษาด้วยการฉีดรานิบิซูแมบ (0.5 มก.) ตามความจำเป็นภายใต้การติดตามด้วย SS-OCTA และบรรลุการมองเห็น สุดท้าย 20/20 หลังการฉีดทั้งหมด 6 ครั้ง 4)
แนวทางสองทิศทางด้วยยา anti-VEGF และสเตียรอยด์ ถือว่ามีประสิทธิภาพ 4) ในกรณีที่มี CNV การฉีดเบวาซิซูแมบ เข้าในวุ้นตา อาจใช้เป็นทางเลือกแรก 8)
โดยทั่วไปสเตียรอยด์ ชนิดทั่วร่างกายเริ่มต้นด้วยขนาด 1 มก./กก./วัน (60–80 มก./วัน) เป็นเวลา 3–5 วัน จากนั้นค่อยๆ ลดขนาดลง 4) มีรายงานว่าการใช้สเตียรอยด์ ชนิดรับประทานช่วยลดความเสี่ยงของการเกิด iCNV M ลงครึ่งหนึ่ง 3)
การเตรียมสเตียรอยด์ ชนิดฉีดเข้าในวุ้นตา ได้แก่:
การฉีดไตรแอมซิโนโลน เข้าในวุ้นตา (4 มก.): ร่วมกับการรักษาด้วยแสงไดนามิก (PDT ) ทำให้ logMAR BCVA ดีขึ้นจาก 0.52 เป็น 0.20การฝังเดกซาเมทาโซนเข้าในวุ้นตา (0.7 มก./0.35 มก.): ปลดปล่อยอย่างต่อเนื่องนาน 6 เดือน ใช้ร่วมกับ anti-VEGFการฝังฟลูโอซิโนโลน อะซีโทไนด์ (0.59 มก.): ปลดปล่อยอย่างต่อเนื่องนาน 36 เดือน มีประโยชน์ในกรณีที่ไม่ทนต่อการรักษาทั่วร่างกายหรือในสตรีที่วางแผนตั้งครรภ์
ไมโคฟีโนเลต โมเฟทิล : ลดความถี่ของการกำเริบในจอประสาทตา อักเสบชนิดพั้นคเทตอินเทอร์นาที่เป็นซ้ำไซโรลิมัส (ราปามัยซิน) : ยับยั้งการหลั่ง IL-2 เคยใช้ในการรักษาเส้นเลือดใหม่ในคอรอยด์ ใกล้รอยบุ๋มจอตา
มีรายงานประสิทธิภาพของ PDT ในกรณีที่มีเส้นเลือดใหม่ในคอรอยด์ ร่วมกับเพรดนิโซโลนชนิดรับประทาน (1 มก./กก./วัน) ทำให้การมองเห็น ดีขึ้น 15 ตัวอักษรหลังการทำ PDT เฉลี่ย 2 ครั้ง
Q
จำเป็นต้องฉีดยา anti-VEGF กี่ครั้งสำหรับเส้นเลือดใหม่ในคอรอยด์ในโรคจุดขาวในชั้นคอรอยด์ชั้นใน?
A
แตกต่างกันไปตามแต่ละกรณี มีรายงานการฉีด 6 ครั้งโดยใช้การให้ยาแบบ pro re nata ภายใต้การนำของ SS-OCTA 4) ควรประเมินกิจกรรมของเส้นเลือดใหม่ในคอรอยด์ ด้วยการตรวจภาพเป็นระยะ และอาจต้องให้ยาเพิ่มเติมเมื่อมีการกลับเป็นซ้ำ
พยาธิสรีรวิทยาของโรคจุดขาวในชั้นคอรอยด์ ชั้นในยังไม่เป็นที่เข้าใจอย่างสมบูรณ์ สมมติฐานหลักคือเป็นโรคอักเสบที่เริ่มต้นจากคอรอยด์ ชั้นใน
ในการศึกษาทางพยาธิวิทยาของเส้นเลือดใหม่ในคอรอยด์ ทุติยภูมิจากโรคจุดขาวในชั้นคอรอยด์ ชั้นใน พบการแทรกซึมของลิมโฟไซต์ในระดับคอรอยด์ ชั้นใน ในขณะที่หลอดเลือดฝอยคอรอยด์ ยังคงปกติ การค้นพบนี้สนับสนุนสมมติฐานในระดับจุลภาคว่าโรคจุดขาวในชั้นคอรอยด์ ชั้นในเป็นโรคอักเสบที่เริ่มต้นจากคอรอยด์
ในการตรวจ ICG บริเวณที่มีการเรืองแสงน้อยสอดคล้องกับภาวะเลือดเลี้ยงคอรอยด์ น้อยเฉพาะที่ และจุดเรืองแสงมากเฉพาะที่บนผนังหลอดเลือดอาจบ่งชี้ถึงภาวะหลอดเลือดอักเสบ เนื่องจากหลอดเลือดคอรอยด์ ขนาดใหญ่พาดผ่านบริเวณที่มีการเรืองแสงน้อยเหล่านี้ จึงเชื่อว่ากระบวนการหลอดเลือดอักเสบจำกัดอยู่ที่หลอดเลือดขนาดเล็กและหลอดเลือดฝอยคอรอยด์
เส้นเลือดใหม่ในคอรอยด์ ที่เกี่ยวข้องกับโรคจุดขาวในชั้นคอรอยด์ ชั้นในเป็นชนิดที่ 2 (เหนือเยื่อบุผิวรงควัตถุจอตา) และเกิดขึ้นผ่านความเสียหายต่อเยื่อบรูค และเยื่อบุผิวรงควัตถุจอตา หน่วยเส้นเลือดใหม่ที่ขาดเพอริไซต์แสดงความไวสูงต่อยาต้าน VEGF ทำให้เพอริไซต์เป็นเป้าหมายการรักษาที่มีศักยภาพ
ในการตรวจ OCT -A รอยโรคอักเสบของคอรอยด์ และจอตาที่มีการเคลื่อนไหวจะแสดงเป็นบริเวณที่ไม่สามารถตรวจพบสัญญาณการไหลเวียนเลือดในระดับหลอดเลือดฝอยคอรอยด์ 7) ยังคงเป็นที่ถกเถียงกันว่าการมีส่วนร่วมปฐมภูมิของหลอดเลือดฝอยคอรอยด์ เกิดขึ้นก่อนการเปลี่ยนแปลงของจอตาชั้นนอกหรือในทางกลับกัน 7)
ผู้ป่วยกลุ่มอาการจุดขาว และครอบครัวมีความชุกของโรคภูมิคุ้มกันตนเองทั่วร่างกายสูงกว่า 6) มีรายงานว่าผู้ป่วยโรคจุดขาวในชั้นคอรอยด์ ชั้นในมีแฮปโลไทป์ IL-10 และอัลลีล HLA-DRB1*15 และเชื่อว่าโรคนี้เกิดจากปัจจัยทางพันธุกรรมร่วมกับปัจจัยสิ่งแวดล้อม 6)
Jampol และ Becker (2003) เสนอให้รวม MEWDS , MCP , PIC และ AZOOR เข้าเป็นแนวคิดทางคลินิกเดียวที่เรียกว่า “AZOOR complex” สมมติฐานคือความโน้มเอียงทางพันธุกรรมร่วมกับสิ่งกระตุ้นจากสิ่งแวดล้อมที่หลากหลายนำไปสู่ฟีโนไทป์ทางคลินิกที่แตกต่างกัน 6)
Liu และคณะ (2024) รายงานกรณีติดตามผล 91 เดือนของ solitary punctate chorioretinitis (SPC) ซึ่งเป็นชนิดย่อยของ punctate inner choroidopathy SPC เป็นชนิดย่อยที่มีรอยโรคเดี่ยวปรากฏใกล้รอยบุ๋มจอตา และมีอุบัติการณ์ของการเกิดเส้นเลือดใหม่ในคอรอยด์ ทุติยภูมิต่ำกว่า (16% เทียบกับประมาณ 50%) เมื่อเทียบกับ punctate inner choroidopathy ในช่วง 91 เดือน รอยโรคยังคงเป็นเดี่ยว และโครงสร้างคล้ายหลอดเลือดบน OCTA หายไปเอง การมองเห็น สุดท้ายฟื้นคืนเป็น 0.8 และไม่จำเป็นต้องใช้การรักษาด้วย anti-VEGF 2)
Stattin และคณะ (2021) แสดงให้เห็นด้วยภาพ en face ของ SS-OCTA ว่าการเปลี่ยนแปลงโครงสร้างหลอดเลือดของเส้นเลือดใหม่ในคอรอยด์ (กิ่งก้าน, ห่วง, การเชื่อมต่อ) สามารถติดตามได้เมื่อเวลาผ่านไป และ SS-OCTA สามารถตรวจจับการเปลี่ยนแปลงของเส้นเลือดใหม่ได้แม้ไม่มีสัญญาณทางอ้อมของกิจกรรมบน SD-OCT 4) การประเมินกิจกรรมของเส้นเลือดใหม่ในคอรอยด์ และการตัดสินใจรักษาโดยอาศัยผล OCTA อาจกลายเป็นวิธีการมาตรฐานในการจัดการ punctate inner choroidopathy ในอนาคต
ในรายงานของ Scott และคณะ (2024) ไม่พบการกลับเป็นซ้ำของ punctate inner choroidopathy เมื่อฉีดวัคซีน COVID-19 ภายใต้การกดภูมิคุ้มกัน 3) บทบาทของการกดภูมิคุ้มกันเชิงป้องกันระหว่างการฉีดวัคซีนสำหรับผู้ป่วยที่มีความเสี่ยงสูงเป็นหัวข้อที่ต้องศึกษาในอนาคต
Walters และคณะ (2021) รายงานกรณีที่พบได้ยากของการอยู่ร่วมกันของ punctate inner choroidopathy ระยะยาวกับ multiple evanescent white dot syndrome ที่เริ่มมีอาการเฉียบพลัน การอยู่ร่วมกันของ punctate inner choroidopathy และ multiple evanescent white dot syndrome สนับสนุนแนวคิดของ AZOOR complex และบ่งชี้ถึงการมีอยู่ของพื้นฐานทางพันธุกรรมร่วมกัน 6)
Olazaran L, Jiménez A, González de los Mártires P, et al. White Dot Syndromes: Report of Three Cases. Case Rep Ophthalmol. 2024;15:202-211.
Liu C, Liu M, Lan X, Zhu J, Zhang Z. 91-month follow-up of solitary punctate chorioretinitis in a Chinese patient. BMC Ophthalmol. 2024;24:297.
Scott DAR, Niederer RL. Punctate Inner Choroidopathy (PIC ) disease recurrence with inflammatory choroidal neovascular membrane (iCNV M) post-COVID-19 vaccine. Eur J Ophthalmol. 2024;34(5):NP78-NP82.
Stattin M, Forster J, Ahmed D, Krepler K, Ansari-Shahrezaei S. Swept Source-Optical Coherence Tomography Angiography for Management of Secondary Choroidal Neovascularization in Punctate Inner Choroidopathy. Case Rep Ophthalmol. 2021;12:232-238.
Leclaire MD, Clemens CR, Eter N, Mihailovic N. Choroidale Neovaskularisation infolge einer “punctate inner choroidopathy”, dargestellt mittels optischer Kohärenztomographie-Angiographie. Ophthalmologe. 2021;118:842-846.
Walters AR, Choi RY, Flaxel CJ. Multiple Evanescent White Dot Syndrome Presenting in a Patient With Punctate Inner Choroidopathy. J VitreoRetinal Dis. 2021;5(3):270-274.
Testi I, Vermeirsch S, Pavesio C. Multimodal imaging in white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(「15. 点状脈絡膜内層症(PIC )」節). 日本眼科学会雑誌. 2019;123(6):635-696.