โรคตาอักเสบจากความเห็นใจ (sympathetic ophthalmia) คือภาวะยูเวียอักเสบชนิดแกรนูโลมาโตซัสทั้งสองข้างที่เกิดขึ้นหลังการบาดเจ็บทะลุหรือการผ่าตัดภายในลูกตาข้างเดียว
ตาที่ได้รับบาดเจ็บหรือผ่าตัดเรียกว่า “ตากระตุ้น” และตาอีกข้างเรียกว่า “ตาที่ถูกกระตุ้นให้เกิดอาการ”
อุบัติการณ์พบได้น้อย: 0.2-0.5% หลังการบาดเจ็บทะลุลูกตา และ 0.01-0.05% หลังการผ่าตัด 4)
พยาธิกำเนิดเหมือนกับโรคโวกท์-โคยานางิ-ฮาราดะ (โรคฮาราดะ ) ซึ่งเกี่ยวข้องกับภูมิต้านทานตนเองชนิดทีเซลล์ต่อโปรตีนเมลานิน
การรักษาขึ้นอยู่กับการแทรกแซงตั้งแต่เนิ่นๆ ด้วยการให้สเตียรอยด์ แบบพัลส์และยากดภูมิคุ้มกัน โดยใช้แนวทางของ VKH 3)
การตัดตากระตุ้นออกจะพิจารณาเฉพาะเมื่อไม่มีความหวังในการฟื้นฟูการมองเห็น และมีการอักเสบรุนแรงในตาที่ถูกกระตุ้นให้เกิดอาการ 5, 8)
ด้วยการแพร่หลายของการผ่าตัดแบบแผลเล็กในช่วงไม่กี่ปีที่ผ่านมา กรณีหลังผ่าตัดมีแนวโน้มลดลง 9)
โรคตาอักเสบจากความเห็นใจ (SO) เป็นโรคภูมิต้านตนเองที่หายากซึ่งทำให้เกิดยูเวียอักเสบชนิดแกรนูโลมาโตซัสทั้งสองข้างหลังการบาดเจ็บทะลุหรือการผ่าตัดภายในลูกตาข้างเดียว การสัมผัสของเนื้อเยื่อยูเวียกับระบบภูมิคุ้มกันเนื่องจากการบาดเจ็บหรือการผ่าตัดกระตุ้นให้เกิดการตอบสนองทางภูมิต้านตนเองต่อโปรตีนเมลานิน
ตาที่ได้รับบาดเจ็บหรือผ่าตัดเรียกว่า ตากระตุ้น และตาอีกข้างเรียกว่า ตาที่ถูกกระตุ้นให้เกิดอาการ แนวคิดนี้เป็นที่รู้จักตั้งแต่สมัยฮิปโปเครตีส โดยมีเอกสารที่เก่าแก่ที่สุดย้อนไปถึงปี ค.ศ. 1500 แนวคิดสมัยใหม่ถูกกำหนดโดย Mackenzie ในช่วงปี ค.ศ. 1840 8)
สาเหตุ อัตราการเกิด หมายเหตุ หลังการบาดเจ็บทะลุลูกตา 0.2–0.5%4) พบบ่อยในเพศชาย (สัมพันธ์กับการบาดเจ็บ) หลังการผ่าตัดที่ทะลุผนังลูกตา 0.01–0.05%4) พบบ่อยหลังการผ่าตัดหลายครั้ง หลังการผ่าตัดจอตาและวุ้นตา 0.01–0.06%7) การศึกษาไปข้างหน้าในสหราชอาณาจักร/ไอร์แลนด์
ไม่มีความแตกต่างทางเชื้อชาติ และเกิดได้ในทุกช่วงอายุ ในการสำรวจไปข้างหน้าโดย Kilmartin และคณะ (2000) ในสหราชอาณาจักรและไอร์แลนด์ ยืนยันว่าเป็นโรคที่หายากมาก โดยมีอุบัติการณ์รายปี 0.03 ต่อประชากรล้านคน7)
ระยะเวลาตั้งแต่ได้รับบาดเจ็บจนถึงเริ่มมีอาการส่วนใหญ่อยู่ระหว่าง 2 สัปดาห์ถึงหลายเดือน ในการศึกษาย้อนหลังโดย Chan และคณะ (1995) จาก 32 รายของ NIE รายงานช่วงเวลาตั้งแต่ 5 วันถึง 66 ปี แสดงให้เห็นถึงความเป็นไปได้ที่จะเกิดอาการหลังจากระยะเวลานาน5) ในช่วงไม่กี่ปีที่ผ่านมา การปรับปรุงเครื่องมือและเทคนิคการผ่าตัดทำให้แผลผ่าตัดเล็กลง ส่งผลให้กรณีหลังผ่าตัดมีแนวโน้มลดลง9)
Q
การผ่าตัดชนิดใดที่อาจเป็นสาเหตุได้?
A
การผ่าตัดภายในลูกตาเกือบทุกชนิดสามารถเป็นสาเหตุได้ พบได้บ่อยหลังการผ่าตัดหลายครั้ง เช่น การผ่าตัดจอประสาทตา กลับเข้าที่หรือการผ่าตัดน้ำวุ้นตา การผ่าตัดทำลายซิลิอารีบอดี ้มีอัตราการเกิดโรคสูงกว่าเล็กน้อย ด้วยการผ่าตัดน้ำวุ้นตา แบบแผลเล็กสมัยใหม่ (25-27G) อัตราการเกิดโรคต่ำมาก 9)
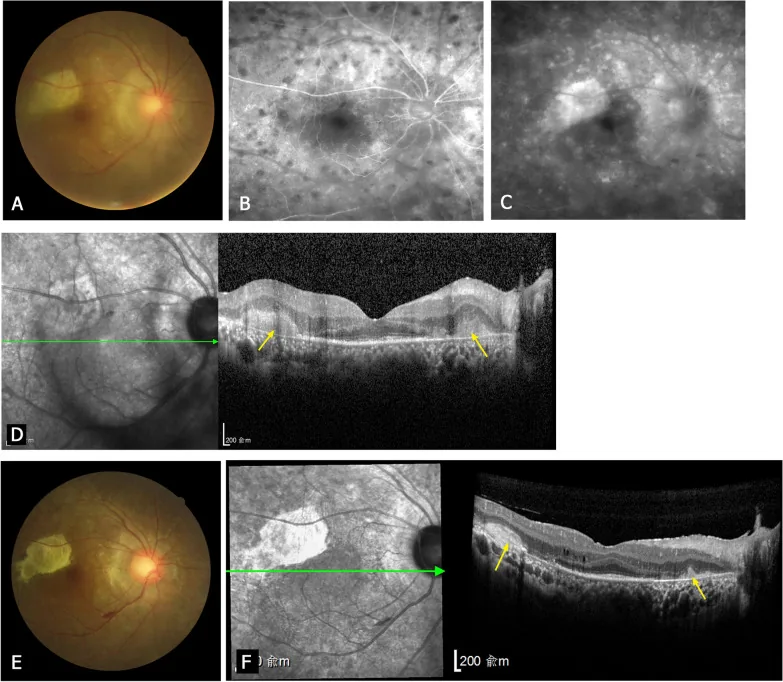
ภาพจอประสาทตา การตรวจหลอดเลือดด้วยฟลูออเรสซีน และ OCT ของโรคตาอักเสบซิมพาเทติก แสดงรอยโรคคอรอยด์และจอประสาทตาสีขาวเหลือง และความขุ่นของน้ำวุ้นตา Zhuang H, et al. Clinical classification, visual outcomes, and optical coherence tomographic features of 48 patients with posterior sympathetic ophthalmia. Orphanet J Rare Dis. 2022. Figure 3. PM
CI D: PMC8895912. License: CC BY.
ภาพหลายรูปแบบแสดงผลการตรวจส่วนหลังของตาในโรคตาอักเสบซิมพาเทติก จอประสาทตา แสดงรอยโรคอักเสบของคอรอยด์ และจอประสาทตา สีขาวเหลืองและความขุ่นของน้ำวุ้นตา และสามารถยืนยันรอยโรคอักเสบได้ด้วยการตรวจหลอดเลือดด้วยฟลูออเรสซีน และ OCT ภาพเหล่านี้สอดคล้องกับผลการตรวจส่วนหลังของตาในโรคตาอักเสบซิมพาเทติกที่กล่าวถึงในหัวข้อ “อาการหลักและผลการตรวจทางคลินิก”
ในช่วงเริ่มต้นของโรค จะมีอาการปวดศีรษะ สูญเสียการได้ยิน หูอื้อ ร่วมกับการมองเห็น ลดลงและภาพบิดเบี้ยว ในตาทั้งสองข้าง การมองเห็น ระยะใกล้ลดลงมักเป็นอาการเริ่มแรก
ตามัวและการมองเห็น ลดลง : เกิดขึ้นทั้งสองข้าง การเริ่มต้นอาจเป็นแบบค่อยเป็นค่อยไปหรือเฉียบพลันปวดตา และตาแดง ซิลิอารีบอดี ้กลัวแสง : เพิ่มความไวต่อแสง
อาการนอกตารวมถึงอาการระคายเคืองเยื่อหุ้มสมอง (ปวดศีรษะ คลื่นไส้ คอแข็ง) อาการหูชั้นใน (สูญเสียการได้ยินแบบประสาทรับเสียง หูอื้อ เวียนศีรษะ) และอาการทางผิวหนัง (จุดด่างขาว ผมร่วง ผมหงอก) อาจแสดงอาการนอกตาเช่นเดียวกับโรคฮาราดะ
ผลการตรวจระยะเฉียบพลัน
ส่วนหน้าของตา : คราบเคอราติกพรีซิพิเทตแบบไขมันหมู การอักเสบในช่องหน้าตา (เซลล์, แฟลร์) ม่านตาติด หลัง ก้อนคอปเป/บูซัคกา
ส่วนหลังของตา : จานประสาทตา แดงและบวม จอประสาทตาลอก แบบมีน้ำใต้จอประสาทตา คอรอยด์หนา ตัว น้ำวุ้นตา ขุ่น
ก้อนดาเลน-ฟุคส์ : ก้อนสีขาวเหลืองระหว่างเยื่อบุผิวรงควัตถุจอประสาทตา และเยื่อบรูค (ลักษณะทางพยาธิวิทยาร่วมกับโรคฮาราดะ )
ผลการตรวจระยะฟื้นตัวและเรื้อรัง
จอประสาทตา สีพระอาทิตย์ตกจอประสาทตา จากการสูญเสียเม็ดสีเมลานินของคอรอยด์ และจอประสาทตา
รอยฝ่อหลายจุดบริเวณรอบนอก : เกิดขึ้นหลายจุดในช่วงพักฟื้น
ต้อกระจก ทุติยภูมิและต้อหินทุติยภูมิ สเตียรอยด์
ความดันลูกตา อาจสูงขึ้นจากต้อหิน อักเสบ หรือต่ำลงจากความผิดปกติของซิลิอารีบอดี การศึกษาในกลุ่มประชากรขนาดใหญ่รายงานว่าผู้ป่วยประมาณ 30-40% อาจมีสายตา 20/200 หรือแย่ลงในการตรวจครั้งสุดท้าย 4)
Q
แตกต่างจากโรคฮาราดะอย่างไร?
A
พยาธิสภาพเหมือนกับโรคฮาราดะ แต่ปัจจัยกระตุ้นต่างกัน ในโรคฮาราดะ ไม่มีประวัติการบาดเจ็บที่ตามาก่อน และอุบัติการณ์ของอาการทางระบบ (เม็ดเลือดขาวในน้ำไขสันหลังเพิ่มขึ้นและอาการทางผิวหนัง) สูงกว่า ในโรคฮาราดะ อาการทางส่วนหลังมักเกิดก่อน แล้วจึงเกิดการอักเสบของส่วนหน้าตามมา ในโรคตาอักเสบจาก sympathetic ร่องรอยการบาดเจ็บหรือการผ่าตัดที่ตากระตุ้นเป็นกุญแจสำคัญในการวินิจฉัย
พยาธิสภาพของโรคตาอักเสบจาก sympathetic ถือว่าเหมือนกันทุกประการกับโรคฮาราดะ (VKH) การบาดเจ็บหรือการผ่าตัดที่ทำให้เนื้อเยื่อยูเวียสัมผัสกับภายนอก ทำให้ระบบภูมิคุ้มกันรับรู้เนื้อเยื่อยูเวีย และเกิดโรคภูมิต้านตนเองชนิดทีเซลล์ต่อโปรตีนเมลานินของตนเอง
ปัจจัยเสี่ยงหลัก :
การบาดเจ็บทะลุลูกตา : การบาดเจ็บที่ทำให้เนื้อเยื่อยูเวียยื่นหรือสัมผัสภายนอกเป็นลักษณะที่พบบ่อยที่สุด การศึกษาของ Galor และคณะ (2009) พบว่าการบาดเจ็บเป็นสาเหตุที่พบบ่อยที่สุดของตากระตุ้น 4) การผ่าตัดภายในลูกตา (ที่มีการเจาะผนังลูกตา):
การผ่าตัดน้ำวุ้นตา หรือการผ่าตัดจอประสาทตา กลับที่ (ความเสี่ยงสูงหากทำหลายครั้ง)การผ่าตัดทำลายซิลิอารีบอดี (อุบัติการณ์ค่อนข้างสูง)
การผ่าตัดต้อกระจก (พบน้อย) · การผ่าตัดต้อหิน (พบน้อย)
ความโน้มเอียงทางพันธุกรรมที่เกี่ยวข้องกับ HLA : มีรายงานความสัมพันธ์กับ HLA-DRB1*04, HLA-DR4, HLA-DQ4 8)
โรคตาอักเสบจากภูมิคุ้มกันทำลายตนเองที่เกี่ยวข้องกับยา Immune Checkpoint Inhibitor (ICI ) : มีรายงานผู้ป่วยที่กลับมาเป็นซ้ำหลังจากได้รับยาเพมโบรลิซูแมบ ต้องระมัดระวังเป็นพิเศษในผู้ป่วยมะเร็งที่มีประวัติการบาดเจ็บที่ตามาก่อน 2)
การวินิจฉัยทำได้อย่างครอบคลุมโดยอาศัยประวัติการบาดเจ็บทะลุลูกตาหรือการผ่าตัดลูกตาภายใน ผลการตรวจตา ผลการตรวจภาพ และอาการนอกตา แม้ว่าประวัติการบาดเจ็บจะไม่ชัดเจน รอยแผลเป็นที่ลูกตาเมื่อตรวจสามารถเป็นเบาะแสในการวินิจฉัยได้
ประวัติการบาดเจ็บทะลุลูกตา/การผ่าตัดลูกตาภายใน (ข้อกำหนดบังคับ)ม่านตาอักเสบชนิดแกรนูโลมา ทัสทั้งสองข้าง (ผลการตรวจเดียวกันกับ VKH)อาการนอกตา (การระคายเคืองเยื่อหุ้มสมอง, หูชั้นใน, ผิวหนัง)
จอประสาทตา สีพระอาทิตย์ตกดินในระยะฟื้นตัวทำให้วินิจฉัยได้ง่ายขึ้นก้อน Dalen-Fuchs (ยืนยันทางพยาธิวิทยา)
OCT (เครื่องตรวจชั้นตาด้วยแสง)คอรอยด์ จอประสาทตาลอก แบบมีน้ำ และบวมของหัวประสาทตา EDI-OCT แสดงความหนาของคอรอยด์ เพิ่มขึ้นอย่างชัดเจนในระยะเฉียบพลัน (>400 ไมครอน) 8) FA (การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน )ฟลูออเรสซีน จำนวนมากที่ขั้วหลัง (แบบผิวหนังสัตว์เลื้อยคลาน) มีน้ำใต้จอประสาทตา ICGA (การถ่ายภาพหลอดเลือดด้วยอินโดไซยานีนกรีน)คอรอยด์ ผ่านจุดเรืองแสงน้อยOCT -A (การถ่ายภาพหลอดเลือดด้วยเครื่องตรวจชั้นตา)คอรอยด์ คาดว่าจะนำไปใช้ในการติดตามโรค 8) อัลตราซาวนด์ B-scan : ยืนยันความหนาของคอรอยด์ (สัญญาณ T)
โรคที่ต้องแยก ความแตกต่างจากจักษุอักเสบจากภูมิแพ้ตนเอง โรคฮาราดะ (VKH)ไม่มีประวัติการบาดเจ็บ อาการทั่วร่างกาย (น้ำไขสันหลัง ผิวหนัง) พบบ่อย 3) ซาร์คอยโดซิส รอยโรคปอด ACE สูง ต่อมน้ำเหลืองฮิลัสโตทั้งสองข้าง ม่านตาอักเสบจากวัณโรค ติดเชื้อ (QFT, T-SPOT บวก) พบวัณโรคทั่วร่างกาย ม่านตาอักเสบจากซิฟิลิส การวินิจฉัยแยกโรคโดยการตรวจทางซีรั่มวิทยา (RP R, TPHA) เยื่อบุตาอักเสบ ส่วนหลังปวดตา อย่างรุนแรง พบสัญญาณ T
จำเป็นต้องแยกม่านตาอักเสบ จากการติดเชื้อ (วัณโรค ซิฟิลิส) ก่อนเริ่มการรักษาด้วยยากดภูมิคุ้มกัน 3)
Q
การตัดตาที่ได้รับบาดเจ็บออกจะป้องกันการเกิดโรคได้หรือไม่?
A
มีรายงานคลาสสิกว่าการตัดตาที่ถูกกระตุ้นภายใน 2 สัปดาห์หลังการบาดเจ็บจะทำให้ม่านตาอักเสบ ในตาอีกข้างไม่เรื้อรังและพยากรณ์โรคดี 5) อย่างไรก็ตาม ด้วยความก้าวหน้าของการรักษาด้วยยากดภูมิคุ้มกันสมัยใหม่ กรณีที่ไม่ต้องตัดตากำลังเพิ่มขึ้น 8) การตัดตาหลังเกิดโรคไม่ช่วยให้การอักเสบในตาอีกข้างดีขึ้น ควรพิจารณาการตัดตาเป็นรายกรณี
โรคตาอักเสบจาก sympathetic มีพยาธิสภาพเดียวกับโรคฮาราดะ และการรักษาจะใช้แนวทางของ VKH 3) เมื่อยืนยันว่าไม่มีการติดเชื้อแล้ว ควรเริ่มการรักษาด้วยการปรับภูมิคุ้มกันทันที
ระยะการรักษา ยาและขนาดยา หมายเหตุ การรักษาแบบพัลส์ (ทางเลือกแรก) เมทิลเพรดนิโซโลน 1 กรัม/วัน × 3 วัน ฉีดเข้าหลอดเลือดดำ ระงับการอักเสบอย่างรวดเร็ว การรักษาด้วยขนาดสูง (ต่อ) เพรดนิโซโลน 1-2 มก./กก./วัน รับประทาน ต่อเนื่องเป็นเวลาหลายเดือนแล้วค่อยๆ ลดลง ระยะลดขนาดยา 60 มก./วัน → ลด 10 มก. ทุก 4 วัน → 40 มก./4 สัปดาห์ → 20 มก./4 สัปดาห์ → 10 มก./4 สัปดาห์ → 5 มก./4 สัปดาห์ หยุดยาภายใน 6 เดือนหรือมากกว่า
การรักษาด้วยสเตียรอยด์ ขนาดสูงทำให้จอประสาทตาลอก แบบเซรุ่มหายไปอย่างรวดเร็ว และการศึกษาโดย Galor และคณะ (2009) รายงานว่าการมองเห็น สุดท้ายที่ 20/40 หรือดีกว่าเกิดขึ้นในประมาณ 50% ของกรณี 4) สเตียรอยด์ ชนิดรับประทานจะลดขนาดยาอย่างช้าๆ และหยุดยาภายใน 6 เดือนหรือมากกว่าแม้ไม่มีอาการกำเริบ
ยาหยอดตาสเตียรอยด์ : เบตาเมทาโซน 0.1% วันละ 3-4 ครั้ง ปรับตามระดับการอักเสบยาขยายม่านตา : ยาหยอดตา Midrin-P วันละ 1 ครั้ง (ตอนกลางคืน) เพื่อป้องกันการยึดติดของม่านตา ด้านหลัง
ในกรณีที่มีอาการกำเริบซ้ำระหว่างการลดสเตียรอยด์ ให้ใช้ยากดภูมิคุ้มกันร่วมด้วย
ไซโคลสปอริน (Neoral)เมโธเทรกเซท (MTX)FA ST แสดงให้เห็นว่า MTX มีประสิทธิภาพเทียบเท่าหรือดีกว่า MMF ในการปรับปรุงการมองเห็น และจอประสาทตาลอก แบบเซรุ่มในระยะเฉียบพลัน 10) ไมโคฟีโนเลต โมเฟทิล (MMF) : 1.5 กรัม วันละ 2 ครั้ง มีฤทธิ์ประหยัดสเตียรอยด์ 10) อะซาไธโอพรีน
ยาชีววัตถุ (กรณีดื้อต่อการรักษา)
อะดาลิมูแมบ ม่านตาอักเสบที่ไม่ติดเชื้อ อินฟลิซิแมบ ก่อนเริ่มใช้ยา TNF inhibitor ต้องตรวจคัดกรองวัณโรคและไวรัสตับอักเสบบีตามแนวทางการรักษาม่านตาอักเสบ และแนวทางการใช้ TNF inhibitor 3)
สเตียรอยด์
การใช้สเตียรอยด์ ขนาดสูงทั่วร่างกายอาจทำให้เกิดผลข้างเคียง เช่น การเกิดหรือแย่ลงของเบาหวาน ความดันโลหิตสูง การติดเชื้อ นอนไม่หลับ อาการทางจิต แผลในกระเพาะอาหาร กระดูกพรุน ควรตรวจเลือดและปัสสาวะก่อนเริ่มการรักษา และใช้ยาป้องกันกระเพาะอาหารและแคลเซียมเสริม การลดขนาดยาต้องทำอย่างช้าๆ การหยุดยาทันทีอาจทำให้เกิดอาการถอนยา
ยังมีการถกเถียงเกี่ยวกับการตัดลูกตาข้างที่ก่อโรค รายงานคลาสสิกระบุว่าการตัดภายใน 2 สัปดาห์หลังเริ่มมีอาการอาจช่วยหลีกเลี่ยงการกลายเป็นเรื้อรังในตาข้างที่ถูกกระทบ 5) อย่างไรก็ตาม ด้วยความก้าวหน้าของการรักษาด้วยยากดภูมิคุ้มกันสมัยใหม่ หลายกรณีไม่จำเป็นต้องตัด 8, 9) เงื่อนไขที่ควรพิจารณาตัด :
การมองเห็น ของตาข้างที่ก่อโรคแย่มากและไม่มีโอกาสฟื้นตัวและม่านตาอักเสบ ในตาข้างที่ถูกกระทบรุนแรงและควบคุมได้ยาก
การวิเคราะห์อภิมานเมื่อเร็วๆ นี้ไม่พบหลักฐานที่สอดคล้องกันเกี่ยวกับผลของการตัดหลังเกิดโรค จึงจำเป็นต้องใช้การตัดสินใจที่เป็นกลาง 8, 9)
Q
ควรตัดลูกตาข้างที่ก่อโรคออกดีหรือไม่?
A
ด้วยการรักษาสมัยใหม่ ไม่จำเป็นต้องตัดเสมอไป ตาข้างที่ก่อโรคอาจยังคงมีการมองเห็น อยู่บ้างและสามารถรักษาไว้ได้หากได้รับการรักษาด้วยสเตียรอยด์ อย่างเหมาะสม การตัดจะพิจารณาเฉพาะในเงื่อนไขที่การมองเห็น ของตาข้างที่ก่อโรคแย่มากไม่มีโอกาสฟื้นตัว และการอักเสบในตาข้างที่ถูกกระทบรุนแรงเท่านั้น สิ่งสำคัญคือต้องปรึกษาแพทย์ผู้รักษาและตัดสินใจอย่างรอบคอบ
กลไกการเกิดโรคตาอักเสบจาก sympathetic ophthalmia มีความคล้ายคลึงกับโรคฮาราดะ หลายประการ ดวงตาเป็นอวัยวะที่มีภูมิคุ้มกันพิเศษ และโดยปกติแอนติเจนภายในยูเวียจะไม่ถูกจดจำโดยระบบภูมิคุ้มกันของร่างกายได้ง่าย 1) การบาดเจ็บแบบทะลุหรือการผ่าตัดภายในตาทำให้ภูมิคุ้มกันพิเศษนี้เสียไป ทำให้แอนติเจนภายในตา เช่น โปรตีนเมลานิน สัมผัสกับระบบภูมิคุ้มกัน
การตอบสนองทางภูมิคุ้มกัน :
เซลล์ CD4+ Th1/Th17 แทรกซึมเข้ามาอย่างเด่นชัดและผลิต IFN-γ และ IL-17
เซลล์ CD8+ ที่เป็นพิษต่อเซลล์จะแทรกซึมตามมาและโจมตีเมลาโนไซต์ (ไทโรซิเนส, TRP -1, TRP -2, gp100) เป็นเป้าหมาย 8)
การทำลาย Blood-ocular barrier และ Blood-retinal barrier ทำให้เกิดการตอบสนองภูมิต้านตนเองต่อแอนติเจนภายในตา 1)
ปัจจัยทางพันธุกรรมที่เกี่ยวข้องกับ HLA-DR4 และ HLA-DRB1*04 เพิ่มความไวต่อการเกิดโรค 8)
ลักษณะทางพยาธิวิทยาเนื้อเยื่อ :
ก้อน Dalen-Fuchs : กลุ่มของเซลล์เยื่อบุผิวที่มีเม็ดสีอยู่ระหว่าง retinal pigment epithelium และ Bruch membrane ก่อตัวเป็น granuloma ร่วมกับลิมโฟไซต์และเซลล์ยักษ์หลายนิวเคลียสการคงไว้ของ choroidal capillary bed : ในโรคฮาราดะ การอักเสบจะลุกลามไปยัง choroidal capillary bed แต่ใน sympathetic ophthalmia มักจะคงไว้ไม่ลุกลามไปยังจอประสาทตา : โดยปกติกระบวนการอักเสบจะไม่ถึงจอประสาทตา ในส่วนหน้าของตา ม่านตา จะหนาตัวขึ้นพร้อมกับการแทรกซึมแบบ nodular
เมื่อใช้ immune checkpoint inhibitors (ICI ) การสัมผัสกับแอนติเจนภายในตาก่อนหน้านี้อาจกระตุ้นให้เกิดการกระตุ้นเซลล์ T โดยไม่ได้ตั้งใจ 2)
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
ในการวิเคราะห์กลุ่มย่อย VKH ของ FA ST Uveitis Trial (RCT แบบปกปิดสองทาง) โดย Acharya และคณะ (2024) พบว่า MTX มีประสิทธิภาพเท่าเทียมหรือดีกว่า MMF ในการปรับปรุงผลการตรวจคอรอยด์ และจอประสาทตา ในระยะเฉียบพลัน (จอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตา และคอรอยด์หนา ตัว) 10) เนื่องจากโรคตาอักเสบจากภูมิคุ้มกันต่อต้านตนเอง (sympathetic ophthalmia) มีพยาธิสรีรวิทยาเดียวกันกับ VKH ผลการทดลองนี้จึงสามารถนำไปใช้กับการเลือกใช้ยากดภูมิคุ้มกันสำหรับโรคตาอักเสบจากภูมิคุ้มกันต่อต้านตนเองได้
OCT -A ซึ่งสามารถประเมินปริมาณการไหลเวียนเลือดในหลอดเลือดฝอยคอรอยด์ ได้ กำลังถูกศึกษาในฐานะตัวบ่งชี้ทางชีวภาพ เพื่อตรวจหากิจกรรมของโรคที่แฝงอยู่หลังจากการอักเสบสงบลงทางคลินิก 8) การติดตามความหนาของคอรอยด์ ตามช่วงเวลาด้วย EDI-OCT ก็คาดว่าจะเป็นตัวบ่งชี้ทำนายการกลับเป็นซ้ำ
ด้วยการแพร่หลายของการผ่าตัดวุ้นตา แบบ 27G และ 25G อุบัติการณ์หลังผ่าตัดลดลงอย่างมีนัยสำคัญเมื่อเทียบกับการผ่าตัดแบบเปิดแผลแบบดั้งเดิม ในการทบทวนของ Patel และคณะ (2022) การปรับปรุงเทคนิคการผ่าตัดสมัยใหม่ถือเป็นสาเหตุหลักของการลดลงของอุบัติการณ์ 9) ในทางกลับกัน อุบัติการณ์หลังการบาดเจ็บนั้นยากที่จะลดลงหากไม่มีการป้องกันการบาดเจ็บ และยังคงต้องใช้ความระมัดระวัง
ยาชีววัตถุ เช่น adalimumab และ infliximab มีประสบการณ์การใช้สะสมในผู้ป่วย VKH และโรคตาอักเสบจากภูมิคุ้มกันต่อต้านตนเองที่ดื้อต่อการรักษา 6) อย่างไรก็ตาม ส่วนใหญ่เป็นรายงานผู้ป่วยและชุดผู้ป่วยขนาดเล็ก และการเลือกใช้ยาจะพิจารณาเป็นรายบุคคลตามความรุนแรงของการอักเสบ การกลับเป็นซ้ำ และภาวะแทรกซ้อนทางระบบ
มีการรายงานการกลับเป็นซ้ำของโรคตาอักเสบจากภูมิคุ้มกันต่อต้านตนเองหลังการให้ยา pembrolizumab ซึ่งกลายเป็นความท้าทายทางคลินิกใหม่ในยุคของการบำบัดด้วยภูมิคุ้มกันมะเร็ง 2) แนะนำให้เพิ่มการเฝ้าระวังทางจักษุวิทยาเมื่อเริ่มใช้ ICI ในผู้ป่วยที่มีประวัติการบาดเจ็บที่ตา
Agarwal M, Radosavljevic A, Tyagi M, Pichi F, Al Dhanhani AA, Agarwal A, Cunningham ET Jr. Sympathetic Ophthalmia - An Overview. Ocul Immunol Inflamm. 2023;31(4):793-809. doi:10.1080/09273948.2022.2058554.
Lee J, Shin JY, Lee JS, Lee SC, Hong MH, Lee CS. Recurrent Sympathetic Ophthalmia with Annular Choroidal Detachment after Pembrolizumab Treatment: A Case Report. Ocul Immunol Inflamm. 2020;28(6):864-867. doi:10.1080/09273948.2019.1604975.
日本眼炎症学会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696.
Galor A, Davis JL, Flynn HW Jr, et al. Sympathetic ophthalmia: incidence of ocular complications and vision loss in the sympathizing eye. Am J Ophthalmol. 2009;148(5):704-710.
Chan CC, Roberge FG, Whitcup SM, Nussenblatt RB. 32 cases of sympathetic ophthalmia: a retrospective study at the NEI, NIH. Arch Ophthalmol. 1995;113(5):597-601.
Paulbuddhe V, Addya S, Gurnani B, Singh D, Tripathy K, Chawla R. Sympathetic Ophthalmia: Where Do We Currently Stand on Treatment Strategies? Clin Ophthalmol. 2021;15:4201-4218. doi:10.2147/OPTH.S289688. PMID:34707340. PMCI D:PMC8542579. https://pmc.ncbi.nlm.nih.gov/articles/PMC8542579/
Kilmartin DJ, Dick AD, Forrester JV. Prospective surveillance of sympathetic ophthalmia in the UK and Republic of Ireland. Br J Ophthalmol. 2000;84(3):259-263.
Chu XK, Chan CC. Sympathetic ophthalmia: to the twenty-first century and beyond. J Ophthalmic Inflamm Infect. 2013;3:49.
Patel SS, Hariprasad SM. Sympathetic ophthalmia: a mini-review. Semin Ophthalmol. 2022;37(3):313-321.
Acharya NR, Rathinam SR, Thundikandy R, et al. Outcomes in Patients With Vogt-Koyanagi-Harada Disease From the FA ST Uveitis Trial. Am J Ophthalmol. 2024;267:100-111.