活动性病变
黄白色脉络膜视网膜病变:后极部可见小型、边界清晰的黄灰色斑点。视乳头周围不受累。
无眼内炎症:点状内层脉络膜病变的特征是不伴有前房炎症和玻璃体炎3)。
神经感觉层视网膜脱离:活动性病变上方可能伴有浆液性视网膜脱离。

点状内层脉络膜病变(punctate inner choroidopathy)是1984年由Watzke等人首次报告的特发性炎症性脉络膜疾病。它被归类为白点综合征之一,属于侵犯外视网膜、脉络膜毛细血管层和脉络膜的炎症性疾病群7)。根据葡萄膜炎诊疗指南(日眼会志 2019;123(6):635-696),它被定位为非感染性、以眼底病变为主的后部葡萄膜炎,具有缓慢发病、单眼或双眼性的特点8)。
主要发生于近视的年轻女性(约90%为女性)5)。大规模研究报告平均发病年龄为36岁,平均近视度数为-4.5屈光度5)。好发于中度近视眼的年轻女性,急性期在后极部可见数个小型黄白色病灶,随时间推移变为萎缩病灶。
点状内层脉络膜病变与多灶性脉络膜炎(MFC)在侵犯脉络膜、视网膜色素上皮(RPE)和外视网膜方面有共同点,提示可能属于同一疾病谱7)。两者的鉴别关键在于有无玻璃体炎和病变分布范围。点状内层脉络膜病变无玻璃体炎,病变局限于后极部;而MFC伴有玻璃体炎,病变可延伸至周边部6)。
点状内层脉络膜病变无玻璃体炎,病变局限于后极部;而MFC伴有玻璃体炎和前房炎症,病变可延伸至中周边部。两者可能属于同一疾病谱。
点状内层脉络膜病变最常见的首发症状是单眼暗点和视力下降。
眼底所见:后极部局限分布12至25个100–300μm大小的黄白色小斑点,呈随机模式。病变发生在外层视网膜、RPE和内层脉络膜水平。80%为双眼性,但常左右不对称1)。
点状内层脉络膜病变的特征总结如下。
活动性病变
黄白色脉络膜视网膜病变:后极部可见小型、边界清晰的黄灰色斑点。视乳头周围不受累。
无眼内炎症:点状内层脉络膜病变的特征是不伴有前房炎症和玻璃体炎3)。
神经感觉层视网膜脱离:活动性病变上方可能伴有浆液性视网膜脱离。
瘢痕期病变
SD-OCT描述了点状内层脉络膜病变的五阶段演变过程2)。
点状内层脉络膜病变的病因不明,但被认为是一种多基因易感性基础上的自身免疫性疾病,由感染、疫苗接种或压力等环境刺激诱发。
| 因素 | 详情 |
|---|---|
| 性别 | 女性约占90–93% |
| 年龄 | 18–40岁(平均36岁) |
| 近视 | −3.25至−10.0 D |
已有报道COVID-19感染后点状内层脉络膜病变的发病和再激活。SARS-CoV-2感染可能在有遗传易感性的个体中诱发自身免疫失调。此外,也有报道COVID-19疫苗接种后点状内层脉络膜病变复发3)。
Scott等人(2024)报告了一例38岁女性在接种辉瑞-BioNTech COVID-19疫苗7天后点状内层脉络膜病变复发,并伴有炎症性脉络膜新生血管膜(iCNVM)。在免疫抑制状态下接种疫苗未出现复发,但在非免疫抑制状态下接种第四剂后复发3)。
已有报道在COVID-19疫苗接种后点状内层脉络膜病变复发3)。但疫苗的益处远大于眼内炎症复发的风险。有病史者应在接种前后咨询眼科医生进行随访观察。
点状内层脉络膜病变的诊断基于临床发现。结合辅助影像学检查进行确诊。组织胞浆菌素皮肤试验为阴性。
FA中,活动性病变在动脉早期显示高荧光,晚期出现渗漏和染色7)。比临床检查发现更多病变。CNVM表现为不规则的网状新生血管网络。
ICG在后极部和视盘周围显示中期低荧光病变7)。在32%的患眼中检测到亚临床低荧光斑点,提高诊断能力。
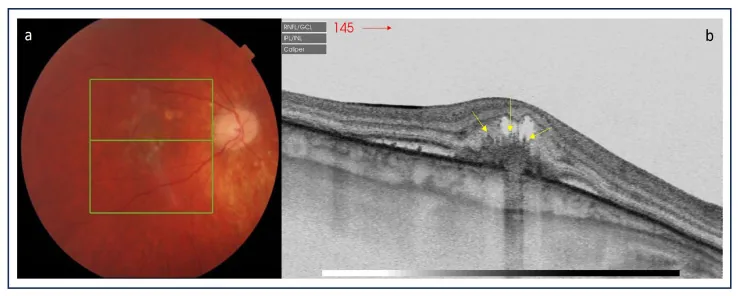
SD-OCT对点状内层脉络膜病变的诊断和随访有用。活动性病变显示RPE局灶性高反射隆起和椭圆体带(EZ)中断7)。脉络膜新生血管(CNV)阳性病变的高度、宽度和体积大于CNV阴性病变,伴有EZ和Bruch膜中断以及外层视网膜模糊。
深度增强成像OCT(EDI-OCT)显示活动性病变正下方的脉络膜厚度增加,治疗后减少(“海绵征”)。这有助于与近视性脉络膜新生血管鉴别。
OCTA是点状内层脉络膜病变诊断中的重要影像学手段。它能以高检出率识别传统FA或SD-OCT难以发现的继发性脉络膜新生血管。
使用OCTA检查,可以在许多点状内层脉络膜病变患者中证明脉络膜新生血管的存在,包括FA未能得出结论的病例。
Leclaire等人(2021)报告了在FAG和SD-OCT中未检测到、仅在OCT-A中发现的继发性脉络膜新生血管病例,提示临床上无症状的继发性脉络膜新生血管可能有很多未被发现5)。
Stattin等人(2021)报告使用SS-OCTA监测点状内层脉络膜病变继发脉络膜新生血管的血管密度变化,并将其作为抗VEGF治疗决策的指导依据4)。
活动性点状内层脉络膜病变表现为低自发荧光1)。围绕活动性病变的高自发荧光晕环可能是炎症未受控制的间接征象。萎缩性瘢痕病变也表现为低自发荧光斑1)。
眼底自发荧光是一种无创、快速的检查方法,有助于评估病变分布、监测治疗效果和检测复发1)。
约41%的患者出现生理盲点扩大,也可见中心暗点和旁中心暗点。45%的患者视野正常。
需要鉴别的疾病如下:
多发性一过性白点综合征几乎为单眼发病,数周内自然缓解,几乎不留瘢痕或脉络膜新生血管6)。点状内层脉络膜病变多为双眼发病,留有萎缩性瘢痕,且脉络膜新生血管并发症发生率高。OCTA上血流征象的有无也有助于鉴别。
如果没有脉络膜新生血管的证据,视力预后良好,大多数病例无需治疗。唯一的例外是当存在非常接近固视点的活动性炎症病变时,可考虑药物治疗。
对于中心凹附近的活动性病变,可采用曲安奈德后Tenon囊下注射或口服类固醇(泼尼松龙40-60mg/天逐渐减量)8)。如果中心凹外的脉络膜新生血管对类固醇无反应,可尝试光凝治疗。
合并脉络膜新生血管的病例需要积极治疗。
这是治疗合并脉络膜新生血管的点状内层脉络膜病变的主要方法。使用贝伐珠单抗、雷珠单抗和阿柏西普。
Stattin等人(2021)在SS-OCTA监测下,对点状内层脉络膜病变继发的脉络膜新生血管按需给予雷珠单抗(0.5mg),共注射6次,最终视力达到20/204)。
抗VEGF药物与类固醇的双向方法被认为是有效的4)。对于合并CNV的病例,玻璃体内注射贝伐珠单抗有时被用作一线治疗8)。
全身性类固醇通常以1mg/kg/天(60-80mg/天)开始,持续3-5天,然后逐渐减量4)。有报告称口服类固醇可将iCNVM发生风险降低一半3)。
玻璃体内类固醇制剂包括以下:
在合并脉络膜新生血管的病例中,PDT的有效性已有报道。与口服泼尼松龙(1mg/kg/天)联合使用时,平均2次PDT后视力改善15个字母。
因病例而异。在SS-OCTA指导下的按需给药中,有报告称进行了6次注射4)。需要定期进行影像检查评估脉络膜新生血管的活动性,复发时可能需要追加给药。
点状内层脉络膜病变的病理生理学尚未完全阐明。主流假说认为它是一种起源于内层脉络膜的炎症性疾病。
对点状内层脉络膜病变继发CNVM的病理研究表明,脉络膜毛细血管层得以保留,而内层脉络膜水平存在淋巴细胞浸润。这一发现从超微结构上支持了点状内层脉络膜病变是一种起源于脉络膜的炎症性疾病的假说。
在ICG检查中,低荧光区域对应局灶性脉络膜低灌注,血管壁上的局灶性高荧光点可能提示血管炎。由于大的脉络膜血管穿过这些低荧光区域,因此认为血管炎过程局限于小血管和脉络膜毛细血管层。
点状内层脉络膜病变相关的脉络膜新生血管为2型(视网膜色素上皮下),通过破坏Bruch膜和视网膜色素上皮而发生。周细胞稀少的新生血管单元对抗VEGF药物高度敏感,表明周细胞可能是一个重要的治疗靶点。
在OCT-A上,活动性炎症性脉络膜视网膜病变在脉络膜毛细血管层水平显示血流信号不可检测7)。脉络膜毛细血管层的原发性受累是否先于外层视网膜改变,还是相反,仍存在争议7)。
白点综合征患者及其家属中全身性自身免疫性疾病的患病率较高6)。据报道,点状内层脉络膜病变患者携带IL-10单倍型和HLA-DRB1*15等位基因,提示遗传易感性与环境因素共同作用导致发病6)。
Jampol和Becker(2003)提出将MEWDS、MCP、PIC和AZOOR整合为一个单一的临床概念,称为“AZOOR复合体”。该假说认为遗传易感性与多种环境触发因素相结合,导致不同的临床表型6)。
Liu等人(2024)报告了一例孤立性点状脉络膜视网膜炎(SPC)的91个月随访病例,SPC是点状内层脉络膜病变的一个亚型,表现为单个病灶出现在黄斑中心凹附近,其脉络膜新生血管的继发发生率低于点状内层脉络膜病变(16% vs 约50%)。在91个月的病程中,病灶保持孤立性,OCTA上的血管样结构自然消退。最终视力恢复到0.8,无需抗VEGF治疗2)。
Stattin等人(2021)通过SS-OCTA的en face图像显示,可以随时间追踪脉络膜新生血管的血管结构变化(分支、环、吻合),并且即使SD-OCT没有间接活动性表现,SS-OCTA也能捕捉到新生血管的变化4)。基于OCTA结果的脉络膜新生血管活动性评估和治疗决策,可能成为未来点状内层脉络膜病变管理的标准方法。
Scott等人(2024)的报告显示,在免疫抑制状态下接种COVID-19疫苗时,未观察到点状内层脉络膜病变的复发3)。对于高风险患者,疫苗接种时预防性免疫抑制的作用是未来需要研究的问题。
Walters等人(2021)报告了一例罕见的病例,一名长期患有点状内层脉络膜病变的患者急性发作多发性一过性白点综合征。点状内层脉络膜病变与多发性一过性白点综合征的共存支持了AZOOR复合体的概念,并提示存在共同的遗传基础6)。