匐行性脉络膜炎(SC)是一种原因不明的慢性进行性炎症性疾病,累及视网膜色素上皮 、脉络膜毛细血管层 和脉络膜 。
这是一种罕见疾病,占所有后葡萄膜炎 的1%~5%,好发于青壮年。
特征性表现为从视盘周围呈匐行性扩展的灰黄色脉络膜 视网膜 病变。
反复复发和缓解,当萎缩性瘢痕累及中心凹 时会导致不可逆的视力 下降。
结核性匐行样脉络膜 炎(SLC)的治疗方案差异很大,因此鉴别诊断极为重要。
尚无确定的治疗方法,主要采用糖皮质激素和免疫抑制剂的长期联合治疗。
高达35%的患者合并脉络膜新生血管 ,影响视力 预后。
匐行性脉络膜炎(serpiginous choroiditis; SC)是一种原因不明的双侧、慢性进行性、复发性炎症性疾病,累及视网膜色素上皮 (RPE )、脉络膜毛细血管层 (choriocapillaris)和脉络膜 1) 。也称为地图状脉络膜 炎或匐行性脉络膜炎。被归类为白点综合征 (white dot syndromes)的一种类型4) 。
在非结核流行地区,这是一种罕见疾病,占后葡萄膜炎 的1.6%5.3%2) 。根据葡萄膜炎 诊疗指南(日眼会志 2019;123(6):635-696),日本眼炎症学会的临床统计显示,它占所有葡萄膜炎 的0.3% 7) 。发病年龄在3050岁,男性略多4) 。尚未确认与全身性疾病有明确关联,但已有与系统性红斑狼疮 、免疫性血小板减少性紫癜、抗磷脂抗体综合征等自身免疫性疾病合并的病例报道3) 。
病变主要位于脉络膜毛细血管层 ;脉络膜毛细血管层 的闭塞性血管炎和继发性内皮细胞损伤导致RPE 、外层视网膜 和脉络膜 萎缩2) 。20%~50%的病例中心视力 受损,随访时间越长,发生率越高2) 。高达25%的眼最终视力 低于20/200。
Q
匐行性脉络膜炎只发生在单眼吗?
A
通常为双侧性,但进展不对称。典型表现为双眼可见不同愈合阶段的病变1) 。单眼发病也有罕见报道。
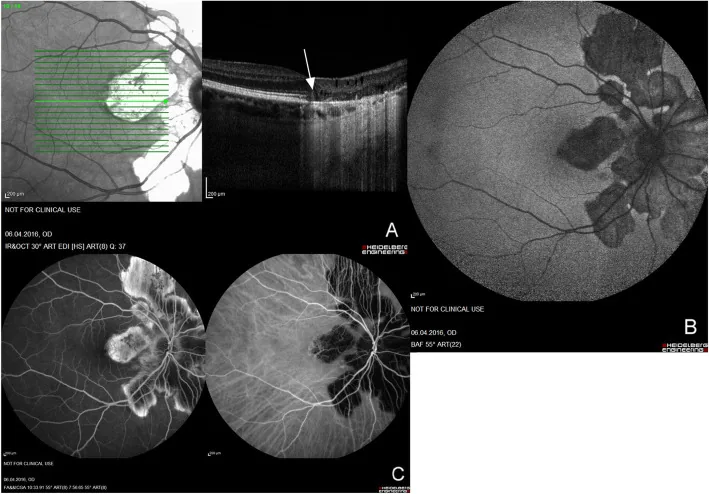
匐行性脉络膜炎的多模态影像。视盘周围可见匐行性脉络膜视网膜病变。 Macedo S, et al. Optical coherence tomography angiography (
OCTA ) findings in Serpiginous Choroiditis. BMC Ophthalmol. 2020. Figure 1. PM
CI D: PMC7325353. License: CC BY.
眼底自发荧光 、荧光素眼底血管造影 和OCT 显示从视盘周围离心性扩展的匍行性脉络膜 视网膜 病变。展示了匍行性脉络膜 炎的典型临床和影像学表现。
匍行性脉络膜 炎的主要自觉症状如下。
视力 下降中心凹 时变得显著。黄斑 型从早期即出现严重视力 下降1) 。旁中心暗点 :患者自觉与活动性病变部位相对应的暗点4) 。视物变形 黄斑部 炎症和萎缩导致物体看起来扭曲。闪光感 闪光感 4) 。无痛性 :炎症局限于后段,因此不伴有疼痛。
匍行性脉络膜 炎的典型眼底所见是从视盘周围离心性匍行扩展的灰黄色脉络膜 视网膜 病变。80%的病例表现为视盘周围型1) 。
活动期
灰黄色视网膜 下病变 :出现在视盘周围或黄斑部 、边界不清的病变。
活动性前缘 :在病变边缘可见匍行进展的活动性区域。
前房 炎症前房 细胞1) 。玻璃体 炎和血管炎通常轻微或缺如。
瘢痕期
脉络膜 视网膜 萎缩斑RPE 和脉络膜 毛细血管板萎缩,可见脉络膜 大血管。伴有色素沉着。
复发性病变 :在现有萎缩斑的边缘或远离部位出现新的活动性病变。
匍行性进展 :反复复发,在后极部出现不规则的萎缩性和色素沉着性病变。病变可能越过血管弓延伸至赤道部。
匍行性脉络膜 炎的亚型包括黄斑部 匍行性脉络膜 炎和安比吉纳型脉络膜 炎。黄斑 型保留视乳头周围区域,从黄斑部 发病,脉络膜新生血管 风险高,视力 预后不良2) 。安比吉纳型脉络膜 炎兼具急性后极部多发性鳞状色素上皮病变(APMPPE )和匍行性脉络膜 炎的特征,表现为后极部散在的多发性鳞状病变4) 。葡萄膜炎 诊疗指南指出,在视神经乳头 附近突然出现大型(相当于视乳头直径至数倍)的黄白色渗出性病变7) 。
复发间隔为3个月至4年不等2) 。活动性病变在数周内消退,但活动性体征可能持续1至9个月2) 。
匍行性脉络膜 炎的确切病因不明,但免疫源性机制被认为是主要原因1) 。对皮质类固醇 和免疫抑制剂的反应,以及报道的与HLA-B7和HLA-A2的关联频率增加支持了这一假说3) 。
提出的病因和相关因素如下:
自身免疫学说 :指出与视网膜 S抗原有关。已报道与HLA-B7、HLA-A2、HLA-B8、HLA-Dw3等遗传易感性相关,但尚未建立一致的相关性3) 。感染性触发因素 :据报道,结核分枝杆菌、梅毒螺旋体、疱疹病毒等感染可能作为免疫学触发因素参与1) 7) 。有些病例在病毒前驱症状后发病。COVID-19感染后发病 :有报道在SARS-CoV-2感染后新发黄斑 型SC的病例1) 。指出感染后炎症细胞因子升高可能诱发自身免疫/自身炎症调节障碍。与消化道疾病的关联 :有报道在溃疡性结肠炎和艰难梭菌感染背景下发病的病例3) 。提示肠道菌群失调可能引发自身免疫反应。
Q
匐行性脉络膜炎会遗传吗?
A
这不是一种明确的遗传性疾病。但已有报道称与HLA-B7等遗传易感性相关,并指出免疫学敏感性可能存在个体差异3) 。
匐行性脉络膜炎的诊断基于特征性眼底表现和多模态成像。排除感染性疾病极为重要。
使用裂隙灯 显微镜和间接检眼镜,可观察到从视盘周围延伸的灰黄色地图状病变和萎缩瘢痕。前房 细胞轻度,玻璃体 炎通常轻微1) 。
检查方法 活动期的特征性表现 FA 早期低荧光、晚期高荧光(渗漏) ICGA 全程低荧光 眼底自发荧光 高自发荧光边缘和低自发荧光晕
荧光素眼底血管造影 (FA )缺损 的高荧光。吲哚青绿血管造影(ICGA ) :活动性病变从早期到晚期均呈低荧光,反映脉络膜 循环障碍1) 4) 。眼底自发荧光 (FAF )1) 。静止期病变呈均匀的低自发荧光。光学相干断层扫描 (OCT )RPE 不规则、外层断裂和视网膜下液 1) 3) 。脉络膜 厚度在急性炎症期增加,消退后变薄1) 。OCT血管成像 (OCTA )脉络膜毛细血管层 显示严重的血流减少区域1) 4) 。对检测脉络膜新生血管 也有用。
排除结核病是首要任务。特别是来自流行地区的患者,必须进行包括干扰素-γ释放试验(IGRA)和结核菌素试验在内的结核病检查5) 。
为排除其他疾病,进行以下检查:
梅毒(酶免疫测定法、FTA-ABS)
弓形虫(IgM和IgG抗体)
疱疹病毒(房水 PCR)
结节病 (ACE、溶菌酶)系统性血管炎(ANCA、抗GBM抗体)
HIV
葡萄膜炎 诊疗指南中列举的鉴别诊断包括白塞病 、结核性脉络膜 炎、疱疹病毒性视网膜 炎、眼弓形虫病 、细菌性眼内炎 、真菌性眼内炎 、梅毒性葡萄膜炎 和眼内淋巴瘤7) 。
需要与匍行性脉络膜 炎鉴别的主要疾病如下。
结核性匍行样脉络膜 炎(SLC) :由于免疫抑制剂可能加重结核,鉴别最为重要。SLC常表现为多发、散在的病灶,多不邻近视 乳头,即使黄斑 受累也倾向于保留中心凹 。常伴有玻璃体 炎5) 。急性后部多灶性鳞状色素上皮病变 (APMPPE )1) 。多灶性脉络膜炎 (MFC)脉络膜 视网膜 病变和玻璃体 炎4) 。弓形虫病 :表现为邻近陈旧瘢痕的活动性病灶,伴有局灶性玻璃体 炎。
Q
与结核性匍行样脉络膜炎的区别是什么?
A
结核性匍行样脉络膜 炎(SLC)表现为多发、散在的病变和玻璃体 炎,倾向于保留中心凹 。匍行性脉络膜 炎从视乳头周围连续扩展,玻璃体 炎轻微。SLC必须进行抗结核治疗,单用免疫抑制剂无法防止复发5) 。
关于匍行性脉络膜 炎的治疗尚无随机对照试验,也没有确立的标准疗法。由于疾病罕见,治疗基于病例积累和专家共识2) 。
使用口服皮质类固醇 或后Tenon囊下注射曲安奈德 (MacuAid)。海外有使用免疫抑制剂的零星报道,但由于疾病反复复发和缓解,客观疗效判定困难,且对复发常无效。
对于活动性病变,高剂量全身性皮质类固醇 是一线治疗1) 2) 。
口服泼尼松龙 :起始剂量40–80 mg/日,逐渐减量7) 。也有报告起始剂量为60–80 mg/日1) 3) 。甲泼尼龙静脉冲击 :可使用1 g/日2) 。地塞米松玻璃体内植入剂 类固醇 副作用,已有有效性报告2) 。
类固醇 减量或停药后预防复发,免疫抑制剂不可或缺3) 。在排除结核后开始使用。
抗代谢药 硫唑嘌呤 (150 mg/日1) )、甲氨蝶呤 、吗替麦考酚酯 7) 。钙调神经磷酸酶抑制剂 :环孢素 A。有报告采用硫唑嘌呤 、环孢素 、泼尼松龙三联疗法,但长期维持缓解困难2) 。烷化剂 :苯丁酸氮芥和环磷酰胺。被认为是治疗匍行性脉络膜 炎最有效且强效的药物类别2) 。生物制剂 NF α药物如阿达木单抗 、英夫利西单抗 。已有阿达木单抗 的有效性报告3) 7) 。结核感染相关病例 :需要抗结核治疗(4药联合2个月 + 2药联合6–12个月)7) 。
专家共识调查显示,匍行性脉络膜 炎的首选免疫抑制剂为甲氨蝶呤 (38.0%)、吗替麦考酚酯 (27.6%)、硫唑嘌呤 (23.1%),生物制剂 中最推荐阿达木单抗 (91.0%)6) 。
在17例接受苯丁酸氮芥治疗的匍行性脉络膜 炎患者中,以白细胞计数3,000–4,500 cells/μL为目标调整剂量,显示出良好的耐受性和预防复发效果2) 。推荐剂量为≤0.2 mg/kg/日,总剂量≤2.2 g。
Maleki等人的4例系列报告中,对苯丁酸氮芥联合全身性类固醇 治疗抵抗的难治性病例,加用地塞米松玻璃体内植入剂 后停用类固醇 并继续苯丁酸氮芥治疗,实现了≥48个月的缓解2) 。治疗成功的关键是将白细胞计数稳定在毒性水平(3,000–4,500 cells/μL)。
脉络膜新生血管 (CNV )合并率高达35%。采用抗VEGF药物 (贝伐珠单抗 、雷珠单抗 )玻璃体内注射 治疗2) 。黄斑 型SC的CNV 发病风险尤其高2) 。
免疫抑制剂可能加重结核病。治疗开始前必须明确排除结核。
苯丁酸氮芥的副作用包括骨髓抑制、淋巴瘤和白血病风险,需要每周进行血液检查2) 。
长期全身使用类固醇 期间,苯丁酸氮芥对白细胞计数的控制容易变得不稳定2) 。
Q
匍行性脉络膜炎能治好吗?
A
有报道称部分患者使用烷化剂后获得长期缓解(“治愈”)2) 。但该病多为复发与缓解交替的慢性疾病,需要长期免疫抑制治疗 和随访。
匍行性脉络膜 炎的核心病理是脉络膜毛细血管层 的闭塞性血管炎2) 。组织学上,脉络膜 可见淋巴细胞浸润,血管周围偶见淋巴细胞聚集2) 3) 。未见肉芽肿形成3) 。
病理生理过程理解如下:
脉络膜 毛细血管闭塞脉络膜 毛细血管闭塞,引起局部缺血。OCTA 显示为血流减少区域1) 4) 。RPE 和外层视网膜 损伤脉络膜 毛细血管缺血,RPE 和外层视网膜 发生变性和萎缩4) 。炎症的扩散与扩大 :病变从活动性病灶边缘呈匍行性扩展。复发发生在现有萎缩斑边缘或远处部位。脉络膜 厚度波动脉络膜 厚度增加,炎症消退后变薄。一例病例中,初诊时342 μm,1个月后378 μm,4个月后233 μm1) 。
匐行性脉络膜炎的病理组织学上与鸟枪弹样脉络膜视网膜病变 (birdshot chorioretinopathy)相似2) 。两种疾病均以淋巴细胞为主的脉络膜 浸润为特征,被认为具有共同的免疫介导机制。
在合并溃疡性结肠炎的病例中,T细胞主导的炎症被认为是共同的病理基础3) 。推测肠黏膜自身抗体可能与脉络膜 抗原发生交叉反应,肠道菌群变化可能破坏调节性T细胞和效应T细胞之间的平衡3) 。
有报告称一例患者在COVID-19感染后1个月发生黄斑 型匐行性脉络膜炎1) 。观察到脉络膜 内高反射灶,推测为活化的小胶质细胞或受损的RPE 细胞聚集。提示SARS-CoV-2可能在易感宿主中作为炎症触发因素,诱发自身免疫调节障碍。
已有多个报告称COVID-19感染后发生或复发匐行性脉络膜炎和匐行性脉络膜炎(ampiginous choroiditis)的病例1) 。
有报告称一例患者在COVID-19感染后1个月出现匐行性脉络膜炎复发1) 。此外,两名20多岁的患者在COVID-19感染约1周后发生双侧匐行性脉络膜炎。这些发现提示SARS-CoV-2可能成为脉络膜 炎症的触发因素,但尚未证明因果关系。
Maleki等人(2021年)研究了4例对苯丁酸氮芥和类固醇 标准联合治疗耐药的病例,报告称加用地塞米松玻璃体内植入剂 或英夫利西单抗 并停用类固醇 后,苯丁酸氮芥的白细胞控制稳定,并获得了长期缓解2) 。他们提出全身性类固醇 会减弱苯丁酸氮芥效果的假说,认为转换为局部类固醇 可能是治疗成功的关键。
抗TNF α抗体阿达木单抗 正在被研究作为匐行性脉络膜炎的类固醇 减量疗法。
在一例合并溃疡性结肠炎的匐行性脉络膜炎患者中,引入阿达木单抗 后,匐行性脉络膜炎和溃疡性结肠炎均维持缓解达5个月3) 。然而,也有报告称在使用阿达木单抗 期间疾病进展,因此其有效性尚未确定。
Seddigh S, Pinto A, Zaki AM, Gupta RR. Serpiginous choroiditis after COVID-19 infection. J Vitreoretinal Dis. 2025;9(2):246-252.
Maleki A, Maldonado Cerda A, Garcia CM, et al. Chlorambucil combination therapy in refractory serpiginous choroiditis: a cure? Am J Ophthalmol Case Rep. 2021;21:101014.
Pollmann AS, Mishra AV, Betsch DM, Francisconi CLM. Serpiginous choroiditis presenting in association with Clostridium difficile infection and ulcerative colitis. J Vitreoretinal Dis. 2021;5(2):177-181.
Testi I, Vermeirsch S, Pavesio C. Multimodal imaging in white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
Agrawal R, Gunasekeran DV, Grant R, et al. Consensus on the management of tubercular uveitis: Collaborative Ocular Tuberculosis Study (COTS) group. Ophthalmology. 2021;128:266-276.
Niederer RL, Al-Janabi A, Engelbrecht C, et al. Immunomodulatory therapy prescribing practices for non-infectious uveitis: a survey of international experts. Br J Ophthalmol. 2024;108:482-489.
日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(「16. 地図状脈絡膜炎」節). 日本眼科学会雑誌. 2019;123(6):635-696.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。