活動期
灰黃色視網膜下病變:出現在視神經盤周圍或黃斑部、邊界不清的病變。
活動性前緣:在病變邊緣可見蛇行進展的活動性區域。
前房發炎:可能伴隨輕度前房細胞1)。玻璃體炎與血管炎通常輕微或缺如。

蛇行狀脈絡膜炎(serpiginous choroiditis; SC)是一種原因不明的雙側性、慢性進行性、復發性發炎性疾病,侵犯視網膜色素上皮(RPE)、脈絡膜微血管板(choriocapillaris)及脈絡膜1)。也稱為地圖狀脈絡膜炎或匐行性脈絡膜炎。被歸類為白點症候群(white dot syndromes)的一種類型4)。
在非結核流行地區,這是一種罕見疾病,佔後葡萄膜炎的1.6%5.3%2)。根據葡萄膜炎診療指引(日眼會誌 2019;123(6):635-696),日本眼發炎學會的臨床統計顯示,它佔所有葡萄膜炎的0.3%7)。發病年齡在3050歲,男性略多4)。尚未確認與全身性疾病有明確關聯,但已有與全身性紅斑性狼瘡、免疫性血小板減少性紫斑病、抗磷脂抗體症候群等自體免疫疾病合併的病例報告3)。
病變主要位於脈絡膜微血管板;脈絡膜微血管板的阻塞性血管炎及繼發性內皮細胞損傷導致RPE、外層視網膜及脈絡膜萎縮2)。20%~50%的病例中心視力受損,追蹤時間越長,發生率越高2)。高達25%的眼睛最終視力低於20/200。
通常為雙側性,但進展不對稱。典型表現為雙眼可見不同癒合階段的病變1)。單眼發病也有罕見報告。
蛇行狀脈絡膜炎的主要自覺症狀如下。
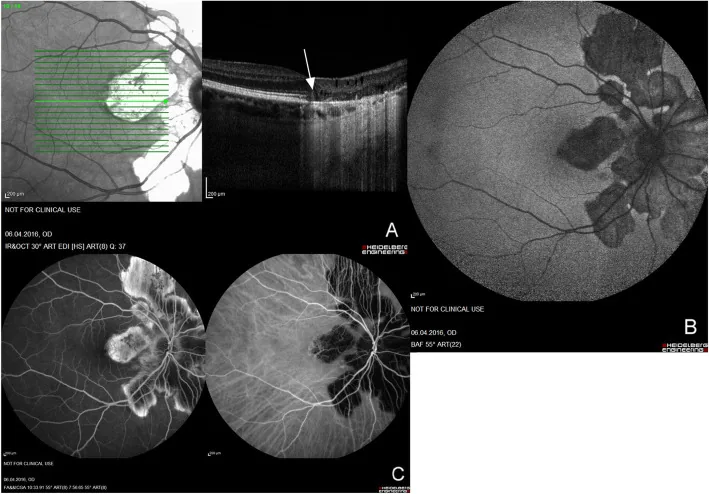
蛇行狀脈絡膜炎的典型眼底所見是從視神經盤周圍離心性蛇行狀擴展的灰黃色脈絡膜視網膜病變。80%的病例呈現視神經盤周圍型1)。
活動期
灰黃色視網膜下病變:出現在視神經盤周圍或黃斑部、邊界不清的病變。
活動性前緣:在病變邊緣可見蛇行進展的活動性區域。
前房發炎:可能伴隨輕度前房細胞1)。玻璃體炎與血管炎通常輕微或缺如。
瘢痕期
脈絡膜視網膜萎縮斑:由於RPE和脈絡膜微血管板萎縮,可透見脈絡膜大血管。伴有色素沉著。
復發性病變:在現有萎縮斑的邊緣或遠離部位出現新的活動性病變。
匐行性進展:反覆復發,在後極部出現不規則的萎縮性和色素沉著性病變。病變可能越過血管弓延伸至赤道部。
匐行性脈絡膜炎的亞型包括黃斑部匐行性脈絡膜炎和安比吉納型脈絡膜炎。黃斑型保留視乳頭周圍區域,從黃斑部發病,脈絡膜新生血管風險高,視力預後不良2)。安比吉納型脈絡膜炎兼具急性後極部多發性鱗狀色素上皮病變(APMPPE)和匐行性脈絡膜炎的特徵,表現為後極部散在的多發性鱗狀病變4)。葡萄膜炎診療指南指出,在視神經乳頭附近突然出現大型(相當於視乳頭直徑至數倍)的黃白色滲出性病變7)。
復發間隔為3個月至4年不等2)。活動性病變在數週內消退,但活動性徵象可能持續1至9個月2)。
匐行性脈絡膜炎的確切病因不明,但免疫源性機制被認為是主要原因1)。對皮質類固醇和免疫抑制劑的反應,以及報導的與HLA-B7和HLA-A2的關聯頻率增加支持了這一假說3)。
提出的病因和相關因素如下:
這不是一種明確的遺傳性疾病。但已有報導稱與HLA-B7等遺傳易感性相關,並指出免疫學敏感性可能存在個體差異3)。
匐行性脈絡膜炎的診斷基於特徵性眼底表現和多模態成像。排除感染性疾病極為重要。
使用裂隙燈顯微鏡和間接檢眼鏡,可觀察到從視盤周圍延伸的灰黃色地圖狀病變和萎縮疤痕。前房細胞輕度,玻璃體炎通常輕微1)。
| 檢查方法 | 活動期的特徵性表現 |
|---|---|
| FA | 早期低螢光、晚期高螢光(滲漏) |
| ICGA | 全程低螢光 |
| 眼底自體螢光 | 高自體螢光邊緣與低自體螢光暈 |
排除結核病是首要任務。特別是來自流行地區的患者,必須進行包括干擾素-γ釋放試驗(IGRA)和結核菌素試驗在內的結核病檢查5)。
為排除其他疾病,進行以下檢查:
葡萄膜炎診療指引中列出的鑑別診斷包括貝西氏症、結核性脈絡膜炎、疱疹病毒視網膜炎、眼弓形蟲症、細菌性眼內炎、真菌性眼內炎、梅毒性葡萄膜炎和眼內淋巴瘤7)。
需要與蛇行狀脈絡膜炎鑑別的主要疾病如下。
結核性蛇行樣脈絡膜炎(SLC)表現為多發、散在病變和玻璃體炎,傾向於保留中心凹。蛇行狀脈絡膜炎從視神經盤周圍連續擴展,玻璃體炎輕微。SLC必須進行抗結核治療,單用免疫抑制劑無法防止復發5)。
關於蛇行狀脈絡膜炎的治療尚無隨機對照試驗,也沒有確立的標準療法。由於疾病罕見,治療基於病例累積和專家共識2)。
使用口服皮質類固醇或後Tenon囊下注射曲安奈德(MacuAid)。海外有使用免疫抑制劑的零星報告,但由於疾病反覆復發和緩解,客觀療效判定困難,且對復發常無效。
對於活動性病變,高劑量全身性皮質類固醇是第一線治療1)2)。
類固醇減量或停藥後預防復發,免疫抑制劑不可或缺3)。在排除結核後開始使用。
專家共識調查顯示,匍行性脈絡膜炎的首選免疫抑制劑為甲氨蝶呤(38.0%)、嗎替麥考酚酯(27.6%)、硫唑嘌呤(23.1%),生物製劑中最推薦阿達木單抗(91.0%)6)。
在17例接受苯丁酸氮芥治療的匍行性脈絡膜炎患者中,以白血球計數3,000–4,500 cells/μL為目標調整劑量,顯示出良好的耐受性和預防復發效果2)。推薦劑量為≤0.2 mg/kg/日,總劑量≤2.2 g。
Maleki等人的4例系列報告中,對苯丁酸氮芥聯合全身性類固醇治療抵抗的難治性病例,加用地塞米松玻璃體內植入劑後停用類固醇並繼續苯丁酸氮芥治療,實現了≥48個月的緩解2)。治療成功的關鍵是將白血球計數穩定在毒性水平(3,000–4,500 cells/μL)。
脈絡膜新生血管(CNV)合併率高達35%。採用抗VEGF藥物(貝伐珠單抗、雷珠單抗)玻璃體內注射治療2)。黃斑型SC的CNV發病風險尤其高2)。
有報導稱部分患者使用烷化劑後獲得長期緩解(「治癒」)2)。但該病多為復發與緩解交替的慢性疾病,需要長期免疫抑制治療和追蹤。
匍行性脈絡膜炎的核心病理是脈絡膜毛細血管層的閉塞性血管炎2)。組織學上,脈絡膜可見淋巴球浸潤,血管周圍偶見淋巴球聚集2)3)。未見肉芽腫形成3)。
病理生理過程理解如下:
蛇行狀脈絡膜炎的病理組織學上與鳥槍彈樣脈絡膜視網膜病變(birdshot chorioretinopathy)相似2)。兩種疾病均以淋巴球為主的脈絡膜浸潤為特徵,被認為具有共同的免疫媒介機制。
在合併潰瘍性結腸炎的病例中,T細胞主導的炎症被認為是共同的病理基礎3)。推測腸黏膜自體抗體可能與脈絡膜抗原發生交叉反應,腸道菌叢變化可能破壞調節性T細胞和效應T細胞之間的平衡3)。
有報告稱一例患者在COVID-19感染後1個月發生黃斑型蛇行狀脈絡膜炎1)。觀察到脈絡膜內高反射灶,推測為活化的小膠質細胞或受損的RPE細胞聚集。提示SARS-CoV-2可能在易感宿主中作為炎症觸發因素,誘發自體免疫調節障礙。
已有數個報告稱COVID-19感染後發生或復發蛇行狀脈絡膜炎和安比吉納斯脈絡膜炎(ampiginous choroiditis)的病例1)。
有報告稱一例患者在COVID-19感染後1個月出現蛇行狀脈絡膜炎復發1)。此外,兩名20多歲的患者在COVID-19感染約1週後發生雙側安比吉納斯脈絡膜炎。這些發現提示SARS-CoV-2可能成為脈絡膜炎症的觸發因素,但尚未證明因果關係。
Maleki等人(2021年)研究了4例對苯丁酸氮芥和類固醇標準合併治療耐藥的病例,報告稱加用地塞米松玻璃體內植入劑或英夫利西單抗並停用類固醇後,苯丁酸氮芥的白血球控制穩定,並獲得了長期緩解2)。他們提出全身性類固醇會減弱苯丁酸氮芥效果的假說,認為轉換為局部類固醇可能是治療成功的關鍵。
抗TNFα抗體阿達木單抗正在被研究作為蛇行狀脈絡膜炎的類固醇減量療法。
在一例合併潰瘍性結腸炎的蛇行狀脈絡膜炎患者中,引入阿達木單抗後,蛇行狀脈絡膜炎和潰瘍性結腸炎均維持緩解達5個月3)。然而,也有報告稱在使用阿達木單抗期間疾病進展,因此其有效性尚未確定。