急性後部多發性斑狀色素上皮病變(APMPPE)是一種急性炎症性疾病,特徵為雙眼後極部視網膜色素上皮 層出現多發性盤狀白斑。
好發於20~30歲(平均25歲),無性別差異。可能出現前驅感冒樣症狀。
螢光眼底血管攝影 (FA )中的「螢光逆轉現象」(早期低螢光→晚期高螢光)是診斷特徵。白斑通常在7~12天內消退,留下脫色素,有很強的自然緩解傾向,視力 預後良好。
罕見情況下可合併腦血管炎(中樞神經血管炎),出現神經症狀時需緊急檢查。
重症病例(轉變為地圖狀脈絡膜 炎者)視力 預後可能不良。
OCT -A評估脈絡膜 微血管血流缺失對活動性評估有用。 急性後部多發性鱗狀色素上皮病變(acute posterior multifocal placoid pigment epitheliopathy; APMPPE)是1968年Gass首次報告的一種雙眼急性炎症性疾病10) 。其特徵為雙眼眼底後極部出現視網膜 深層至視網膜色素上皮 (RPE )層次的盤狀白斑。
根據葡萄膜炎 診療指引(日眼會誌 2019;123(6):635-696)的分類,它被歸類為非感染性、以眼底病變為主的後部葡萄膜炎 ,具有雙眼性、急性發作、一過性病程的臨床特點1) 。
發病機轉被認為是脈絡膜 微血管板輸入小動脈發生的遲發型過敏反應(IV型過敏)導致的閉塞性血管炎。病毒感染(流感、腮腺炎等)被懷疑為誘因,但詳細情況不明。
好發年齡為20~30歲(平均25歲),無性別差異1) 。多為雙眼發病。半數以上病例報告有前驅感冒樣症狀1) 。罕見情況下曾有與全身性血管炎、腎病、腦膜腦炎、甲狀腺炎的關聯報告1) 。
Q
APMPPE只發生在年輕人身上嗎?
A
好發年齡為40歲以下的年輕成人,老年人和兒童發病罕見。如果在40歲以後發現類似病變,需要與匐行性脈絡膜炎 (地圖狀脈絡膜 炎)鑑別。
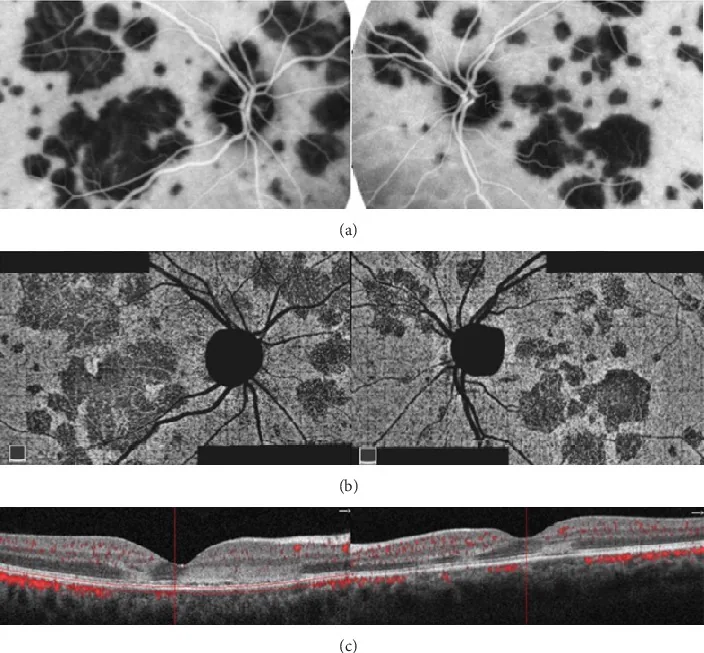
APMPPE的多模態影像。ICGA、OCTA和OCT顯示雙眼後極部多發斑片狀病變。 Oliveira MA, et al. Management of Acute Posterior Multifocal Placoid Pigment Epitheliopathy (APMPPE): Insights from Multimodal Imaging with
OCTA . Case Rep Ophthalmol Med. 2020. Figure 5. PM
CI D: PMC7094199. License: CC BY.
雙眼後極部可見多發地圖狀、斑片狀病變,
ICGA 呈低螢光,
OCTA 顯示相應
脈絡膜 毛細血管層血流減少區域。
OCT 顯示從外叢狀層到
RPE 的高反射改變,為APMPPE的典型表現。
主要表現為輕度視力 下降、中心暗點 、視物變形和小視症。
可伴有閃光感和旁中心暗點 1) 。
通常無眼前段炎症(眼痛 、充血 )。
雙眼後極部視網膜 深層至RPE 水平出現多發灰白色(奶油色至白色)盤狀白斑。病灶邊界清晰,大小約1/4至1/2視盤直徑,基本均勻,數量從數個到多個,融合和擴大趨勢不明顯。可伴有輕度視盤充血 水腫和輕度玻璃體 細胞1) 。與多發性一過性白點症候群 (MEWDS )的白斑相比,APMPPE的白斑較大,這是鑑別要點。
急性期所見
眼底白斑 :後極部邊界清晰的1/4至1/2視盤直徑的灰白色盤狀白斑多發。由脈絡膜 毛細血管閉塞導致RPE 和視網膜 外層缺血性水腫混濁。
視網膜 外層損傷OCT 顯示橢圓體帶(IS/OS線)高反射紊亂1) 。橢圓體帶的破壞引起自覺症狀2) 。
FAF (眼底自發螢光)OCT 與自發螢光所見密切相關9) 。
緩解期所見
白斑消退 :白斑在7至12天內從中心開始消退,消失後殘留輕度色素脫失改變。
OCT 恢復感光細胞 層變薄1) 。
脈絡膜 視網膜 萎縮脈絡膜 視網膜 萎縮斑1) 。
Q
APMPPE的白斑會消失嗎?
A
多數情況下,白斑在發病後7~12天消退,留下脫色素後消失。視力 預後通常良好,復發罕見。但轉變為地圖狀脈絡膜 炎(匐行性脈絡膜炎 )的病例可能出現進展,因此需要定期追蹤。
推測本質是脈絡膜 微血管板輸入小動脈的延遲型過敏反應(IV型過敏)導致的閉塞性血管炎。OCT血管攝影 (OCT -A)在急性期病變區域顯示脈絡膜微血管層 級的血流訊號缺失(flow void),支持脈絡膜 微血管缺血是病理核心的觀點3) 。Klufas等人報告,在三種斑狀脈絡膜 視網膜 炎(APMPPE、PPM 、RPC )中,OCT -A檢測脈絡膜 微血管血流訊號缺失與FA 和ICGA 具有高度一致性4) 。
部分病例在類流感症狀(流感、腮腺炎等)、上呼吸道感染或疫苗接種後發病。
已有報告與全身性血管炎(腦血管炎)、腎病、結節性多動脈炎 、甲狀腺炎相關1) 。
如果感冒症狀後出現突然的視力 下降或中心暗點 ,請立即就診眼科。
APMPPE尚無確定的預防方法。
Q
APMPPE有中風風險嗎?
A
雖然罕見,但有報告指出APMPPE合併中樞神經系統血管炎的病例。若出現神經症狀(劇烈頭痛、意識改變、癱瘓),需緊急進行腦部MRI/MRA檢查,並與神經內科協作處理。
APMPPE的診斷基於特徵性眼底表現和螢光血管造影(FA /ICGA )結果。多模態成像可對病理進行多方面的評估2) 。
檢查方法 特徵性表現 FA (螢光素 眼底血管造影)急性期:早期低螢光→晚期高螢光(「螢光逆轉現象」)1) ICGA (吲哚青綠血管造影)從早期到晚期持續低螢光。慢性期:縮小、邊界模糊5) SD-OCT 急性期:橢圓體帶高反射紊亂。緩解期:感光細胞 層變薄1) OCT -A脈絡膜 毛細血管層的血流缺失。與FA /ICGA 高度一致4) FAF (眼底自發螢光)急性期:病灶低自發螢光或高自發螢光。與OCT 表現相關9) 多焦視網膜電圖 急性期黃斑部 附近振幅明顯平坦化
FA 中出現的早期低螢光→晚期高螢光,即「螢光逆轉現象」,是APMPPE最具特徵性的表現。其解釋為:早期由於閉塞性血管炎,脈絡膜 毛細血管板的染料流入受阻;晚期周圍滲出導致高螢光1) 。ICGA 從早期到晚期始終顯示低螢光,更直接反映脈絡膜 毛細血管板缺血5) 。
OCT -A是一種非侵入性影像工具,可評估APMPPE中脈絡膜 毛細血管的血流障礙。Furino等人報告,在急性APMPPE病變中,OCT -A檢測脈絡膜 毛細血管血流空區與FA 和ICGA 具有高度一致性8) 。恢復期觀察到血流空區縮小伴隨視功能改善,因此可作為活動性監測的生物標誌物 。
地圖狀(匐行性)脈絡膜 炎 :40多歲、單眼、進行性擴大、地圖狀、預後不良1) Vogt-小柳-原田病 滲出性視網膜剝離 、多發性視網膜 下滲漏點1) 多發性消失性白點症候群 (MEWDS ) :年輕女性、範圍廣泛至赤道部、FA 早期高螢光1) 持續性斑狀黃斑 病變(PPM )/ relentless placoid chorioretinitis(RPC ) :與APMPPE類似,存在在「placoid chorioretinitis spectrum」內重新分類的討論4) 7)
Q
APMPPE和MEWDS如何區分?
A
病變大小、FA 表現和雙眼性三點是鑑別關鍵。APMPPE的白斑比MEWDS 大(1/4至1/2視盤直徑),多為雙眼性,FA 顯示早期低螢光→晚期高螢光的逆轉現象。MEWDS 多為單眼,白斑小而廣泛,FA 早期即顯示高螢光1) 。
有很強的自然緩解傾向,許多病例無需特殊治療即可自然恢復1) 。輕症病例以觀察為基本原則。Jones(1995)的長期追蹤報告也顯示,許多病例最終恢復了良好視力 10) 。
當視力 下降顯著、合併視乳頭炎或黃斑 附近有病變時,考慮以下治療。
普賴鬆錠 (5 mg):從30 mg/日開始,在2週至1個月內逐漸減量卡那克林錠 (卡利定原酶25~50單位):每次1錠,每日3次(作為脈絡膜 微循環改善藥合併使用)
對於進展為匐行性脈絡膜 病變或合併中樞神經系統血管炎的病例,考慮類固醇脈衝療法 (大劑量甲基普賴鬆龍靜脈注射)或免疫抑制劑1) 。如果發生脈絡膜新生血管 (CNV ),考慮玻璃體內注射 抗VEGF藥物 ,但這是罕見的併發症。對於進展為持續性斑塊狀黃斑 病變(PPM )的病例,如Kolomeyer和Brucker在其系統性回顧中指出的,可能需要長期管理7) 。
Q
類固醇治療是必須的嗎?
A
輕症病例僅透過觀察即可自然恢復。當視力 下降顯著、視乳頭附近發炎嚴重或伴有中樞神經系統症狀時,考慮類固醇 治療。葡萄膜炎 診療指引也指出「無需特殊治療即可自然恢復」是基本方針1) 。
APMPPE的病理被理解為以脈絡膜 微血管板閉塞為中心的缺血性變化。
推測其本質是發生在脈絡膜 微血管板輸入小動脈的延遲型過敏反應(IV型過敏)導致的閉塞性血管炎。閉塞 → RPE 和視網膜 外層缺血性變化(水腫、混濁)→ 形成盤狀白斑。Mrejen等人顯示脈絡膜 病變可延伸至更深層,提示可能不僅累及脈絡膜 微血管板,還累及中、大血管層級3) 。
在OCT -A上,觀察到內層脈絡膜 層級的血流空區,與APMPPE類似,在「斑塊狀病變譜系」(包括持續性斑塊狀黃斑 病變和頑固性斑塊狀脈絡膜 視網膜 炎)這一疾病組的病理基礎上,一致發現脈絡膜 毛細血管缺血4) 。Klufas等人報告稱,三種疾病在OCT -A上的脈絡膜 毛細血管血流空區呈現共同模式,支持了斑塊狀脈絡膜 視網膜 炎譜系的概念。
螢光逆轉現象的機制:造影早期,由於染料流入脈絡膜 毛細血管受阻,呈現低螢光;晚期,染料從周圍正常組織滲出,轉為高螢光。ICGA 始終顯示低螢光,也反映了脈絡膜 毛細血管的閉塞性變化5) 。FAF 可以非侵入性評估RPE 損傷的分佈,並與OCT 表現高度對應9) 。
COVID-19感染/疫苗後的APMPPE :有報告稱感染後出現急性APMPPE樣病變,病毒誘發的免疫反應與其關係受到關注。合併中樞神經血管炎 :對於伴有神經症狀的病例,腦部MRI/MRA的推薦力度增強。已有數個APMPPE合併腦中風或腦血管炎的病例報告,表明不僅眼部症狀,全身性監測也很重要6) 。多模態影像的進步 :通過OCT -A監測脈絡膜 毛細血管血流空區可能成為活動性評估的生物標誌物 8) 。由於其非侵入性且可重複進行,正成為補充FA 和ICGA 的重要檢查手段。疾病類型重新分類 :包括持續性斑塊狀黃斑 病變和頑固性斑塊狀脈絡膜 視網膜 炎在內的「斑塊狀脈絡膜 視網膜 炎譜系」的整體理解正在推進4) 。Mirza和Jampol(2012)整理了頑固性斑塊狀脈絡膜 視網膜 炎作為獨立疾病概念的特徵,並討論了其與APMPPE的連續性6) 。
日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(「13. 急性後部多発性斑状色素上皮症」節). 日本眼科学会雑誌. 2019;123(6):635-696.
Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
Mrejen S, Sarraf D, Chexal S, et al. Choroidal involvement in acute posterior multifocal placoid pigment epitheliopathy. Ophthalmic Surg Lasers Imaging Retina. 2016;47:20-26.
Klufas MA, Phasukkijwatana N, Iafe NA, et al. Optical coherence tomography angiography reveals choriocapillaris flow reduction in placoid chorioretinitis. Ophthalmol Retina. 2017;1(1):77-91.
Park D, Schatz H, McDonald HR, Johnson RN. Indocyanine green angiography of acute multifocal posterior placoid pigment epitheliopathy. Ophthalmology. 1995;102:1877-1883.
Mirza RG, Jampol LM. Relentless placoid chorioretinitis. Int Ophthalmol Clin. 2012;52(4):237-242.
Kolomeyer AM, Brucker AJ. Persistent placoid maculopathy: a systematic review. Retina. 2018;38(10):1881-1895.
Furino C, Shalchi Z, Grassi MO, et al. Optical coherence tomography angiography in acute posterior multifocal placoid pigment epitheliopathy. Ophthalmic Surg Lasers Imaging Retina. 2019;50(7):428-436.
Souka AA, Hillenkamp J, Gora F, Gabel VP, Framme C. Correlation between optical coherence tomography and autofluorescence in acute posterior multifocal placoid pigment epitheliopathy. Graefes Arch Clin Exp Ophthalmol. 2006;244(10):1219-1223.
Jones NP. Acute posterior multifocal placoid pigment epitheliopathy. Br J Ophthalmol. 1995;79:384-389.
開啟下方的 AI 助手,並將複製的內容貼到聊天欄。