โรคเยื่อบุผิวเม็ดสีจอประสาทตา อักเสบเฉียบพลันแบบหลายจุดที่ขั้วหลัง (APMPPE ) เป็นโรคอักเสบเฉียบพลันที่มีจุดขาวรูปจานหลายจุดในระดับเยื่อบุผิวเม็ดสีจอประสาทตา ที่ขั้วหลังของตาทั้งสองข้าง
มักเกิดในช่วงอายุ 20-30 ปี (เฉลี่ย 25 ปี) ไม่มีความแตกต่างทางเพศ อาจมีอาการคล้ายไข้หวัดนำมาก่อน
ปรากฏการณ์ ‘การกลับกันของการเรืองแสง’ (การเรืองแสงน้อยในระยะแรก → การเรืองแสงมากในระยะหลัง) ในการตรวจหลอดเลือดด้วยฟลูออเรสซีน (FA ) เป็นลักษณะเฉพาะในการวินิจฉัย
รอยโรคสีขาวมักจะหายไปภายใน 7-12 วัน เหลือรอยด่างจาง มีแนวโน้มที่จะดีขึ้นเองและพยากรณ์โรคทางสายตาดี
พบน้อยมากที่จะเกิดร่วมกับหลอดเลือดสมองอักเสบ (หลอดเลือดระบบประสาทส่วนกลางอักเสบ) เมื่อมีอาการทางระบบประสาทต้องตรวจสอบอย่างเร่งด่วน
ในกรณีรุนแรง (เปลี่ยนเป็นคอรอยด์ อักเสบแบบแผนที่) อาจทำให้พยากรณ์โรคทางสายตาไม่ดี
การประเมินช่องว่างการไหลของคอริโอแคปิลลาริสด้วย OCT -A มีประโยชน์ในการประเมินการดำเนินโรค
โรค Acute posterior multifocal placoid pigment epitheliopathy (APMPPE ) เป็นโรคอักเสบเฉียบพลันของตาทั้งสองข้างที่รายงานครั้งแรกโดย Gass ในปี 1968 10) มีลักษณะเฉพาะคือมีรอยโรคสีขาวรูปจานหลายจุดในชั้นลึกของจอประสาทตา จนถึงระดับเยื่อบุผิวรงควัตถุจอประสาทตา (RPE ) ที่ขั้วหลังของตาทั้งสองข้าง
ในการจำแนกประเภทตามแนวทางการรักษาม่านตาอักเสบ (วารสารจักษุวิทยาญี่ปุ่น 2019;123(6):635-696) จัดเป็นม่านตาอักเสบ ส่วนหลังชนิดไม่ติดเชื้อที่เกิดจากรอยโรคที่จอประสาทตา เป็นหลัก โดยมีลักษณะทางคลินิกคือเป็นทั้งสองข้าง เริ่มต้นเฉียบพลัน และดำเนินโรคชั่วคราว 1)
กลไกการเกิดโรคสันนิษฐานว่าเป็นหลอดเลือดอักเสบชนิดอุดตันจากปฏิกิริยาภูมิไวเกินชนิด delayed-type (ภูมิแพ้ชนิดที่ 4) ที่เกิดขึ้นในหลอดเลือดแดงอาร์เทอริโอลนำเข้าของชั้นคอริโอแคปิลลาริส การติดเชื้อไวรัส (ไข้หวัดใหญ่ คางทูม ฯลฯ) สงสัยว่าเป็นปัจจัยกระตุ้น แต่รายละเอียดยังไม่ทราบแน่ชัด
อายุที่พบบ่อยคือ 20-30 ปี (เฉลี่ย 25 ปี) ไม่มีความแตกต่างทางเพศ 1) มักเป็นทั้งสองข้าง มีรายงานอาการคล้ายไข้หวัดนำมาก่อนในมากกว่าครึ่งหนึ่งของกรณี 1) พบน้อยมากที่มีรายงานความสัมพันธ์กับหลอดเลือดอักเสบทั่วร่างกาย โรคไต เยื่อหุ้มสมองและสมองอักเสบ และต่อมไทรอยด์อักเสบ 1)
Q
APMPPE เกิดเฉพาะในคนหนุ่มสาวหรือไม่?
A
อายุที่พบบ่อยคือผู้ใหญ่ตอนต้นอายุต่ำกว่า 40 ปี พบน้อยในผู้สูงอายุหรือเด็ก หากพบรอยโรคคล้ายกันหลังจากอายุ 40 ปี สิ่งสำคัญคือต้องแยกจากคอรอยด์ อักเสบแบบเซอร์พิจิโนซา (คอรอยด์ อักเสบแบบแผนที่)
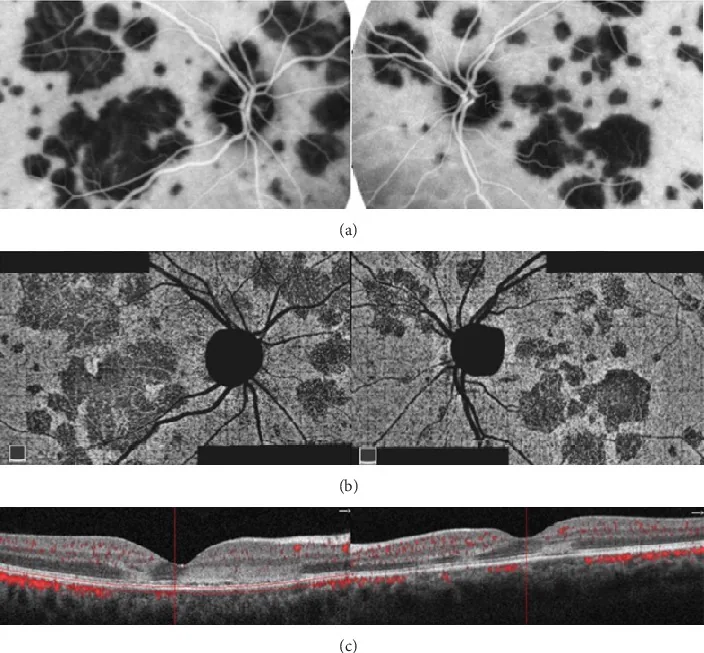
ภาพ multimodal ของ APMPPE รอยโรคแบบจุดหลายจุดที่ขั้วหลังของตาทั้งสองข้างแสดงใน ICGA, OCTA และ OCT Oliveira MA, et al. Management of Acute Posterior Multifocal Placoid Pigment Epitheliopathy (
APMPPE ): Insights from Multimodal Imaging with
OCTA . Case Rep Ophthalmol Med. 2020. Figure 5. PM
CI D: PMC7094199. License: CC BY.
พบรอยโรคแบบแผนที่และจุดหลายจุดที่ขั้วหลังของตาทั้งสองข้าง ซึ่งแสดงเป็นบริเวณเรืองแสงต่ำใน
ICGA และเป็นบริเวณที่การไหลเวียนเลือดในหลอดเลือดฝอย
คอรอยด์ ลดลงใน
OCTA ใน
OCT พบการเปลี่ยนแปลงการสะท้อนแสงสูงจากชั้น plexiform ชั้นนอกถึง
RPE ซึ่งเป็นลักษณะเฉพาะของ
APMPPE
การมองเห็น ลดลงเล็กน้อย จุดบอดกลาง (central scotoma) การเห็นภาพบิดเบี้ยว (metamorphopsia) และการเห็นภาพเล็กลง (micropsia) เป็นอาการหลักอาจมีอาการเห็นแสงวาบ (photopsia) และจุดบอดข้างศูนย์กลาง (paracentral scotoma) ร่วมด้วย1)
โดยปกติจะไม่พบการอักเสบของส่วนหน้าของตา (ปวดตา , ตาแดง )
พบจุดขาวรูปจานสีเทาขาว (สีครีมถึงขาว) หลายจุดในชั้นลึกของจอตาจนถึงระดับ RPE ที่ขั้วหลังของตาทั้งสองข้าง รอยโรคมีขอบเขตชัดเจน ขนาด 1/4 ถึง 1/2 เท่าของเส้นผ่านศูนย์กลางหัวประสาทตา เกือบสม่ำเสมอ ปรากฏจำนวนตั้งแต่ไม่กี่จุดถึงหลายจุด มีแนวโน้มน้อยที่จะรวมตัวหรือขยายใหญ่ อาจพบหัวประสาทตาแดง และบวมเล็กน้อย และเซลล์ในวุ้นตา เล็กน้อย1) จุดเหล่านี้มีขนาดใหญ่กว่าจุดใน MEWDS ซึ่งเป็นจุดที่ใช้แยกโรค
ลักษณะในระยะเฉียบพลัน
จุดขาวในจอตา : จุดขาวรูปจานหลายจุด ขอบเขตชัดเจน ขนาด 1/4 ถึง 1/2 เท่าของเส้นผ่านศูนย์กลางหัวประสาทตา ที่ขั้วหลัง เกิดจากอาการบวมน้ำจากการขาดเลือดและความขุ่นของ RPE และจอตาชั้นนอกเนื่องจากการอุดตันของหลอดเลือดฝอยคอรอยด์
ความผิดปกติของจอตาชั้นนอก : OCT แสดงการรบกวนการสะท้อนแสงสูงของโซน ellipsoid (เส้น IS/OS)1) การทำลายโซน ellipsoid ทำให้เกิดอาการที่ผู้ป่วยรับรู้2)
FAF (การเรืองแสงเองของจอตา)OCT และการเรืองแสงเองมีความสัมพันธ์กันอย่างใกล้ชิด9)
ลักษณะในระยะสงบ
การหายไปของจุดขาว : จุดขาวจะค่อยๆ หายจากส่วนกลางภายใน 7-12 วัน และหายไปเหลือเพียงการเปลี่ยนแปลงการลดสีเล็กน้อย
การฟื้นตัวใน OCT : โซน ellipsoid อาจฟื้นตัวได้ภายในไม่กี่เดือน แต่ความบางของชั้นเซลล์รับแสง อาจคงอยู่1)
ฝ่อของคอรอยด์ และจอประสาทตา : ในบางกรณี อาจมีรอยฝ่อของคอรอยด์ และจอประสาทตา เล็กน้อยหลงเหลืออยู่ 1)
Q
จุดขาวใน APMPPE หายไปหรือไม่?
A
ในกรณีส่วนใหญ่ จุดขาวจะยุบลงภายใน 7–12 วันหลังจากเริ่มมีอาการ และหายไปเหลือไว้ซึ่งการสูญเสียสี การพยากรณ์โรคด้านการมองเห็น มักจะดีและการกลับเป็นซ้ำพบได้น้อย อย่างไรก็ตาม ในกรณีที่เปลี่ยนเป็นโรคคอรอยด์ แบบแผนที่ (คอรอยด์ อักเสบแบบคดเคี้ยว) อาจพบการดำเนินโรค ดังนั้นจึงจำเป็นต้องติดตามผลอย่างสม่ำเสมอ
สันนิษฐานว่าหลักคือภาวะหลอดเลือดอักเสบอุดตันจากปฏิกิริยาภูมิไวเกินชนิดล่าช้า (ภูมิแพ้ชนิดที่ 4) ต่อหลอดเลือดแดงนำเข้าของแผ่นเส้นเลือดฝอยคอรอยด์ ในการตรวจ OCT -A (OCT angiography) พบ flow void (การสูญเสียสัญญาณการไหลเวียนเลือด) ในระดับคอริโอแคปิลลาริสในรอยโรคระยะเฉียบพลัน ซึ่งสนับสนุนว่าภาวะขาดเลือดของแผ่นเส้นเลือดฝอยคอรอยด์ เป็นแกนกลางของพยาธิกำเนิด 3) Klufas และคณะรายงานว่า OCT -A ตรวจพบ flow void ของคอริโอแคปิลลาริสโดยมีความสอดคล้องสูงกับ FA และ ICGA ในโรคคอรอยด์ อักเสบและจอประสาทตา อักเสบแบบแผ่นสามโรค (APMPPE , PPM , RPC ) 4)
มีกรณีที่เกิดขึ้นหลังจากมีอาการคล้ายไข้หวัดมาก่อน (ไข้หวัดใหญ่ คางทูม ฯลฯ) การติดเชื้อทางเดินหายใจส่วนบน หรือการฉีดวัคซีน
มีการรายงานความสัมพันธ์กับหลอดเลือดอักเสบทั่วร่างกาย (หลอดเลือดอักเสบในสมอง) โรคไต หลอดเลือดแดงอักเสบหลายเส้นแบบเป็นก้อน และต่อมไทรอยด์อักเสบ 1)
หากมีอาการทางระบบประสาท เช่น ปวดศีรษะ สติสัมปชัญญะผิดปกติ หรืออัมพาตครึ่งซีก อาจมีหลอดเลือดอักเสบในกะโหลกศีรษะ จำเป็นต้องตรวจฉุกเฉินรวมถึง MRI สมองและ MRA
Q
APMPPE มีความเสี่ยงต่อโรคหลอดเลือดสมองหรือไม่?
A
แม้จะพบได้ยาก แต่มีรายงานผู้ป่วย APMPPE ที่มีภาวะหลอดเลือดอักเสบในระบบประสาทส่วนกลางร่วมด้วย หากมีอาการทางระบบประสาท (ปวดศีรษะรุนแรง เปลี่ยนแปลงความรู้สึกตัว อัมพาต) ต้องทำ MRI สมองและ MRA อย่างเร่งด่วน และจำเป็นต้องประสานงานกับอายุรแพทย์ระบบประสาท
การวินิจฉัย APMPPE ขึ้นอยู่กับลักษณะเฉพาะของภาพจอประสาทตา และผลการตรวจหลอดเลือดด้วยฟลูออเรสซีน (FA และ ICGA ) การถ่ายภาพหลายรูปแบบช่วยให้ประเมินพยาธิสภาพได้หลายมิติ 2)
วิธีการตรวจ ลักษณะเฉพาะ FA (การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน )ระยะเฉียบพลัน: การเรืองแสงต่ำในระยะแรก → การเรืองแสงสูงในระยะหลัง (ปรากฏการณ์การกลับกันของการเรืองแสง) 1) ICGA (การถ่ายภาพหลอดเลือดด้วยอินโดไซยานีนกรีน)การเรืองแสงต่ำอย่างต่อเนื่องตั้งแต่ต้นจนจบ ระยะเรื้อรัง: เล็กลงและขอบเขตไม่ชัดเจน 5) SD-OCT ระยะเฉียบพลัน: การรบกวนการสะท้อนแสงสูงในบริเวณ ellipsoid zone ระยะสงบ: ชั้นเซลล์รับแสง บางลง 1) OCT -Aช่องว่างการไหลเวียนเลือดที่ระดับคอริโอแคปิลลาริส สอดคล้องสูงกับ FA /ICGA 4) FAF (การเรืองแสงอัตโนมัติของจอประสาทตา )ระยะเฉียบพลัน: การเรืองแสงอัตโนมัติต่ำหรือสูงในรอยโรค สัมพันธ์กับผล OCT 9) คลื่นไฟฟ้าจอประสาทตา แบบหลายจุด การแบนราบของแอมพลิจูดอย่างชัดเจนใกล้จอประสาทตา ส่วนกลางในระยะเฉียบพลัน
ปรากฏการณ์การกลับกันของการเรืองแสง ซึ่งเป็นการเรืองแสงน้อยในระยะแรกตามด้วยการเรืองแสงมากในระยะหลังในการตรวจฟลูออเรสซีน แองจิโอกราฟี เป็นลักษณะที่พบได้บ่อยที่สุดของ APMPPE โดยอธิบายว่าการไหลเข้าของสีสู่แผ่นเส้นเลือดฝอยคอรอยด์ ถูกขัดขวางในระยะแรก (เนื่องจากหลอดเลือดอักเสบชนิดอุดตัน) และการเรืองแสงมากในระยะหลังเกิดจากการรั่วซึมจากบริเวณรอบข้าง1) ในการตรวจอินโดไซยานีนกรีนแองจิโอกราฟี จะพบการเรืองแสงน้อยตั้งแต่ระยะแรกจนถึงระยะหลัง ซึ่งสะท้อนภาวะขาดเลือดของแผ่นเส้นเลือดฝอยคอรอยด์ ได้โดยตรงมากกว่า5)
OCT -A เป็นวิธีการถ่ายภาพแบบไม่รุกล้ำที่สามารถประเมินความผิดปกติของการไหลเวียนเลือดในแผ่นเส้นเลือดฝอยคอรอยด์ ใน APMPPE Furino และคณะรายงานว่า OCT -A สามารถแสดงช่องว่างการไหลของคอริโอแคปิลลาริสได้สอดคล้องกับฟลูออเรสซีน แองจิโอกราฟีและอินโดไซยานีนกรีนแองจิโอกราฟีในรอยโรค APMPPE เฉียบพลัน8) ในระยะฟื้นตัว พบว่าการหดตัวของช่องว่างการไหลสัมพันธ์กับการทำงานของสายตาที่ดีขึ้น จึงมีประโยชน์เป็นตัวบ่งชี้ทางชีวภาพ ในการติดตามกิจกรรมของโรค
คอรอยด์ อักเสบแบบแผนที่ (เซอร์พิจิโนซา)1) โรคโวกท์-โคยานางิ-ฮาราดะ : จอประสาทตาลอก แบบมีน้ำใต้, จุดรั่วใต้จอประสาทตา หลายจุด1) กลุ่มอาการจุดขาว หลายจุดที่หายไป (MEWDS )ฟลูออเรสซีน แองจิโอกราฟี1) จอประสาทตา ส่วนกลางอักเสบแบบแผ่นคงที่ (PPM ) / จอประสาทตา คอรอยด์ อักเสบแบบแผ่นที่ไม่หยุดยั้ง (RPC )จอประสาทตา คอรอยด์ อักเสบแบบแผ่นเนื่องจากคล้ายกับ APMPPE 4) 7)
Q
จะแยก APMPPE ออกจาก MEWDS ได้อย่างไร?
A
สามประเด็นสำคัญในการแยกโรค: ขนาดรอยโรค, ผลการตรวจฟลูออเรสซีน แองจิโอกราฟี, และการเป็นสองตา รอยโรคสีขาวของ APMPPE มีขนาดใหญ่กว่า MEWDS (1/4 ถึง 1/2 เท่าของเส้นผ่านศูนย์กลางจานประสาทตา ), มักเป็นสองตา, และแสดงปรากฏการณ์การกลับกันของการเรืองแสง (เรืองแสงน้อยในระยะแรกตามด้วยเรืองแสงมากในระยะหลัง) ในการตรวจฟลูออเรสซีน แองจิโอกราฟี MEWDS มักเป็นตาข้างเดียว, รอยโรคสีขาวเล็กและกระจายกว้าง, และแสดงการเรืองแสงมากในระยะแรกในการตรวจฟลูออเรสซีน แองจิโอกราฟี1)
มีแนวโน้มที่จะหายได้เองสูง มักฟื้นตัวโดยไม่ต้องรักษาเฉพาะ 1) ในกรณีที่ไม่รุนแรง การสังเกตอาการเป็นหลัก แม้ในรายงานการติดตามระยะยาวของ Jones (1995) ก็พบว่าหลายกรณีฟื้นคืนสายตาที่ดีในที่สุด 10)
ในกรณีที่สายตาลดลงอย่างมาก ร่วมกับ papillitis หรือมีรอยโรคใกล้จอประสาทตา ให้พิจารณาดังต่อไปนี้
ยาเม็ด Prednisolone (5 มก.): เริ่มต้นที่ 30 มก./วัน แล้วค่อยๆ ลดลงภายใน 2 สัปดาห์ถึง 1 เดือนยาเม็ด Carnaculin (Kallidinogenase 25-50 หน่วย): 3 เม็ด แบ่งเป็น 3 ครั้ง (ใช้เป็นยาเสริมเพื่อเพิ่มการไหลเวียนระดับจุลภาคของคอรอยด์ )
ในกรณีที่เปลี่ยนไปเป็น choroidopathy แบบ geographc หรือร่วมกับ vasculitis ของระบบประสาทส่วนกลาง ให้พิจารณาการรักษาด้วย steroid pulse (methylprednisolone ขนาดสูงทางหลอดเลือดดำ) หรือการใช้ยากดภูมิคุ้มกัน 1) หากเกิดเส้นเลือดใหม่ในคอรอยด์ (CNV ) ให้พิจารณาการฉีดยา anti-VEGF เข้าแก้วตา แม้ว่าจะเป็นภาวะแทรกซ้อนที่พบได้ยาก ในกรณีที่เปลี่ยนไปเป็น persistent placoid maculopathy (PPM ) อาจต้องจัดการในระยะยาว ดังที่ Kolomeyer และ Brucker ชี้ให้เห็นในการทบทวนอย่างเป็นระบบของพวกเขา 7)
Q
จำเป็นต้องรักษาด้วย steroid เสมอหรือไม่?
A
ในกรณีที่ไม่รุนแรง การสังเกตอาการเพียงอย่างเดียวก็เพียงพอสำหรับการฟื้นตัวตามธรรมชาติ การรักษาด้วย steroid จะพิจารณาในกรณีที่สายตาลดลงอย่างมาก มีการอักเสบรุนแรงใกล้หัวประสาทตา หรือมีอาการทางระบบประสาทส่วนกลาง แนวทางการรักษาม่านตาอักเสบ ก็ระบุว่า “การฟื้นตัวตามธรรมชาติโดยไม่ต้องรักษาเฉพาะ” เป็นหลักการพื้นฐาน 1)
พยาธิกำเนิดของ APMPPE เข้าใจว่าเป็นการเปลี่ยนแปลงจากการขาดเลือดเนื่องจากการอุดตันของ lamina choriocapillaris
สันนิษฐานว่าสาเหตุพื้นฐานคือ vasculitis แบบอุดตันจากปฏิกิริยาภูมิไวเกินชนิดล่าช้า (type IV) ที่ arteriole นำเข้าของ lamina choriocapillaris การอุดตันนำไปสู่การเปลี่ยนแปลงจากการขาดเลือดของ RPE และชั้นนอกของจอประสาทตา (บวมและขุ่น) และเกิดจุดขาวรูปจาน Mrejen และคณะแสดงให้เห็นว่ารอยโรคที่คอรอยด์ สามารถขยายไปถึงชั้นที่ลึกกว่า บ่งชี้ถึงความเป็นไปได้ที่เกี่ยวข้องไม่เพียงแต่ lamina choriocapillaris แต่ยังรวมถึงหลอดเลือดขนาดกลางและขนาดใหญ่ด้วย 3)
ในการตรวจ OCT -A จะพบช่องว่างการไหล (flow void) ในระดับคอรอยด์ ชั้นใน และได้รับการแสดงให้เห็นว่าภาวะขาดเลือดของแผ่นเส้นเลือดฝอยคอรอยด์ (choriocapillaris) เป็นพื้นฐานทางพยาธิสรีรวิทยาที่สอดคล้องกันของกลุ่มโรค “สเปกตรัมความผิดปกติแบบแผ่น” (รวมถึง persistent placoid maculopathy และ relentless placoid chorioretinitis) เช่นเดียวกับ APMPPE 4) Klufas และคณะรายงานว่า flow void ใน choriocapillaris โดย OCT -A แสดงรูปแบบร่วมกันระหว่างโรคทั้งสาม ซึ่งสนับสนุนแนวคิดของสเปกตรัม placoid chorioretinitis
กลไกของปรากฏการณ์การกลับกันของฟลูออเรสเซนต์: ในระยะแรกของการฉีดสี จะเห็นการเรืองแสงน้อย (hypofluorescence) เนื่องจากการไหลของสีเข้าสู่แผ่นเส้นเลือดฝอยคอรอยด์ ถูกขัดขวาง ในระยะหลัง สีจะรั่วจากเนื้อเยื่อปกติโดยรอบ เปลี่ยนเป็นการเรืองแสงมาก (hyperfluorescence) การที่ ICGA แสดงการเรืองแสงน้อยตลอดทั้งการตรวจก็สะท้อนถึงการเปลี่ยนแปลงแบบอุดตันในแผ่นเส้นเลือดฝอยคอรอยด์ 5) FAF สามารถประเมินการกระจายของความเสียหายของ RPE ได้แบบไม่รุกล้ำ และแสดงความสัมพันธ์สูงกับผล OCT 9)
APMPPE หลังการติดเชื้อหรือวัคซีน COVID-19APMPPE เฉียบพลันหลังการติดเชื้อ ซึ่งดึงดูดความสนใจถึงความสัมพันธ์กับการตอบสนองทางภูมิคุ้มกันที่ถูกกระตุ้นโดยไวรัสภาวะหลอดเลือดสมองอักเสบร่วม : คำแนะนำให้ทำ MRI สมองและ MRA มีมากขึ้นในผู้ป่วยที่มีอาการทางระบบประสาท มีรายงานผู้ป่วย APMPPE หลายรายที่มีภาวะแทรกซ้อนโรคหลอดเลือดสมองหรือหลอดเลือดสมองอักเสบ ซึ่งเน้นย้ำถึงความสำคัญของการติดตามทั่วร่างกายนอกเหนือจากอาการทางตา 6) ความก้าวหน้าทางการถ่ายภาพหลายรูปแบบ : การติดตาม flow void ใน choriocapillaris ด้วย OCT -A มีศักยภาพเป็นตัวบ่งชี้ทางชีวภาพ สำหรับการประเมินกิจกรรมของโรค 8) เนื่องจากไม่รุกล้ำและสามารถทำซ้ำได้ วิธีการนี้กำลังกลายเป็นเครื่องมือเสริมที่สำคัญสำหรับการตรวจ FA และ ICGA การจำแนกประเภทย่อยของโรคใหม่ : ความเข้าใจแบบบูรณาการในฐานะ “สเปกตรัม placoid chorioretinitis” ซึ่งรวมถึง persistent placoid maculopathy และ relentless placoid chorioretinitis กำลังก้าวหน้า 4) Mirza และ Jampol (2012) ได้จัดระเบียบลักษณะของ relentless placoid chorioretinitis ในฐานะแนวคิดโรคอิสระ และอภิปรายถึงความต่อเนื่องกับ APMPPE 6)
日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(「13. 急性後部多発性斑状色素上皮症」節). 日本眼科学会雑誌. 2019;123(6):635-696.
Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
Mrejen S, Sarraf D, Chexal S, et al. Choroidal involvement in acute posterior multifocal placoid pigment epitheliopathy. Ophthalmic Surg Lasers Imaging Retina. 2016;47:20-26.
Klufas MA, Phasukkijwatana N, Iafe NA, et al. Optical coherence tomography angiography reveals choriocapillaris flow reduction in placoid chorioretinitis. Ophthalmol Retina. 2017;1(1):77-91.
Park D, Schatz H, McDonald HR, Johnson RN. Indocyanine green angiography of acute multifocal posterior placoid pigment epitheliopathy. Ophthalmology. 1995;102:1877-1883.
Mirza RG, Jampol LM. Relentless placoid chorioretinitis. Int Ophthalmol Clin. 2012;52(4):237-242.
Kolomeyer AM, Brucker AJ. Persistent placoid maculopathy: a systematic review. Retina. 2018;38(10):1881-1895.
Furino C, Shalchi Z, Grassi MO, et al. Optical coherence tomography angiography in acute posterior multifocal placoid pigment epitheliopathy. Ophthalmic Surg Lasers Imaging Retina. 2019;50(7):428-436.
Souka AA, Hillenkamp J, Gora F, Gabel VP, Framme C. Correlation between optical coherence tomography and autofluorescence in acute posterior multifocal placoid pigment epitheliopathy. Graefes Arch Clin Exp Ophthalmol. 2006;244(10):1219-1223.
Jones NP. Acute posterior multifocal placoid pigment epitheliopathy. Br J Ophthalmol. 1995;79:384-389.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต