โรคจอประสาทตา ชั้นนอกแอบแฝงแบบเฉียบพลัน (AZOOR ) เป็นโรคที่ Gass เสนอในปี 1992 มีลักษณะเฉพาะคือข้อบกพร่องของลานสายตาเฉียบพลัน ภาพแสงวาบ และการมองเห็น ลดลง แม้ว่าจอประสาทตา จะดูเกือบปกติ
พบได้บ่อยในหญิงสาวสายตาสั้น มักเป็นข้างเดียว ประมาณ 20% ของผู้ป่วยมีอาการนำคล้ายไข้หวัด
การหายไปของ ellipsoid zone (เส้น IS/OS) ในการตรวจ OCT เป็นสิ่งที่สำคัญที่สุด และสอดคล้องกับตำแหน่งของข้อบกพร่องของลานสายตา
การรวมกันของ mfERG และ ffERG มีประโยชน์ในการวินิจฉัยและพยากรณ์โรค
ยังไม่มีการรักษาที่เป็นมาตรฐาน ในกรณีรุนแรง (สายตาที่แก้ไขแล้วของตาข้างที่ดี < 0.3) อาจพิจารณาการรักษาด้วยสเตียรอยด์ แบบชีพจร
จัดเป็นโรคหนึ่งในกลุ่ม AZOOR complex (MEWDS , AMN , PIC , MFC, AIBSE, AAO R)
แนวทางการวินิจฉัยถูกจัดทำขึ้นโดยสมาคมจักษุวิทยาญี่ปุ่น โดยมีการจำแนกระดับความรุนแรง
ตำแหน่งรอยโรคปฐมภูมิคือส่วนนอกของเซลล์รับแสง ในขณะที่เส้นเลือดฝอยคอรอยด์ ยังคงอยู่ปกติในระยะแรก
ส่วนใหญ่จะคงที่ได้เองภายใน 6 เดือน แต่ความเสียหายต่อชั้นนอกของจอประสาทตา ในระยะลุกลามจะไม่สามารถกลับคืนได้ และไม่สามารถฟื้นฟูการทำงานได้
โรคจอประสาทตา ชั้นนอกแอบแฝงแบบเฉียบพลัน (acute zonal occult outer retinopathy; AZOOR ) เป็นโรคอักเสบเฉียบพลันที่ Gass เสนอและสร้างแนวคิดโรคขึ้นในทศวรรษ 19903) มีลักษณะเฉพาะคือข้อบกพร่องของลานสายตาเฉียบพลัน ภาพแสงวาบ และการมองเห็น ลดลง แม้ว่าจอประสาทตา จะดูเกือบปกติ รอยโรคหลักอยู่ที่เซลล์รับแสง และชั้นนอกของจอประสาทตา และตามชื่อโรค เป็นโรคจอประสาทตา ชั้นนอกที่ “แอบแฝง”
แนวทางการวินิจฉัย AZOOR ถูกจัดทำขึ้นโดยสมาคมจักษุวิทยาญี่ปุ่น โดยมีการจำแนกระดับความรุนแรง เช่น “สายตาที่แก้ไขแล้วของตาข้างที่ดี < 0.3” นอกจากนี้ AZOOR ยังถูกรวมอยู่ในตารางการแยกโรคของ AZOOR complex (ตารางที่ 3) ในแนวทางการรักษาม่านตาอักเสบ (Jpn J Ophthalmol 2019;123(6):635-696)1) เมื่อพบความผิดปกติของลานสายตาที่ไม่สามารถอธิบายได้ด้วยการตรวจจอประสาทตา ควรพิจารณาความเป็นไปได้ของ AZOOR ในการวินิจฉัยแยกโรคเสมอ
AZOOR จัดเป็นโรคหนึ่งในกลุ่ม AZOOR complex (MEWDS , AZOOR , AMN , PIC , MFC, AIBSE, AAO R) และกลุ่มโรคนี้ถูกเข้าใจว่าเป็นสเปกตรัมของโรคอักเสบที่ส่งผลต่อจอประสาทตา ชั้นนอก เซลล์รับแสง และเยื่อบุผิวรงควัตถุจอประสาทตา 1) 2) ด้วยความก้าวหน้าของการถ่ายภาพหลายรูปแบบ ความเข้าใจทางพยาธิสรีรวิทยาแบบบูรณาการของ AZOOR complex จึงลึกซึ้งยิ่งขึ้น2)
มีการรายงานตัวแปรของ AZOOR ดังต่อไปนี้1) :
AAO R (จอประสาทตา ชั้นนอกอักเสบแบบวงแหวนเฉียบพลัน) : ข้างเดียว, ขอบสีเทาขาวเป็นวง, ลุกลามเข้าสู่ศูนย์กลางMORR (โรคจอประสาทตา ชั้นนอกและเยื่อบุผิวรงควัตถุจอประสาทตา แบบหลายเขต) : เริ่มเฉียบพลัน, ดำเนินไป, เกี่ยวข้องกับ RPE ชนิดเริ่มจากรอบนอก : ตัวแปรที่หายาก บริเวณรอบหัวประสาทตาไม่ได้รับผลกระทบ ลุกลามจากรอบนอกเข้าสู่ศูนย์กลาง 11)
พบบ่อย: ตาสั้นในหญิงสาว
ประมาณ 3/4 ของผู้ป่วยเป็นผู้หญิง พบมากในวัยหนุ่มสาวช่วงกลางอายุ 30
เริ่มเป็นข้างเดียว 61% และสุดท้ายเป็นสองข้าง 76% ในการติดตามผลเฉลี่ย 8 ปี
ตาข้างตรงข้ามเกิดโรคช้ากว่าเฉลี่ย 50 เดือน
โรคร่วมภูมิต้านตนเอง: โรคฮาชิโมโตะ (พบบ่อยที่สุด), ปลอกประสาทเสื่อมแข็ง 1)
ประมาณ 20% ของผู้ป่วยมีอาการคล้ายไข้หวัดนำมาก่อน
สำหรับลักษณะทางคลินิกในผู้ป่วยญี่ปุ่น มีรายงานการศึกษาตามรุ่นของผู้ป่วย AZOOR ชาวญี่ปุ่น (Saito S และคณะ, 2015) ซึ่งศึกษาธรรมชาติของสายตาที่เปลี่ยนแปลงไปและปัจจัยพยากรณ์โรค 4) .
Q
ทำไมการมองเห็นลดลงทั้งที่จอประสาทตาปกติ?
A
ตำแหน่งหลักที่ถูกทำลายใน AZOOR คือเซลล์รับแสง (จอประสาทตา ชั้นนอก / โซน ellipsoid) แม้ว่าจอประสาทตา จะดูปกติ OCT จะแสดงการหายไปของโซน ellipsoid (เส้น IS/OS) ซึ่งตรงกับตำแหน่งที่บกพร่องของลานสายตา การขาดการเชื่อมต่อระหว่างส่วนในและส่วนนอกของเซลล์รับแสง ทำให้การทำงานของสายตาลดลง ส่งผลให้การมองเห็น ลดลงและลานสายตาบกพร่องแม้จอประสาทตา จะดูปกติ
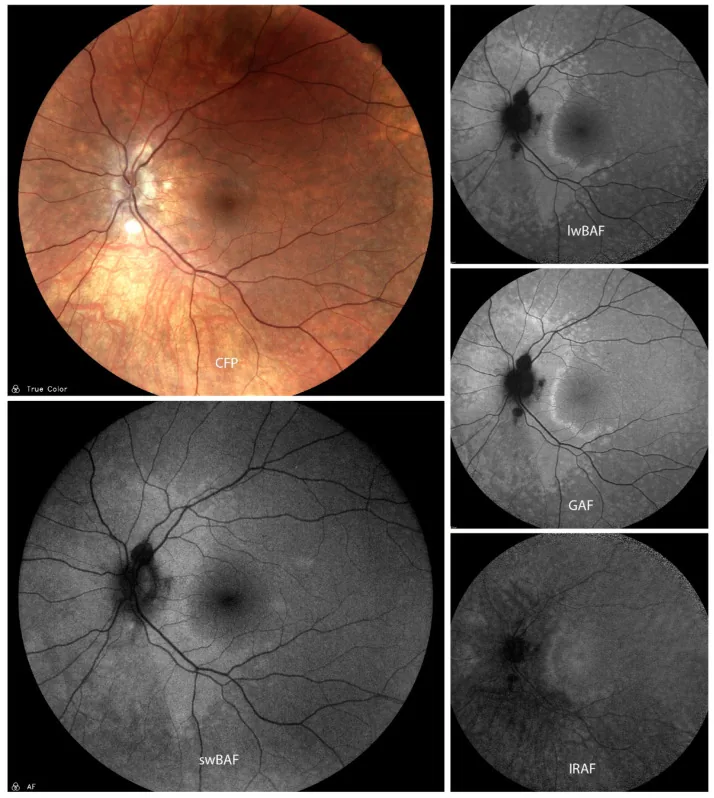
ภาพถ่ายจอประสาทตาแบบหลายรูปแบบของ Acute Zonal Occult Outer Retinopathy แสดงแถบการเรืองแสงเองที่ผิดปกติแผ่จากหัวประสาทตา Mauschitz MM, et al.
Fundus Autofluorescence in Posterior and Panuveitis-An Under-Estimated Imaging Technique: A Review and Case Series. Biomolecules. 2024. Figure 5. PM
CI D: PMC11118036. License: CC BY.
ภาพถ่ายสีจอประสาทตา (CF P) และภาพ autofluorescence ต่างๆ (swBAF (450nm), lwBAF (488nm), GAF (518nm), IRAF (787nm)) ในโรค Acute Posterior Multifocal Placoid Pigment Epitheliopathy (APMPPE ) แสดงรอยโรคที่มี autofluorescence ต่ำและขอบ autofluorescence สูง ซึ่งสอดคล้องกับความผิดปกติของ autofluorescence จอประสาทตา ที่กล่าวถึงในหัวข้อ “2. อาการหลักและผลการตรวจทางคลินิก”
เห็นแสงวาบ : หนึ่งในอาการที่เด่นชัดที่สุด เริ่มต้นเฉียบพลัน
การมองเห็น ลดลงเฉียบพลันและข้อบกพร่องของลานสายตา (1 ถึงหลายตำแหน่ง) 1) จุดบอด Mariotte ขยายใหญ่ขึ้น ข้อบกพร่องลานสายตาส่วนกลางและส่วนปลาย 1)
อาการนำ: อาการคล้ายไข้หวัด (ประมาณ 20% ของผู้ป่วย)
ข้อบกพร่องของลานสายตามักปรากฏเป็นแถบหรือเป็นส่วนๆ และอาจถูกวินิจฉัยผิดว่าเป็นโรคประสาทตาอักเสบ เนื่องจากจอประสาทตา ดูปกติ 1) การตรวจลานสายตา Goldmann พบว่าจุดบอด Mariotte ขยายใหญ่ขึ้นอย่างชัดเจนหรือ scotoma แบบเป็นส่วน
จอประสาทตา ปกติโดยพื้นฐาน และอาจแยกจากโรคประสาทตาอักเสบ ได้ยาก 1) ลักษณะสำคัญของ AZOOR คือการตรวจหลอดเลือดด้วยฟลูออเรสซีน (FA ) มักไม่พบความผิดปกติ ในกรณีเรื้อรัง อาจเกิดการฝ่อของคอรอยด์ และจอประสาทตา แบบกระจายหรือเป็นส่วน
เมื่อเริ่มต้น
จอประสาทตา วุ้นตา FA มักไม่พบความผิดปกติ
OCT 5)
คลื่นไฟฟ้าจอประสาทตา แบบเต็มลาน : แอมพลิจูดลดลงในกรณีที่เสียหายเป็นบริเวณกว้าง ความผิดปกติของระบบเซลล์รูปกรวย > ระบบเซลล์รูปแท่ง
คลื่นไฟฟ้าจอประสาทตา แบบหลายจุด : แอมพลิจูดลดลงสอดคล้องกับตำแหน่งข้อบกพร่องของลานสายตา มีประโยชน์โดยเฉพาะในการตรวจหารอยโรคขนาดเล็ก 1)
ระยะเรื้อรัง
ฝ่อของจอตา : อาจเกิดการฝ่อของคอรอยด์ และจอตาแบบกระจายหรือเป็นบริเวณในบางราย7)
การเปลี่ยนแปลงของ ERG : ERG อาจดีขึ้นเมื่อได้รับการรักษาหรือฟื้นตัวเองในบางราย
การเปลี่ยนแปลงของ OCT : อาจพบการฟื้นตัวบางส่วนของ ellipsoid zone แต่การสูญเสียชั้นนอกอย่างต่อเนื่องทำให้พยากรณ์การมองเห็น ไม่ดี8)
การเปลี่ยนแปลงของลานสายตาผิดปกติ : ในรายที่ฟื้นตัวเอง อาจพบการหดตัวของลานสายตาบกพร่อง
Q
AZOOR แตกต่างจากโรคประสาทตาอักเสบอย่างไร?
A
โรคที่สำคัญที่สุดที่ต้องแยกคือโรคประสาทตาอักเสบ ใน AZOOR จอตาปกติเกือบตลอด และมักไม่มีอาการบวมหรือเลือดคั่งของหัวประสาทตา การลดลงของแอมพลิจูด ERG (โดยเฉพาะ multifocal ERG ) เป็นลักษณะเฉพาะของ AZOOR ในขณะที่โรคประสาทตาอักเสบ ERG มักปกติ นอกจากนี้ อาการเห็นแสงวาบ (photopsia) มักเด่นชัดใน AZOOR และมักไม่มีปวดเมื่อขยับลูกตา1)
นอกจากนี้ หากมีภาวะตาบอดครึ่งซีกขมับข้างเดียว สาเหตุเกิดจากความเสียหายของจอตาด้านจมูก และอาจปรากฏเป็นตาบอดครึ่งซีกขมับที่เคารพเส้นเมริเดียนแนวตั้ง ทำให้เลียนแบบรอยโรคของออปติกไคแอสม และอาจต้องทำ MRI12) RAPD (relative afferent pupillary defect) อาจปรากฏในบางรายระหว่างดำเนินโรค
ไม่ทราบสาเหตุ แต่การติดเชื้อไวรัสหรือการเกี่ยวข้องของภูมิต้านตนเองเป็นสมมติฐานหลักที่เสนอ
ประมาณ 20% ของผู้ป่วยมีอาการนำคล้ายไข้หวัด → สมมติฐานการกระตุ้นจากไวรัส
ความสัมพันธ์กับโรคฮาชิโมโตะและโรคปลอกประสาทเสื่อมแข็ง → สมมติฐานกลไกภูมิต้านตนเอง1)
ตำแหน่งรอยโรคหลัก: เซลล์รับแสง (ellipsoid zone), RPE และ choroidal capillary lamina (หลายทฤษฎี)
เกี่ยวกับตำแหน่งรอยโรคหลักของ AZOOR มีหลายทฤษฎีรวมถึงเซลล์รับแสง , retinal pigment epithelium และ choroidal capillary lamina และยังไม่มีข้อสรุป การหายไปของ ellipsoid zone ใน OCT สะท้อนโดยตรงถึงการแตกของรอยต่อระหว่างส่วนในและส่วนนอกของเซลล์รับแสง (IS/OS line) และการฟื้นตัวของการทำงานในบริเวณนั้นมักทำได้ยาก8)
หญิงสาวและสายตาสั้น
โรครูมภูมิคุ้มกันตนเองร่วม (โรคฮาชิโมโตะ, ปลอกประสาทเสื่อมแข็ง)1)
ความโน้มเอียงทางพันธุกรรมซึ่งเป็นส่วนหนึ่งของกลุ่มอาการ AZOOR + ปัจจัยสิ่งแวดล้อม (การติดเชื้อไวรัส, ตัวกระตุ้นภูมิคุ้มกันตนเอง)2)
โรคลมชัก: การศึกษาในหนูแสดงให้เห็นว่าอาการชักกระตุ้นให้เกิดปฏิกิริยาอักเสบในจอประสาทตา ซึ่งบ่งชี้ถึงความสัมพันธ์ที่เป็นไปได้13)
หลังการผ่าตัดเสริมตาขาว (scleral buckle): มีรายงานผู้ป่วยที่พบลักษณะคล้าย AZOOR หลังจากผ่าตัดมากกว่า 5 ปี14)
จากผู้ป่วย 51 รายของ Gass ประมาณ 28% มีประวัติโรคภูมิต้านตนเอง นอกจากโรคฮาชิโมโตะและปลอกประสาทเสื่อมแข็งแล้ว โรคที่เกิดร่วมที่ทราบ ได้แก่ โรคเกรฟส์, ภาวะไทรอยด์ต่ำ, โรคแอดดิสัน, โรคกล้ามเนื้ออ่อนแรง (myasthenia gravis), โรคโครห์น และ SLE ตรวจพบแอนติบอดีต่อจอประสาทตา ในผู้ป่วย AZOOR ประมาณ 42%15) .
การวินิจฉัย AZOOR สงสัยในผู้ใหญ่วัยหนุ่มสาวอายุ 20-50 ปีที่มีการมองเห็น ลดลงเฉียบพลันในตาข้างเดียว, ความบกพร่องของลานสายตา และเห็นแสงวาบ (photopsia) การวินิจฉัยทำโดยใช้ OCT ร่วมกับ ERG เมื่อมีความผิดปกติของลานสายตาที่ไม่สามารถอธิบายได้ด้วยการตรวจอวัยวะภายในลูกตา สิ่งสำคัญคือต้องรวม AZOOR ไว้ในการวินิจฉัยแยกโรคอย่างจริงจัง
ในผู้ป่วยที่ค่อนข้างอายุน้อยอายุ 20-50 ปีที่มีการมองเห็น ลดลงเฉียบพลันในตาข้างเดียว, ความบกพร่องของลานสายตา และเห็นแสงวาบ ให้ทำ OCT ก่อน หาก OCT แสดงความผิดปกติของชั้นนอกจอประสาทตา ที่สอดคล้องกับตำแหน่งของความบกพร่องของลานสายตา ให้สงสัย AZOOR อย่างมาก จากนั้นยืนยันด้วย ERG และ multifocal ERG 1) .
วิธีการตรวจ ผลการตรวจ OCT การหายไปของ ellipsoid zone และ interdigitation zone ที่สอดคล้องกับตำแหน่งของความบกพร่องของลานสายตา มีประโยชน์ในการพยากรณ์โรค5) คลื่นไฟฟ้าจอประสาทตา แบบเต็มลานสายตา แอมพลิจูดลดลงในความผิดปกติแบบกว้าง ความผิดปกติของระบบเซลล์รูปกรวย > เซลล์รูปแท่ง คลื่นไฟฟ้าจอประสาทตา แบบหลายจุด แอมพลิจูดลดลงสอดคล้องกับตำแหน่งที่บกพร่องของลานสายตา ความไวสูงในการตรวจหารอยโรคขนาดเล็ก1) การเรืองแสงอัตโนมัติของจอตา (อินฟราเรด) ยืนยันขอบเขตระหว่างบริเวณรอยโรคและปกติ การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน ผลปกติโดยพื้นฐาน เครื่องวัดลานสายตาโกลด์แมนน์ จุดบอดมาริออตต์ขยายใหญ่ขึ้น จุดบอดกลาง จุดบอดเป็นบริเวณ1) ทัศนศาสตร์ปรับค่าได้ การมองเห็น ความผิดปกติของการเรียงตัวของเซลล์รับแสง คลื่นไฟฟ้าจอประสาทตา แบบรูปแบบ (PERG ) อาจแสดงรูปแบบ P50 ลดลงโดย N95 ปกติ คลื่นไฟฟ้าตา อาจแสดงการตอบสนองต่อแสงลดลงและอัตราส่วนอาร์เดนลดลง
OCT ยังมีประโยชน์ในการพยากรณ์โรค ในบริเวณที่ชั้นนอก (ellipsoid zone) หายไป ไม่สามารถคาดหวังการฟื้นฟูการทำงานได้ ดังนั้นการประเมินชั้นนอกด้วย OCT จึงเป็นพื้นฐานในการกำหนดแผนการรักษาและอธิบายการพยากรณ์โรค 5) เมื่อบริเวณที่เสียหายแคบ ERG แบบหลายจุดหรือ ERG เฉพาะจุดมีประโยชน์ในการวินิจฉัยมากกว่า ERG แบบเต็มลานสายตา 1)
โรค จุดที่ใช้แยก เส้นประสาทตา อักเสบแยกโดย ERG ในเส้นประสาทตา อักเสบ ERG ปกติ มีปวดเมื่อขยับตา MEWDS เห็นจุดขาว (ใน AZOOR จอประสาทตา ปกติ) ERG แบบหลายจุดก็ลดลง AMN รอยโรคจุดด่างสีน้ำตาลแดงที่จอตา รอยโรครูปลิ่มที่ชั้นนิวเคลียสชั้นนอกใน OCT AIBSE ความขุ่นสีเทาขาวรอบหัวประสาทตา การขยายจุดบอด Mariotte เป็นลักษณะเฉพาะ AAO R ความขุ่นสีเทาขาวเป็นวงในชั้นลึกของจอประสาทตา โรคปลอกประสาทเสื่อมแข็ง แยกโดยผล MRI อาการทั่วร่างกาย และผลการตรวจเส้นประสาทตา อักเสบ np-AIR (จอประสาทตา อักเสบจากภูมิคุ้มกันตนเองที่ไม่สัมพันธ์กับเนื้องอก) เริ่มแบบกึ่งเฉียบพลันถึงเรื้อรัง, FAF เรืองแสงมากแบบกระจาย, EOG ปกติ โรคจอประสาทตา ชั้นนอกจากซิฟิลิส (SOR) คล้ายกับ AZOOR มาก จำเป็นต้องตรวจซีรั่มซิฟิลิส 1)
เพื่อแยกการติดเชื้อ ตรวจซิฟิลิส, CMV, VZV และ HS V หากมีภาวะตาบอดครึ่งซีกด้านขมับ ให้ทำ MRI เพื่อแยกรอยโรคที่ออปติกไคแอสมาออก 12) .
Q
การตรวจใดที่ขาดไม่ได้ในการวินิจฉัย AZOOR?
A
การรวมกันของ OCT และคลื่นไฟฟ้าจอประสาทตา แบบหลายจุด (mfERG ) เป็นกุญแจสำคัญในการวินิจฉัย OCT แสดงการหายไปของ ellipsoid zone ที่สอดคล้องกับความบกพร่องของลานสายตา และ mfERG แสดงการลดลงของแอมพลิจูดในบริเวณที่สอดคล้องกัน คลื่นไฟฟ้าจอประสาทตา เต็มลานสายตา (full-field ERG ) มีประโยชน์ในการประเมินความเสียหายในวงกว้าง และ FA มักไม่แสดงความผิดปกติ ซึ่งช่วยแยกจากม่านตาอักเสบ ส่วนหลังอื่นๆ 1) การสังเกตอวัยวะด้วยแสงปรับตัว (AO ) สามารถมองเห็นความผิดปกติของการเรียงตัวของเซลล์รับแสง ในบริเวณรอยโรคได้
ไม่มีการรักษาที่ชัดเจน มีทั้งกรณีที่หายเองและกรณีที่พยากรณ์โรคทางสายตาไม่ดี
กรณีไม่รุนแรง : สังเกตอาการโดยไม่ต้องรักษากรณีรุนแรง (ค่าสายตาที่แก้ไขดีที่สุดในตาข้างที่ดีกว่า < 0.3): พิจารณาการรักษาด้วยสเตียรอยด์ แบบชีพจร
เนื่องจากสาเหตุสันนิษฐานว่าเป็นภูมิต้านตนเองหรือการอักเสบ การรักษาด้วยสเตียรอยด์ แบบชีพจรจึงอาจทำได้โดยเฉพาะในกรณีรุนแรง อย่างไรก็ตาม เป็นการยากที่จะแยกแยะว่าการฟื้นตัวเกิดจากการหายเองหรือจากผลของสเตียรอยด์
ช่องทางการให้ยา ชื่อยา ขนาดและวิธีการใช้ การให้ทางหลอดเลือดดำ (แบบชีพจร) เมทิลเพรดนิโซโลน (โซลู-เมดรอล®) 1,000 มก. + โซลิตา-T3 500 มล. หยดทางหลอดเลือดดำนาน 1 ชั่วโมง เป็นเวลา 3 วัน รับประทาน (การรักษาต่อเนื่อง) ยาเม็ดเพรดนิโซโลน (เพรดนิน®) 5 มก. 8-6 เม็ด (40-30 มก.) แบ่งให้วันละ 2 ครั้ง แล้วค่อยๆ ลดลง
สำหรับผลของการรักษาด้วยสเตียรอยด์ แบบชีพจรนั้น ยากที่จะแยกความแตกต่างจากการฟื้นตัวตามธรรมชาติ และหลักฐานอยู่ในระดับรายงานผู้ป่วยเท่านั้น ปัจจุบันยังไม่มีการทดลองแบบสุ่มที่มีกลุ่มควบคุม (RCT)
มีการรายงานการฉีดสเตียรอยด์ เข้าแก้วตาเช่นกัน แต่ต้องระวังความเสี่ยงของผลข้างเคียง เช่น ต้อกระจก ความดันลูกตา สูง และจอประสาทตา อักเสบชนิดเซรุ่มส่วนกลาง (CSR) 16)
สำหรับกรณีที่ดื้อต่อการรักษา มีรายงานดังนี้:
MMF + ไซโคลสปอรีน + IVIg : มีรายงานการปรับปรุง BCVA ด้วยการใช้ไมโคฟีโนเลต โมเฟทิล 2 กรัม/วัน + ไซโคลสปอรีน 200 มก./วัน + IVIg 2 กรัม/กก. เดือนละครั้ง 17) ไซโคลสปอรีน : มีตัวอย่างการใช้ในขนาด 4.5 มก./กก./วันอะดาลิมูแมบ (ฮิวมิรา)การรักษาด้วยยาต้านไวรัส : อะไซโคลเวียร์และวาลาไซโคลเวียร์ไม่แสดงผลชัดเจนในรายงานของ Gass 3)
ในกรณีที่มีเยื่อหุ้มเส้นเลือดใหม่คอรอยด์ (CNV M) การฉีดยา anti-VEGF เข้าแก้วตา (เช่น bevacizumab, aflibercept) อาจเป็นข้อบ่งชี้ 1)
ในกรณีที่กลับเป็นซ้ำหรือเรื้อรัง ควรพิจารณาใช้ยากดภูมิคุ้มกัน (เช่น cyclosporin) การรักษาตามโรคในกลุ่ม AZOOR complex ถือเป็นแนวทางอ้างอิง
Q
สเตียรอยด์ช่วยให้การมองเห็นดีขึ้นหรือไม่?
A
มีรายงานผู้ป่วยเกี่ยวกับประสิทธิภาพของการรักษาด้วยสเตียรอยด์ แบบ pulse แต่ไม่มีการทดลองแบบสุ่มที่มีกลุ่มควบคุม และยากที่จะแยกแยะจากการหายเอง พิจารณาทำเฉพาะในกรณีรุนแรง (ค่าสายตาที่แก้ไขแล้วของตาข้างที่ดี < 0.3) แต่ในกรณีที่ชั้นจอประสาทตา ชั้นนอกหายไปอย่างต่อเนื่องแม้จะรักษาแล้ว การพยากรณ์การมองเห็น ไม่ดี ในบริเวณที่ zona ellipsoid หายไปใน OCT การฟื้นฟูการทำงานมักทำได้ยาก 8)
พยาธิสรีรวิทยาของ AZOOR คือการบาดเจ็บเฉียบพลันของเซลล์รับแสง และ zona ellipsoid (รอยต่อส่วนใน/ส่วนนอก)
การหายไปของ zona ellipsoid ใน OCT สะท้อนโดยตรงถึงการแตกของรอยต่อส่วนใน/ส่วนนอก (เส้น IS/OS) ในบริเวณที่ zona นี้หายไป การฟื้นตัวของเซลล์รับแสง ทำได้ยาก ทำให้เกิดความบกพร่องทางการมองเห็น ในระยะยาว 5) 8) ในกรณีที่ไม่รุนแรงหรือระยะฟื้นตัว อาจพบความผิดปกติเฉพาะที่ zona interdigitation ในขณะที่ zona ellipsoid อาจยังคงอยู่
การติดเชื้อไวรัส (ประมาณ 20% มีอาการนำคล้ายไข้หวัด) หรือภูมิต้านตนเอง (โรคฮาชิโมโตะ, ปลอกประสาทเสื่อมแข็ง) อาจเกี่ยวข้อง
ตำแหน่งที่บาดเจ็บหลัก: รอยต่อส่วนใน/ส่วนนอกของเซลล์รับแสง (zona ellipsoid) การหายไปของมันสะท้อนโดยตรงใน OCT
มีทฤษฎีต่างๆ เกี่ยวกับการมีส่วนร่วมของแผ่นหลอดเลือดฝอยคอรอยด์ แต่ใน OCT -A มักพบว่าคอริโอแคปิลลาริสยังคงอยู่หรือมีการเปลี่ยนแปลงเพียงเล็กน้อย 2)
ในฐานะโรคหนึ่งในกลุ่ม AZOOR complex เกิดจากปัจจัยทางพันธุกรรมร่วมกับปัจจัยสิ่งแวดล้อม (การติดเชื้อไวรัส/ภูมิต้านตนเอง) 2)
AZOOR complex (MEWDS , AZOOR , AMN , PIC , MFC, AIBSE, AAO R) ถือเป็นโรคที่เกี่ยวข้องกันบนสเปกตรัมเดียวกัน โดยมีพื้นฐานร่วมกันคือความผิดปกติจากการอักเสบที่จอประสาทตา ชั้นนอกและ RPE 2) Jampol และ Becker (2003) เสนอสมมติฐานว่ากลุ่มอาการจุดขาว เหล่านี้มีกลไกภูมิต้านตนเอง/การอักเสบทางพันธุกรรมร่วมกัน 10)
โรคฮาชิโมโตะเป็นโรคภูมิต้านตนเองที่พบบ่อยที่สุด รองลงมาคือโรคปลอกประสาทเสื่อมแข็ง การเกิดร่วมกันนี้บ่งชี้ถึงการโจมตีเซลล์รับแสง และจอประสาทตา ชั้นนอกด้วยกลไกภูมิต้านตนเอง ซึ่งเป็นเบาะแสสำคัญในการทำความเข้าใจพยาธิสภาพของ AZOOR
ในบริเวณที่การหายไปของ ellipsoid zone คงอยู่ การฟื้นตัวของเซลล์รับแสง ทำได้ยาก และการประเมินด้วย OCT เชื่อมโยงโดยตรงกับการพยากรณ์โรคระยะยาว
การวิเคราะห์ภาพถ่ายหลายรูปแบบแสดงให้เห็นว่าตำแหน่งรอยโรคปฐมภูมิของ AZOOR คือ ส่วนนอกของเซลล์รับแสง 18) ในการตรวจหลอดเลือดด้วยสี ICG คอริโอแคปิลลาริสยังคงอยู่และไม่ถูกทำลายในระยะแรก การเรืองแสงเกินใน FAF เกิดจากการสัมผัสของลิโปฟัสซินใน RPE หลังจากการสูญเสียส่วนนอกของเซลล์รับแสง คอรอยด์ ถูกทำลายทุติยภูมิ (collateral damage) และในกรณีที่รุนแรงนำไปสู่การฝ่อของคอรอยด์ และจอประสาทตา
การวิเคราะห์เชิงปริมาณด้วยการถ่ายภาพเชิงปรับแสง (AO -TFI) ยืนยันว่าความหนาแน่นของเซลล์รับแสง (PR) ลดลงอย่างมีนัยสำคัญ ในขณะที่ความหนาแน่นของ RPE ไม่แตกต่างอย่างมีนัยสำคัญ สนับสนุนว่า PR เป็นเป้าหมายหลักในระดับเซลล์ 19) แม้หลังจากการฟื้นตัวของ EZ การบางลงของ ONL และความหนาแน่นของ PR ที่ลดลงยังคงอยู่ ซึ่งอาจทำให้เกิดการแยกกันระหว่างการฟื้นตัวทางสัณฐานวิทยาและความผิดปกติทางการทำงาน
ในการทบทวนของ Qian และคณะ มีการกล่าวว่า “AZOOR เป็นรูปแบบเฉพาะของ AIR” และเสนอกลไกที่แอนติบอดีรั่วจากขอบจานประสาทตา และแพร่กระจายไปใต้จอประสาทตา ทำให้เกิดจุดบอดขนาดใหญ่ที่ต่อเนื่องกับเส้นประสาทตา 17)
ความเข้าใจแบบบูรณาการของ AZOOR complex : การสร้างแนวคิดต่อเนื่องที่มีพื้นฐานร่วมกับ MEWDS , AMN , PIC , MFC, AIBSE, AAO R กำลังดำเนินไป 1) 2) การสังเกตเซลล์รับแสง ด้วยทัศนศาสตร์ปรับตัว (AO ) : สามารถมองเห็นความผิดปกติของการเรียงตัวของเซลล์รับแสง ในบริเวณรอยโรค ทำให้สามารถประเมินขอบเขตของรอยโรคอย่างละเอียดได้ความก้าวหน้าของ AO -TFI (การถ่ายภาพจอตา ด้วยทัศนศาสตร์ปรับตัว) : เทคนิคที่ไม่รุกรานและในร่างกายเพื่อสังเกตและวัดปริมาณ RPE และเซลล์รับแสง ในระดับเซลล์ กำลังได้รับความสนใจ 19) การลดลงของความหนาแน่น PR อย่างต่อเนื่องหลังจากการฟื้นตัวทางสัณฐานวิทยาของ EZ ได้รับการพิสูจน์โดยตรงเป็นครั้งแรก ซึ่งมีส่วนช่วยในการทำความเข้าใจ “การแยกตัวของโครงสร้าง-หน้าที่”การประเมินคอริโอแคปิลลาริสด้วย OCT -A : กำลังมีการวิจัยเพื่ออธิบายบทบาทของการไหลเวียนเลือดคอรอยด์ 2) บริเวณ flow void ใน OCT -A อาจเป็นตัวบ่งชี้สำหรับการประเมินพยาธิสภาพการติดตามการวินิจฉัยและการรักษาด้วย OCTA : ลักษณะ “ท้องฟ้าเต็มไปด้วยดวงดาว” (starry-sky) ในชั้นจอตาชั้นนอกแบบ en-face อาจมีประโยชน์ในการช่วยวินิจฉัย AZOOR และติดตามการตอบสนองต่อการรักษา 16) การจำแนกชนิดย่อยของโรคด้วยการถ่ายภาพหลายรูปแบบ : Mrejen และคณะ (2014) เสนอระบบการจำแนก AZOOR ตามการถ่ายภาพหลายรูปแบบ 6) ซึ่งช่วยให้เข้าใจความสัมพันธ์ระหว่างชนิดย่อยและการพยากรณ์โรคได้ดีขึ้นการรับรู้และการจำแนกชนิดย่อยของ AZOOR : การรับรู้สภาวะทางพยาธิสภาพที่หลากหลายกำลังเพิ่มขึ้น รวมถึงชนิดย่อยที่เริ่มต้นจากรอบนอก (การลุกลามเข้าสู่ศูนย์กลาง, ไม่เกี่ยวข้องกับบริเวณรอบหัวประสาทตา) 11) ความสัมพันธ์ระหว่าง AZOOR และ np-AIR ทุติยภูมิ : มีข้อเสนอว่าการดำเนินโรคของ AZOOR อาจทำให้เกิด np-AIR ทุติยภูมิ (จอตาอักเสบจากภูมิคุ้มกันตนเองที่ไม่สัมพันธ์กับเนื้องอก) ซึ่งเปิดโอกาสสำหรับการบำบัดด้วยภูมิคุ้มกันรวมถึง IVIg 17) การสร้างหลักฐานสำหรับการรักษาด้วยสเตียรอยด์ : ปัจจุบันยังไม่มีการทดลองแบบสุ่มและมีกลุ่มควบคุม (RCT) และการรวบรวมรายงานผู้ป่วยเป็นความท้าทาย 4) ตัวบ่งชี้ทางชีวภาพ สำหรับการพยากรณ์โรคระยะยาวOCT และรูปแบบ mfERG กำลังถูกศึกษาเป็นตัวบ่งชี้เพื่อทำนายความแตกต่างระหว่างกรณีที่ฟื้นตัวเองและกรณีที่ดำเนินโรค 4) 7) ข้อมูลกลุ่มผู้ป่วยชาวญี่ปุ่น : ข้อมูลการติดตามระยะยาวของผู้ป่วย AZOOR ชาวญี่ปุ่นโดย Saito และคณะ มีส่วนช่วยในการระบุปัจจัยพยากรณ์โรค 4) 9) ประเด็นที่ยังไม่ได้รับการแก้ไข : การกำหนดวิธีการรักษาผ่าน RCT, การอธิบายสาเหตุอย่างสมบูรณ์ (ไวรัสเทียบกับภูมิคุ้มกันตนเอง), การตรวจสอบผลของการแทรกแซงตั้งแต่เนิ่นๆ ต่อการปรับปรุงการพยากรณ์โรค และการพัฒนาตัวบ่งชี้ทางชีวภาพ เพื่อการวินิจฉัย
日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(AZOOR complex 鑑別表を含む). 日本眼科学会雑誌. 2019;123(6):635-696.
Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
Gass JD. Acute zonal occult outer retinopathy. Donders Lecture: The Netherlands Ophthalmological Society, Maastricht, Holland, June 19, 1992. J Clin Neuroophthalmol. 1993;13(2):79-97.
Saito S, Saito W, Saito M, et al. Acute zonal occult outer retinopathy in Japanese patients: clinical features, visual function, and factors affecting visual function. PLoS One. 2015;10(4):e0125133.
Saito W, Kase S, Fujiya A, et al. Multimodal imaging in acute zonal occult outer retinopathy. Br J Ophthalmol. 2019;103(7):908-913.
Mrejen S, Khan S, Gallego-Pinazo R, et al. Acute zonal occult outer retinopathy: a classification based on multimodal imaging. JAMA Ophthalmol. 2014;132(9):1089-1098.
Gass JD, Agarwal A, Scott IU. Acute zonal occult outer retinopathy: a long-term follow-up study. Am J Ophthalmol. 2002;134(3):329-339.
Makino S, Tampo H. Optical coherence tomography and electroretinographic findings in patients with acute zonal occult outer retinopathy. Clin Ophthalmol. 2013;7:1.
Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
Li D, Kishi S. Loss of photoreceptor outer segment in acute zonal occult outer retinopathy. Arch Ophthalmol. 2007;125(9):1194-1200.
Ünlü BH, Karti O, Saatci AO . A case of an acute zonal occult outer retinopathy variant characterized with an insidious peripheral onset and centripetal progression. Cureus. 2024;16(5):e59600.
Ahmed Y, Sayal A, Kaplan AJ, Micieli JA. Monocular temporal hemianopia due to acute zonal occult outer retinopathy. Case Rep Ophthalmol. 2022;13(1):44-9.
Karska-Basta I, Romanowska-Dixon B, Pojda-Wilczek D, et al. Acute zonal occult outer retinopathy in a patient suffering from epilepsy: five-year follow-up. Medicina. 2021;57(11):1276.
Fung AT, Lo-Cao E, Cornish EE. Acute zonal occult outer retinopathy-like presentation secondary to scleral buckle. Am J Ophthalmol Case Rep. 2022;28:101716.
Roy R, Dutta Majumder P. Current understanding of acute zonal occult outer retinopathy (AZOOR ). Indian J Ophthalmol. 2024;72(7):935-7.
Özyol E, Özyol P. Acute zonal occult outer retinopathy: optical coherence tomography angiography findings and treatment response. GMS Ophthalmol Cases. 2022;12:Doc16.
Khan S, Saigal K, Moxam J, Maleki A. A case of concomitant acute zonal occult outer retinopathy and secondary nonparaneoplastic autoimmune retinopathy. Case Rep Ophthalmol. 2025;16(1):124-32.
Herbort CP Jr, Arapi I, Papasavvas I, Mantovani A, Jeannin B. Acute zonal occult outer retinopathy (AZOOR ) results from a clinicopathological mechanism different from choriocapillaritis diseases: a multimodal imaging analysis. Diagnostics. 2021;11(7):1184.
Iuliano M, Lombardo M, Falsini B, et al. Structural, functional, and cellular analysis of a case of acute zonal occult outer retinopathy (AZOOR ). Biomedicines. 2025;13(7):1521.