발병 시

급성 대상성 잠재 망막 외층증 (AZOOR)
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 급성 대상 잠재성 망막외층증이란?
섹션 제목: “1. 급성 대상 잠재성 망막외층증이란?”급성 대상 잠재성 망막외층증(acute zonal occult outer retinopathy; AZOOR)은 1990년대 Gass가 제안하고 질환 개념을 확립한 급성 염증성 질환입니다3). 안저 소견이 거의 정상임에도 불구하고 급성 시야결손, 광시증, 시력저하를 일으키는 것이 특징입니다. 시세포 및 망막 외층의 장애가 주된 병변이며, 그 이름대로 ‘잠재성(occult)’ 외망막증입니다.
일본안과학회에서 AZOOR의 진단 가이드라인이 작성되었으며, 중증 분류로 ‘좋은 눈의 교정시력 < 0.3’이 정의되어 있습니다. 포도막염 진료 가이드라인(일안회지 2019;123(6):635-696)의 AZOOR 복합체 감별표(표3)에도 AZOOR가 수록되어 있습니다1). 안저 소견으로 설명할 수 없는 시야 이상을 발견했을 때, 감별 진단에 AZOOR의 가능성을 항상 고려해야 합니다.
AZOOR는 AZOOR 복합체(MEWDS, AZOOR, AMN, PIC, MFC, AIBSE, AAOR)의 한 질환으로 위치하며, 이 질환군은 외망막, 시세포, RPE를 주된 병변 부위로 하는 염증성 질환의 연속체(스펙트럼)로 이해됩니다1)2). 다중모드 영상의 발전으로 AZOOR 복합체의 통합적 병태 이해가 깊어지고 있습니다2).
다음과 같은 AZOOR 변이형이 보고되었습니다1):
- AAOR (급성 환상 외층 망막병증): 편측성, 환상 회백색 경계선, 구심성 진행
- MORR (다발성 외층 망막색소상피병증): 급성 발병, 진행성, RPE 관여
- 말단 발병형: 드문 변이. 유두주위는 비침범, 말단에서 구심성으로 진행 11)
- 호발: 젊은 여성의 근시안
- 환자의 약 3/4가 여성이며, 30대 중반을 중심으로 한 젊은 연령층에 많음
- 단안 발병이 61%로 시작하여, 중앙값 8년 추적 관찰 시 최종적으로 76%가 양안성으로 진행
- 반대안 발병은 평균 50개월 지연됨
- 자가면역 질환 동반: 하시모토병 (가장 많음), 다발성 경화증 1)
- 발병의 약 20%에서 감기 유사 전구 증상 인정
일본인 환자의 임상적 특징에 대해서는 일본인 AZOOR 증례의 코호트 연구(Saito S 등, 2015)가 보고되었으며, 시기능의 자연 경과 및 예후 인자가 검토되고 있습니다 4).
AZOOR의 주요 장애 부위는 시세포(외망막, ellipsoid zone)입니다. 안저의 외관이 정상으로 보여도 OCT에서는 시야 결손 부위에 일치한 ellipsoid zone(IS/OS 라인)의 소실이 확인됩니다. 시세포 내절 외절 접합부의 파괴가 시기능 저하를 일으키기 때문에, 안저가 정상으로 보여도 시력·시야 장애가 발생합니다.
2. 주요 증상 및 임상 소견
섹션 제목: “2. 주요 증상 및 임상 소견”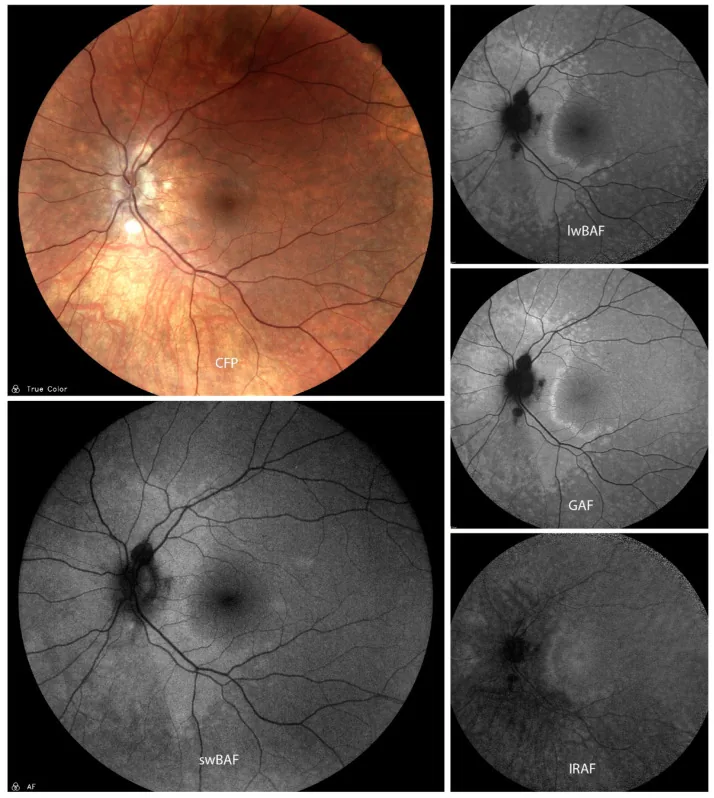
자각 증상
섹션 제목: “자각 증상”- 광시증(Photopsia): 가장 특징적인 증상 중 하나. 급성 발병.
- 급성 시력 저하 및 시야 결손(1~수 개소) 1)
- Mariotte 맹점 확대, 중심 시야 결손, 주변 시야 결손 1)
- 전구 증상: 감기 유사 증상(약 20%에서 발생)
시야 결손은 띠 모양 또는 구역성으로 나타나는 경우가 많으며, 안저가 정상으로 보여 시신경염으로 오진될 수 있습니다 1). Goldmann 시야 검사에서는 Mariotte 맹점의 현저한 확대나 구역성 암점이 확인됩니다.
안저 소견
섹션 제목: “안저 소견”안저는 기본적으로 정상이며, 시신경염과의 감별이 어려운 경우가 있습니다 1). 형광 안저 혈관 조영(FA)에서도 보통 이상이 없는 것이 AZOOR의 중요한 특징입니다. 장기적인 경우 미만성 또는 구역성 맥락망막 위축이 나타날 수 있습니다.
만성기
또한, 단안성 이측 반맹을 나타내는 경우는 비측 망막의 장애에 의한 것이며, 수직 자오선을 존중한 이측 반맹으로 나타날 수 있으므로 시교차 병변을 모방하여 MRI가 필요한 경우도 있습니다12). RAPD(상대적 구심성 동공 장애)는 일부 증례에서 경과 중에 나타날 수 있습니다.
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”병태생리 가설
섹션 제목: “병태생리 가설”원인은 알려져 있지 않지만, 바이러스 감염 또는 자가면역 관여가 주요 가설로 제시되고 있습니다.
- 발병의 약 20%에서 감기 유사 전구 증상 → 바이러스 감염 유발 가설
- 하시모토병, 다발성 경화증과의 동반 → 자가면역 기전 가설1)
- 주요 장애 부위: 시세포(타원체대), RPE, 맥락막 모세혈관판 (여러 설)
AZOOR의 주된 병변 부위에 대해서는 시세포, 망막색소상피, 맥락막 모세혈관판 등 다양한 설이 있으며 아직 결론이 나지 않았습니다. OCT에서 타원체대 소실은 시세포 내절/외절 접합부(IS/OS 라인)의 파괴를 직접 반영하며, 해당 영역의 기능 회복은 어려운 경우가 많습니다8).
위험 요인
섹션 제목: “위험 요인”- 젊은 여성, 근시
- 자가면역 질환 동반(하시모토병, 다발성 경화증)1)
- AZOOR 복합체로서의 유전적 소인 + 환경 요인(바이러스 감염, 자가면역 유발)2)
- 간질: 쥐 연구에서 간질 발작이 망막에 염증 반응을 유도하는 것으로 나타나 관련 가능성이 있음13)
- 공막 돌륭술 후: 수술 후 5년 이상 경과 후 AZOOR 유사 소견이 나타난 증례 보고가 있음14)
Gass의 51예 중 약 28%에서 자가면역 질환의 병력이 있었다. 하시모토병, 다발성 경화증 외에도 그레이브스병, 갑상선 기능 저하증, 애디슨병, 중증 근무력증, 크론병, 전신성 홍반성 루푸스 등이 동반 질환으로 알려져 있다. 항망막 항체는 AZOOR 환자의 약 42%에서 검출된다15).
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”AZOOR의 진단은 20~50세의 젊은 환자에서 급성 단안 시력 저하, 시야 결손, 광시증이 나타날 때 의심하며, OCT와 ERG를 조합하여 시행한다. 안저 소견으로 설명할 수 없는 시야 이상이 있을 때는 적극적으로 AZOOR을 감별 진단에 포함시키는 것이 중요하다.
권장 검사 진행 방법
섹션 제목: “권장 검사 진행 방법”20~50대의 비교적 젊은 환자에서 급성 단안 시력 저하, 시야 결손이 나타나고 광시증을 동반하는 경우, 먼저 OCT를 시행한다. 시야 결손 부위에 일치하여 OCT에서 망막 외층 이상이 보이면 AZOOR이 강력히 의심된다. 이어서 ERG, 다초점 ERG로 확인한다1).
검사 소견
섹션 제목: “검사 소견”| 검사법 | 소견 |
|---|---|
| OCT | 시야 결손 부위에 일치하는 타원체대 소실, interdigitation zone 소실. 예후 예측에 유용5) |
| 전시야 ERG | 광범위 손상 시 진폭 감소. 원추계 이상 > 간상계 |
| 다초점 ERG | 시야 결손 부위에 일치하는 진폭 감소. 좁은 범위 병변 검출에 민감도 높음1) |
| 안저 자가형광(적외선) | 병변부와 정상부 경계 확인 |
| FA | 기본적으로 정상 소견 |
| Goldmann 시야 | Mariotte 맹점 확대, 중심 암점, 구역성 암점1) |
| 적응 광학(AO) | 시세포 배열 이상의 가시화 |
| PERG(패턴 ERG) | P50 감소, N95 정상 패턴을 보일 수 있음 |
| EOG | 광반응(light rise) 감소, Arden 비율 감소를 보일 수 있음 |
OCT는 예후 예측에도 유용합니다. 외층(ellipsoid zone)이 소실된 부위에서는 해당 영역의 기능 회복을 기대할 수 없으므로, OCT에서의 외층 평가가 치료 방침 결정과 예후 설명의 근거가 됩니다 5). 손상 범위가 좁은 경우 전시야 ERG보다 다초점 ERG나 국소 ERG가 진단에 더 유용합니다 1).
감별 진단(포도막염 진료 가이드라인 표3) 1)
섹션 제목: “감별 진단(포도막염 진료 가이드라인 표3) 1)”| 질환 | 감별 포인트 |
|---|---|
| 시신경염 | ERG로 감별. 시신경염에서는 ERG 정상, 안구 운동 시 통증 있음. |
| MEWDS | 백점이 보임(AZOOR는 안저 정상). 다초점 ERG도 저하. |
| AMN | 황반부 적갈색 반점 병변, OCT에서 외핵층 쐐기형 병변. |
| AIBSE | 유두 주위 환상 회백색 혼탁, Mariotte 맹점 확대가 특징적. |
| AAOR | 망막 심층의 환상 회백색 혼탁. |
| 다발성 경화증 | MRI 소견, 전신 증상, 시신경염 소견으로 감별. |
| np-AIR (비종양동반 자가면역망막병증) | 아급성~만성 발병, FAF 미만성 과형광, EOG 정상 |
| 매독성 외층망막병증 (SOR) | AZOOR과 매우 유사. 매독 혈청 검사 필수 1) |
감염 배제를 위해 매독, CMV, VZV, HSV 검사를 시행합니다. 측두반맹이 있는 경우 MRI로 시교차 병변을 배제합니다 12).
5. 표준 치료법
섹션 제목: “5. 표준 치료법”기본 방침
섹션 제목: “기본 방침”확립된 치료법은 없으며, 자연 회복 사례와 시력 예후 불량 사례가 혼재합니다.
- 경증 사례: 치료 없이 경과 관찰
- 중증 사례 (좋은 눈의 최대교정시력 < 0.3): 스테로이드 펄스 요법 고려
자가면역 및 염증이 병인으로 추정되므로, 특히 중증 사례에서 스테로이드 펄스 요법이 시행되기도 합니다. 그러나 회복이 자연 회복인지 스테로이드 효과인지 구분하기 어렵습니다.
스테로이드 펄스 요법 프로토콜
섹션 제목: “스테로이드 펄스 요법 프로토콜”| 투여 경로 | 약제명 | 용량 및 용법 |
|---|---|---|
| 정맥 점적 (펄스) | 메틸프레드니솔론 (솔루메드롤®) | 1,000 mg + 솔리타-T3 500 mL를 1시간에 걸쳐 정맥 점적, 3일간 |
| 경구 (후속 요법) | 프레드니솔론 (프레도닌®) 정 5 mg | 8 |
스테로이드 펄스 요법의 효과는 자연 회복과 구별하기 어려운 측면이 있으며, 증거는 증례 보고 수준에 머물러 있습니다. 현재 무작위 대조 시험(RCT)은 존재하지 않습니다.
유리체강 내 스테로이드 주사
섹션 제목: “유리체강 내 스테로이드 주사”유리체강 내 스테로이드 주사도 보고되었으나, 백내장, 안압 상승, 중심성 장액성 맥락망막병증(CSR) 등의 부작용 위험에 주의해야 합니다16).
면역억제 요법 및 기타
섹션 제목: “면역억제 요법 및 기타”난치성 사례에 대해 다음이 보고되었습니다:
- MMF + 사이클로스포린 + IVIg: 마이코페놀레이트 모페틸 2g/일 + 사이클로스포린 200mg/일 + IVIg 2g/kg 월 1회 병용으로 BCVA 개선이 보고되었습니다17)
- 사이클로스포린: 4.5mg/kg/일 사용 사례가 있습니다
- 아달리무맙 (휴미라): 효과적인 사례가 보고되었습니다
- 항바이러스 요법: 아시클로버와 발라시클로버는 Gass 등의 보고에서 명확한 효과가 나타나지 않았습니다3)
CNVM 동반 증례
섹션 제목: “CNVM 동반 증례”맥락막 신생혈관막(CNVM)이 동반된 경우, 항VEGF 유리체강내 주사(베바시주맙, 아플리버셉트 등)가 적응이 될 수 있습니다 1).
난치성 및 재발성 증례
섹션 제목: “난치성 및 재발성 증례”재발 또는 만성화된 경우 면역억제제(시클로스포린 등) 병용을 고려합니다. AZOOR 복합 관련 질환의 치료에 준한 대응이 참고됩니다.
스테로이드 펄스 요법이 효과적이라는 증례 보고는 있으나 무작위 비교 시험은 존재하지 않으며, 자연 회복과의 구별이 어렵습니다. 중증 증례(좋은 눈의 교정시력 < 0.3)에 한해 시행을 고려하지만, 치료해도 외층 망막 소실이 지속되는 예에서는 시력 예후가 불량합니다. OCT에서 ellipsoid zone이 소실된 부위의 기능 회복은 어려운 경우가 많습니다 8).
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”AZOOR의 병태는 광수용체 및 ellipsoid zone(IS/OS 접합부)의 급성 장애입니다.
장애 부위와 OCT의 관계
섹션 제목: “장애 부위와 OCT의 관계”OCT ellipsoid zone의 소실은 광수용체 내절/외절 접합부(IS/OS 라인)의 파괴를 직접 반영합니다. 이 영역이 소실된 부위에서는 광수용체의 회복이 어렵고 장기적인 시기능 장애의 원인이 됩니다 5)8). 경증 증례나 회복기에서는 interdigitation zone만 이상을 보이고 ellipsoid zone은 유지되는 경우가 있습니다.
발병 기전
섹션 제목: “발병 기전”- 바이러스 감염(약 20%에서 감기 유사 전구 증상) 또는 자가면역(하시모토병, 다발성 경화증 동반)이 관여합니다.
- 주요 장애 부위: 광수용체 내절/외절 접합부(ellipsoid zone). OCT에서의 소실이 직접 반영됩니다.
- 맥락막모세혈관판의 관여에 대한 여러 설이 있지만, OCT-A에서는 맥락막모세혈관이 보존되거나 경미한 변화에 그치는 경우가 많다2)
- AZOOR 복합체의 한 질환으로, 유전적 소인 + 환경 요인(바이러스 감염, 자가면역)으로 발병한다2)
AZOOR 복합체로서의 이해
섹션 제목: “AZOOR 복합체로서의 이해”AZOOR 복합체(MEWDS, AZOOR, AMN, PIC, MFC, AIBSE, AAOR)는 동일한 질병 스펙트럼상에 있는 관련 질환으로 간주되며, 외망막과 RPE를 주요 부위로 하는 염증성 장애라는 공통 기반을 가진다2). Jampol과 Becker(2003)는 이러한 백점증후군이 공통의 유전적 자가면역/염증 기전에 기반한다는 가설을 제안했다10).
자가면역 질환과의 연관성
섹션 제목: “자가면역 질환과의 연관성”하시모토병이 가장 흔히 동반되는 자가면역 질환이며, 다음으로 다발성 경화증이 많다. 이러한 동반은 자가면역 기전에 의한 시세포 및 외망막 공격을 시사하며, AZOOR의 병태 이해에 중요한 단서를 제공한다.
타원체대 소실이 지속되는 부위에서는 시세포의 회복이 어렵고, OCT 평가가 장기 예후 예측에 직접 연결된다.
일차 병변 부위: 광수용체 외절
섹션 제목: “일차 병변 부위: 광수용체 외절”다중모드 영상 분석을 통해 AZOOR의 일차 병변 부위는 광수용체 외절임이 밝혀졌다18). ICG 형광 조영술에서 맥락막모세혈관이 보존되어 있어, 맥락막 모세혈관은 초기에 손상되지 않는다. FAF 과형광은 광수용체 외절 소실로 인해 RPE의 리포푸신이 노출되어 발생한다. 맥락막은 이차적으로 손상(부수적 손상)되며, 진행된 경우 맥락망막 위축으로 이어진다.
적응광학 안저촬영(AO-TFI)을 통한 정량 분석에서는 광수용체(PR) 밀도가 유의하게 감소하는 반면, RPE 밀도는 유의한 차이가 없음이 확인되어, PR이 일차 표적임을 세포 수준에서 지지한다19). EZ 회복 후에도 ONL 얇아짐과 PR 밀도 감소가 지속되며, 형태적 회복과 기능적 장애 사이에 괴리가 발생할 수 있다.
Qian 등의 리뷰에서는 “AZOOR는 AIR의 특이적 형태”라고 주장하며, 시신경 유두 가장자리에서 항체 누출을 통해 면역 산물이 망막하로 확산되어 시신경에 연속되는 큰 암점을 형성한다는 기전이 제안되었다17).
7. 최신 연구와 향후 전망
섹션 제목: “7. 최신 연구와 향후 전망”- AZOOR 복합체의 통합 이해: MEWDS, AMN, PIC, MFC, AIBSE, AAOR와 공통 기반을 가진 연속체 개념의 확립이 진행 중이다1)2)
- 적응광학(AO)을 이용한 시세포 관찰: 병변 부위의 시세포 배열 이상을 시각화할 수 있어 병변 범위의 상세 평가가 진행되고 있습니다.
- AO-TFI(적응광학 안저촬영)의 발전: 비침습적, 생체 내에서 RPE 및 광수용체를 세포 수준에서 관찰하고 정량화할 수 있는 기술로 주목받고 있습니다19). EZ가 형태적으로 회복된 후에도 PR 밀도 감소가 지속된다는 사실이 처음으로 직접 증명되어 ‘구조-기능 해리’ 규명에 기여했습니다.
- OCT-A 맥락막모세혈관 평가: 맥락막 혈류의 관련성을 규명하기 위한 연구가 진행 중입니다2). OCT-A flow void가 병태 평가의 지표가 될 가능성이 있습니다.
- OCTA를 통한 진단 및 치료 모니터링: En-face 외망막 슬라이브에서의 별하늘 모양은 AZOOR의 진단 보조 및 치료 반응 모니터링에 활용될 가능성이 있습니다16).
- 다중모드 영상을 통한 병형 분류: Mrejen 등(2014)은 AZOOR의 다중모드 영상 기반 분류 체계를 제안했습니다6). 이를 통해 병형과 예후의 관련성 규명이 진행되고 있습니다.
- AZOOR 변이형의 인식과 분류: 말초 발병형 변이(구심성 진행, 유두주위 비침범)를 비롯한 다양한 병태에 대한 인식이 진행되고 있습니다11).
- AZOOR와 이차성 np-AIR의 연관성: AZOOR가 진행됨에 따라 이차성 np-AIR(비종양연관 자가면역 망막병증)을 유발할 가능성이 제기되었으며, IVIg를 포함한 면역요법에의 응용이 기대됩니다17).
- 스테로이드 치료의 근거 구축: 현재 RCT는 존재하지 않으며, 증례 보고의 축적이 과제입니다4).
- 장기 예후 바이오마커: 자연 회복 예와 진행 예의 차이를 예측하는 지표로서 OCT에서의 타원체대 보존, 다초점 ERG 패턴의 활용이 검토되고 있습니다4)7).
- 일본인 증례 코호트 데이터: Saito 등에 의한 일본인 AZOOR 환자의 장기 추적 데이터가 예후 인자 식별에 기여하고 있습니다4)9).
- 미해결 과제: RCT에 의한 치료법 확립, 병인(바이러스 vs 자가면역)의 완전 규명, 조기 중재의 예후 개선 효과 검증, 진단 바이오마커 개발.
8. 참고문헌
섹션 제목: “8. 참고문헌”- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(AZOOR complex 鑑別表を含む). 日本眼科学会雑誌. 2019;123(6):635-696.
- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- Gass JD. Acute zonal occult outer retinopathy. Donders Lecture: The Netherlands Ophthalmological Society, Maastricht, Holland, June 19, 1992. J Clin Neuroophthalmol. 1993;13(2):79-97.
- Saito S, Saito W, Saito M, et al. Acute zonal occult outer retinopathy in Japanese patients: clinical features, visual function, and factors affecting visual function. PLoS One. 2015;10(4):e0125133.
- Saito W, Kase S, Fujiya A, et al. Multimodal imaging in acute zonal occult outer retinopathy. Br J Ophthalmol. 2019;103(7):908-913.
- Mrejen S, Khan S, Gallego-Pinazo R, et al. Acute zonal occult outer retinopathy: a classification based on multimodal imaging. JAMA Ophthalmol. 2014;132(9):1089-1098.
- Gass JD, Agarwal A, Scott IU. Acute zonal occult outer retinopathy: a long-term follow-up study. Am J Ophthalmol. 2002;134(3):329-339.
- Makino S, Tampo H. Optical coherence tomography and electroretinographic findings in patients with acute zonal occult outer retinopathy. Clin Ophthalmol. 2013;7:1.
- Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
- Li D, Kishi S. Loss of photoreceptor outer segment in acute zonal occult outer retinopathy. Arch Ophthalmol. 2007;125(9):1194-1200.
- Ünlü BH, Karti O, Saatci AO. A case of an acute zonal occult outer retinopathy variant characterized with an insidious peripheral onset and centripetal progression. Cureus. 2024;16(5):e59600.
- Ahmed Y, Sayal A, Kaplan AJ, Micieli JA. Monocular temporal hemianopia due to acute zonal occult outer retinopathy. Case Rep Ophthalmol. 2022;13(1):44-9.
- Karska-Basta I, Romanowska-Dixon B, Pojda-Wilczek D, et al. Acute zonal occult outer retinopathy in a patient suffering from epilepsy: five-year follow-up. Medicina. 2021;57(11):1276.
- Fung AT, Lo-Cao E, Cornish EE. Acute zonal occult outer retinopathy-like presentation secondary to scleral buckle. Am J Ophthalmol Case Rep. 2022;28:101716.
- Roy R, Dutta Majumder P. Current understanding of acute zonal occult outer retinopathy (AZOOR). Indian J Ophthalmol. 2024;72(7):935-7.
- Özyol E, Özyol P. Acute zonal occult outer retinopathy: optical coherence tomography angiography findings and treatment response. GMS Ophthalmol Cases. 2022;12:Doc16.
- Khan S, Saigal K, Moxam J, Maleki A. A case of concomitant acute zonal occult outer retinopathy and secondary nonparaneoplastic autoimmune retinopathy. Case Rep Ophthalmol. 2025;16(1):124-32.
- Herbort CP Jr, Arapi I, Papasavvas I, Mantovani A, Jeannin B. Acute zonal occult outer retinopathy (AZOOR) results from a clinicopathological mechanism different from choriocapillaritis diseases: a multimodal imaging analysis. Diagnostics. 2021;11(7):1184.
- Iuliano M, Lombardo M, Falsini B, et al. Structural, functional, and cellular analysis of a case of acute zonal occult outer retinopathy (AZOOR). Biomedicines. 2025;13(7):1521.
