급성기 소견

다발성 소실성 백점 증후군(MEWDS)
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 다발소실성백점증후군이란?
섹션 제목: “1. 다발소실성백점증후군이란?”다발소실성백점증후군(multiple evanescent white dot syndrome; MEWDS)은 1984년 Jampol 등이 처음 보고한7) 급성 염증성 질환입니다. 근시인 젊은 여성의 한쪽 눈에 호발하며, 안저 후극부에서 적도부까지 망막 심층~RPE 수준의 다수의 희미한 회백색 반점이 나타납니다. 수주 경과에 따라 백색 반점은 거의 소실되고 시력도 개선되는 자연 회복형 질환입니다.
포도막염 진료 가이드라인(일안회지 2019;123(6):635-696)에서의 분류는 비감염성·안저 병변 위주의 후포도막염으로 위치되며, 단안성·급성 발병·일과성 경과라는 특성이 기재되어 있습니다1).
MEWDS는 AZOOR 복합체(MEWDS, AZOOR, AMN, PIC, MFC, AIBSE, AAOR)의 한 질환으로 위치되며, 이 질환군은 외망막·시세포·RPE를 주 병변으로 하는 염증성 질환의 연속체(스펙트럼)로 간주됩니다2). 백점증후군 중에서도 MEWDS는 다중모드 영상으로 병태생리가 가장 밝혀진 질환 중 하나입니다2).
- 호발 연령: 20~50대
- 성비: 여성에 압도적으로 많으며 남녀 비 1:41)
- 연간 발병률: 인구 10만 명당 약 0.22예10)
- 근시안에 호발하며, 단안성인 경우가 많음
- 절반의 증례에서 발병 1~2주 전에 감기 유사 전구 증상이 나타남1)
- 선행 요인으로 감기 유사 증상 외에도 경구 피임약 복용, 백신 접종, 상기도 감염이 알려져 있음1)
- 양안성은 극히 드물며, 문헌상 6~7예에 불과함2, 4). 양안성인 경우 항상 좌우 비대칭 경과를 보임
- 비전형적인 연령의 증례도 보고되었으며, 최연소는 9세 여아13), 최고령은 75세 남성임10)
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”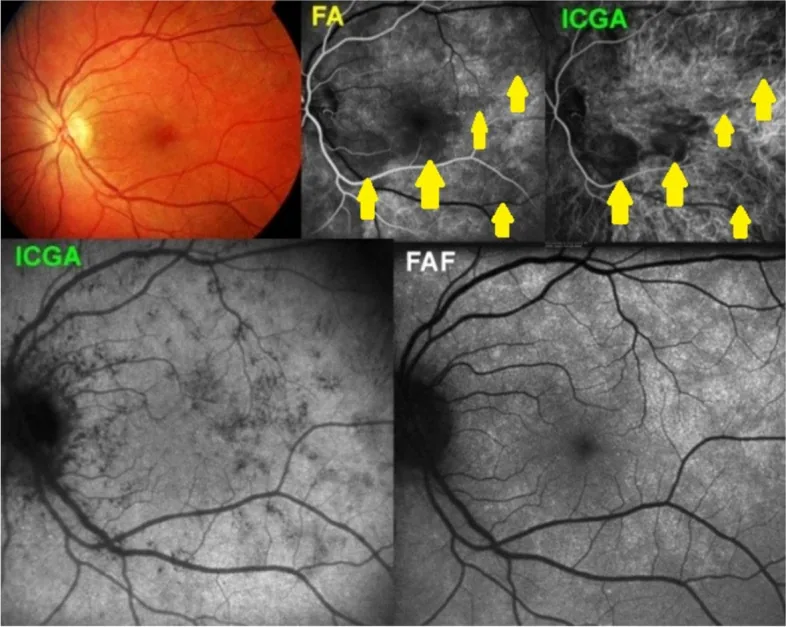
자각 증상
섹션 제목: “자각 증상”- 급성 단안 시력 저하, 시야 흐림, 광시증, 비문증, 시야 결손1)
- Mariotte 맹점 확대, 중심 암점, 시야 협착1)
- 급성기 ERG 또는 다초점 ERG에서 황반부 부근의 진폭 현저한 평탄화1)
안저 소견
섹션 제목: “안저 소견”후극부에서 적도부에 걸쳐 망막 심층에서 RPE에 산재하는 옅은 반점상 병소가 다발한다1). 흰 반점의 크기는 100200μm로 크기가 다양하며 서로 융합되기도 한다. 시신경 유두 경미한 발적, 경미한 유리체 세포가 나타날 수 있다1). 중심와 과립상 변화(foveal granularity; 오렌지노란색 과립상 외관)는 근적외선 FAF로 확인할 수 있는 진단적 소견이며, 증례의 74~96%에서 나타나고, 흰 반점 소실 후에도 유일한 소견일 수 있다2)5).
기타 임상 소견은 다음과 같다.
- 상대적 구심성 동공 장애(RAPD): 드물게 양성
- 시신경 유두 부종: 유두 주변 장액성 망막하액을 동반할 수 있음
- 망막 정맥 혈관초 및 망막 출혈: 드문 소견
관해기 소견
광시증은 외망막과 타원체대(ellipsoid zone, 광수용체 내절-외절 접합부)의 손상으로 인해 발생하는 것으로 생각됩니다. 광수용체가 제대로 기능하지 않으면 비정상적인 광자극 신호가 생성되어 존재하지 않는 빛이 보이는 것처럼 느껴집니다. 일반적으로 질환이 회복됨에 따라 사라집니다.
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”병태생리
섹션 제목: “병태생리”MEWDS의 주요 병변 부위는 외망막과 타원체대(IS/OS)이며, 맥락막모세혈관판은 원칙적으로 보존됩니다2). ICGA 후기 저형광이 관찰되지만, 이는 맥락막모세혈관판의 허혈보다는 RPE 기능 장애로 인한 색소 섭취 이상으로 인해 발생할 가능성이 제기되었습니다2). 맥락막모세혈관판 손상(ICGA 소견)은 흰 점이 없는 시신경유두 주변에서도 관찰되며, 임상적으로 보이는 병변보다 더 광범위할 수 있습니다1).
유발 요인 및 위험 인자
섹션 제목: “유발 요인 및 위험 인자”- 원인 불명. 자가면역 또는 바이러스 감염 유발 가설이 있습니다.
- 선행 요인: 감기 유사 증상(인플루엔자, 볼거리 등), 경구 피임약 복용, 예방접종, 상기도 감염1)
- 근시안(특히 중등도~고도 근시)
- AZOOR 복합체의 한 질환으로, 유전적 소인(예: IL-10 일배체형)과 환경적 요인(바이러스, 백신, 약물)이 결합하여 발병하는 것으로 생각됩니다2)7)
- 예방접종: B형 간염, 인플루엔자, HPV, 수막구균, COVID-19 백신 접종 후 발병이 보고되었습니다15, 11). 예방접종부터 MEWDS 발병까지의 중앙값은 14일(범위 1~90일)로 보고되었습니다.
- COVID-19 감염: SARS-CoV-2 감염 후 MEWDS 발병 사례가 여러 건 보고되었으며, COVID-19 팬데믹 기간 동안 MEWDS 보고 수가 유의하게 증가했습니다14). 감염 후 발병까지 평균 29.6일(범위 0~70일)입니다.
면역학적 기전으로, 백신 유래 mRNA가 RIG-I를 통해 I형 인터페론(IFN-I)을 유도하여 RPE 세포의 장벽 기능 장애를 일으킬 가능성이 제시되었습니다15). 분자 모방(molecular mimicry)이나 아주반트 매개 염증도 추정됩니다. MEWDS 환자에서 HLA-B51 일배체형의 빈도가 정상군보다 3.5배 높다는 예비 보고도 있습니다12).
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”MEWDS의 진단은 특징적인 안저 소견과 다중 모드 영상을 통해 이루어집니다.
영상 검사
섹션 제목: “영상 검사”| 검사법 | 특징적 소견 |
|---|---|
| FA | 백반 부위는 조영 초기부터 화환 모양의 과형광을 보이며 후기까지 지속됩니다. 시신경 유두 누출이 있습니다2)6) |
| ICGA | 백반 부위는 후기 저형광을 보입니다. 임상 소견보다 광범위한 저형광 영역이 나타납니다. 유두 주변에도 저형광 반점이 나타납니다1)2) |
| FAF (안저 자가형광) | 급성기에 고자가형광을 보입니다. 저형광과 과형광이 혼재됩니다. 진단에 유용합니다1)2) |
| SD-OCT | 활동기에 타원체대의 현저한 혼란·소실, RPE의 국소적 비후가 나타납니다2)3) |
| OCT-A | 맥락막모세혈관 혈류는 원칙적으로 유지됩니다 (일부에서 flow void 보고 있음)4)8) |
| 다초점 ERG | 황반부 진폭 평탄화(급성기). 회복과 함께 정상화 1) |
| Goldmann 시야 | Mariotte 맹점 확대, 중심암점 1) |
진단의 포인트
섹션 제목: “진단의 포인트”MEWDS의 특징으로 FA에서 초기부터 과형광을 보이는 점이 APMPPE와의 중요한 감별점이다. APMPPE는 조영 초기 저형광 → 후기 과형광의 역전 현상을 보이는 반면, MEWDS는 초기부터 과형광이 지속된다 2)6). 또한 OCT에서는 활동기에 ellipsoid zone(IS/OS선)이 불규칙해지지만, 이 불규칙성이 개선됨에 따라 시력이 회복되는 것이 병태 이해에 중요한 소견이다 3).
감별 진단(포도막염 진료 가이드라인 ‘표3’에서) 1)
섹션 제목: “감별 진단(포도막염 진료 가이드라인 ‘표3’에서) 1)”| 질환 | 감별 포인트 |
|---|---|
| APMPPE | 양안성, 대형 플라크, FA 형광 역전(초기 저형광 → 후기 과형광) |
| AZOOR | 안저 정상, ERG 이상만 있음 |
| AIBSE | 유두 주위 환상 회백색 혼탁, Mariotte 맹점 확대 |
| AMN | 황반부 적갈색 반점 병변 |
| AAOR | 망막 심층의 환상 회백색 혼탁 |
| PIC | 중등도 근시 여성, 후극부 소형 황백반, CNV 합병률 높음, 양안성 많음 |
| 산탄맥락망막병증/다초점맥락막염 | 염증 지속, 양안성 |
| 유육종증/안내림프종 | 전신 합병, 염증 지속 |
5. 표준 치료법
섹션 제목: “5. 표준 치료법”기본 방침
섹션 제목: “기본 방침”특별한 치료 없이 자연 치유가 기대되므로, 경증 증례는 경과 관찰이 기본입니다1). 흰 반점은 수주 내에 자연 소실되며 시력 예후는 양호합니다. 경과에 따라 ERG는 진정되고 정상화됩니다1).
항염증 치료의 적응증
섹션 제목: “항염증 치료의 적응증”시력 저하가 현저하거나 유두부종이 동반된 경우에만 다음을 고려합니다.
- 경구 프레드니솔론: 30 mg/일부터 점감. 시력 저하가 현저하거나 유두부종이 동반된 예에 단기 사용을 목표로 합니다.
- 칼나크린 정: 미세순환 개선을 목적으로 병용되는 경우가 있습니다.
- 자연 회복 경향이 강한 질환이므로 대부분의 증례에서는 치료가 필요하지 않습니다1).
- 경과에 따라 ERG는 정상화되고 시력 회복이 기대됩니다1).
COVID-19 관련 MEWDS 7예의 리뷰에서 5예(71%)가 어떤 형태로든 치료를 받았으며, COVID-19 관련 예는 바이러스성 MEWDS 전반에 비해 다소 중증화될 가능성이 시사됩니다14). 불완전한 시력 회복 예도 보고되어 있어, COVID-19 관련 예에는 주의 깊은 경과 관찰이 필요합니다.
만성 재발 예
섹션 제목: “만성 재발 예”재발은 10% 미만이지만, 만성 재발 예에는 사이클로스포린 사용이 보고되어 있습니다2).
CNV 동반 예
섹션 제목: “CNV 동반 예”맥락막 신생혈관이 동반된 경우 항VEGF 약물 유리체내 주사(베바시주맙, 라니비주맙, 애플리버셉트)를 고려합니다1). CNV 동반은 드물지만 시력 예후 불량의 원인이 되므로 주의가 필요합니다. CNV 활동성 평가에는 OCT-A가 유용하며, 항VEGF 요법의 치료 판단 및 효과 판정에 도움이 됩니다8).
기본적으로 자연 회복 경향이 강한 질환이므로 대부분의 경우 치료가 필요하지 않습니다. 포도막염 진료 가이드라인에서도 ‘특별한 치료 없이 자연 회복’이 기본 방침으로 되어 있습니다1). 시력 저하가 현저한 중증 예나 유두부종을 동반한 예에 한해 스테로이드 경구 투여로 회복을 빠르게 하는 경우가 있습니다.
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”MEWDS의 주요 손상 부위는 외망막과 타원체대(IS/OS 접합부)이며, 맥락막모세혈관판은 원칙적으로 보존됩니다2). 이는 APMPPE와의 중요한 병태적 차이입니다.
외망막 및 타원체대 손상
섹션 제목: “외망막 및 타원체대 손상”OCT 소견에서 활동기에는 타원체대(망막 광수용체 내절/외절 접합부)가 불규칙해지거나 소실됩니다. 이러한 혼란이 호전됨에 따라 시력이 회복된다고 보고되어 있으며, 외망막 손상의 일과성 및 가역성이 MEWDS의 본질입니다3). 최근의 en face swept-source OCT는 기존의 단층 영상으로 인식하기 어려웠던 병변 범위의 확장도 가시화하고 있습니다3).
ICGA와 맥락막모세혈관
섹션 제목: “ICGA와 맥락막모세혈관”ICGA 후기 저형광이 관찰되지만, 이는 맥락막모세혈관판의 허혈보다는 RPE 기능 장애로 인한 색소 섭취 이상에 의해 발생할 가능성이 지적되고 있습니다2). OCT-A에서는 맥락막모세혈관판의 혈류가 원칙적으로 보존되며, 일부 증례에서만 일시적인 flow void가 보고되었습니다4)8). Swept-source OCT-A를 이용한 연구에서는 MEWDS에서 맥락막모세혈관의 보존이 확인되었습니다4).
중심와 과립상 변화 (foveal granularity)
섹션 제목: “중심와 과립상 변화 (foveal granularity)”근적외선 FAF에서 확인되는 중심와 과립상 변화는 중심와 광수용체층의 손상을 반영하는 특징적인 소견입니다2)5). 멀티컬러 이미징(근적외선 반사 및 청색 반사)에서도 확인할 수 있으며, 활동기 진단에 유용한 것으로 알려져 있습니다.
AZOOR 복합체로서의 위치
섹션 제목: “AZOOR 복합체로서의 위치”AZOOR 복합체로서 MEWDS, AZOOR, PIC, MFC 등을 통합적으로 보는 개념이 제안되었으며, 유전적 소인(IL-10 일배체형 등)에 다양한 환경 요인(바이러스 감염, 백신, 약물)이 더해져 발병하는 것으로 생각됩니다2)7). Jampol과 Becker(2003)는 이러한 질환들이 공통의 유전적 자가면역/염증 기전에 기반한다는 가설을 제안했습니다7).
7. 최신 연구와 향후 전망
섹션 제목: “7. 최신 연구와 향후 전망”- OCT-A를 통한 맥락막모세혈관 기능 평가: swept-source OCT-A로 맥락막모세혈관의 flow void를 일시적으로 검출한 보고가 있으며, 맥락막모세혈관판의 관여에 대한 재평가가 진행 중입니다4)8). 일부 증례에서는 맥락막모세혈관의 혈류 감소도 관찰되어 병태의 다양성이 시사됩니다8).
- En face swept-source OCT: 백점 병변의 형태, 분포, 내층 경계를 3차원적으로 가시화하는 새로운 진단 방법으로 보고가 증가하고 있습니다3).
- AZOOR 복합체 개념의 발전: MEWDS, AZOOR, PIC, AMN, AIBSE, AASR을 단일 스펙트럼으로 통합적으로 이해하는 연구가 진행되고 있습니다2)9). Zicarelli 등(2020)은 MEWDS의 병태에 대한 새로운 해석을 제안했습니다9).
- 멀티컬러 이미징: 근적외선 반사 및 청색 반사를 이용한 임상 진단 보조 도구 개발. 중심와 과립(foveal granularity)의 비침습적 평가가 가능해졌습니다5).
- COVID-19 감염 후 또는 백신 후 MEWDS: 감염 후 또는 mRNA 백신 접종 후 발병 사례가 전 세계적으로 증가하고 있으며, 면역 유발 요인으로서의 위치에 주목이 집중되고 있습니다.
- 재발률 및 장기 예후 데이터: 대규모 장기 추적 연구의 축적이 기다려집니다.
COVID-19와 MEWDS의 연관성
섹션 제목: “COVID-19와 MEWDS의 연관성”Chen 등(2024)은 COVID-19 감염 후 발생한 MEWDS 7예를 문헌적으로 검토하여 평균 연령 38.4세, 여성 5예, 평균 감염-발병 간격 29.6일임을 보고했습니다14). 2예(29%)가 양안성이었고, 5예(71%)가 치료를 받았으며, COVID-19 관련 예에서는 불완전한 시력 회복 및 치료 개입의 필요성이 일반 예보다 높을 가능성을 시사했습니다.
COVID-19 백신 관련 MEWDS에 대해서는 27예의 체계적 검토가 있으며, 중앙값 연령 34.1세, 여성 우세, 접종부터 발병까지 중앙값 14.7일이었습니다14). mRNA 백신(Pfizer-BioNTech)이 가장 많았습니다.
백신 접종과 재발
섹션 제목: “백신 접종과 재발”Ramirez Marquez 등(2022)은 HPV 백신과 수막구균 백신을 동시 접종한 후 MEWDS가 발생하고, 이후 COVID-19 감염 및 BNT162b2 백신 접종을 거쳐 반대쪽 눈에 2회 재발을 보인 17세 여성을 보고했습니다11).
비전형적 증례 보고
섹션 제목: “비전형적 증례 보고”Yasuda 등(2022)은 BNT162b2 mRNA 백신 2차 접종 다음 날 MEWDS가 발생한 67세 일본 여성을 보고했습니다 15). 중등도의 유리체염을 동반하였고 시력이 0.2까지 감소했으나 치료 없이 0.8까지 회복되었습니다.
Wiley 등(2022)은 17세 여성이 SARS-CoV-2 백신 접종 2일 후 양안 시신경유두부종과 MEWDS 유사 백점 병변을 보였고, 뇌척수액 검사에서 개방압 55 cmH2O, 백혈구 수 48 cells/μL의 포도막뇌막증후군을 나타낸 증례를 보고했습니다 16). MEWDS에서 포도막뇌막증후군이 동반된 것은 첫 보고였습니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(「14. MEWDS」節、表3 MEWDSと鑑別すべき疾患). 日本眼科学会雑誌. 2019;123(6):635-696.
- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- Pichi F, Srivastava SK, Chexal S, et al. En face swept-source optical coherence tomography and optical coherence tomography angiography of multiple evanescent white dot syndrome: new insights into pathogenesis. Retina. 2016;36(Suppl 1):S178-S188.
- Yannuzzi NA, Swaminathan SS, Zheng F, et al. Swept-source OCT angiography shows sparing of the choriocapillaris in multiple evanescent white dot syndrome. Ophthalmic Surg Lasers Imaging Retina. 2017;48(1):69-74.
- Mantovani A, Invernizzi A, Staurenghi G, Herbort CP Jr. Multimodal imaging of foveal granularity in multiple evanescent white dot syndrome. Ocul Immunol Inflamm. 2019;27(1):141-147.
- Dell’omo R, Wong R, Marino M, Konstantopoulou K, Pavesio C. Relationship between fluorescein angiography and indocyanine green angiography findings in multiple evanescent white dot syndrome. Br J Ophthalmol. 2010;94(1):59-63.
- Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
- Khochtali S, Dridi T, Abroug N, et al. Swept-source optical coherence tomography angiography shows choriocapillaris flow reduction in multiple evanescent white dot syndrome. J Curr Ophthalmol. 2020;32(2):211-215.
- Zicarelli F, Mantovani A, Preziosa C, Staurenghi G. Multiple evanescent white dot syndrome: a new interpretation. Ocul Immunol Inflamm. 2020;28(6):862-870.
- Wang L, Lankry P, Rabinovitch D, et al. An elderly man with atypical multiple evanescent white dot syndrome. Case Rep Ophthalmol. 2022;13:892-896.
- Ramirez Marquez E, Ayala Rodríguez SC, Rivera L, et al. Contralateral recurrences of post-vaccination multiple evanescent white dot syndrome. Cureus. 2022;14(12):e32300.
- Smeller L, Toth-Molnar E, Sohar N. White dot syndrome report in a SARS-CoV-2 patient. Case Rep Ophthalmol. 2022;13:744-750.
- Shepherd EA, Herst BS, Parlitsis GJ, et al. Multiple evanescent white-dot syndrome in a 9-year-old girl. J Vitreoretinal Dis. 2022;6(6):470-473.
- Chen N, Mandell M, Arjmand P. Multimodal imaging findings of multiple evanescent white dot syndrome in COVID-19 patients. IDCases. 2024;38:e02110.
- Yasuda E, Matsumiya W, Maeda Y, et al. Multiple evanescent white dot syndrome following BNT162b2 mRNA COVID-19 vaccination. Am J Ophthalmol Case Rep. 2022;26:101532.
- Wiley ZC, Pakravan M, Charoenkijkajorn C, et al. Uveomeningeal syndrome presenting with bilateral optic disc edema and multiple evanescent white dots syndrome (MEWDS). Am J Ophthalmol Case Rep. 2022;26:101538.
