急性期所見

多發性消失性白點症候群(MEWDS)
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是多發性消失性白點症候群?
Section titled “1. 什麼是多發性消失性白點症候群?”多發性消失性白點症候群(multiple evanescent white dot syndrome; MEWDS)是1984年Jampol等人首次報告的7)急性炎症性疾病。好發於近視的年輕女性單眼,眼底後極部至赤道部出現大量位於視網膜深層至RPE層次的淡灰白色斑。數週內白點幾乎消失,視力也改善,是一種自然緩解型疾病。
在葡萄膜炎診療指引(日眼會誌 2019;123(6):635-696)中,被歸類為非感染性、以眼底病變為主的後葡萄膜炎,具有單眼性、急性發作、一過性病程的特點1)。
MEWDS被認為是AZOOR複合體(MEWDS, AZOOR, AMN, PIC, MFC, AIBSE, AAOR)中的一種疾病,這些疾病群被視為以外視網膜、感光細胞和RPE為主要病變的炎症性疾病的連續譜2)。在白點症候群中,MEWDS是透過多模態成像對其病理生理學了解最深入的疾病之一2)。
- 好發年齡:20~50歲
- 性別比例:女性佔絕對優勢,男女比1:41)
- 年發生率:約每10萬人0.22例10)
- 好發於近視眼,多為單眼
- 半數病例在發病前1-2週有感冒樣前驅症狀1)
- 誘發因素包括感冒樣症狀、口服避孕藥、疫苗接種和上呼吸道感染1)
- 雙眼發病極為罕見,文獻中僅有6-7例2, 4)。雙眼發病時病程常不對稱
- 也有非典型年齡的報導,最年輕者為9歲女童13),最年長者為75歲男性10)
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”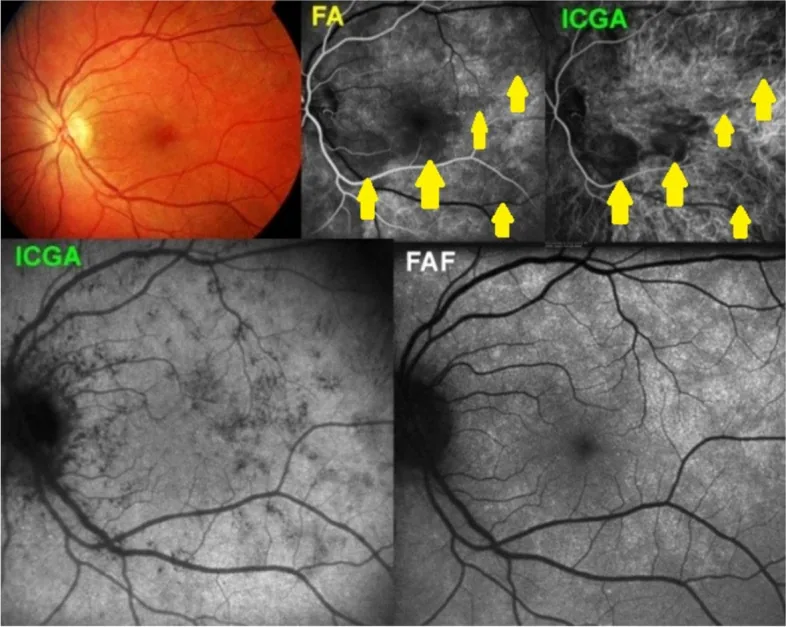
從後極部到赤道部,視網膜深層至RPE散在淡白色斑狀病灶1)。白斑大小100~200 μm,大小不一,可互相融合。可能出現輕度視神經盤充血及輕度玻璃體細胞1)。中心凹顆粒狀變化(橙黃色顆粒狀外觀)是近紅外FAF可確認的診斷性所見,見於74%~96%的病例,白斑消失後仍可能是唯一所見2)5)。
其他臨床所見包括:
緩解期所見
光視症被認為是由外視網膜和橢圓體帶(感光細胞內節外節連接處)的損傷引起的。感光細胞功能異常時,會產生異常的光刺激訊號,使人感覺到不存在的光。通常隨著疾病恢復而消失。
3. 原因與風險因素
Section titled “3. 原因與風險因素”MEWDS的主要病變部位是外視網膜和橢圓體帶(IS/OS),而脈絡膜微血管層通常保持完好2)。ICGA晚期可見低螢光,但有人指出這可能是由於RPE功能障礙導致的色素攝取異常,而非脈絡膜微血管缺血2)。脈絡膜微血管層損傷(ICGA表現)在無視網膜白點的視乳頭周圍也可觀察到,且可能比臨床可見的病灶範圍更廣1)。
誘因與風險因素
Section titled “誘因與風險因素”- 原因不明。存在自體免疫或病毒感染誘發的假說。
- 前驅因素:感冒樣症狀(流感、腮腺炎等)、口服避孕藥、疫苗接種、上呼吸道感染1)
- 近視眼(尤其是中度至高度近視)
- 作為AZOOR複合體中的一種疾病,認為由遺傳易感性(如IL-10單倍型)加上環境因素(病毒、疫苗、藥物)共同作用而發病2)7)
- 疫苗接種:已有接種B肝疫苗、流感疫苗、HPV疫苗、腦膜炎球菌疫苗和COVID-19疫苗後發病的報導15, 11)。從疫苗接種到MEWDS發病的中位時間為14天(範圍1-90天)。
- COVID-19感染:已有多個SARS-CoV-2感染後發生MEWDS的病例報導,在COVID-19大流行期間MEWDS的報告數量顯著增加14)。從感染到發病的平均時間為29.6天(範圍0-70天)。
作為免疫學機制,有研究提示疫苗來源的mRNA透過RIG-I誘導第一型干擾素(IFN-I),可能導致RPE細胞的屏障功能障礙15)。分子擬態和佐劑介導的發炎也被推測。一項初步報告顯示,MEWDS患者中HLA-B51單倍型的頻率是正常組的3.5倍12)。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”MEWDS的診斷基於特徵性眼底所見和多模態影像。
| 檢查方法 | 特徵性所見 |
|---|---|
| FA | 白斑在造影早期呈花環狀過螢光,持續至晚期。視神經盤滲漏2)6) |
| ICGA | 白斑在晚期呈低螢光。低螢光區域比臨床所見更廣泛。視盤周圍也出現低螢光斑1)2) |
| FAF(眼底自發螢光) | 急性期呈高自發螢光。低螢光與過螢光混合。對診斷有用1)2) |
| SD-OCT | 活動期橢圓體帶明顯紊亂或消失,RPE局部增厚2)3) |
| OCT-A | 脈絡膜微血管血流通常保留(部分有血流缺失的報告)4)8) |
| 多焦ERG | 黃斑部振幅平坦化(急性期)。隨恢復而正常化1) |
| Goldmann視野 | Mariotte盲點擴大、中心暗點1) |
MEWDS的特徵是FA從早期即顯示高螢光,這是與APMPPE的重要鑑別點。APMPPE表現為造影早期低螢光→晚期高螢光的逆轉現象,而MEWDS則從早期開始持續高螢光2)6)。此外,OCT在活動期可見橢圓體帶(IS/OS線)不規則,但這種紊亂的改善伴隨視力恢復,是理解病理的重要所見3)。
鑑別診斷(來自葡萄膜炎診療指南「表3」)1)
Section titled “鑑別診斷(來自葡萄膜炎診療指南「表3」)1)”| 疾病 | 鑑別要點 |
|---|---|
| APMPPE | 雙眼性、大斑塊、FA螢光逆轉(早期低螢光→晚期高螢光) |
| AZOOR | 眼底正常、僅ERG異常 |
| AIBSE | 視乳頭周圍環狀灰白色混濁、Mariotte盲點擴大 |
| AMN | 黃斑部紅褐色斑狀病變 |
| AAOR | 視網膜深層環狀灰白色混濁 |
| PIC | 中度近視女性、後極部小型黃白斑、CNV合併率高、多為雙眼性 |
| 鳥槍彈樣脈絡膜視網膜病變/多灶性脈絡膜炎 | 炎症遷延、雙眼性 |
| 類肉瘤病/眼內淋巴瘤 | 全身合併、炎症遷延 |
5. 標準治療方法
Section titled “5. 標準治療方法”由於無需特殊治療即可期待自然痊癒,輕症病例以觀察為基本1)。白斑在數週內自然消失,視力預後良好。隨著病程,ERG趨於平靜並正常化1)。
抗發炎治療的適應症
Section titled “抗發炎治療的適應症”僅在視力下降顯著或合併視乳頭水腫時,考慮以下治療。
- 口服普賴蘇濃:從30 mg/日開始逐漸減量。適用於視力下降明顯或合併視乳頭水腫的短期使用。
- 卡那克林錠:有時合併使用以改善微循環。
- 由於該疾病有很強的自然緩解傾向,大多數病例無需治療1)。
- 隨著病程進展,ERG恢復正常,視力有望恢復1)。
一項對7例COVID-19相關MEWDS的回顧顯示,5例(71%)接受了某種治療,提示COVID-19相關病例可能比一般病毒性MEWDS稍重14)。也有視力恢復不完全的報告,因此COVID-19相關病例需要仔細追蹤。
慢性復發病例
Section titled “慢性復發病例”復發率低於10%,但慢性復發病例有使用環孢素的報告2)。
合併CNV的病例
Section titled “合併CNV的病例”合併脈絡膜新生血管時,考慮玻璃體內注射抗VEGF藥物(貝伐珠單抗、雷珠單抗、阿柏西普)1)。CNV雖罕見,但可能導致視力預後不良,需注意。OCT-A有助於評估CNV活動性,對抗VEGF治療決策和療效判斷有幫助8)。
基本上,該疾病有很強的自然緩解傾向,大多數病例無需治療。葡萄膜炎診療指引也指出「無需特殊治療,自然恢復」是基本方針1)。僅在視力下降顯著的重症病例或合併視乳頭水腫時,口服類固醇可能加速恢復。
6. 病理生理學與詳細發病機轉
Section titled “6. 病理生理學與詳細發病機轉”MEWDS的主要受損部位是外層視網膜和橢圓體帶(IS/OS接合處),而脈絡膜微血管層原則上得以保留2)。這是與APMPPE的重要病理差異。
外層視網膜與橢圓體帶損傷
Section titled “外層視網膜與橢圓體帶損傷”OCT表現顯示,活動期橢圓體帶(視網膜感光細胞內節外節接合處)變得不規則或消失。據報導,隨著這種紊亂的改善,視力得以恢復,表明外層視網膜損傷的暫時性和可逆性是MEWDS的本質3)。近年來的en face swept-source OCT還能可視化傳統斷層影像難以識別的病灶範圍3)。
ICGA與脈絡膜微血管
Section titled “ICGA與脈絡膜微血管”ICGA晚期可見低螢光,但有人指出這可能是由於RPE功能障礙導致的色素攝取異常,而非脈絡膜微血管缺血所致2)。OCT-A顯示脈絡膜微血管血流原則上得以保留,僅部分病例報告有暫時性血流空區4)8)。使用swept-source OCT-A的研究證實了MEWDS中脈絡膜微血管的保留4)。
中心窩顆粒狀變化(foveal granularity)
Section titled “中心窩顆粒狀變化(foveal granularity)”近紅外FAF上觀察到的中心窩顆粒狀變化是反映中心窩感光細胞層損傷的特徵性表現2)5)。多色成像(近紅外反射和藍色反射)也可確認,被認為有助於活動期的診斷。
作為AZOOR複合體的定位
Section titled “作為AZOOR複合體的定位”AZOOR複合體的概念被提出,將MEWDS、AZOOR、PIC、MFC等整合考慮。認為遺傳易感性(如IL-10單倍型)加上多種環境因素(病毒感染、疫苗、藥物)導致發病2)7)。Jampol和Becker(2003)提出這些疾病基於共同的遺傳性自體免疫/發炎機轉的假說7)。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”- OCT-A評估脈絡膜毛細血管功能:使用掃頻源OCT-A可短暫檢測脈絡膜毛細血管的流空現象,目前正在重新評估脈絡膜毛細血管板的參與情況4)8)。部分病例也觀察到脈絡膜毛細血管血流減少,提示病情的多樣性8)。
- En face掃頻源OCT:作為一種新的診斷方法,能夠三維可視化白點病變的形狀、分佈和內層邊界,相關報告正在增加3)。
- AZOOR複合體概念的進展:將MEWDS、AZOOR、PIC、AMN、AIBSE和AASR作為單一譜系進行整合理解的研究正在推進2)9)。Zicarelli等人(2020)提出了對MEWDS病理的新解釋9)。
- 多色成像:利用近紅外反射和藍色反射開發臨床診斷輔助工具。現已能夠非侵入性評估中心凹顆粒狀改變5)。
- COVID-19感染後或疫苗接種後MEWDS:感染後或mRNA疫苗接種後發病的病例在全球範圍內報告增加,其作為免疫觸發因素的角色受到關注。
- 復發率和長期預後數據:有待大規模長期追蹤研究的積累。
COVID-19與MEWDS的關聯
Section titled “COVID-19與MEWDS的關聯”Chen等人(2024)文獻回顧了7例COVID-19感染後發生的MEWDS,報告平均年齡38.4歲,女性5例,平均感染至發病間隔29.6天14)。2例(29%)為雙眼,5例(71%)接受了治療,提示COVID-19相關病例可能比典型病例更易出現視力恢復不完全和需要治療干預。
關於COVID-19疫苗相關MEWDS,一項27例的系統綜述報告中位年齡34.1歲,女性佔優勢,接種至發病中位間隔14.7天14)。mRNA疫苗(輝瑞-BioNTech)最為常見。
疫苗接種與復發
Section titled “疫苗接種與復發”Ramirez Marquez等人(2022)報告了一名17歲女性,在同時接種HPV疫苗和腦膜炎球菌疫苗後發生MEWDS,隨後在COVID-19感染和BNT162b2疫苗接種後,對側眼出現兩次復發11)。
非典型病例報告
Section titled “非典型病例報告”Yasuda等人(2022)報告了一名67歲日本女性在接種第二劑BNT162b2 mRNA疫苗次日發生MEWDS 15)。伴有中度玻璃體炎,視力降至0.2,但未經治療恢復至0.8。
Wiley等人(2022)報告了一名17歲女性在接種SARS-CoV-2疫苗2天後出現雙側視神經盤水腫和MEWDS樣白點病變,腦脊髓液檢查顯示開放壓55 cmH2O、白血球計數48個/μL的葡萄膜腦膜症候群 16)。這是首次報告MEWDS合併葡萄膜腦膜症候群。
8. 參考文獻
Section titled “8. 參考文獻”- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(「14. MEWDS」節、表3 MEWDSと鑑別すべき疾患). 日本眼科学会雑誌. 2019;123(6):635-696.
- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- Pichi F, Srivastava SK, Chexal S, et al. En face swept-source optical coherence tomography and optical coherence tomography angiography of multiple evanescent white dot syndrome: new insights into pathogenesis. Retina. 2016;36(Suppl 1):S178-S188.
- Yannuzzi NA, Swaminathan SS, Zheng F, et al. Swept-source OCT angiography shows sparing of the choriocapillaris in multiple evanescent white dot syndrome. Ophthalmic Surg Lasers Imaging Retina. 2017;48(1):69-74.
- Mantovani A, Invernizzi A, Staurenghi G, Herbort CP Jr. Multimodal imaging of foveal granularity in multiple evanescent white dot syndrome. Ocul Immunol Inflamm. 2019;27(1):141-147.
- Dell’omo R, Wong R, Marino M, Konstantopoulou K, Pavesio C. Relationship between fluorescein angiography and indocyanine green angiography findings in multiple evanescent white dot syndrome. Br J Ophthalmol. 2010;94(1):59-63.
- Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
- Khochtali S, Dridi T, Abroug N, et al. Swept-source optical coherence tomography angiography shows choriocapillaris flow reduction in multiple evanescent white dot syndrome. J Curr Ophthalmol. 2020;32(2):211-215.
- Zicarelli F, Mantovani A, Preziosa C, Staurenghi G. Multiple evanescent white dot syndrome: a new interpretation. Ocul Immunol Inflamm. 2020;28(6):862-870.
- Wang L, Lankry P, Rabinovitch D, et al. An elderly man with atypical multiple evanescent white dot syndrome. Case Rep Ophthalmol. 2022;13:892-896.
- Ramirez Marquez E, Ayala Rodríguez SC, Rivera L, et al. Contralateral recurrences of post-vaccination multiple evanescent white dot syndrome. Cureus. 2022;14(12):e32300.
- Smeller L, Toth-Molnar E, Sohar N. White dot syndrome report in a SARS-CoV-2 patient. Case Rep Ophthalmol. 2022;13:744-750.
- Shepherd EA, Herst BS, Parlitsis GJ, et al. Multiple evanescent white-dot syndrome in a 9-year-old girl. J Vitreoretinal Dis. 2022;6(6):470-473.
- Chen N, Mandell M, Arjmand P. Multimodal imaging findings of multiple evanescent white dot syndrome in COVID-19 patients. IDCases. 2024;38:e02110.
- Yasuda E, Matsumiya W, Maeda Y, et al. Multiple evanescent white dot syndrome following BNT162b2 mRNA COVID-19 vaccination. Am J Ophthalmol Case Rep. 2022;26:101532.
- Wiley ZC, Pakravan M, Charoenkijkajorn C, et al. Uveomeningeal syndrome presenting with bilateral optic disc edema and multiple evanescent white dots syndrome (MEWDS). Am J Ophthalmol Case Rep. 2022;26:101538.
