發病時

急性帶狀潛在性視網膜外層病變(AZOOR)
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是急性帶狀潛在性視網膜外層病變?
Section titled “1. 什麼是急性帶狀潛在性視網膜外層病變?”急性帶狀潛在性視網膜外層病變(acute zonal occult outer retinopathy; AZOOR)是1990年代由Gass提出並確立疾病概念的急性炎症性疾病3)。其特徵是儘管眼底檢查大致正常,但出現急性視野缺損、閃光感和視力下降。病變主要位於感光細胞和視網膜外層,正如其名,是一種「潛在性」外層視網膜病變。
日本眼科學會制定了AZOOR的診斷指南,將重症定義為較好眼矯正視力<0.3。在葡萄膜炎診療指南(日眼會誌2019;123(6):635-696)的AZOOR複合體鑑別表(表3)中也收錄了AZOOR1)。當出現眼底檢查無法解釋的視野異常時,鑑別診斷中應始終考慮AZOOR的可能性。
AZOOR被視為AZOOR複合體(MEWDS、AZOOR、AMN、PIC、MFC、AIBSE、AAOR)中的一種疾病,這些疾病被理解為以外層視網膜、感光細胞和RPE為主要病變部位的炎症性疾病的連續譜1)2)。多模態影像學的發展加深了對AZOOR複合體病理生理的綜合理解2)。
已報導的AZOOR變異型如下1):
- AAOR(急性環狀外層視網膜病變):單側、環狀灰白色邊界、向心性進展
- MORR(多帶狀外層視網膜色素上皮病變):急性發作、進行性、RPE受累
- 周邊發病型:罕見變異。視乳頭周圍未受累,從周邊向心性進展11)
- 好發:年輕女性的近視眼
- 約3/4的患者為女性,以30歲左右的年輕人為主
- 單眼發病佔61%,中位追蹤8年後最終76%發展為雙眼
- 對側眼發病平均延遲50個月
- 合併自體免疫疾病:橋本病(最常見)、多發性硬化症1)
- 約20%的病例有感冒樣前驅症狀
關於日本患者的臨床特徵,已有日本AZOOR病例的隊列研究(Saito S等,2015)報導,探討了視功能的自然病程和預後因素4)。
AZOOR的主要損傷部位是感光細胞(外層視網膜、橢圓體帶)。即使眼底外觀正常,OCT也能在與視野缺損對應的區域看到橢圓體帶(IS/OS線)消失。感光細胞內節外節連接處的破壞導致視功能下降,因此即使眼底正常,也會出現視力和視野障礙。
2. 主要症狀和臨床所見
Section titled “2. 主要症狀和臨床所見”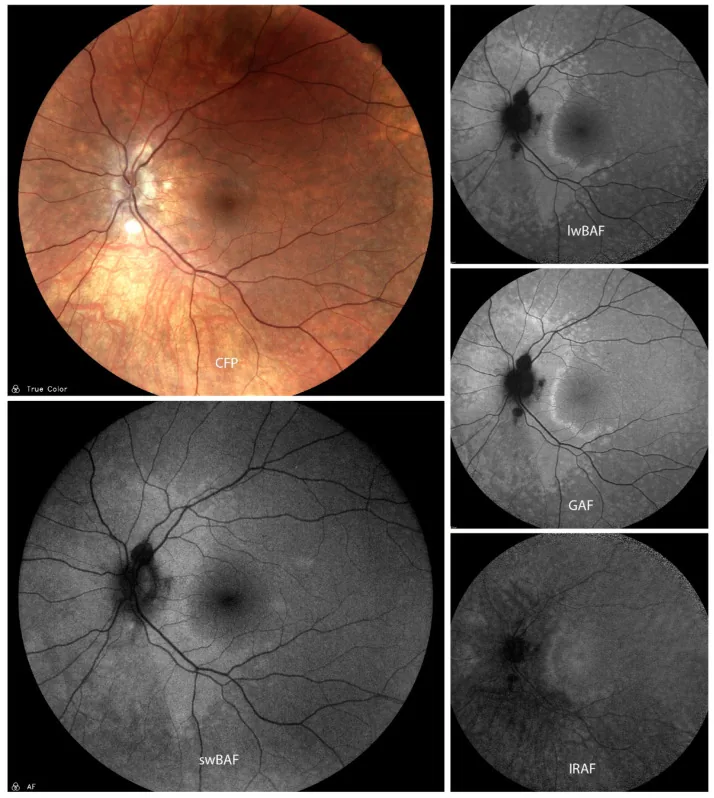
- 閃光感:最具特徵性的症狀之一。急性發作。
- 急性視力下降、視野缺損(1至數個部位)1)
- Mariotte盲點擴大、中心視野缺損、周邊視野缺損1)
- 前驅症狀:感冒樣症狀(約20%的病例)
視野缺損常呈帶狀或扇形分佈,由於眼底外觀正常,有時會被誤診為視神經炎1)。Goldmann視野檢查可發現Mariotte盲點顯著擴大或扇形暗點。
眼底基本正常,有時難以與視神經炎鑑別1)。螢光素眼底血管攝影(FA)通常無異常,這是AZOOR的重要特徵。長期病例可能出現瀰漫性或扇形脈絡膜視網膜萎縮。
慢性期
此外,當出現單眼顳側偏盲時,是由於鼻側視網膜損傷所致,可能表現為尊重垂直子午線的顳側偏盲,因此可能模仿視交叉病變,有時需要MRI檢查12)。部分病例在病程中可能出現RAPD(相對性瞳孔傳入障礙)。
3. 原因與風險因素
Section titled “3. 原因與風險因素”病理生理假說
Section titled “病理生理假說”原因不明,但主要假說包括病毒感染或自體免疫參與。
- 約20%的病例有感冒樣前驅症狀 → 病毒感染誘因假說
- 合併橋本病、多發性硬化 → 自體免疫機制假說1)
- 主要損傷部位:感光細胞(橢圓體帶)、RPE、脈絡膜微血管層(多種學說)
關於AZOOR的主要病變部位,有感光細胞、視網膜色素上皮、脈絡膜微血管層等多種學說,尚無定論。OCT上橢圓體帶消失直接反映了感光細胞內節/外節連接部(IS/OS線)的破壞,該區域的功能恢復通常困難8)。
- 年輕女性、近視眼
- 合併自體免疫疾病(橋本病、多發性硬化症)1)
- 作為AZOOR複合體的遺傳易感性+環境因素(病毒感染、自體免疫觸發)2)
- 癲癇:大鼠研究顯示癲癇發作可誘發視網膜發炎反應,可能存在關聯13)
- 鞏膜扣帶術後:有病例報告術後5年以上出現AZOOR樣表現14)
在Gass的51例病例中,約28%有自體免疫疾病史。除橋本病和多發性硬化症外,已知的合併疾病還包括格雷夫斯病、甲狀腺功能減退症、艾迪生病、重症肌無力、克隆氏症和系統性紅斑狼瘡。約42%的AZOOR患者可檢測到抗視網膜抗體15)。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”AZOOR的診斷基於20-50歲年輕患者出現急性單眼視力下降、視野缺損和閃光感,結合OCT和ERG進行。當眼底檢查無法解釋視野異常時,積極將AZOOR納入鑑別診斷非常重要。
建議的檢查步驟
Section titled “建議的檢查步驟”對於20-50歲相對年輕的患者,出現急性單眼視力下降、視野缺損並伴有閃光感時,首先進行OCT檢查。如果OCT在視野缺損對應區域顯示視網膜外層異常,則高度懷疑AZOOR。隨後通過ERG和多焦ERG確認1)。
| 檢查方法 | 所見 |
|---|---|
| OCT | 與視野缺損對應的橢圓體帶消失、嵌合體帶消失。有助於預後預測5) |
| 全視野ERG | 廣泛損害時振幅降低。錐體系統異常 > 桿體系統 |
| 多焦ERG | 與視野缺損部位一致的振幅降低。對檢測小範圍病變敏感度高1) |
| 眼底自發螢光(紅外光) | 確認病變區與正常區的邊界 |
| FA | 基本正常所見 |
| Goldmann視野 | Mariotte盲點擴大、中心暗點、區域性暗點1) |
| 自適應光學(AO) | 視細胞排列異常的可視化 |
| PERG(模式ERG) | 可能出現P50降低、N95正常的模式 |
| EOG | 可能出現光反應(light rise)降低、Arden比降低 |
OCT 對預後預測也很有用。在外層(橢圓體帶)消失的區域,該區域的功能恢復無法預期,因此 OCT 的外層評估成為治療決策和預後解釋的依據 5)。當受影響範圍較小時,多焦 ERG 或局部 ERG 比全視野 ERG 更有助於診斷 1)。
鑑別診斷(葡萄膜炎診療指南表3)1)
Section titled “鑑別診斷(葡萄膜炎診療指南表3)1)”| 疾病 | 鑑別要點 |
|---|---|
| 視神經炎 | 透過 ERG 鑑別。視神經炎時 ERG 正常,有眼球運動痛。 |
| MEWDS | 可見白點(AZOOR 眼底正常)。多焦 ERG 也降低。 |
| AMN | 黃斑部紅褐色斑狀病變;OCT 上外核層楔形病變。 |
| AIBSE | 視乳頭周圍環狀灰白色混濁,Mariotte 盲點擴大為特徵。 |
| AAOR | 視網膜深層環狀灰白色混濁。 |
| 多發性硬化症 | 透過 MRI 所見、全身症狀和視神經炎所見鑑別。 |
| np-AIR(非腫瘤伴隨性自體免疫性視網膜病變) | 亞急性至慢性發病,FAF瀰漫性高螢光,EOG正常 |
| 梅毒性外層視網膜病變(SOR) | 與AZOOR非常相似。必須進行梅毒血清學檢查1) |
為排除感染,需進行梅毒、CMV、VZV、HSV檢查。若出現顳側偏盲,應透過MRI排除視交叉病變12)。
5. 標準治療方法
Section titled “5. 標準治療方法”尚無確定的治療方法,自然恢復和視力預後不良的病例並存。
- 輕症病例:不治療,觀察追蹤
- 重症病例(較好眼的最佳矯正視力<0.3):考慮類固醇脈衝療法
由於病因被認為與自體免疫和發炎有關,尤其在重症病例中,可能會採用類固醇脈衝療法。但恢復是自然恢復還是類固醇的效果難以區分。
類固醇脈衝療法方案
Section titled “類固醇脈衝療法方案”| 給藥途徑 | 藥物名稱 | 劑量與用法 |
|---|---|---|
| 靜脈滴注(脈衝) | 甲基潑尼松龍(舒汝美卓佑®) | 1000 mg + 索利塔-T3 500 mL,1小時靜脈滴注,連續3天 |
| 口服(後續治療) | 潑尼松龍(普賴鬆®)錠 5 mg | 8至6錠(40至30 mg),分2次服用,逐漸減量 |
類固醇脈衝療法的效果難以與自然恢復區分,證據僅限於病例報告。目前尚無隨機對照試驗(RCT)。
玻璃體內類固醇注射
Section titled “玻璃體內類固醇注射”玻璃體內類固醇注射也有報告,但需注意白內障、眼壓升高和中心性漿液性脈絡膜視網膜病變(CSR)等副作用風險16)。
免疫抑制療法及其他
Section titled “免疫抑制療法及其他”對於難治性病例,已有以下報告:
- MMF + 環孢素 + IVIg:黴酚酸酯2克/天 + 環孢素200毫克/天 + IVIg 2克/公斤每月一次聯合使用,已報告可改善BCVA17)
- 環孢素:有使用4.5毫克/公斤/天的病例
- 阿達木單抗(復邁):有有效病例的報告
- 抗病毒治療:阿昔洛韋和伐昔洛韋在Gass等人的報告中未顯示明確療效3)
合併CNVM的病例
Section titled “合併CNVM的病例”合併脈絡膜新生血管膜(CNVM)時,可能適用抗VEGF玻璃體內注射(貝伐珠單抗、阿柏西普等)1)。
難治性與復發性病例
Section titled “難治性與復發性病例”對於復發或慢性化病例,考慮合併使用免疫抑制劑(如環孢素)。可參考基於AZOOR複合體相關疾病的治療方案。
有病例報告顯示類固醇脈衝療法有效,但缺乏隨機對照試驗,且難以與自然恢復區分。僅在重症病例(較好眼的最佳矯正視力<0.3)中考慮實施,但即使治療,若外層視網膜持續消失,視力預後不良。OCT上橢圓體帶消失的區域功能恢復通常困難8)。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”AZOOR的病理是光感受器和橢圓體帶(IS/OS連接處)的急性損傷。
損傷部位與OCT的關係
Section titled “損傷部位與OCT的關係”OCT上橢圓體帶的消失直接反映光感受器內節/外節連接處(IS/OS線)的破壞。該區域消失的部位光感受器難以恢復,導致長期視功能障礙5)8)。在輕症或恢復期,可能僅指間區異常而橢圓體帶保留。
- 病毒感染(約20%有感冒樣前驅症狀)或自身免疫(合併橋本病或多發性硬化)可能參與。
- 主要損傷部位:光感受器內節/外節連接處(橢圓體帶)。OCT上的消失直接反映損傷。
- 關於脈絡膜毛細血管板的參與有多種說法,但在OCT-A上,脈絡膜毛細血管通常保持完整或僅有輕微變化2)
- 作為AZOOR複合體的一種疾病,由遺傳易感性加上環境因素(病毒感染、自體免疫)引發2)
作為AZOOR複合體的理解
Section titled “作為AZOOR複合體的理解”AZOOR複合體(MEWDS、AZOOR、AMN、PIC、MFC、AIBSE、AAOR)被認為是同一疾病譜上的相關疾病,具有以外層視網膜和RPE為主要部位的發炎性障礙的共同基礎2)。Jampol和Becker(2003)提出了這些白點症候群基於共同的遺傳性自體免疫/發炎機制的假說10)。
與自體免疫疾病的關聯
Section titled “與自體免疫疾病的關聯”橋本病是最常合併的自體免疫疾病,其次是多發性硬化症。這些合併提示自體免疫機制對視細胞和外層視網膜的攻擊,為理解AZOOR的病理提供了重要線索。
在橢圓體帶持續消失的部位,視細胞的恢復很困難,OCT評估直接關係到長期預後預測。
原發病變部位:光受器外節
Section titled “原發病變部位:光受器外節”多模態影像分析表明,AZOOR的原發病變部位是光受器外節18)。ICG血管造影顯示脈絡膜毛細血管保持完整,脈絡膜毛細血管在初期不受損。FAF高螢光是由於光受器外節消失導致RPE脂褐素暴露所致。脈絡膜繼發性受損(附帶損傷),在進展病例中導致脈絡膜視網膜萎縮。
使用自適應光學眼底攝影(AO-TFI)的定量分析證實,光受器(PR)密度顯著降低,而RPE密度無顯著差異,從細胞水平支持PR是主要靶點19)。即使在EZ恢復後,ONL變薄和PR密度降低仍持續存在,形態恢復和功能障礙之間可能出現分離。
Qian等人的綜述主張「AZOOR是AIR的一種特殊形式」,提出了一種機制:抗體從視盤邊緣漏出,免疫產物擴散到視網膜下,形成與視神經相連的大暗點17)。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”- AZOOR複合體的整合理解:與MEWDS、AMN、PIC、MFC、AIBSE、AAOR具有共同基礎的連續體概念正在建立中1)2)
- 自適應光學(AO)觀察感光細胞:可視化病變區域的感光細胞排列異常,促進對病變範圍的詳細評估。
- AO-TFI(自適應光學眼底攝影)的進展:作為一種非侵入性、體內觀察和量化RPE及光受體細胞層級的技術而受到關注19)。首次直接證明EZ形態恢復後PR密度降低持續存在,有助於闡明「結構-功能分離」。
- OCT-A脈絡膜微血管評估:正在研究以闡明脈絡膜血流的參與2)。OCT-A血流空區可能作為疾病評估的指標。
- OCTA診斷與治療監測:en-face外層視網膜切片的星空樣外觀可能有助於AZOOR的診斷輔助和治療反應監測16)。
- 多模態影像疾病分型:Mrejen等人(2014)提出基於多模態影像的AZOOR分類系統6)。這促進了疾病類型與預後關係的闡明。
- AZOOR變異型的識別與分類:對多種疾病形式(包括周邊發病變異型:向心性進展、視乳頭周圍未受影響)的認識正在加深11)。
- AZOOR與繼發性np-AIR的關聯:有觀點認為AZOOR進展可能導致繼發性np-AIR(非副腫瘤性自體免疫性視網膜病變),並期待應用於包括IVIg在內的免疫治療17)。
- 類固醇治療證據的建立:目前尚無RCT,病例報告的累積是挑戰4)。
- 長期預後生物標誌物:OCT上橢圓體帶的保留和多焦ERG模式正在被研究作為預測自然恢復與進展病例差異的指標4)7)。
- 日本患者隊列數據:Saito等人對日本AZOOR患者的長期追蹤數據有助於識別預後因素4)9)。
- 未解決的問題:通過RCT確立治療方法、完全闡明病因(病毒 vs 自體免疫)、驗證早期介入對預後的改善效果、開發診斷生物標誌物。
8. 參考文獻
Section titled “8. 參考文獻”- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(AZOOR complex 鑑別表を含む). 日本眼科学会雑誌. 2019;123(6):635-696.
- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- Gass JD. Acute zonal occult outer retinopathy. Donders Lecture: The Netherlands Ophthalmological Society, Maastricht, Holland, June 19, 1992. J Clin Neuroophthalmol. 1993;13(2):79-97.
- Saito S, Saito W, Saito M, et al. Acute zonal occult outer retinopathy in Japanese patients: clinical features, visual function, and factors affecting visual function. PLoS One. 2015;10(4):e0125133.
- Saito W, Kase S, Fujiya A, et al. Multimodal imaging in acute zonal occult outer retinopathy. Br J Ophthalmol. 2019;103(7):908-913.
- Mrejen S, Khan S, Gallego-Pinazo R, et al. Acute zonal occult outer retinopathy: a classification based on multimodal imaging. JAMA Ophthalmol. 2014;132(9):1089-1098.
- Gass JD, Agarwal A, Scott IU. Acute zonal occult outer retinopathy: a long-term follow-up study. Am J Ophthalmol. 2002;134(3):329-339.
- Makino S, Tampo H. Optical coherence tomography and electroretinographic findings in patients with acute zonal occult outer retinopathy. Clin Ophthalmol. 2013;7:1.
- Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
- Li D, Kishi S. Loss of photoreceptor outer segment in acute zonal occult outer retinopathy. Arch Ophthalmol. 2007;125(9):1194-1200.
- Ünlü BH, Karti O, Saatci AO. A case of an acute zonal occult outer retinopathy variant characterized with an insidious peripheral onset and centripetal progression. Cureus. 2024;16(5):e59600.
- Ahmed Y, Sayal A, Kaplan AJ, Micieli JA. Monocular temporal hemianopia due to acute zonal occult outer retinopathy. Case Rep Ophthalmol. 2022;13(1):44-9.
- Karska-Basta I, Romanowska-Dixon B, Pojda-Wilczek D, et al. Acute zonal occult outer retinopathy in a patient suffering from epilepsy: five-year follow-up. Medicina. 2021;57(11):1276.
- Fung AT, Lo-Cao E, Cornish EE. Acute zonal occult outer retinopathy-like presentation secondary to scleral buckle. Am J Ophthalmol Case Rep. 2022;28:101716.
- Roy R, Dutta Majumder P. Current understanding of acute zonal occult outer retinopathy (AZOOR). Indian J Ophthalmol. 2024;72(7):935-7.
- Özyol E, Özyol P. Acute zonal occult outer retinopathy: optical coherence tomography angiography findings and treatment response. GMS Ophthalmol Cases. 2022;12:Doc16.
- Khan S, Saigal K, Moxam J, Maleki A. A case of concomitant acute zonal occult outer retinopathy and secondary nonparaneoplastic autoimmune retinopathy. Case Rep Ophthalmol. 2025;16(1):124-32.
- Herbort CP Jr, Arapi I, Papasavvas I, Mantovani A, Jeannin B. Acute zonal occult outer retinopathy (AZOOR) results from a clinicopathological mechanism different from choriocapillaritis diseases: a multimodal imaging analysis. Diagnostics. 2021;11(7):1184.
- Iuliano M, Lombardo M, Falsini B, et al. Structural, functional, and cellular analysis of a case of acute zonal occult outer retinopathy (AZOOR). Biomedicines. 2025;13(7):1521.
