发病时

急性带状隐匿性视网膜外层病变(AZOOR)
一目了然的要点
Section titled “一目了然的要点”1. 什么是急性带状隐匿性外层视网膜病变?
Section titled “1. 什么是急性带状隐匿性外层视网膜病变?”急性带状隐匿性外层视网膜病变(acute zonal occult outer retinopathy; AZOOR)是1990年代由Gass提出并确立疾病概念的急性炎症性疾病3)。其特征是尽管眼底检查基本正常,但出现急性视野缺损、闪光感和视力下降。病变主要位于感光细胞和视网膜外层,正如其名,是一种“隐匿性”外层视网膜病变。
日本眼科学会制定了AZOOR的诊断指南,将重症定义为较好眼矫正视力<0.3。在葡萄膜炎诊疗指南(日眼会志2019;123(6):635-696)的AZOOR复合体鉴别表(表3)中也收录了AZOOR1)。当出现眼底检查无法解释的视野异常时,鉴别诊断中应始终考虑AZOOR的可能性。
AZOOR被视为AZOOR复合体(MEWDS、AZOOR、AMN、PIC、MFC、AIBSE、AAOR)中的一种疾病,这些疾病被理解为以外层视网膜、感光细胞和RPE为主要病变部位的炎症性疾病的连续谱1)2)。多模态成像的发展加深了对AZOOR复合体病理生理的综合理解2)。
已报道的AZOOR变异型如下1):
- AAOR(急性环状外层视网膜病变):单侧、环状灰白色边界、向心性进展
- MORR(多带状外层视网膜色素上皮病变):急性发作、进行性、RPE受累
- 周边发病型:罕见变异。视乳头周围未受累,从周边向心性进展11)
- 好发:年轻女性的近视眼
- 约3/4的患者为女性,以30岁左右的年轻人为主
- 单眼发病占61%,中位随访8年后最终76%发展为双眼
- 对侧眼发病平均延迟50个月
- 合并自身免疫性疾病:桥本病(最常见)、多发性硬化症1)
- 约20%的病例有感冒样前驱症状
关于日本患者的临床特征,已有日本AZOOR病例的队列研究(Saito S等,2015)报道,探讨了视功能的自然病程和预后因素4)。
AZOOR的主要损伤部位是感光细胞(外层视网膜、椭圆体带)。即使眼底外观正常,OCT也能在与视野缺损对应的区域看到椭圆体带(IS/OS线)消失。感光细胞内节外节连接处的破坏导致视功能下降,因此即使眼底正常,也会出现视力和视野障碍。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”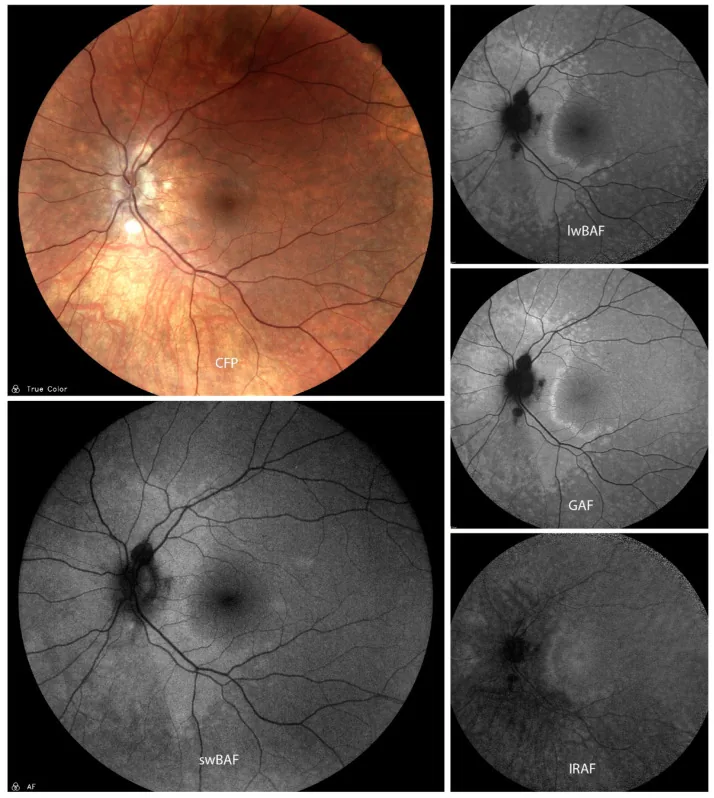
- 闪光感:最具特征性的症状之一。急性发作。
- 急性视力下降、视野缺损(1至数个部位)1)
- Mariotte盲点扩大、中心视野缺损、周边视野缺损1)
- 前驱症状:感冒样症状(约20%的病例)
视野缺损常呈带状或扇形分布,由于眼底外观正常,有时会被误诊为视神经炎1)。Goldmann视野检查可发现Mariotte盲点显著扩大或扇形暗点。
眼底基本正常,有时难以与视神经炎鉴别1)。荧光素眼底血管造影(FA)通常无异常,这是AZOOR的重要特征。长期病例可能出现弥漫性或扇形脉络膜视网膜萎缩。
慢性期
此外,当出现单眼颞侧偏盲时,是由于鼻侧视网膜损伤所致,可能表现为尊重垂直子午线的颞侧偏盲,因此可能模仿视交叉病变,有时需要MRI检查12)。部分病例在病程中可能出现RAPD(相对性瞳孔传入障碍)。
3. 病因与风险因素
Section titled “3. 病因与风险因素”病理生理假说
Section titled “病理生理假说”病因不明,但主要假说包括病毒感染或自身免疫参与。
- 约20%的病例有感冒样前驱症状 → 病毒感染诱因假说
- 合并桥本病、多发性硬化 → 自身免疫机制假说1)
- 主要损伤部位:感光细胞(椭圆体带)、RPE、脉络膜毛细血管层(多种学说)
关于AZOOR的主要病变部位,有感光细胞、视网膜色素上皮、脉络膜毛细血管层等多种学说,尚无定论。OCT上椭圆体带消失直接反映了感光细胞内节/外节连接部(IS/OS线)的破坏,该区域的功能恢复通常困难8)。
- 年轻女性、近视眼
- 合并自身免疫性疾病(桥本病、多发性硬化症)1)
- 作为AZOOR复合体的遗传易感性+环境因素(病毒感染、自身免疫触发)2)
- 癫痫:大鼠研究表明癫痫发作可诱发视网膜炎症反应,可能存在关联13)
- 巩膜扣带术后:有病例报告术后5年以上出现AZOOR样表现14)
在Gass的51例病例中,约28%有自身免疫性疾病史。除桥本病和多发性硬化症外,已知的合并疾病还包括格雷夫斯病、甲状腺功能减退症、艾迪生病、重症肌无力、克罗恩病和系统性红斑狼疮。约42%的AZOOR患者可检测到抗视网膜抗体15)。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”AZOOR的诊断基于20-50岁年轻患者出现急性单眼视力下降、视野缺损和闪光感,结合OCT和ERG进行。当眼底检查无法解释视野异常时,积极将AZOOR纳入鉴别诊断非常重要。
推荐的检查步骤
Section titled “推荐的检查步骤”对于20-50岁相对年轻的患者,出现急性单眼视力下降、视野缺损并伴有闪光感时,首先进行OCT检查。如果OCT在视野缺损对应区域显示视网膜外层异常,则高度怀疑AZOOR。随后通过ERG和多焦ERG确认1)。
| 检查方法 | 所见 |
|---|---|
| OCT | 与视野缺损对应的椭圆体带消失、嵌合体带消失。有助于预后预测5) |
| 全视野ERG | 广泛损害时振幅降低。锥体系统异常 > 杆体系统 |
| 多焦ERG | 与视野缺损部位一致的振幅降低。对检测小范围病变敏感度高1) |
| 眼底自发荧光(红外光) | 确认病变区与正常区的边界 |
| FA | 基本正常所见 |
| Goldmann视野 | Mariotte盲点扩大、中心暗点、区域性暗点1) |
| 自适应光学(AO) | 视细胞排列异常的可视化 |
| PERG(模式ERG) | 可能出现P50降低、N95正常的模式 |
| EOG | 可能出现光反应(light rise)降低、Arden比降低 |
OCT 对预后预测也很有用。在外层(椭圆体带)消失的区域,该区域的功能恢复无法预期,因此 OCT 的外层评估成为治疗决策和预后解释的依据 5)。当受累范围较小时,多焦 ERG 或局部 ERG 比全视野 ERG 更有助于诊断 1)。
鉴别诊断(葡萄膜炎诊疗指南表3)1)
Section titled “鉴别诊断(葡萄膜炎诊疗指南表3)1)”| 疾病 | 鉴别要点 |
|---|---|
| 视神经炎 | 通过 ERG 鉴别。视神经炎时 ERG 正常,有眼球运动痛。 |
| MEWDS | 可见白点(AZOOR 眼底正常)。多焦 ERG 也降低。 |
| AMN | 黄斑部红褐色斑状病变;OCT 上外核层楔形病变。 |
| AIBSE | 视乳头周围环状灰白色混浊,Mariotte 盲点扩大为特征。 |
| AAOR | 视网膜深层环状灰白色混浊。 |
| 多发性硬化 | 通过 MRI 表现、全身症状和视神经炎表现鉴别。 |
| np-AIR(非肿瘤伴随性自身免疫性视网膜病变) | 亚急性至慢性起病,FAF弥漫性强荧光,EOG正常 |
| 梅毒性外层视网膜病变(SOR) | 与AZOOR非常相似。必须进行梅毒血清学检查1) |
为排除感染,需进行梅毒、CMV、VZV、HSV检查。若出现颞侧偏盲,应通过MRI排除视交叉病变12)。
5. 标准治疗方法
Section titled “5. 标准治疗方法”尚无确定的治疗方法,自然恢复和视力预后不良的病例并存。
- 轻症病例:不治疗,观察随访
- 重症病例(较好眼的最佳矫正视力<0.3):考虑类固醇冲击疗法
由于病因被认为与自身免疫和炎症有关,尤其在重症病例中,可能会采用类固醇冲击疗法。但恢复是自然恢复还是类固醇的效果难以区分。
类固醇冲击疗法方案
Section titled “类固醇冲击疗法方案”| 给药途径 | 药物名称 | 剂量和用法 |
|---|---|---|
| 静脉滴注(冲击) | 甲泼尼龙(美卓乐®) | 1000 mg + 索利塔-T3 500 mL,1小时静脉滴注,连续3天 |
| 口服(后续治疗) | 泼尼松龙(泼尼松®)片 5 mg | 8至6片(40至30 mg),分2次服用,逐渐减量 |
类固醇冲击疗法的效果难以与自然恢复区分,证据仅限于病例报告。目前尚无随机对照试验(RCT)。
玻璃体内类固醇注射
Section titled “玻璃体内类固醇注射”玻璃体内类固醇注射也有报道,但需注意白内障、眼压升高和中心性浆液性脉络膜视网膜病变(CSR)等副作用风险16)。
免疫抑制疗法及其他
Section titled “免疫抑制疗法及其他”对于难治性病例,已有以下报道:
- MMF + 环孢素 + IVIg:霉酚酸酯2克/天 + 环孢素200毫克/天 + IVIg 2克/公斤每月一次联合使用,已报道可改善BCVA17)
- 环孢素:有使用4.5毫克/公斤/天的病例
- 阿达木单抗(修美乐):有有效病例的报道
- 抗病毒治疗:阿昔洛韦和伐昔洛韦在Gass等人的报告中未显示明确疗效3)
合并CNVM的病例
Section titled “合并CNVM的病例”合并脉络膜新生血管膜(CNVM)时,可能适用抗VEGF玻璃体内注射(贝伐珠单抗、阿柏西普等)1)。
难治性和复发性病例
Section titled “难治性和复发性病例”对于复发或慢性化病例,考虑联合使用免疫抑制剂(如环孢素)。可参考基于AZOOR复合体相关疾病的治疗方案。
有病例报告显示类固醇冲击疗法有效,但缺乏随机对照试验,且难以与自然恢复区分。仅在重症病例(较好眼的最佳矫正视力<0.3)中考虑实施,但即使治疗,若外层视网膜持续消失,视力预后不良。OCT上椭圆体带消失的区域功能恢复通常困难8)。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”AZOOR的病理是光感受器和椭圆体带(IS/OS连接处)的急性损伤。
损伤部位与OCT的关系
Section titled “损伤部位与OCT的关系”OCT上椭圆体带的消失直接反映光感受器内节/外节连接处(IS/OS线)的破坏。该区域消失的部位光感受器难以恢复,导致长期视功能障碍5)8)。在轻症或恢复期,可能仅指间区异常而椭圆体带保留。
- 病毒感染(约20%有感冒样前驱症状)或自身免疫(合并桥本病或多发性硬化)可能参与。
- 主要损伤部位:光感受器内节/外节连接处(椭圆体带)。OCT上的消失直接反映损伤。
- 关于脉络膜毛细血管板的参与有多种说法,但在OCT-A上,脉络膜毛细血管通常保持完整或仅有轻微变化2)
- 作为AZOOR复合体的一种疾病,由遗传易感性加环境因素(病毒感染、自身免疫)引发2)
作为AZOOR复合体的理解
Section titled “作为AZOOR复合体的理解”AZOOR复合体(MEWDS、AZOOR、AMN、PIC、MFC、AIBSE、AAOR)被认为是同一疾病谱上的相关疾病,具有以外层视网膜和RPE为主要部位的炎症性障碍的共同基础2)。Jampol和Becker(2003)提出了这些白点综合征基于共同的遗传性自身免疫/炎症机制的假说10)。
与自身免疫性疾病的关联
Section titled “与自身免疫性疾病的关联”桥本病是最常合并的自身免疫性疾病,其次是多发性硬化症。这些合并提示自身免疫机制对视细胞和外层视网膜的攻击,为理解AZOOR的病理提供了重要线索。
在椭圆体带持续消失的部位,视细胞的恢复很困难,OCT评估直接关系到长期预后预测。
原发病变部位:光感受器外节
Section titled “原发病变部位:光感受器外节”多模态影像分析表明,AZOOR的原发病变部位是光感受器外节18)。ICG血管造影显示脉络膜毛细血管保持完整,脉络膜毛细血管在初期不受损。FAF高荧光是由于光感受器外节消失导致RPE脂褐素暴露所致。脉络膜继发性受损(附带损伤),在进展病例中导致脉络膜视网膜萎缩。
使用自适应光学眼底成像(AO-TFI)的定量分析证实,光感受器(PR)密度显著降低,而RPE密度无显著差异,从细胞水平支持PR是主要靶点19)。即使在EZ恢复后,ONL变薄和PR密度降低仍持续存在,形态恢复和功能障碍之间可能出现分离。
Qian等人的综述主张“AZOOR是AIR的一种特殊形式”,提出了一种机制:抗体从视盘边缘漏出,免疫产物扩散到视网膜下,形成与视神经相连的大暗点17)。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”- AZOOR复合体的整合理解:与MEWDS、AMN、PIC、MFC、AIBSE、AAOR具有共同基础的连续体概念正在建立中1)2)
- 自适应光学(AO)观察光感受器:能够可视化病变区域的光感受器排列异常,促进对病变范围的详细评估。
- AO-TFI(自适应光学眼底成像)的进展:作为一种非侵入性、体内观察和量化RPE及光感受器细胞水平的技术而受到关注19)。首次直接证明EZ形态恢复后PR密度降低持续存在,有助于阐明“结构-功能分离”。
- OCT-A脉络膜毛细血管评估:正在研究以阐明脉络膜血流的参与2)。OCT-A血流空区可能作为疾病评估的指标。
- OCTA诊断和治疗监测:en-face外层视网膜切片的星空样外观可能有助于AZOOR的诊断辅助和治疗反应监测16)。
- 多模态成像疾病分型:Mrejen等人(2014)提出了基于多模态成像的AZOOR分类体系6)。这促进了疾病类型与预后关系的阐明。
- AZOOR变异型的识别与分类:对多种疾病形式(包括外周发病变异型:向心性进展、视乳头周围未受累)的认识正在加深11)。
- AZOOR与继发性np-AIR的关联:有观点认为AZOOR进展可能导致继发性np-AIR(非副肿瘤性自身免疫性视网膜病变),并期待应用于包括IVIg在内的免疫治疗17)。
- 类固醇治疗证据的建立:目前尚无RCT,病例报告的积累是挑战4)。
- 长期预后生物标志物:OCT上椭圆体带的保留和多焦ERG模式正在被研究作为预测自然恢复与进展病例差异的指标4)7)。
- 日本患者队列数据:Saito等人对日本AZOOR患者的长期随访数据有助于识别预后因素4)9)。
- 未解决的问题:通过RCT确立治疗方法、完全阐明病因(病毒 vs 自身免疫)、验证早期干预对预后的改善效果、开发诊断生物标志物。
8. 参考文献
Section titled “8. 参考文献”- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(AZOOR complex 鑑別表を含む). 日本眼科学会雑誌. 2019;123(6):635-696.
- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- Gass JD. Acute zonal occult outer retinopathy. Donders Lecture: The Netherlands Ophthalmological Society, Maastricht, Holland, June 19, 1992. J Clin Neuroophthalmol. 1993;13(2):79-97.
- Saito S, Saito W, Saito M, et al. Acute zonal occult outer retinopathy in Japanese patients: clinical features, visual function, and factors affecting visual function. PLoS One. 2015;10(4):e0125133.
- Saito W, Kase S, Fujiya A, et al. Multimodal imaging in acute zonal occult outer retinopathy. Br J Ophthalmol. 2019;103(7):908-913.
- Mrejen S, Khan S, Gallego-Pinazo R, et al. Acute zonal occult outer retinopathy: a classification based on multimodal imaging. JAMA Ophthalmol. 2014;132(9):1089-1098.
- Gass JD, Agarwal A, Scott IU. Acute zonal occult outer retinopathy: a long-term follow-up study. Am J Ophthalmol. 2002;134(3):329-339.
- Makino S, Tampo H. Optical coherence tomography and electroretinographic findings in patients with acute zonal occult outer retinopathy. Clin Ophthalmol. 2013;7:1.
- Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
- Li D, Kishi S. Loss of photoreceptor outer segment in acute zonal occult outer retinopathy. Arch Ophthalmol. 2007;125(9):1194-1200.
- Ünlü BH, Karti O, Saatci AO. A case of an acute zonal occult outer retinopathy variant characterized with an insidious peripheral onset and centripetal progression. Cureus. 2024;16(5):e59600.
- Ahmed Y, Sayal A, Kaplan AJ, Micieli JA. Monocular temporal hemianopia due to acute zonal occult outer retinopathy. Case Rep Ophthalmol. 2022;13(1):44-9.
- Karska-Basta I, Romanowska-Dixon B, Pojda-Wilczek D, et al. Acute zonal occult outer retinopathy in a patient suffering from epilepsy: five-year follow-up. Medicina. 2021;57(11):1276.
- Fung AT, Lo-Cao E, Cornish EE. Acute zonal occult outer retinopathy-like presentation secondary to scleral buckle. Am J Ophthalmol Case Rep. 2022;28:101716.
- Roy R, Dutta Majumder P. Current understanding of acute zonal occult outer retinopathy (AZOOR). Indian J Ophthalmol. 2024;72(7):935-7.
- Özyol E, Özyol P. Acute zonal occult outer retinopathy: optical coherence tomography angiography findings and treatment response. GMS Ophthalmol Cases. 2022;12:Doc16.
- Khan S, Saigal K, Moxam J, Maleki A. A case of concomitant acute zonal occult outer retinopathy and secondary nonparaneoplastic autoimmune retinopathy. Case Rep Ophthalmol. 2025;16(1):124-32.
- Herbort CP Jr, Arapi I, Papasavvas I, Mantovani A, Jeannin B. Acute zonal occult outer retinopathy (AZOOR) results from a clinicopathological mechanism different from choriocapillaritis diseases: a multimodal imaging analysis. Diagnostics. 2021;11(7):1184.
- Iuliano M, Lombardo M, Falsini B, et al. Structural, functional, and cellular analysis of a case of acute zonal occult outer retinopathy (AZOOR). Biomedicines. 2025;13(7):1521.
