急性后部多发性斑状色素上皮病变(APMPPE )是一种急性炎症性疾病,表现为双眼后极部视网膜色素上皮 水平出现多发性盘状白斑。
好发于20~30岁(平均25岁),无性别差异。可有前驱感冒样症状。
荧光素眼底血管造影 (FA )中的“荧光逆转现象”(早期低荧光→晚期高荧光)是诊断特征。白斑通常在7~12天内消退,残留脱色素,有很强的自然缓解倾向,视力 预后良好。
罕见情况下可合并脑血管炎(中枢神经血管炎),出现神经症状时需紧急检查。
重症病例(转为地图状脉络膜 炎者)视力 预后可能不良。
OCT -A评估脉络膜 毛细血管血流缺失对活动性评估有用。 急性后部多发性鳞状色素上皮病变(acute posterior multifocal placoid pigment epitheliopathy; APMPPE )是1968年Gass首次报告的一种双眼急性炎症性疾病10) 。其特征为双眼眼底后极部出现视网膜 深层至视网膜色素上皮 (RPE )水平的盘状白斑。
根据葡萄膜炎 诊疗指南(日眼会志 2019;123(6):635-696)的分类,它被归类为非感染性、以眼底病变为主的后部葡萄膜炎 ,具有双眼性、急性发作、一过性病程的临床特点1) 。
发病机制被认为是脉络膜 毛细血管板输入小动脉发生的迟发型超敏反应(IV型过敏)导致的闭塞性血管炎。病毒感染(流感、腮腺炎等)被怀疑为诱因,但详情不明。
好发年龄为20~30岁(平均25岁),无性别差异1) 。多为双眼发病。半数以上病例报告有前驱感冒样症状1) 。罕见情况下有与全身性血管炎、肾病、脑膜脑炎、甲状腺炎的关联报道1) 。
Q
APMPPE只发生在年轻人身上吗?
A
好发年龄为40岁以下的年轻成人,老年人和儿童发病罕见。如果在40岁以后发现类似病变,需要与匍行性脉络膜 炎(地图状脉络膜 炎)鉴别。
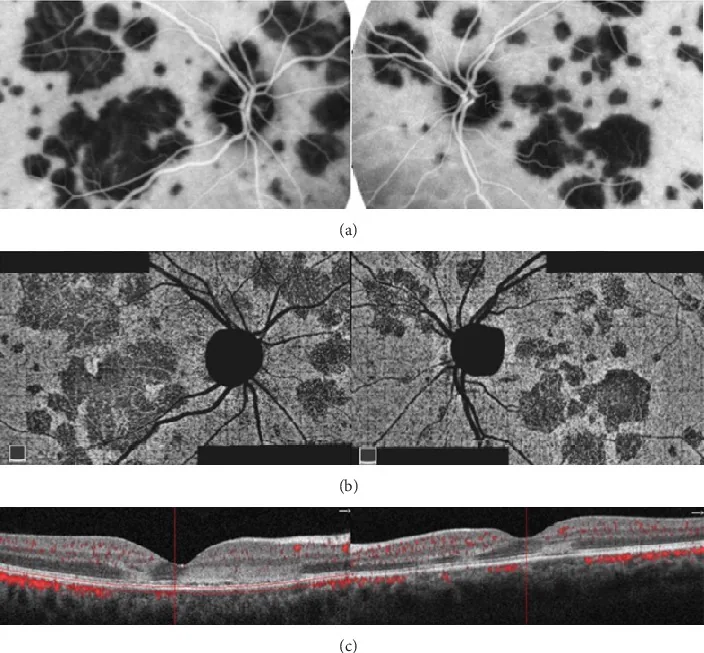
APMPPE的多模态影像。ICGA、OCTA和OCT显示双眼后极部多发斑片状病变。 Oliveira MA, et al. Management of Acute Posterior Multifocal Placoid Pigment Epitheliopathy (
APMPPE ): Insights from Multimodal Imaging with
OCTA . Case Rep Ophthalmol Med. 2020. Figure 5. PM
CI D: PMC7094199. License: CC BY.
双眼后极部可见多发地图状、斑片状病变,
ICGA 呈低荧光,
OCTA 显示相应
脉络膜毛细血管层 血流减少区域。
OCT 显示从外丛状层到
RPE 的高反射改变,为
APMPPE 的典型表现。
主要表现为轻度视力 下降、中心暗点 、视物变形 和小视症。
可伴有闪光感 和旁中心暗点 1) 。
通常无眼前段炎症(眼痛 、充血 )。
双眼后极部视网膜 深层至RPE 水平出现多发灰白色(奶油色至白色)盘状白斑。病灶边界清晰,大小约1/4至1/2视盘直径,基本均匀,数量从数个到多个,融合和扩大趋势不明显。可伴有轻度视盘充血 水肿和轻度玻璃体 细胞1) 。与多发性一过性白点综合征 (MEWDS )的白斑相比,APMPPE 的白斑较大,这是鉴别要点。
急性期所见
眼底白斑 :后极部边界清晰的1/4至1/2视盘直径的灰白色盘状白斑多发。由脉络膜 毛细血管闭塞导致RPE 和视网膜 外层缺血性水肿混浊。
视网膜 外层损伤OCT 显示椭圆体带(IS/OS线)高反射紊乱1) 。椭圆体带的破坏引起自觉症状2) 。
FAF (眼底自发荧光 )OCT 与自发荧光所见密切相关9) 。
缓解期所见
白斑消退 :白斑在7至12天内从中心开始消退,消失后残留轻度色素脱失改变。
OCT 恢复感光细胞 层变薄1) 。
脉络膜 视网膜 萎缩脉络膜 视网膜 萎缩斑1) 。
Q
APMPPE的白斑会消失吗?
A
多数情况下,白斑在发病后7~12天消退,留下脱色素后消失。视力 预后通常良好,复发罕见。但转为地图状脉络膜 炎(匐行性脉络膜炎 )的病例可能出现进展,因此需要定期随访。
推测本质是脉络膜 毛细血管板输入小动脉的迟发型超敏反应(IV型过敏)导致的闭塞性血管炎。OCT血管成像 (OCT -A)在急性期病变区域显示脉络膜 毛细血管水平的血流信号缺失(flow void),支持脉络膜 毛细血管缺血是病理核心的观点3) 。Klufas等人报告,在三种斑状脉络膜 视网膜 炎(APMPPE 、PPM 、RPC )中,OCT -A检测脉络膜 毛细血管血流信号缺失与FA 和ICGA 具有高度一致性4) 。
部分病例在流感样症状(流感、腮腺炎等)、上呼吸道感染或疫苗接种后发病。
已有报道与全身性血管炎(脑血管炎)、肾病、结节性多动脉炎 、甲状腺炎相关1) 。
如果感冒症状后出现突然的视力 下降或中心暗点 ,请立即就诊眼科。
APMPPE 尚无确定的预防方法。
Q
APMPPE有中风风险吗?
A
虽然罕见,但有报道称APMPPE 合并中枢神经系统血管炎的病例。如果出现神经症状(剧烈头痛、意识改变、瘫痪),需紧急进行脑部MRI/MRA检查,并与神经内科协作处理。
APMPPE 的诊断基于特征性眼底表现和荧光血管造影(FA /ICGA )结果。多模态成像可对病理进行多方面的评估2) 。
检查方法 特征性表现 FA (荧光素眼底血管造影 )急性期:早期低荧光→晚期高荧光(“荧光逆转现象”)1) ICGA (吲哚青绿血管造影)从早期到晚期持续低荧光。慢性期:缩小、边界模糊5) SD-OCT 急性期:椭圆体带高反射紊乱。缓解期:感光细胞 层变薄1) OCT -A脉络膜毛细血管层 的血流缺失。与FA /ICGA 高度一致4) FAF (眼底自发荧光 )急性期:病灶低自发荧光或高自发荧光。与OCT 表现相关9) 多焦视网膜电图 急性期黄斑 区附近振幅明显平坦化
FA 中出现的早期低荧光→晚期高荧光,即“荧光逆转现象”,是APMPPE 最具特征性的表现。其解释为:早期由于闭塞性血管炎,脉络膜 毛细血管板的染料流入受阻;晚期周围渗出导致高荧光1) 。ICGA 从早期到晚期始终显示低荧光,更直接反映脉络膜 毛细血管板缺血5) 。
OCT -A是一种无创影像学手段,可评估APMPPE 中脉络膜 毛细血管的血流障碍。Furino等人报道,在急性APMPPE 病变中,OCT -A检测脉络膜 毛细血管血流空区与FA 和ICGA 具有高度一致性8) 。恢复期观察到血流空区缩小伴随视功能改善,因此可作为活动性监测的生物标志物 。
地图状(匍行性)脉络膜 炎 :40多岁、单眼、进行性扩大、地图状、预后不良1) Vogt-小柳-原田病 渗出性视网膜脱离 、多发性视网膜 下渗漏点1) 多发性一过性白点综合征 (MEWDS )FA 早期高荧光1) 持续性斑状黄斑 病变(PPM )/ relentless placoid chorioretinitis(RPC ) :与APMPPE 类似,存在在“placoid chorioretinitis spectrum”内重新分类的讨论4) 7)
Q
APMPPE和MEWDS如何区分?
A
病变大小、FA 表现和双眼性三点是鉴别关键。APMPPE 的白斑比MEWDS 大(1/4至1/2视盘直径),多为双眼性,FA 显示早期低荧光→晚期高荧光的逆转现象。MEWDS 多为单眼,白斑小而广泛,FA 早期即显示高荧光1) 。
有很强的自然缓解倾向,许多病例无需特殊治疗即可自然恢复1) 。轻症病例以观察为主。Jones(1995)的长期随访报告也显示,许多病例最终恢复了良好视力 10) 。
当视力 下降显著、合并视乳头炎或黄斑 附近有病变时,考虑以下治疗。
泼尼松龙片 (5 mg):从30 mg/日开始,在2周至1个月内逐渐减量卡那克林片 (卡利定原酶25~50单位):每次1片,每日3次(作为脉络膜 微循环改善药联合使用)
对于进展为匍行性脉络膜 病变或合并中枢神经系统血管炎的病例,考虑类固醇冲击疗法 (大剂量甲泼尼龙静脉注射)或免疫抑制剂1) 。如果发生脉络膜新生血管 (CNV ),考虑玻璃体内注射 抗VEGF药物 ,但这是罕见的并发症。对于进展为持续性斑块状黄斑 病变(PPM )的病例,如Kolomeyer和Brucker在其系统综述中指出的那样,可能需要长期管理7) 。
Q
类固醇治疗是必须的吗?
A
轻症病例仅通过观察即可自然恢复。当视力 下降显著、视乳头附近炎症严重或伴有中枢神经系统症状时,考虑类固醇 治疗。葡萄膜炎 诊疗指南也指出“无需特殊治疗即可自然恢复”是基本方针1) 。
APMPPE 的病理被理解为以脉络膜 毛细血管闭塞为中心的缺血性改变。
推测其本质是发生在脉络膜 毛细血管输入小动脉的迟发型超敏反应(IV型变态反应)导致的闭塞性血管炎。闭塞 → RPE 和视网膜 外层缺血性改变(水肿、混浊)→ 形成盘状白斑。Mrejen等人显示脉络膜 病变可延伸至更深层,提示可能不仅累及脉络膜 毛细血管,还累及中、大血管水平3) 。
在OCT -A上,观察到内层脉络膜 水平的血流空区,与APMPPE 类似,在“斑块状病变谱系”(包括持续性斑块状黄斑 病变和顽固性斑块状脉络膜 视网膜 炎)这一疾病组的病理基础上,一致发现脉络膜 毛细血管缺血4) 。Klufas等人报告称,三种疾病在OCT -A上的脉络膜 毛细血管血流空区呈现共同模式,支持了斑块状脉络膜 视网膜 炎谱系的概念。
荧光逆转现象的机制:造影早期,由于染料流入脉络膜 毛细血管受阻,呈现低荧光;晚期,染料从周围正常组织渗出,转为高荧光。ICGA 始终显示低荧光,也反映了脉络膜 毛细血管的闭塞性变化5) 。FAF 可以无创评估RPE 损伤的分布,并与OCT 表现高度对应9) 。
COVID-19感染/疫苗后的APMPPE :有报告称感染后出现急性APMPPE 样病变,病毒诱发的免疫反应与其关系受到关注。合并中枢神经血管炎 :对于伴有神经症状的病例,脑部MRI/MRA的推荐力度增强。已有多个APMPPE 合并脑卒中或脑血管炎的病例报告,表明不仅眼部症状,全身性监测也很重要6) 。多模态影像的进步 :通过OCT -A监测脉络膜 毛细血管血流空区可能成为活动性评估的生物标志物 8) 。由于其无创且可重复进行,正成为补充FA 和ICGA 的重要检查手段。疾病类型的重新分类 :包括持续性斑块状黄斑 病变和顽固性斑块状脉络膜 视网膜 炎在内的“斑块状脉络膜 视网膜 炎谱系”的整体理解正在推进4) 。Mirza和Jampol(2012)整理了顽固性斑块状脉络膜 视网膜 炎作为独立疾病概念的特征,并讨论了其与APMPPE 的连续性6) 。
日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(「13. 急性後部多発性斑状色素上皮症」節). 日本眼科学会雑誌. 2019;123(6):635-696.
Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
Mrejen S, Sarraf D, Chexal S, et al. Choroidal involvement in acute posterior multifocal placoid pigment epitheliopathy. Ophthalmic Surg Lasers Imaging Retina. 2016;47:20-26.
Klufas MA, Phasukkijwatana N, Iafe NA, et al. Optical coherence tomography angiography reveals choriocapillaris flow reduction in placoid chorioretinitis. Ophthalmol Retina. 2017;1(1):77-91.
Park D, Schatz H, McDonald HR, Johnson RN. Indocyanine green angiography of acute multifocal posterior placoid pigment epitheliopathy. Ophthalmology. 1995;102:1877-1883.
Mirza RG, Jampol LM. Relentless placoid chorioretinitis. Int Ophthalmol Clin. 2012;52(4):237-242.
Kolomeyer AM, Brucker AJ. Persistent placoid maculopathy: a systematic review. Retina. 2018;38(10):1881-1895.
Furino C, Shalchi Z, Grassi MO, et al. Optical coherence tomography angiography in acute posterior multifocal placoid pigment epitheliopathy. Ophthalmic Surg Lasers Imaging Retina. 2019;50(7):428-436.
Souka AA, Hillenkamp J, Gora F, Gabel VP, Framme C. Correlation between optical coherence tomography and autofluorescence in acute posterior multifocal placoid pigment epitheliopathy. Graefes Arch Clin Exp Ophthalmol. 2006;244(10):1219-1223.
Jones NP. Acute posterior multifocal placoid pigment epitheliopathy. Br J Ophthalmol. 1995;79:384-389.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。